TiO2/蒙脱土复合材料光催化降解丁基黄药性能研究
2022-05-30陈运双马瑞雪蒋潇宇李国栋赵思凯沈岩柏
陈运双 马瑞雪 蒋潇宇 李国栋 赵思凯 沈岩柏
(东北大学资源与土木工程学院,辽宁 沈阳 110819)
黄药对硫化矿物有较好的捕收能力,是硫化矿浮选过程中常用的捕收剂[1-2]。选矿废水中残留的黄药有一定的生物毒性和稳定性,如若不加以处理就直接排放会对周围环境及人体健康造成潜在威胁[3]。目前,处理含黄药废水的方法有吸附法、混凝沉淀法、催化氧化法及生物降解法等[4-8],其中光催化技术降解效率高且绿色环保,应用前景广阔[9]。
TiO2是一种常见的光催化材料,具有成本低廉、催化效果好等优点[10-11]。但单一的TiO2在使用过程中存在光能利用率低、光生电子/空穴对易复合、回收困难等问题[12-13],严重限制了其大规模应用。有研究表明,将TiO2负载于多孔矿物载体上可以有效固定TiO2,促进光催化反应的同时还可以增强其回收性能[14]。蒙脱土(MMT)具有典型的二维结构,比表面积较大,孔道结构丰富,化学稳定性强,是TiO2纳米颗粒的优良载体矿物材料。目前,TiO2/MMT复合材料的制备已成为国内外的研究热点之一。
TiO2/MMT复合材料常见的制备方法有水解沉淀法[15]、溶胶-凝胶法[16]及水热/溶剂热法[17-18],这些方法大多通过原位合成使MMT对TiO2的成核过程和结晶形貌产生影响,从而提升光催化性能,但受反应条件限制,往往不适用于催化材料的大规模工业化生产。考虑到不同的固体在形成界面后,界面两侧的原子种类与浓度存在一定的差异,在一定能量驱动下可以发生微观的扩散运动,这种固相扩散的方案可以用于负载型材料的大规模合成。为此,本研究以MMT为载体,依据固相扩散原理,采用固相研磨—粉末烧结法制备TiO2/MMT复合材料,并利用 XRD、FTIR、SEM等检测手段对所制备的材料进行结构表征与分析;再通过黄药模拟废液的光催化降解试验及机理试验研究TiO2/MMT复合材料的光催化性能及作用机理。
1 试验原料及方法
1.1 试验原料
试验中所用的无水乙醇(ET)、异丙醇(IPA)、乙二胺四乙酸二钠(EDTA-2Na)、1,4-对苯醌(BQ)、硝酸银(AgNO3)均购自国药集团化学试剂有限公司,分析纯;商用TiO2和MMT分别购自麦克林生化科技有限公司和国药集团化学试剂有限公司,化学纯;乙基黄药(SEX)、异丙基黄药(SIPX)、丁基黄药(SBX)和异戊基黄药(SIAX)均来自于铁岭选矿药剂厂,工业纯;试验用水为TS-DI-20L/H型纯水机制备的去离子水。
1.2 TiO2/MMT复合材料的制备
采用固相研磨—粉末烧结法制备TiO2/MMT复合材料。控制TiO2和MMT总质量为1 g,称取不同质量的TiO2和MMT于玛瑙研钵中,加入3 mL的ET作为分散剂研磨30 min;待其干燥后放入管式炉中,以10℃/min的升温速率将材料升温至400℃,持续保温6 h后自然冷却至室温,即制得TiO2/MMT复合材料。其中,TiO2的负载量以TiO2在TiO2/MMT复合材料中的质量百分数来标定,分别制备了负载量为10%、20%、40%、60%和80%的 TiO2/MMT复合材料以用于光催化降解黄药的研究。
1.3 材料的表征与分析
使用X射线衍射仪(XRD-7000型)、傅里叶变换红外光谱仪(Nicolet380型)、扫描电子显微镜(SEMZEISS Ultra Plus型)、紫外/可见/近红外漫反射测试仪(UV-3600型)和稳态/瞬态荧光光谱仪(FLS1000型)对所制备材料的结晶物相、表面化学、微观形貌和光化学特性进行表征分析。
1.4 光催化降解黄药试验
以SBX为主要目标污染物来评价所获光催化剂的降解性能。用去离子水配制不同浓度的SBX模拟废液,取一定质量的光催化剂于50 mL模拟废液中,在PL-03双旋转运动通气型光化学反应仪中进行光催化降解试验。试验时,先进行30 min暗反应以使光催化剂与SBX之间达到吸附-解吸平衡,再打开350W高压汞灯(使用390 nm截止滤光片过滤可见光)进行光催化反应。光催化反应期间,每5min取1次样品,每次取样约4 mL,将取样样品在10000 r/min的转速下离心3 min后,取上清液并转移至比色皿内,利用紫外分光光度计(UV1901 PC)测量模拟废液在最大特征吸收波长301 nm处的吸光度[19]。
根据朗伯-比尔定律,在一定浓度范围内,吸光度与吸光物质的浓度成正比,因此可以用来判断降解过程中黄药浓度的变化。图1为试验所配制SBX溶液的吸光度与浓度的标准曲线图,显示出SBX溶液的浓度与其在301 nm波长处吸光度之间具有良好的线性关系,表明可以根据实时吸光度与初始吸光度的比值(A/A0)来计算模拟废液中SBX的残余比例[20],有文献表明,其他种类黄药的浓度变化也可利用分光光度法进行测定[21]。此外,根据后续光催化降解试验的结果,SBX的降解速率可以用如下所示的一级动力学模型来表示[22]:

图1 吸光度-SBX浓度的标准曲线Fig.1 Standard curve of SBX between absorbance and concentration

其中,C和C0分别为模拟废液中SBX的实时浓度与初始浓度,mg/L;k为反应动力学系数,min-1;t为光照时间,min。
2 试验结果与讨论
2.1 TiO2/MMT复合材料的表征
2.1.1 XRD分析
图2为不同TiO2负载量条件下TiO2/MMT复合材料的XRD图谱。

图2 TiO2、MMT和TiO2/MMT复合材料的XRD图谱Fig.2 XRD patterns of TiO2,MM T and TiO 2/MM T com posite materials
由图2可知:①根据标准卡片JCPDS 13—0315,位于 5.89°、35.15°、36.14°和 62.12°处的峰分别对应MMT的(001)、(110)、(006)和(300)晶面,19.77°、26.62°和 29.86°处均为 Si—O—Si的特征峰,21.85°处为Si—O—Al的特征峰[23-24]。②纳米颗粒存在锐钛矿和金红石2种晶型。根据标准卡片JCPDS 21—1272, 位 于 25.28°、 37.80°、 48.05°、55.06°、68.76°、70.31°、75.03°和 82.66°处的峰分别对应锐钛矿型 TiO2的(101)、(004)、(200)、(211)、(116)、(220)、(215)和(224)晶面;根据标准卡片JCPDS 21—1276,位于 27.4°、54.3°、62.7°处的峰分别对应金红石型TiO2的(110)、(211)和(002)晶面。钛矿型TiO2的特征衍射峰强度远高于金红石型TiO2的,表明纳米颗粒中的TiO2以锐钛矿型为主。
分析图谱还可以发现,当TiO2与MMT复合后,MMT的(001)晶面衍射峰消失,但在5°附近表现出较高的坡度,表明该晶面衍射角朝小角度方向发生了较大幅度的偏移,这是由于MMT在分散剂中研磨时层间力被破坏,层间距扩大所导致的[25];随着光催化剂中TiO2含量的增加,TiO2的特征峰逐渐增强,而位于 19.77°、21.85°、26.62°和 29.86°的 MMT 晶相衍射峰逐渐减弱并消失,表明TiO2和MMT之间并非简单的物理混合,MMT的晶型被部分破坏[23],验证了固相扩散作用的发生。
2.1.2 FTIR分析
图3为不同TiO2负载量条件下TiO2/MMT复合材料的FTIR光谱。

图3 TiO 2、MM T和TiO 2/MMT复合材料的FTIR图谱Fig.3 FTIR spectra of TiO2,MMT and TiO2/MMT composite materials
由图3(a)可知,TiO2图谱中出现了横跨500~800 cm-1的吸收峰,这主要来源于Ti—O键的伸缩振动[26];MMT图谱中3 440 cm-1和1 646 cm-1处的吸收峰分别对应MMT层间水分子中羟基的伸缩振动和弯曲振动[22],3 625 cm-1处的吸收峰来源于MMT中Al—OH键的伸缩振动[24],1 092 cm-1和1 034 cm-1处的吸收峰对应于Si—O键的不对称伸缩振动[23],而500~1 000 cm-1之间的多个强度较小的吸收峰可归因于 MMT铝氧八面体内 Al—O键的振动[27-28]。
由图3(b)可知,随着TiO2负载量的增加,位于500~1 000 cm-1范围内的多个Al—O键振动吸收峰的强度逐渐减弱,并最终形成一个较宽的吸收带,这是TiO2晶体吸收带与MMT特征吸收带的叠加作用导致的[14]。与此同时,1 092 cm-1和1 034 cm-1处Si—O键的2个伸缩振动峰也发生兼并,并在1 054 cm-1处形成一个新的吸收峰,表明TiO2与MMT的复合影响了Si—O键的振动,这与XRD的表征结果相呼应。
2.1.3 SEM分析
为了进一步明确TiO2和MMT之间的结合状态,利用SEM对TiO2、MMT以及80% TiO2/MMT复合材料进行了高倍率扫描,结果如图4所示。
由图4(a)、(b)可知,TiO2为直径25 nm左右的球形颗粒,而MMT呈现出微米级别的片层状结构,这种二维结构拥有较大的比表面积,可以为TiO2纳米颗粒提供大量的附着位点。

图4 MM T、TiO 2和80% TiO 2/MM T复合材料的SEM图Fig.4 SEM images of MMT、TiO2 and 80% TiO2/MMT composite materials
由图4(c)可知,MMT片层或颗粒上聚集有大量的TiO2纳米颗粒,覆盖率高且分散性优良,说明在固相研磨与粉末烧结的作用下,TiO2纳米颗粒可以均匀地固结在MMT表面并将其完全包覆。
2.2 TiO2/MMT复合材料光催化降解黄药性能
2.2.1 TiO2负载量对SBX光催化降解效果的影响
以50 mL浓度为20 mg/L的SBX溶液为模拟废液,加入0.2 g/L的TiO2/MMT复合材料,并在紫外光条件下进行光催化降解试验,结果如图5所示。

图5 TiO2负载量对SBX光催化降解效果的影响Fig.5 Influence of TiO2 addition on the photocatalytic degradation effect of SBX
由图5可知,TiO2/MMT复合材料在紫外光条件下可以有效降解SBX,且降解速率满足一级动力学模型。图5(a)显示,在不加入任何光催化剂的情况下,空白对照组中 SBX在30 min内仅自然降解了28.05%,表明自然条件下的降解率偏低;加入MMT原料后,SBX的降解量比空白组更少,这是由于MMT的加入导致液相体系更加浑浊,从而阻碍了光的照射,同时MMT本身也并不具备光催化作用,进而影响了SBX在光照下的自然分解;随着TiO2负载量的增加,SBX的降解速率逐渐提高,其中80% TiO2/MMT复合材料在30 min内对SBX的降解率高达99.52%,几乎可以将SBX完全分解。单一TiO2原料同样表现出优异的降解效果,结合图5(b)可知,其一级反应动力学系数与80% TiO2/MMT复合材料的持平,表明两者具有极其相近的光降解速率。
为了出现探究上述现象的原因,通过紫外-可见光吸收光谱(UV-Vis)和光致发光光谱(PL)对单一TiO2纳米颗粒和80% TiO2/MMT复合材料进行光化学性能表征,结果如图6所示。
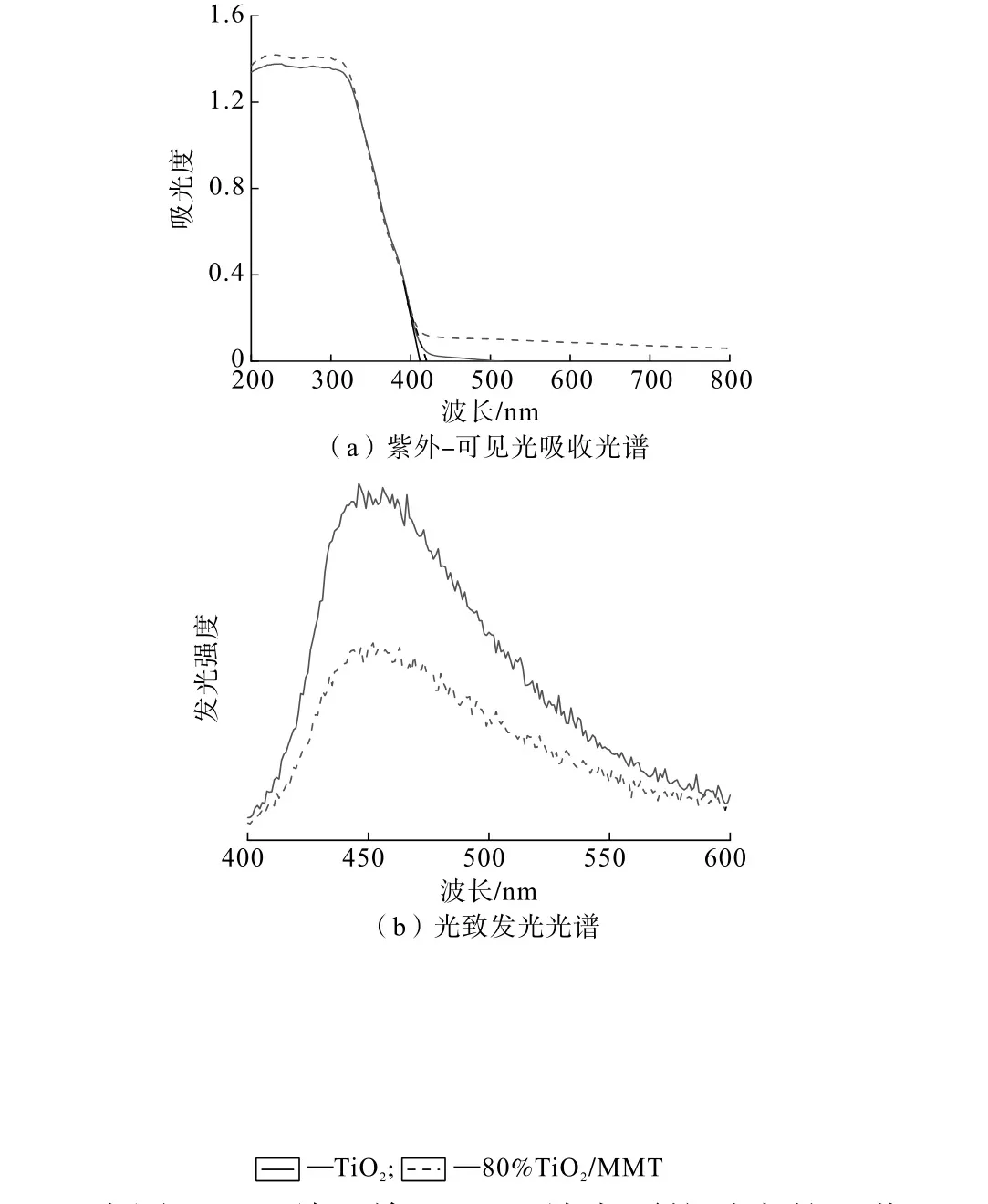
图6 TiO2和80% TiO2/MMT复合材料的紫外-可见光吸收光谱及光致发光光谱Fig.6 UV-Vis spectrogram and PL spectra of TiO 2 and 80% TiO 2/MM T composite materials
由图6(a)可知,单一TiO2纳米颗粒对光的吸收边界位于412 nm,而80% TiO2/MMT复合材料的光吸收范围拓展至421 nm处,同时80% TiO2/MMT复合材料在200~300 nm波段呈现出更高的吸光度,即复合材料对紫外光的吸收性能更强,表明TiO2纳米颗粒与MMT的复合可以明显提升产物对光的利用效率,更有利于光催化降解效果的提升。同时,由图6(b)可知,单一TiO2纳米颗粒表现出较高的PL信号强度,表明其光生电子/空穴对易复合;对比可知,80% TiO2/MMT的PL信号峰值强度降低了近50%,表明MMT不仅是起到了载体固定的作用,同时也有效提升了复合材料中光生载流子的分离效率,这有利于其在光催化降解过程中产生出更多的活性自由基,从而显著增强光催化降解效果。
此外,进一步对光催化体系的浊度进行了测定,结果表明单一 TiO2催化体系的浊度高达303.6 NTU,而80% TiO2/MMT复合材料体系的浊度仅为128.2 NTU。较高的浊度导致单一TiO2催化体系中的光传播效率较低,从而影响了其降解效果,同时浊度的差异在一定程度上也表明80% TiO2/MMT复合材料具有更为优异的回收性能。综合所获光催化剂的催化效果与经济实用性,TiO2的适宜负载量确定为80%。
2.2.2 光催化剂用量对SBX光催化降解效果的影响
以50 mL浓度为20 mg/L的SBX溶液为模拟废液,在紫外光条件下考察80% TiO2/MMT复合材料用量对SBX光催化降解效果的影响,结果如图7所示。
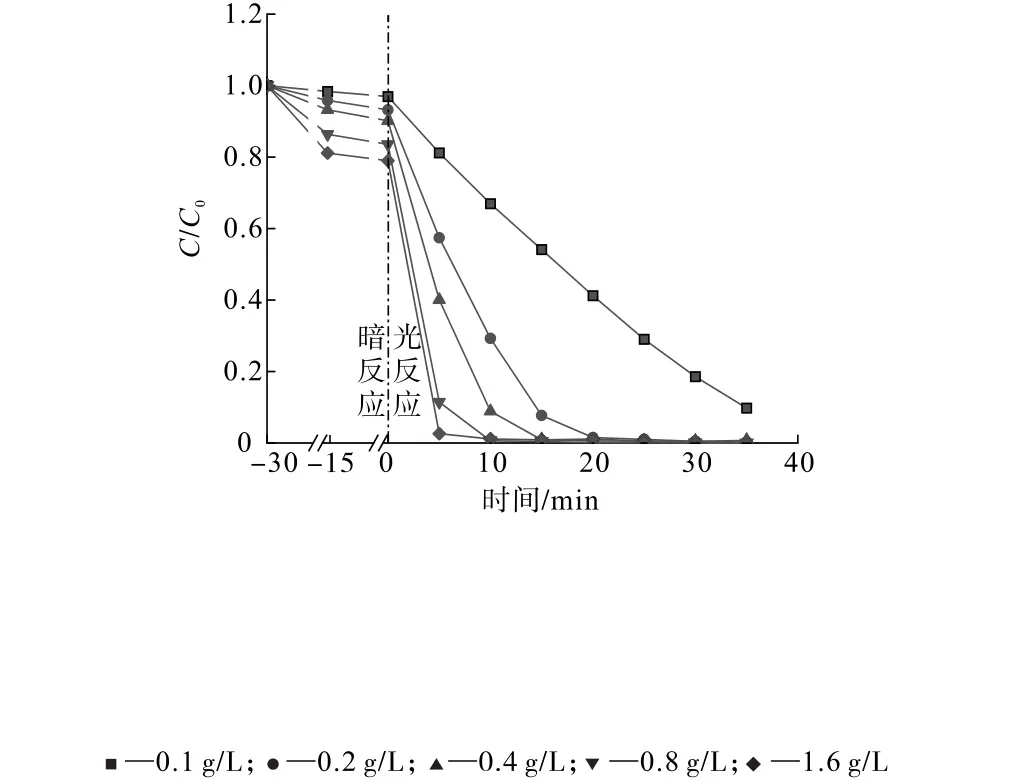
图7 80% TiO 2/MM T复合材料用量对SBX光催化降解效果的影响Fig.7 Influence of 80% TiO2/MMT composite materials dosage on the photocatalytic degradation effect of SBX
由图7可知,80% TiO2/MMT复合材料在暗反应30 min后对SBX的吸附-脱附基本达到平衡,且吸附量随着光催化剂用量的增加而提高;在光催化剂用量为1.6 g/L时,SBX的吸附率可达21.02%。在光催化反应中,SBX的降解率随着时间的延长而增加,光催化降解速率也随着光催化剂用量的增加而明显提高,这归因于复合材料表面的吸附位点和催化活性位点的增多。在光催化剂用量分别为0.1、0.2、0.4、0.8和1.6 g/L时,30 min后的光催化降解率分别为81.43%、99.52%、99.54%、99.96和 99.97%。 考虑到光催化剂用量大于0.2 g/L时,SBX的降解率均可达到99.5%以上,从经济角度出发,80% TiO2/MMT复合材料的适宜用量为0.2 g/L。
2.2.3 SBX初始浓度对其光催化降解效果的影响
固定80% TiO2/MMT复合材料用量为0.2 g/L,在50 mL不同浓度的SBX模拟废液中进行光催化降解试验,结果如图8所示。

图8 80% TiO2/MMT复合材料对不同初始浓度SBX光催化降解效果的影响Fig.8 Influence of initial concentration of SBX on the photocatalytic degradation effect for 80% TiO2/MMT composite materials
由图8可知,随着SBX初始浓度的增加,80% TiO2/MMT复合材料对其光催化降解速率逐渐降低。当SBX初始浓度为10 mg/L时,光照15 min后降解率即可达到98.46%;在光照30 min后,SBX初始浓度为 20、30、40 mg/L的模拟废液中SBX也基本被完全降解。较高浓度SBX废液的降解需要更长的时间,这是因为所用光催化剂的吸附和催化活性位点有限,因此吸附与催化速率也存在上限阈值;随着SBX分子数量的增多,发生在复合材料表面的竞争吸附和降解行为也会导致完全降解时间的延长。但随着光照时间的延长,SBX分子最终均能被光催化剂完全降解。考虑到选矿厂实际所排废水中黄药浓度一般为5~50 mg/L[29],可以发现该复合材料对实际黄药废水同样具有较好的降解效果。
2.2.4 光催化剂对不同种类黄药的适用性
在实际浮选作业过程中,由于硫化矿矿物种类和性质的不同,常会使用不同种类的黄药或其复配产品[1]。为进一步探究所制备光催化复合材料的适用性,固定光催化剂用量为0.2 g/L、黄药模拟废液的初始浓度为20 mg/L,考察80% TiO2/MMT复合材料对SEX、SIPX、SBX及SIAX等4种黄药的光催化降解效果,结果如图9所示。
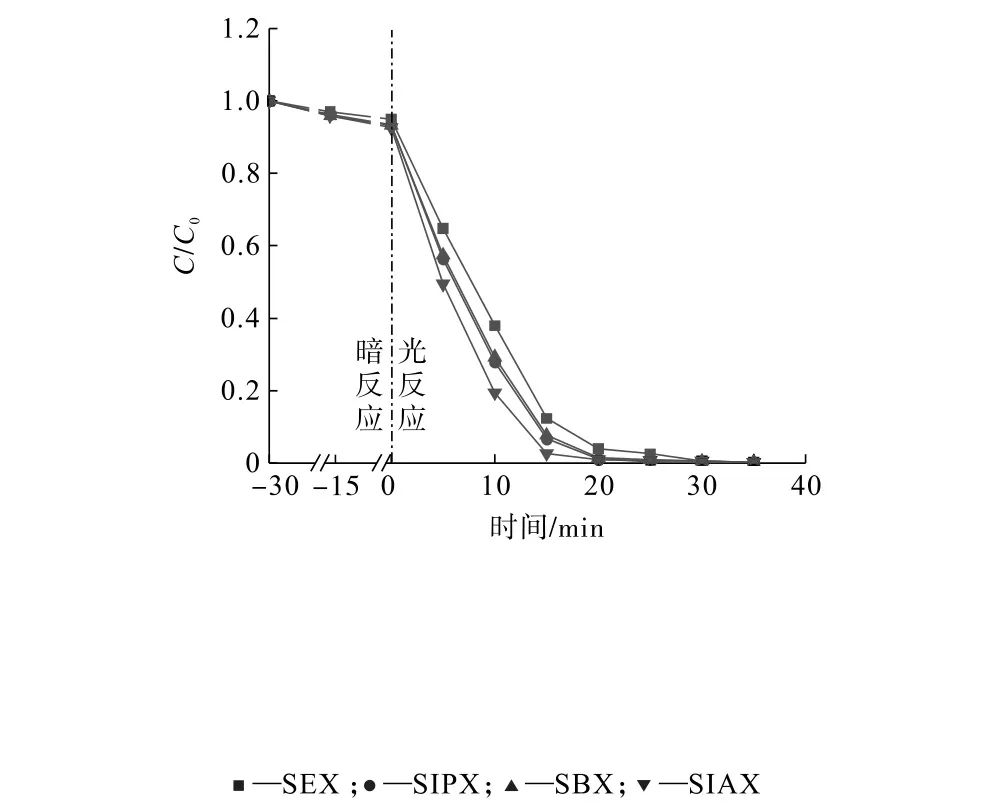
图9 80% TiO 2/MM T复合材料对不同种类黄药的光催化降解效果Fig.9 Influence of photocatalytic degradation of 80% TiO2/MMT composite materials for different kinds of xanthates
由图9可知,4种黄药在30 min内均可以达到99%以上的光催化降解率,表明该复合材料可以有效降解多种类型的黄药,具有较强的适用性。值得注意的是,烃基中含有支链的黄药相对于不含支链的黄药更容易被降解,这与传统认知中带有支链的黄药本身化学稳定性更差有关。同时,随着黄药分子量的增加,复合材料对其光催化降解速率也整体呈上升趋势,这是由于复杂的分子链结构会对黄药分子的极性产生影响,使其更容易被吸附在光催化剂表面并与催化位点相结合,从而更容易被降解[14]。
2.2.5 光催化剂的重复利用性
光催化剂的重复利用性能直接体现材料的长期稳定性,并为实际黄药废水的降解提供有效支撑。本试验在50 mL浓度为20 mg/L的SBX模拟废液中进行,80% TiO2/MMT复合材料的用量为0.2 g/L,在光照30 min后测量SBX的降解率,而后采用离心方式对光催化剂进行回收,再用无水乙醇洗涤—离心3次,待其在60℃下烘干6 h后即可用于下一次试验,光重复利用性试验结果如图10所示。

图10 80% TiO 2/MM T复合材料光催化降解SBX的重复利用性Fig.10 Reproducibility of 80% TiO2/MMT composite materials after photocatalytic degradation of SBX
由图10可知,随着重复利用次数的增加,该复合材料在光照30min后对SBX的降解率仅有轻微的下降。特别是在重复使用4次后,SBX的降解率仍然可达97.33%,表明该复合材料具备极好的稳定性和重复利用性。
2.3 光催化降解SBX机理分析
2.3.1 自由基猝灭试验
通过设计自由基淬灭试验,探究了SBX在光催化降解过程中起主要作用的活性自由基种类。试验在50 mL浓度为20 mg/L的SBX模拟废水中进行,80% TiO2/MMT光催化剂用量为0.2 g/L,通过添加IPA、AgNO3、EDTA-2Na和BQ来分别捕获催化过程中的羟基自由基(·OH)、光生电子(e-)、光生空穴(h+)和超氧自由基(·O2-),从而确定有效的活性自由基。光催化反应30 min后,80% TiO2/MMT复合材料在不同捕获剂条件下对SBX的降解效果如图11所示。
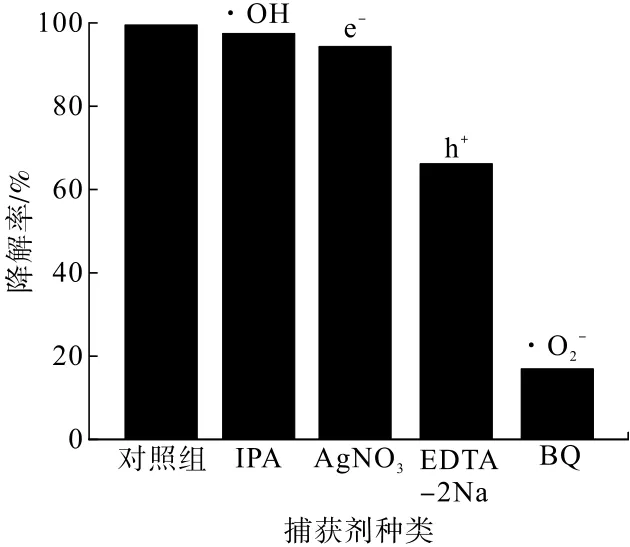
图11 80% TiO 2/MMT复合材料在不同捕获剂条件下对SBX的降解效果Fig.11 Degradation effect of 80% TiO 2/MM T composites to SBX under different capture agents
由图11可知,未添加捕获剂的空白组降解率高达99.52%;当光催化体系中加入IPA和AgNO3后,SBX的降解率有小幅降低,表明·OH和e-在降解过程中发挥的作用效果较弱;而当光催化体系中加入EDTA-2Na和BQ时,SBX的降解率急剧下降,表明h+和·O2-是主要的反应活性物质,其在降解SBX的过程中起到关键作用,且·O2-的贡献率更大。
2.3.2 SBX降解产物分析
为了揭示80% TiO2/MMT复合材料在紫外光条件下光催化降解SBX后的产物,利用紫外-可见分光光度计对SBX模拟废液进行了实时全波长扫描,结果如图12所示。
由图12可知,在暗反应阶段,模拟废液仅在301 nm和226 nm处出现2个吸光度峰,两者均为SBX的特征吸收峰;在开启紫外光照20 min后,这2处的特征吸收峰均基本消失。同时可以发现,在光催化反应开始之后,模拟废液在348 nm处出现了一个新的吸收峰,表明在光催化过程中生成了过黄药[30-33];但这一特征吸收峰的强度很低,且没有随着光照时间的延长而升高,说明过黄药仅是SBX光催化降解过程的中间产物。随着光照时间的延长,模拟废液中不再出现任何吸收峰,表明SBX及其中间产物均被完全分解为无机物小分子。

图12 SBX模拟废液的实时吸光度曲线Fig.12 Real-time absorbance curves of SBX simulated wastewater
为了探究黄药中S元素的去向,向光催化反应30 min后的模拟废液中滴入BaCl4水溶液,结果发现模拟废液中出现轻微的浑浊,表明降解后的模拟废液中可能存在SO42-。综合分析自由基猝灭试验和模拟废液的全波长扫描结果,推测80% TiO2/MMT复合材料在紫外光条件下降解SBX可能的反应式如下[14]:
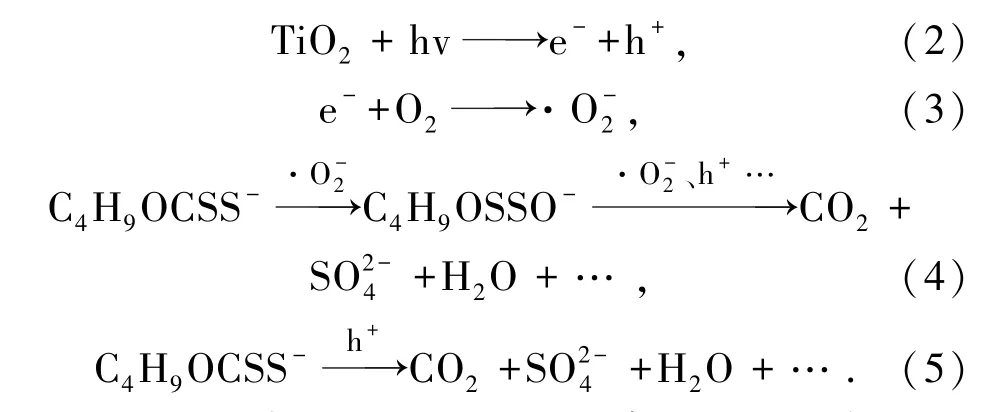
图13形象展示了SBX的降解过程,当80% TiO2/MMT复合材料处于紫外光条件下时,材料价带顶的电子受激发而跃迁至导带底,从而产生电子/空穴对。其中,光生电子的电势较低,可以捕获光催化剂表面的O2分子而生成·O2-自由基,部分SBX分子在·O2-的作用下氧化生成过黄药,随后又立即在其他活性基的氧化作用下被继续分解。与此同时,h+也可以直接与SBX分子进行反应,使其矿化为CO2和SO42-等对环境友好的小分子无机物,最终达到净化黄药废液的目的。

图13 80% TiO2/MMT复合材料在紫外光下对SBX的降解机理Fig.13 Photodegradation mechanism of 80% TiO2/MMT composites to SBX under UV light
3 结 论
(1)采用固相研磨—粉末烧结法可以成功制备出TiO2/MMT复合材料光催化剂。TiO2在MMT表面固定后分散均匀,材料吸收带边轻微红移且紫外光吸收强度更高,提高了光催化剂的回收性和光催化性能。
(2)TiO2负载量、光催化剂用量、SBX初始浓度等因素均会对TiO2/MMT复合材料的光催化降解效果产生影响。在TiO2负载量为80%、光催化剂用量为0.2 g/L、SBX初始浓度为20 mg/L时,紫外光照30 min后即可使SBX完全降解;80% TiO2/MMT复合材料具有极佳的重复使用性能,并在紫外光条件下可有效降解多种类型的黄药。
(3)80% TiO2/MMT复合材料光催化降解SBX的过程中产生了过黄药这一中间产物,最终再被完全氧化分解为无机物小分子。通过自由基猝灭试验发现,·O2-和h+是主要的反应活性物质。
