lncRNA BLACAT1在下咽鳞状细胞癌中介导自噬调控肿瘤细胞的化疗敏感性
2022-05-30迪丽努尔尼加提古丽娜尔吐尔地
迪丽努尔·尼加提,杨 娜,古丽娜尔·吐尔地
(新疆维吾尔自治区人民医院放疗中心,新疆 乌鲁木齐 830000)
下咽鳞状细胞癌(hypopharyngeal squamous cell carcinoma,HSCC)是一种发生于下咽部的侵袭性恶性肿瘤,约占所有头颈部鳞状细胞癌的5%。近年来,由于诊断技术和治疗方式的改进,HSCC患者的生存率有所提高,但由于下咽组织结构特殊,发病部位较为隐匿,多数患者确诊时已处于晚期,并伴肿瘤转移或复发,导致其5年生存率低于50%[1-2]。化疗是HSCC的有效辅助治疗手段;然而,化疗抗性的出现和发展在很大程度上限制了其治疗效果[3]。因此,深入了解HSCC化疗抗性产生的分子机制对于HSCC的诊断、治疗和预后至关重要。
长链非编码RNA(long non-coding RNA,lncRNA)是一种长度超过200个核苷酸且没有蛋白质编码潜力的调控型RNA,在各种基因表达和生物过程中发挥重要调节作用。越来越多的证据表明,lncRNA在包括HSCC在内的癌症发展及转移中起关键作用,且其介导的化疗抗性在大量研究中均有报道。如lncRNA UCA1在口腔鳞状细胞癌的进展中发挥致癌作用,可调控肿瘤细胞的增殖、侵袭和凋亡,其表达降低可增强顺铂(cisplatin,DDP)诱导的细胞凋亡和化疗敏感性[4];lncRNA膀胱癌相关转录因子1(bladder cancer associated transcript 1,BLACAT1)在喉鳞状细胞癌中高表达,可通过促进肿瘤细胞迁移和抑制肿瘤细胞凋亡来触发细胞对化疗药物的耐受性[5]。
lncRNA BLACAT1位于人类染色体1q32.1的基因座上,最初被发现于膀胱癌中,随后研究发现其在胃癌、小细胞肺癌和结直肠癌等多种癌症中过表达,并可促进癌细胞的增殖、迁移及侵袭等恶性行为过程[6-8]。然而,lncRNA BLACAT1在HSCC中的表达、功能以及对化疗敏感性的作用尚不清楚。因此,本研究拟探讨lncRNA BLACAT1在HSCC组织中的表达及其对肿瘤细胞DDP敏感性的影响,初步探究可能的作用机制,旨在为HSCC的靶向诊治提供新思路。
1 资料与方法
1.1 临床资料
选取2018年6月至2020年12月在我院耳鼻咽喉科就诊且接受HSCC肿瘤手术切除的患者40例,其中男33例,女7例;年龄35~68岁,平均(54.22±5.71)岁。收集术中切除的HSCC肿瘤组织标本及对应癌旁正常黏膜组织(癌旁组织,距离肿瘤外缘2 cm以上),迅速置于液氮中冷冻后移至-80 ℃冰箱保存,所有肿瘤组织标本经病理科2位医师证实为HSCC。患者术前均未行放疗、化疗或免疫治疗等,临床资料完整,本研究经过我院医学伦理委员会审核(KY20180423031),病例标本收集前均告知患者或家属。
1.2 主要材料与试剂
人HSCC细胞株FaDu及DDP耐药细胞株FaDu/DDP(武汉淼灵生物),DDP(美国Sigma公司),胰蛋白酶和DMEM培养液(美国GibcoBRL公司),反转录试剂盒和荧光定量测定试剂盒(大连Takara公司),TRIzol试剂和LipofectAMINE 3000转染试剂盒(美国Invitrogen公司),CCK-8试剂盒和Annexin V-FITC/PI试剂盒(日本同仁化学公司),免疫荧光染色试剂盒(北京索莱宝生物公司),BCA蛋白测定试剂盒和ECL发光液(上海碧云天生物研究所),兔抗人LC3B多克隆抗体、兔抗人Beclin-1多克隆抗体、兔抗人p62多克隆抗体、FITC偶联的山羊抗兔、辣根过氧化物酶(horseradish peroxidase,HRP)标记的山羊抗兔或山羊抗鼠以及兔抗人GAPDH多克隆抗体(英国Abcam公司)。引物序列及siRNA序列由上海吉凯基因化学技术有限公司合成。
1.3 RNA提取及qRT-PCR检测
应用TRIzol法分别提取HSCC组织、癌旁组织、FaDu细胞和FaDu/DDP细胞的总RNA,NanoVueTM Plus光度计检测RNA的纯度和浓度,取合格的RNA样品(A260/A280为1.8~2.1)进行逆转录,按照试剂盒说明书合成cDNA,再以cDNA为模板,使用SYBR®Premix Ex TaqTMⅡ试剂盒进行qRT-PCR扩增。扩增条件为:95 ℃ 5 min,循环1次;95 ℃ 30 s、60 ℃ 30 s、58 ℃ 30 s,循环40次。采用比较循环阈值2-ΔΔCt计算基因的相对表达水平,以GAPDH为内参,各组设置3个复孔。引物序列如下:lncRNA BLACAT1上游5’-TGACGTCTTACTACACCCATCCT-3’,下游5’-CTGCCACCTATAGGAAATGCG-3’;GAPDH上游5’-TGTGA-AGGTCGGTGTGAAC-3’,下游5’-CAGATGGTGATGGG-CTGCC-3’。
1.4 CCK-8检测细胞存活率
取生长状态良好的FaDu细胞和FaDu/DDP细胞,按照1×104/孔的密度单层接种于96孔板,于37 ℃、5% CO2的孵育器中培养24 h后,分别加入不同浓度(3.125、6.25、12.5、25、50、100 μmol/L)的DDP进行处理,每个浓度设置5个复孔,培养48 h后,每孔加入10 μL CCK-8试剂液混匀继续培养4 h,采用全自动酶标仪在450 nm处检测各孔细胞光密度(OD)值,计算细胞存活率。细胞存活率=(实验OD值-背景OD值)/(未经处理OD值-背景OD值)×100%。
1.5 细胞转染、分组与DDP处理
转染前24 h,取状态良好的FaDu/DDP细胞按照1×104/孔的密度单层接种于24孔板,置于37 ℃、5% CO2的孵育器中培养。采用LipofectAMINE 3000转染siRNA序列至FaDu/DDP细胞,其中对照组FaDu/DDP细胞正常培养;si-NC组FaDu/DDP细胞转染siRNA阴性对照;si-BLACAT1组FaDu/DDP细胞转染siRNA-BLACAT1。转染后收集细胞,qRT-PCR测定各组细胞内lncRNA BLACAT1 mRNA表达量,以确定转染是否成功。
使用不同浓度(3.125、6.25、12.5、25、50、100 μmol/L)的DDP处理各转染组FaDu/DDP细胞,其中DDP组FaDu/DDP细胞仅加入不同浓度DDP处理,si-NC+DDP组FaDu/DDP细胞转染siRNA阴性对照后加入不同浓度DDP处理;si-BLACAT1+DDP组FaDu/DDP细胞转染siRNA-BLACAT1后加入不同浓度DDP处理。培养48 h后,CCK-8检测细胞存活率,非线性回归计算si-BLACAT1+DDP组的IC50值。
1.6 流式细胞术检测细胞凋亡情况
收集转染后经DDP处理的各组FaDu/DDP细胞,胰酶消化,重悬于500 μL结合缓冲液中,接着在细胞悬浮液中依次加入5 μL Annexin V-FITC和10 μL PI双染色剂,混匀后室温避光孵育15 min,流式细胞仪测定细胞凋亡情况。
1.7 自噬结构分析
PBS洗涤各组FaDu/DDP细胞,加入含4%多聚甲醛和0.2%戊二醛的PBS固定,再用1%四氧化锇固定,采用乙醇和丙酮进行分级脱水,包埋后切成超薄切片,采用3%柠檬酸铅—醋酸双氧铀染色,铜网烤干,透射电子显微镜下成像,观察细胞自噬情况。
1.8 免疫荧光染色观察自噬斑点
各组FaDu/DDP细胞进行爬片,PBS洗涤后,4%多聚甲醛固定20 min,配制0.3% Triton X-100溶液并加入细胞中透化处理10 min,再用山羊血清封闭10 min,于4 ℃下加入兔抗人LC3B多克隆抗体(1∶200)反应过夜;次日PBS洗涤,添加FITC偶联的山羊抗兔二抗(1∶500)室温避光反应1 h,再以DAPI复染5 min,封片。在共聚焦激光荧光显微镜下计数细胞内LC3B荧光斑点数。
1.9 Western blot检测相关蛋白表达
收集各组FaDu/DDP细胞,采用RIPA裂解细胞,离心收集蛋白样品,BCA法测定蛋白浓度。制备10% SDS-PAGE,按照每个泳道40 μg蛋白的量上样,进行电泳分离,电转移至PVDF膜上;TBST洗涤后置于5%山羊血清中室温封闭2 h,弃去封闭液,TBST洗涤,加入一抗(LC3-Ⅰ、LC3-Ⅱ、Beclin-1和p62),均按照1∶1 000稀释,4 ℃下孵育过夜。次日TBST洗膜后,与对应HRP标记的二抗(1∶5 000)室温共同孵育2 h,结束后取膜,TBST再次洗涤,ECL试剂液显影,Image J软件分析各蛋白条带灰度值,以GAPDH为内参蛋白,计算各蛋白表达量。
1.10 统计学分析

2 结果
2.1 HSCC组织及癌旁组织中lncRNA BLACAT1的表达
qRT-PCR检测结果显示,HSCC组织中lncRNA BLACAT1 mRNA相对表达量显著高于癌旁组织(P<0.01),见图1。

**:与癌旁组织比较,P<0.01
2.2 FaDu细胞及FaDu/DDP细胞中lncRNA BLACAT1的表达
qRT-PCR检测结果显示,与FaDu细胞比较,FaDu/DDP细胞中lncRNA BLACAT1 mRNA相对表达量较高(P<0.05),见图2。

*:与FaDu细胞比较,P<0.05
2.3 抑制lncRNA BLACAT1对DDP处理后FaDu/DDP细胞活性的影响
qRT-PCR检测结果显示,si-BLACAT1组细胞lncRNA BLACAT1 mRNA相对表达量低于对照组和si-NC组(P<0.05),见图3a。CCK-8检测结果显示,经不同浓度DDP处理后FaDu细胞和FaDu/DDP细胞存活率均呈下降趋势,当DDP作用浓度在6.25 μmol/L及以上时,FaDu/DDP细胞存活率高于FaDu细胞(P<0.05),见图3b。经3.125 μmol/L及以上浓度DDP处理后,si-BLACAT1+DDP组细胞存活率低于DDP组和si-NC+DDP组(P<0.05),见图3c。si-BLACAT1+DDP组细胞对DDP的IC50值为24.29 μmol/L,因此后续选择25 μmol/L浓度作为DDP的处理浓度。

a:转染后各组FaDu/DDP细胞中lncRNA BLACAT1 mRNA的表达;b:不同浓度DDP处理后FaDu/DDP细胞存活率;c:不同浓度DDP处理后各转染组FaDu/DDP细胞存活率 *:与对照组比较,P<0.05;#:与si-NC组比较,P<0.05;△:与FaDu细胞比较,P<0.05;▲:与DDP组比较,P<0.05;&:与si-NC+DDP组比较,P<0.05
2.4 抑制lncRNA BLACAT1对DDP处理后FaDu/DDP细胞凋亡的影响
流式细胞术结果显示,与对照组比较,DDP组和si-NC+DDP组FaDu/DDP细胞凋亡率升高(P<0.05);与DDP组和si-NC+DDP组比较,si-BLACAT1+DDP组细胞凋亡率也升高(P<0.05),见图4。

a:流式细胞术检测FaDu/DDP细胞凋亡水平;b:FaDu/DDP细胞凋亡率 *:与对照组比较,P<0.05;#:与DDP组比较,P<0.05;△:与si-NC+DDP组比较,P<0.05
2.5 抑制lncRNA BLACAT1对DDP处理后FaDu/DDP细胞自噬的影响
透射电子显微镜观察细胞自噬超微结构,结果显示,对照组有一些自噬体和自噬溶酶体形成,DDP组和si-NC+DDP组内自噬溶酶体形成均较多,且DDP组可见自噬体,而si-BLACAT1+DDP组细胞中未观察到自噬体及自噬溶酶体,见图5。免疫荧光染色结果显示,各组细胞均有绿色斑点,DDP组和si-NC+DDP组细胞内LC3B荧光斑点数较对照组增加(P<0.05);si-BLACAT1+DDP组细胞内LC3B荧光斑点数较DDP组和si-NC+DDP组均减少(P<0.05),见图6。说明si-BLACAT1+DDP组细胞自噬受到抑制。Western blot检测结果亦显示,与对照组比较,DDP组和si-NC+DDP组FaDu/DDP细胞中LC3-Ⅱ/LC3-Ⅰ水平上调,Beclin-1蛋白表达量上升,p62蛋白表达量下降(P<0.05);与DDP组和si-NC+DDP组比较,si-BLACAT1+DDP组细胞中LC3-Ⅱ/LC3-Ⅰ水平下调,Beclin-1蛋白表达量下降,p62蛋白表达量上升(P<0.05),见图7。
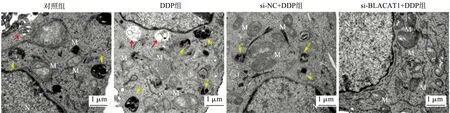
M:线粒体;N:细胞核;红色箭头:自噬体;黄色箭头:自噬溶酶体
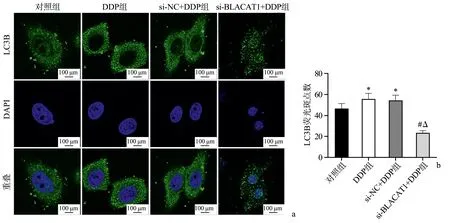
a:免疫荧光染色观察FaDu/DDP细胞中LC3B荧光斑点;b:LC3B荧光斑点数 *:与对照组比较,P<0.05;#:与DDP组比较,P<0.05;△:与si-NC+DDP组比较,P<0.05

a:Western blot检测FaDu/DDP细胞自噬相关蛋白表达;b:FaDu/DDP细胞中LC3-Ⅱ/LC3-Ⅰ水平;c:FaDu/DDP细胞中Beclin-1蛋白相对表达;d:FaDu/DDP细胞中p62蛋白相对表达 1:对照组;2:DDP组;3:si-NC+DDP组;4:si-BLACAT1+DDP组;*:与对照组比较,P<0.05;#:与DDP组比较, P<0.05;△:与si-NC+DDP组比较,P<0.05
3 讨论
HSCC是恶性程度较高的头颈癌之一,近年来其发病率在世界范围内呈升高趋势。虽然有手术切除、化疗和放疗等综合治疗方法,但HSCC患者的预后仍然很差。化疗抗性是导致HSCC治疗失败的重要因素,尽管目前已经进行了大量研究以寻找导致各种肿瘤类型化疗抗性的因素,但关于HSCC化疗抗性的潜在机制仍尚未完全明确。DDP是一种铂类抗癌药物,可用于多种癌症的治疗,但其存在严重的副作用,且患者长期使用DDP会产生化疗抗性,使得该药物的临床应用受到限制[9]。因此,探究HSCC中DDP抗性获得的分子机制对于提高HSCC患者的治疗效果至关重要。
本研究结果显示,HSCC组织中lncRNA BLACAT1的表达明显高于癌旁组织,提示lncRNA BLACAT1可能参与调控HSCC的相关病理过程。lncRNA在细胞生物学行为中的分子机制极其复杂,以往研究表明,lncRNA BLACAT1在不同癌症组织及细胞中广泛异常表达,并具有一定的调控作用。Li等[10]发现在神经胶质瘤组织及其5个不同细胞系中lncRNA BLACAT1表达均升高,并可通过激活Wnt/β-catenin信号通路促进神经胶质瘤细胞的增殖和侵袭。Xu等[11]发现,lncRNA BLACAT1的高表达与非小细胞肺癌的总生存期和无进展生存期缩短显著相关,沉默lncRNA BLACAT1通过调节上皮间质转化和Wnt/β-catenin信号通路从而抑制非小细胞肺癌细胞增殖、迁移和侵袭。本研究发现,FaDu/DDP细胞中lncRNA BLACAT1表达水平高于FaDu细胞,由此推测,lncRNA BLACAT1可能参与HSCC细胞DDP化疗抗性的产生。以往研究探讨了lncRNA BLACAT1在化疗敏感性方面的作用,结果显示,在阿法替尼耐药的非小细胞肺癌细胞中lncRNA BLACAT1表达升高,下调其表达可以逆转肿瘤细胞对阿法替尼的耐药性[12];lncRNA BLACAT1在奥沙利铂抗性胃癌组织和细胞中的表达均高于奥沙利铂敏感的胃癌组织和细胞,沉默lncRNA BLACAT1可促进体内外奥沙利铂抗性胃癌细胞的凋亡,并抑制肿瘤的生长和转移[13]。本研究在FaDu/DDP细胞中抑制lncRNA BLACAT1表达,并经DDP处理后FaDu/DDP细胞存活率降低,细胞凋亡率升高,提示抑制lncRNA BLACAT1表达可提高HSCC耐药细胞对DDP的敏感性,进一步明确了lncRNA BLACAT1参与肿瘤细胞化疗抗性的产生。
有研究显示,参与肿瘤细胞化疗抗性形成的机制较多,如DNA损伤修复、细胞凋亡抗性、溶酶体膜透化、细胞周期阻滞和自噬等[14-15]。自噬作为一种高度进化的保守过程,几乎发生在所有真核细胞中,并与各种生理和病理过程有关;在该过程中无功能和受损细胞器被降解,以获取能量及完成细胞器的更新,满足细胞的基本代谢需要,自噬介导的强大保护作用使得细胞能够对各种内在或外在刺激作出反应。有研究发现,化疗可促进自噬过程,而抑制自噬可增加化疗诱导的细胞凋亡[16-18]。本研究通过DDP处理FaDu/DDP细胞后发现,细胞内自噬体和自噬溶酶体的形成增加,LC3B荧光斑点数增加,LC3-Ⅱ/LC3-Ⅰ水平上调,Beclin-1蛋白表达量上升,p62蛋白表达量下降;而在抑制lncRNA BLACAT1的表达后,细胞内未观察到自噬体及自噬溶酶体,LC3B荧光斑点数减少,LC3-Ⅱ/LC3-Ⅰ水平下调,Beclin-1蛋白表达量下降,p62蛋白表达量上升,表明抑制lncRNA BLACAT1表达可减少FaDu/DDP细胞自噬,从而促进DDP诱导的FaDu/DDP细胞凋亡。
综上所述,lncRNA BLACAT1在HSCC组织及DDP耐药细胞株FaDu/DDP中高表达,通过外源性抑制lncRNA BLACAT1的表达能够减少自噬,逆转FaDu/DDP细胞对DDP的耐药性,提示lncRNA BLACAT1可作为HSCC化疗的耐药分子标志物。但本研究只对lncRNA BLACAT1影响HSCC化疗敏感性的可能机制进行了初步探索,后续需进一步明确其具体分子机制,完善lncRNA BLACAT1在HSCC中的相关作用,为HSCC的精准化治疗提供有力的实验依据。
