AA-SMAS共聚物陶瓷解胶剂的制备及其性能
2022-05-27余帅杰水中和朱火明
余帅杰, 水中和, 朱火明
(1.武汉理工大学 材料科学与工程学院 硅酸盐建筑材料国家重点实验室, 湖北 武汉 430070; 2.佛山市华轩新材料有限公司, 广东 佛山 528000)
0 引言
在陶瓷工业中一般采用湿法制粉的方法制备陶瓷粉料,湿法制粉需要通过雾化干燥塔将泥浆喷雾干燥成粒状粉料,而喷雾干燥工艺需要耗费大量能源[1].据统计,入塔料浆和出塔粉料的平均含水率分别约为40%和7%,蒸发多余水分耗费的能源约占生产总能耗的1/3左右[2].陶瓷解胶剂也称为减水剂、分散剂等,其主要功能是破坏陶瓷料浆粒子的絮凝结构,使含水率较低的料浆依然具有较好的流动性和较低的粘度,从而降低生产过程中用于干燥的时间和能耗[3].
与传统的无机解胶剂相比,聚羧酸合成的自由度大,与黏土颗粒的吸附牢固,制得的料浆流动性和稳定性更好[4-6].磺酸基团电子密度高、极性强、且不受分散介质pH值影响,可以提高聚羧酸解胶剂的静电斥力作用与适应性[7-9].甲基丙烯磺酸钠(SMAS)是一种常用的磺酸基团单体,张艳丽等[10]以丙烯酸(AA)和甲基丙烯磺酸钠为原料,过氧化物为引发剂,在80 ℃条件下制得了PAA-SMAS陶瓷解胶剂.曹文等[11]以甲基丙烯酸(MAA)和甲基丙烯磺酸钠为原料,过硫酸钠为引发剂,对苯二酚为终止剂,在80 ℃条件下制得PMAA-SMAS陶瓷解胶剂.上述两种解胶剂在陶瓷料浆中具有良好的分散效果,但是上述研究还停留在合成工艺直接对分散性能的关联研究,在共聚物分子结构参数方面关注较少,而且反应所需的合成温度较高.
本文根据自由基聚合理论,以AA和SMAS为原料,过硫酸铵-亚硫酸氢钠为氧化还原体系,同时亚硫酸氢钠也作为链转移剂,在较低温度下制备了陶瓷解胶剂PAA-SMAS,全面考察了共聚物合成工艺条件对共聚物相对分子质量(简称分子量,下同)与分子量分布(PDI)的影响,以及不同分子量和单体配比的共聚物对陶瓷料浆流出时间的影响,并研究了解胶剂用量对料浆流出时间、吸附量和Zeta电位的影响.
1 实验部分
1.1 主要试剂
丙烯酸,平湖石化有限公司,工业级;甲基丙烯磺酸钠,寿光市松川工业助剂有限公司,工业级;过硫酸铵(APS),上海易恩化学技术有限公司,A.R;亚硫酸氢钠(NaHSO3),上海易恩化学技术有限公司,A.R;氯化钾,国药集团化学试剂有限公司,G.R;Pc-67,司马化工(佛山)有限公司;Acumer-9300,罗门哈斯(上海)有限公司;由佛山某陶瓷砖厂提供的陶瓷砖原料;聚丙烯酸钠(PAANa),数均分子量7 200,自制.
1.2 陶瓷解胶剂的合成
称取一定量的NaHSO3和去离子水加入1 000 mL四口烧瓶中,充分搅拌溶解,待温度升至50 ℃时,将配置好的AA、SMAS溶液和APS溶液分别缓慢滴入,其中单体占体系溶液总质量的25%,n(AA)∶n(SMAS)=6∶1,在0.5~1 h内滴完,滴加完毕后保温反应2 h.待反应结束后,自然冷却至40 ℃,然后用30%的NaOH溶液将所制得的样品pH调至7~8.反应式如图1所示.
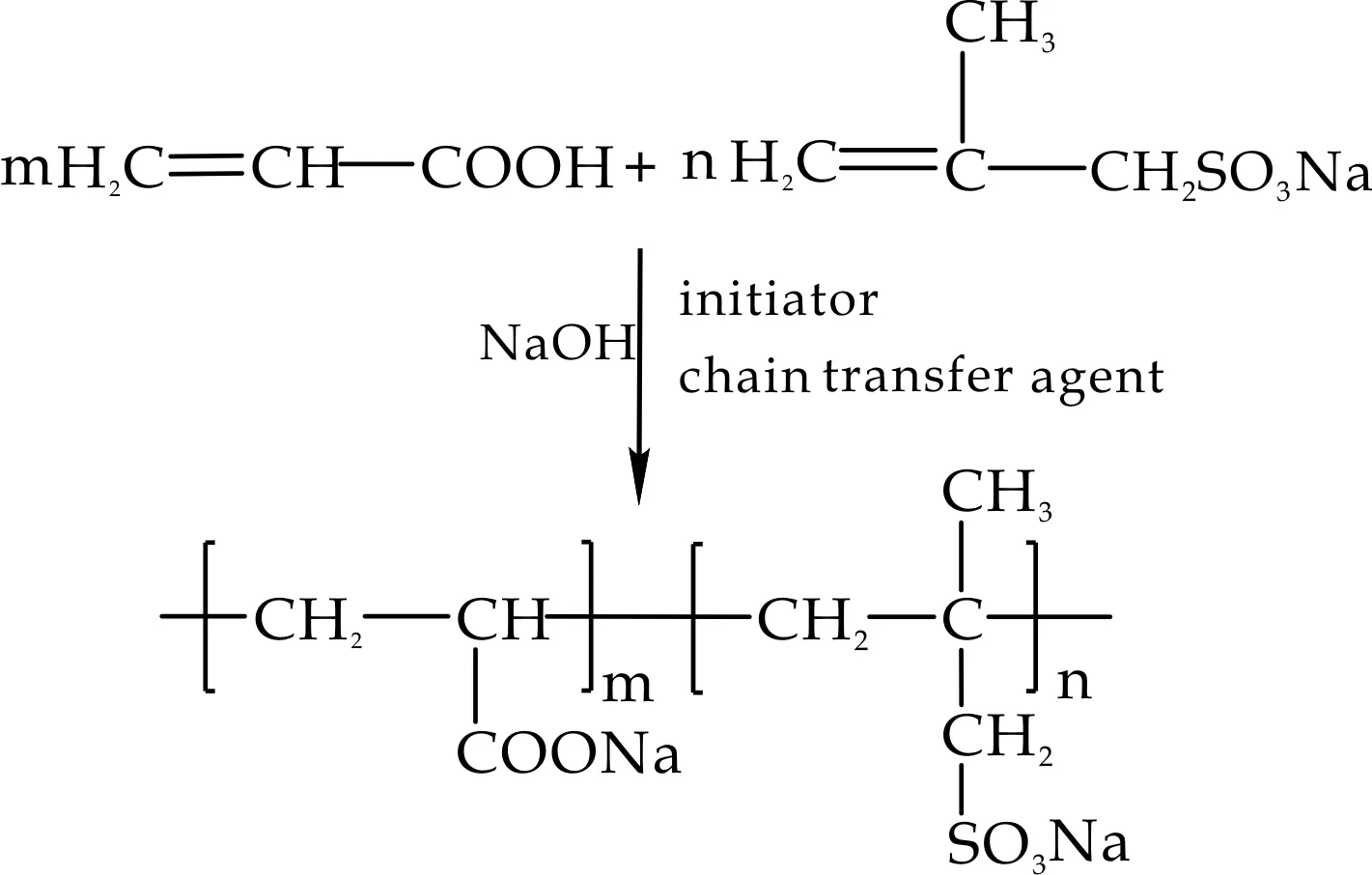
图1 共聚物PAA-SMAS的反应式
1.3 陶瓷料浆的制备
将陶瓷原料置于鼓风干燥箱中,在102 ℃下烘干至恒重,按配方混料均匀,制成混合料.然后将115 g水与0.3%(相对于干陶土质量,下同)的共聚物混合均匀,加入到装有200 g混合料的球磨罐中,采用快速研磨机将料浆研磨均匀.
1.4 检测方法
1.4.1 GPC
采用上海伍丰科学仪器有限公司提供的凝胶渗透色谱仪测定产物的分子量及其分布,流动相: 0.1 mol·L-1KCI溶液,流速:1.0 mL·min-1,标准物质:聚乙二醇,柱温:30 ℃.
1.4.2 FTIR
产物经无水乙醇提纯且干燥后,采用KBr压片法在美国Thermo Scientific公司的Nicolet 6700型傅里叶变换红外光谱仪上采集其红外光谱图.
1.4.31H-NMR
将干燥后的产物溶于D2O溶剂中,采用Bruker公司的AVANCE III型核磁共振波谱仪表征共聚物结构,通过单体和共聚物的特征峰积分面积计算单体转化率[12].
1.4.4 TG-DSC
采用STA449F3型同步热分析仪(德国耐驰仪器公司),N2保护,升温速率10 ℃·min-1,扫描范围40 ℃~600 ℃.
1.4.5 吸附量[13]
将3.0 g细陶土分别加入到30 mL含有7种不同质量浓度的解胶剂溶液(0 g/L、0.2 g/L、0.4 g/L、0.6 g/L、0.8 g/L、1 g/L、2 g/L)中,将悬浮液摇床震荡4 h,静置1 h后用离心机离心2次(每次转速1 000 r·min-1,时间10 min),将离心后的上层清液稀释,采用754PC型紫外可见近红外分光光度计(上海菁华科技仪器有限公司)测定其浓度,依据吸附前后溶液浓度的变化计算吸附量,如式(1)所示:
(1)
式(1)中:Γ为吸附量,mg·g-1;C0为吸附前溶液的浓度,g·L-1;C为吸附后溶液的浓度,g·L-1;Cblank为吸附后空白样品紫外测出的浓度,g·L-1;V为溶液体积,mL;m为细陶土质量,g.
1.4.6 Zeta电位
采用NanoBrook Zeta-PALS(美国brookhaven公司)测定,将1.4.5节中摇床震荡静置后的悬浮液稀释,测定其Zeta电位.
1.4.7 流出时间的测试
将1.3制得的陶瓷料浆装满涂-4型粘度计,静置30 s后测定料浆的流出时间(s).陶瓷料浆流出时间反映了料浆相对粘度的大小,用其来表征料浆的流动性和分散性[14],当料浆的流出时间最短时,料浆的分散达到最佳状态.
2 结果与讨论
2.1 合成条件对共聚物分子量及其分布的影响
2.1.1 链转移剂用量对分子量及其分布的影响
固定其它反应条件不变,考察亚硫酸氢钠用量(以单体质量计,下同)对共聚物分子量及其分布的影响,其结果如图2所示.可以看出,亚硫酸氢钠用量从1%增加到12%,共聚物分子量不断降低,分子量分布变窄.这可能是因为,一方面亚硫酸氢钠起到链转移剂的作用,链转移的结果导致链增长自由基终止,高分子链段变短,聚合物分子量降低.另一方面由于亚硫酸氢钠作为氧化-还原引发体系中的还原剂,亚硫酸氢钠的增加可以与过硫酸铵形成更多的初级自由基,使体系内的活性中心数目增加,分子链段平均长度变短,导致共聚物分子量降低,分子量分布变窄.
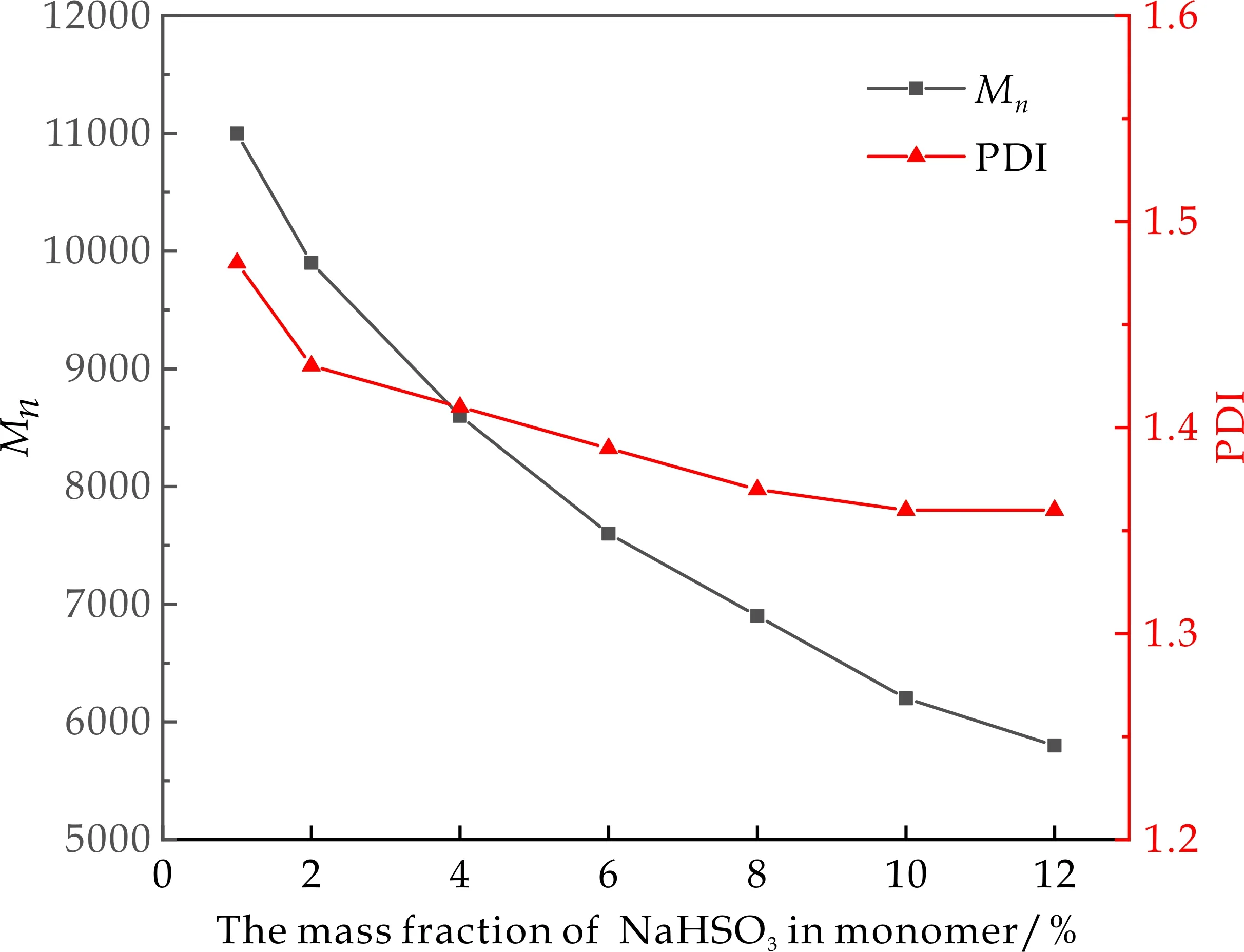
图2 链转移剂用量对分子量及其分布的影响
2.1.2 过硫酸铵用量对分子量及其分布的影响
固定其它反应条件不变,考察过硫酸铵用量对共聚物分子量及其分布的影响,其结果如图3所示.可以看出,过硫酸铵用量在0.2%~2.6%范围内,随着过硫酸铵用量的增加,共聚物分子量及其分布宽度呈现先增加后降低的趋势,当过硫酸铵用量为1.4%时,共聚物分子量达到最大Mn=8 800,PDI=1.39.这可能是因为,刚开始过硫酸铵用量较小,聚合反应速率低,聚合单体反应不充分,分子链段长度差异较小,聚合物分子量及其分布宽度偏低.随着过硫酸铵用量的增加,引发剂分解产生更多的初级自由基,聚合反应速率和单体转化率增大,聚合物分子量及其分布宽度增加;当过硫酸铵用量过大时,产生的自由基过多,体系中形成了大量的小分子链段,导致共聚物分子量及其分布宽度降低.
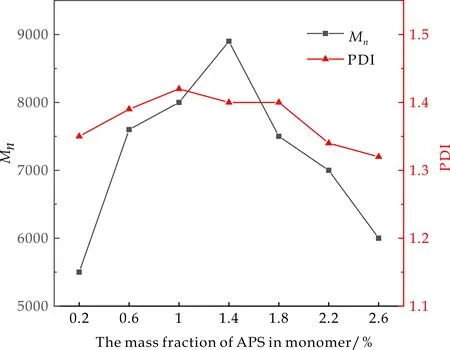
图3 过硫酸铵用量对分子量及其分布的影响
2.1.3 反应温度对分子量及其分布的影响
固定其它反应条件不变,考察温度变化对共聚物分子量及其分布的影响,其结果如图4所示.从图4中可以看出,在40 ℃~80 ℃范围内,随着温度的上升,共聚物分子量先降低后趋于稳定.这可能是因为采用了氧化-还原引发体系,反应活化能低,在较低温度条件下也可引发聚合,所以聚合度较高.随着温度升高,引发剂的分解速率加快,体系内的活性中心数目增加,链转移常数增加,高分子链段的增长受到抑制,共聚物分子量不断下降;当温度继续升高时,引发剂分解速率趋于稳定,共聚物分子量没有显著变化.从图4还可以看出,温度对共聚物分子量分布的影响不明显,共聚物的分子量分布为1.39左右.
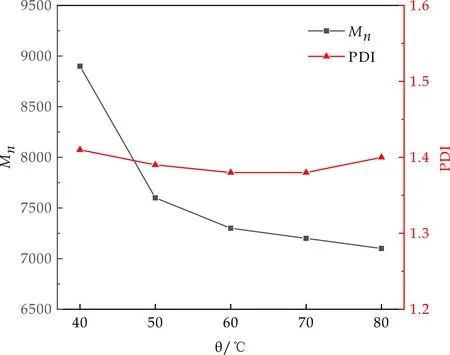
图4 反应温度对分子量及其分布的影响
2.1.4 单体配比对分子量及其分布的影响
固定其它反应条件不变,考察单体配比对共聚物分子量及其分布的影响,其结果如图5所示.可以看出,随着单体配比n(AA)∶n(SMAS)的减小,SMAS单体含量不断增加,共聚物分子量不断降低,分子量分布宽度先增加后降低.这可能是因为,SMAS单体在反应过程中还可以起到链转移剂的作用[15],链自由基与SMAS单体作用,夺取SMAS单体中的氢原子,导致链自由基失去活性而停止增长,从而抑制了高分子链段的增长,所以当SMAS单体含量增加时,聚合物分子量降低,分子量分布变宽,但当SMAS单体含量过多时,链自由基停止在聚合度较低的阶段,导致分子量及其分布宽度同时减小.

图5 单体配比对分子量及其分布的影响
2.2 共聚物的化学分析
2.2.1 FTIR分析
图6为共聚物PAA-SMAS的FTIR.从图6可以看出,在1 640 cm-1处并未观察到明显的C=C双键伸缩振动吸收峰,说明单体已参与自由基共聚合反应.3 423 cm-1处为羧基中-OH的伸缩振动吸收峰;1 566 cm-1,1 410 cm-1处为-COO-的非对称和对称伸缩振动吸收峰;2 943 cm-1处为-CH2-的伸缩振动吸收峰;1 456 cm-1处为-CH-的非对称弯曲振动吸收峰;1 188 cm-1和1 049 cm-1处为磺酸基中-S=O的不对称与对称的伸缩振动峰,且在619 cm-1处存在-S-O-伸缩振动峰.
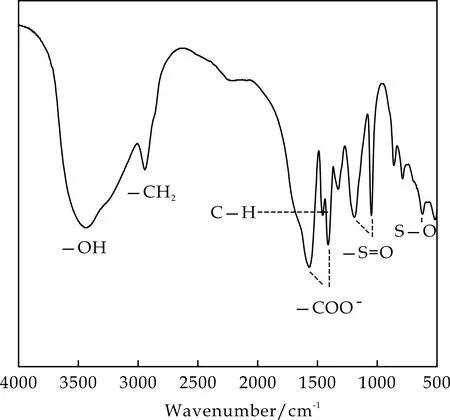
图6 共聚物PAA-SMAS的红外光谱图
2.2.21H-NMR分析
图7为共聚物PAA-SMAS的1H-NMR.从图7可以看出,δ=0.65~1.13为共聚物侧链中-CH3中氢的化学位移,δ=2.78~3.21为共聚物侧链中-CH2-中氢的化学位移,δ=1.21~1.78为共聚物主链中-CH2-中氢的化学位移,δ=1.91~2.29为共聚物主链中-CH-中氢的化学位移,δ=4.79为溶剂D2O的吸收峰,δ=5.01~6.13为未反应单体的双键特征质子峰[16],单体转化率为94.6%.综合1H-NMR和FTIR,确定目标产物已合成.
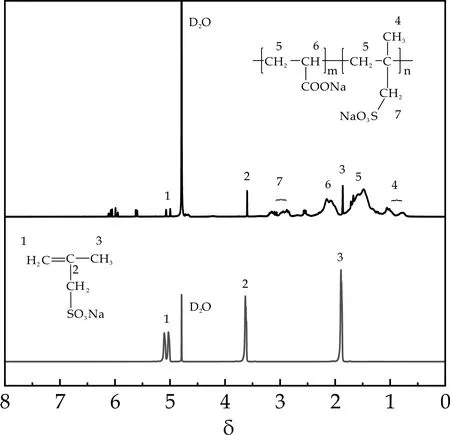
图7 共聚物PAA-SMAS的核磁氢谱图
2.2.3 TG-DSC分析
图8为由不同单体配比合成的共聚物的TG和DSC结果.可以发现,由不同单体配比合成的共聚物失重情况相似,40 ℃~200 ℃阶段失重约为10%,主要是由于水分的蒸发,对应DSC曲线中90 ℃附近的吸热峰.200 ℃~500 ℃阶段的失重量最大,可能与共聚物侧链上的羧基与主链C-C单键分解有关[17],对应DSC曲线中390 ℃和430 ℃附近的吸热峰,500 ℃~600 ℃阶段的失重可能是由于共聚物的进一步分解.
从图8(a)还可知,当n(AA)∶n(SMAS)增加时,共聚物在600 ℃时的残余重量呈现上升趋势,这可能是由于n(AA)∶n(SMAS)增加,分子量增大,而大分子比小分子更加耐热[18].TG-DSC曲线表明共聚物热稳定性较好,可以在较高温条件下使用.
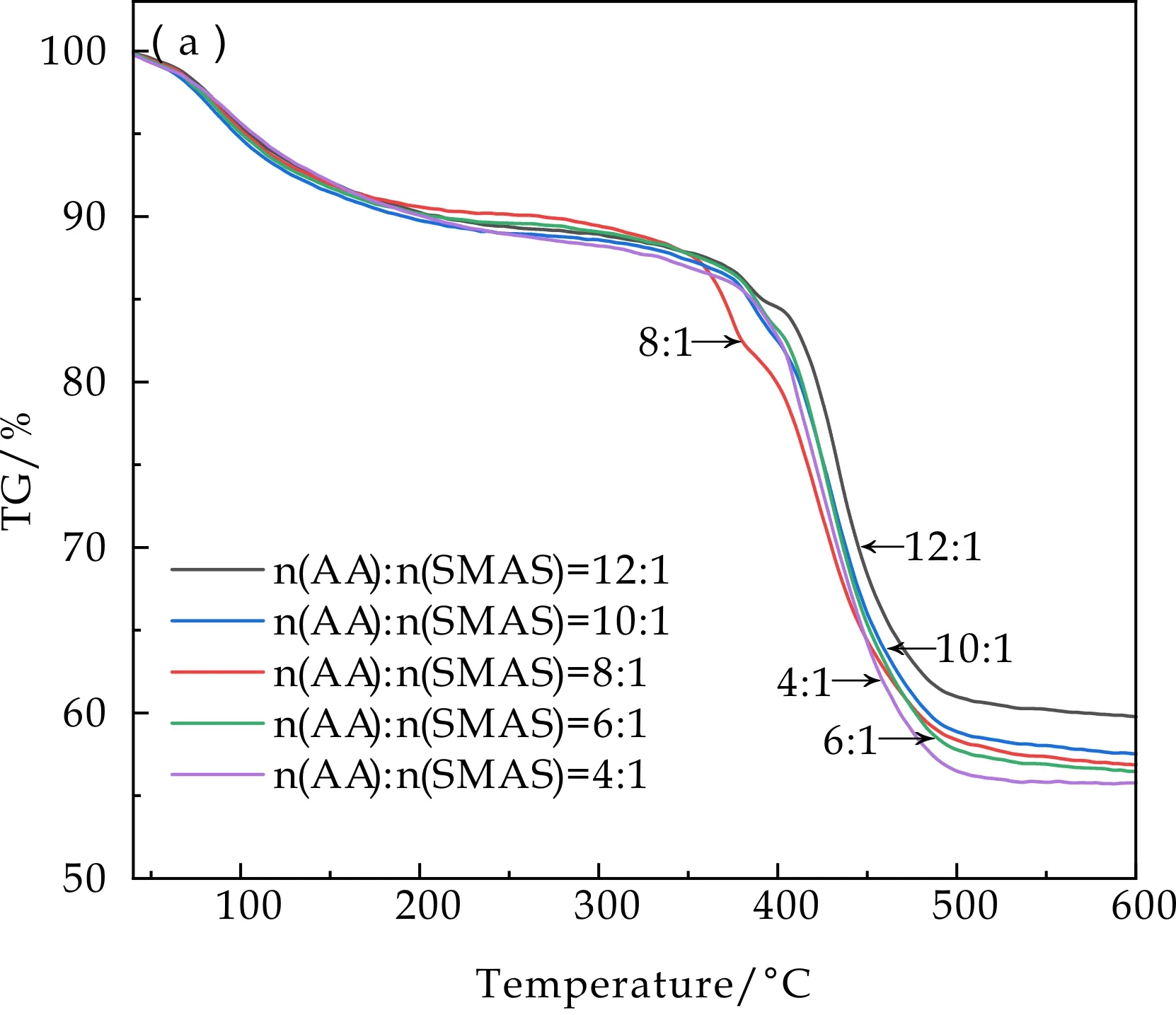
(a)TG曲线
2.3 分子量对陶瓷料浆流出时间的影响
固定单体配比n(AA)∶n(SMAS)=6∶1,选取了4种不同分子量的共聚物,研究了不同分子量的共聚物对陶瓷料浆流出时间的影响,结果如图9所示.可以发现,当共聚物分子量处于6 000~11 000时,随着共聚物分子量的增加,料浆的流出时间先急剧下降后缓慢降低,当共聚物Mn=11 000时,加入0.25%的共聚物,料浆的流出时间为41.5 s,料浆的分散效果达到最好.

图9 分子量对陶瓷料浆流出时间的影响
这可能是因为,小分子量共聚物侧链短,主要通过侧链的-COO-和-SO3-基团以短棒平铺的方式吸附在陶土颗粒表面,吸附量和吸附层厚度小,而且小分子量共聚物每分子带电基团较少,静电斥力作用小,所以料浆流动性差;随着共聚物分子量的增加,共聚物主要以环圈的方式吸附在陶土颗粒表面,吸附量和吸附层厚度更大,空间位阻效应强,而且每分子共聚物含有更多的-COO-和-SO3-基团,静电斥力较强,陶瓷颗粒不容易因相互碰撞而沉降,有利于料浆的分散[19].
2.4 单体配比对陶瓷料浆流出时间的影响
通过改变链转移剂用量,得到分子结构相似的聚合物.聚合物数均分子量在8 300左右,多分散系数在1.41~1.45之间,每种共聚物的分子量分布情况如表1所示.

表1 分子量一定不同单体配比的PAA-SMAS
不同种单体配比的共聚物对陶瓷料浆流出时间的影响如图10所示.可以看出,随着单体配比n(AA)∶n(SMAS)的增加,陶瓷料浆最佳的流出时间先减小后增大.当单体配比n(AA)∶n(SMAS)=8∶1时,共聚物分散效果最佳,加入0.3%的共聚物后陶瓷料浆流出时间为41.7 s.这可能是因为RSO3-与高价阳离子的鳌合比RCOO-弱[20],RCOO-在陶土表面的结合力更强,RCOO-主要起吸附作用[21];而RSO3-的电荷密度高,RSO3-静电斥力作用较强[22].当n(AA)∶n(SMAS)较小时,RCOO-含量低,导致吸附量不足,不利于陶瓷料浆分散,料浆流动性变差.当n(AA)∶n(SMAS)较大时,SMAS单体较少,RSO3-含量不足,静电位阻作用减弱,料浆分散效果不佳.通过图9和图10对比可知,聚合物分子量是影响陶瓷料浆分散效果的重要因素.
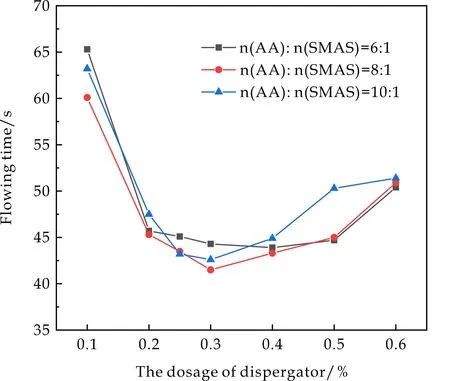
图10 单体配比对陶瓷料浆流出时间的影响
2.5 不同种解胶剂的分散效果对比
图11为PAA-SMAS共聚物解胶剂与市面上常见的陶瓷解胶剂(PAANa、Acumer-9300和Pc-67)的用量对陶瓷料浆流出时间的影响.可以发现,添加PAA-SMAS的陶瓷料浆比添加其他解胶剂的陶瓷料浆具有更短的流出时间,料浆相对粘度更低,分散效果更好.解胶剂用量为0.1%~0.6%时,随着解胶剂用量的增加,陶瓷料浆流出时间先降低后增加,在PAA-SMAS掺量为0.25%时,料浆的流出时间为41.5 s,此时料浆的流出时间最短,料浆的分散达到最佳状态.
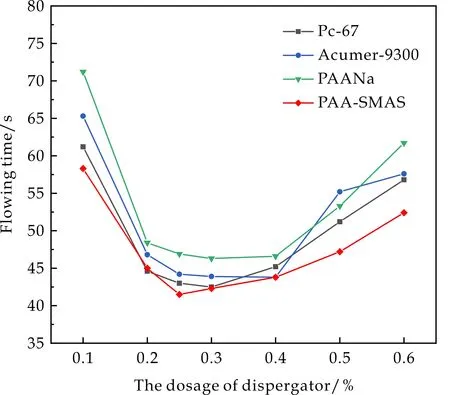
图11 解胶剂用量对陶瓷料浆流出时间的影响
这可能是因为随着解胶剂用量的增加,解胶剂在陶土颗粒表面的吸附量和吸附层厚度增加,静电位阻效应增强,使料浆流动性增加[23];随着解胶剂用量增加,解胶剂在颗粒表面已达到稳定吸附,多余的解胶剂在分散介质中容易形成交联结构而发生絮凝,致使料浆流动性变差[24].
2.6 解胶剂浓度对Zeta电位和吸附量的影响
图12为解胶剂浓度对陶土颗粒表面Zeta电位和吸附量的影响.可以看出,解胶剂浓度从0 g·L-1增加至0.6 g·L-1时,解胶剂在陶土颗粒表面的吸附量从0 mg·g-1增加到2.42 mg·g-1,Zeta电位绝对值从18.44 mv急剧增加至55.46 mv.当解胶剂浓度从0.6 g·L-1增加至2.0 g·L-1,解胶剂在陶土颗粒表面的吸附趋于饱和,Zeta电位绝对值的变化趋于平稳.可能是因为解胶剂吸附在陶土颗粒表面,解胶剂中-COO-和-SO3-基团电离使陶土颗粒表面带上同种电荷,并形成扩散双电子层.随着解胶剂用量的增加,解胶剂在陶土颗粒表面的吸附量增加,形成的双电子层结构逐渐增厚,导致Zeta电位绝对值升高,静电斥力增强.

图12 解胶剂浓度对Zeta电位和吸附量的影响
3 结论
(1)共聚物分子量对料浆分散性能的影响大于单体配比.本文合成了数均分子量为6 000~11 000的共聚物,其中分子量Mn=11 000的共聚物分散效果最佳,此时共聚物PAA-SMAS的合成条件为:n(AA)∶n(SMAS)=6∶1,过硫酸铵用量为0.6%,亚硫酸氢钠用量为1%,反应温度为50 ℃.
(2)当解胶剂用量为0.25%时,其分散效果最佳,料浆的流出时间为41.5 s.与进口的Pc-67和Acumer-9300解胶剂相比,共聚物具有更好的分散效果.
(3)当解胶剂质量浓度为0.6%时,解胶剂在陶土颗粒表面的吸附量从0 mg·g-1增加到2.42 mg·g-1,料浆Zeta电位的绝对值从18.4 mv升高至55.46 mv,当解胶剂质量浓度继续增大时,吸附趋于饱和,Zeta电位绝对值的变化不大.
