固定化硫酸盐还原菌颗粒去除含Cr6+废水的性能研究
2022-05-26王继豪冯秀娟黄哂莅邹彦鋆
王继豪,冯秀娟,2,黄哂莅,邹彦鋆
(1.江西理工大学 江西省环境岩土与工程灾害控制重点实验室,江西 赣州 341000;2.中国矿业大学 矿业工程学院,江苏 徐州 221000)
水中重金属污染问题引起业界和学界的重视,其中Cr6+以强致癌变、致畸变和致突变作用严重危害人类健康[1-2]。硫酸盐还原菌(SRB)是微生物修复中的功能菌之一[3],研究发现,碳源、pH、温度等条件影响SRB活性,而重金属对SRB毒性影响巨大[4-5]。本文用海藻酸钠(SA)进行活性SRB固定化[6-9],羧甲基纤维素(CMC)能增加SA的机械性能[10-12],采用交联-包埋法制成SRB颗粒,探究颗粒对Cr6+的吸附性能,为含铬废水治理提供实验指导。
1 实验部分
1.1 试剂与仪器
普通脱硫弧菌(Desulfovibriovulgaris),购买自中国微生物菌种保藏管理委员会普通微生物中心,菌种编号1.5190;硫酸盐还原菌培养基、羧甲基纤维素钠、海藻酸钠、CaCl2·2H2O、NaCl均为分析纯;GAC经研磨过筛,粒径为100目。
UV752紫外分光光度计;DRP-9162型电热恒温培养箱;DK-S26型电热恒温水浴锅;蔡司Sigma 300扫描电镜(SEM);Thermo Scientific Nicolet 6700傅里叶红外光谱仪(FTIR);Thermo Scientific K-Alpha X射线光电子能谱分析仪(XPS)。
1.2 培养基
采用硫酸盐还原菌专属培养基(postgate培养基)进行菌体培养:K2HPO40.5 g/L,NH4Cl 1 g/L,Na2SO41 g/L,CaCl2·2H2O 0.1 g/L,MgSO4·7H2O 2 g/L,FeSO4·7H2O 0.5 g/L,DL-乳酸钠2 g/L,酵母提取物1 g/L,抗坏血酸0.1 g/L,121 ℃灭菌20 min。
1.3 固定化小球的制备
配制0.5%CMC和2%SA的混合溶液,置于 90 ℃ 的恒温水浴锅内充分溶解,冷却至室温后,加入活性炭和10%SRB悬浊液,搅拌均匀。使用 10 mL 医用注射器将混合物滴入2%CaCl2溶液中交联4 h。取出成型颗粒,用0.9%的生理盐水清洗3遍,4 ℃环境下密闭保存。实验前,在厌氧条件下用postgate培养基激活12 h,使得颗粒内部SRB能够生长富集。
1.4 吸附实验
固定化实验均在电热恒温培养箱中进行,设定温度为37 ℃,固液比10%(M/V)。称量10 g(湿重)固定颗粒于200 mL具塞锥形瓶中,加入100 mL浓度为50 mg/L的Cr6+的废水,CMC浓度0.5%,SA浓度2%,GAC浓度3%。静置反应8 h,取样,根据《水和废水监测分析方法(第四版)》中二苯碳酰二肼分光光度法,于波长540 nm处测定Cr6+的剩余浓度。实验设置3组平行。Cr6+的吸附量按式(1)进行计算。
(1)
式中c0—— Cr6+的初始浓度,mg/L;
c1——Cr6+的剩余浓度,mg/L;
m——固定化SRB颗粒的投加量,g;
V——溶液体积,mL。
实验数据运算处理采用Microsoft Excel 2010,数据作图采用Origin 2018,图形制作采用Adobe Photoshop CS6。
2 结果与讨论
2.1 固定化SRB颗粒条件优化
2.1.1 CMC投加量的影响 CMC投加量对固定化SRB颗粒去除Cr6+的效果见图1。
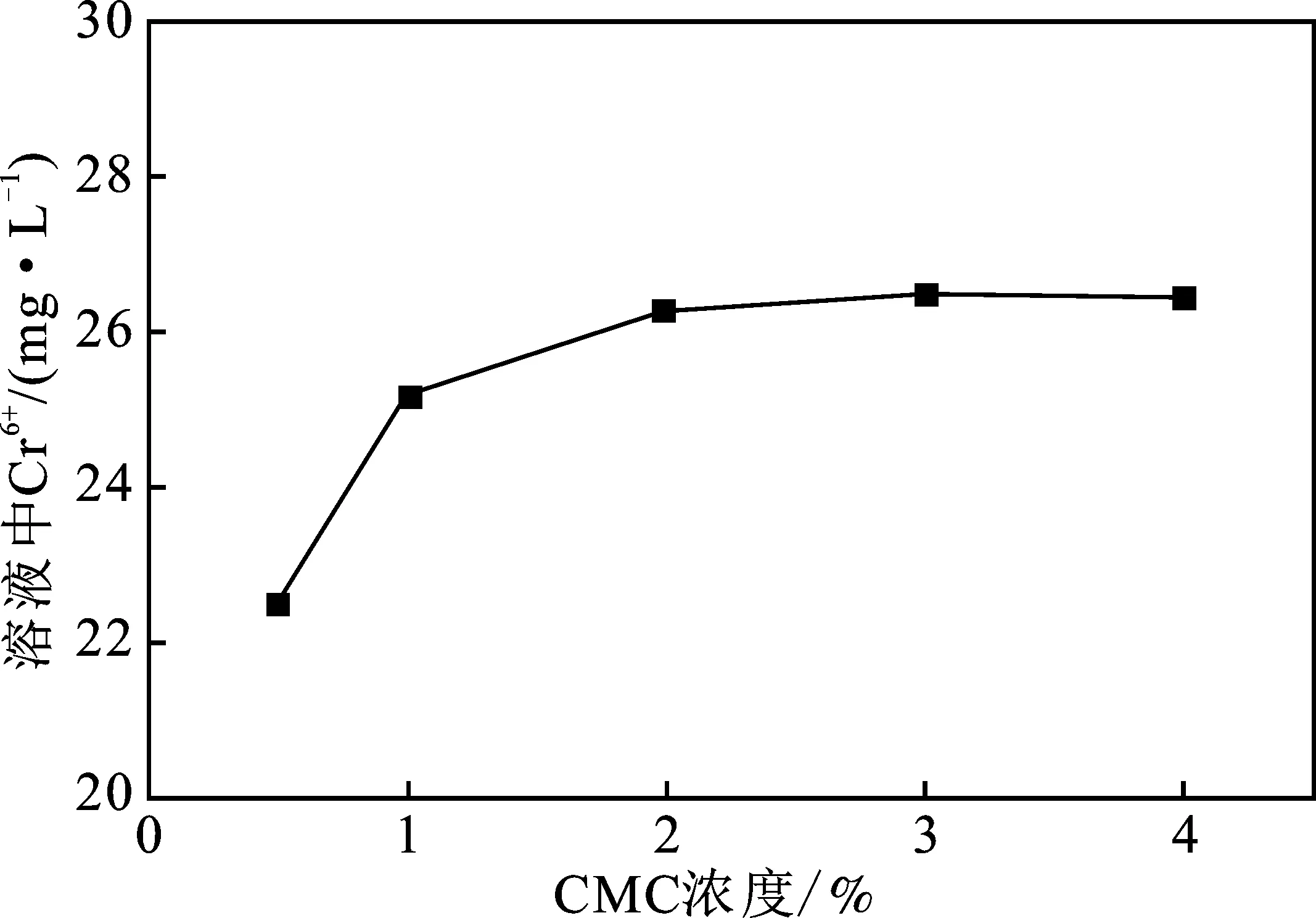
图1 CMC投加量对固定化SRB的性能影响Fig.1 Effect of CMC dosage on the performance of immobilized SRB
由图1可知,随着CMC投加量的增加,溶液中Cr6+的浓度呈现逐渐增大的趋势。其中投加量为0.5%时去除效果最佳,当投加量为2%,3%和4%时,溶液中Cr6+浓度无明显差别。主要为投加CMC能促进SA凝胶乳化和分散[12],形成较大的孔隙密度,有利于SRB附着生长,但是当CMC投加量大于2%时,所形成的SRB凝胶颗粒粘度高,抑制了SRB去除Cr6+的性能。同时,实验过程中发现随着CMC投加量的增加,颗粒拖尾现象严重,形成的颗粒直径较大,在同等质量下,比表面积小,不利于SRB与溶液充分接触。因此,选择0.5%为CMC的最佳投加浓度。
2.1.2 SA投加量的影响 SA投加量对固定化SRB颗粒具有重要影响,单独CMC溶液不能形成颗粒,只有掺杂了SA的胶体滴加入含交联剂CaCl2中溶液中,才能够凝胶成球。SA投加量对固定化SRB颗粒去除Cr6+的效果见图2。
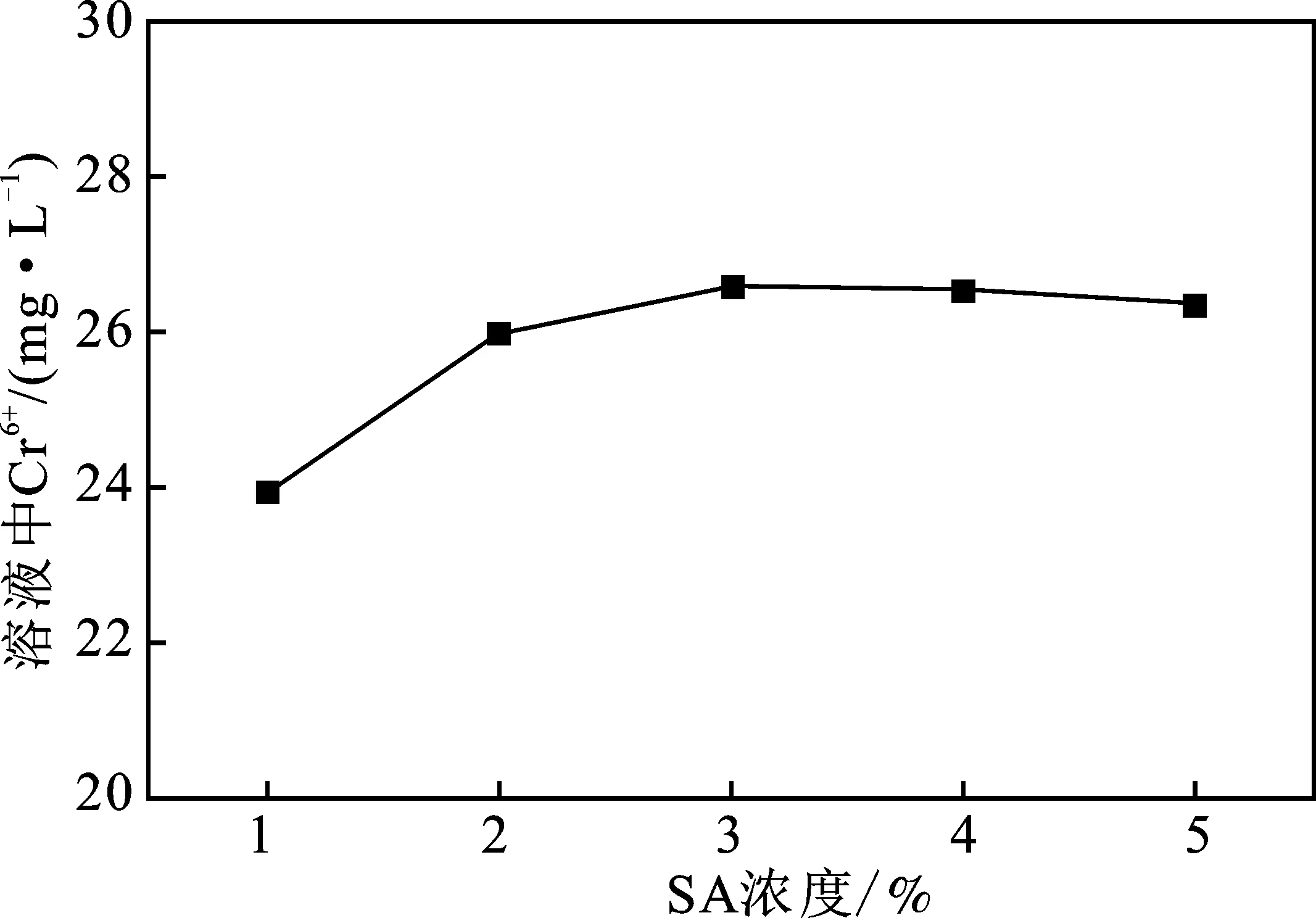
图2 SA投加量对固定化SRB的性能影响Fig.2 Effect of SA dosage on the performance of immobilized SRB
由图2可知,SA投加量为1%时,Cr6+浓度最低,为(23.97±0.23)mg/L。随着SA投加量增加至5%时,由于海藻酸钠含有的羟基和羧基官能团,可以吸附水中部分Cr6+,然而过量添加SA也会导致颗粒机械强度大,影响其内外扩散的传质性能下降。另一方面,戴云飞等发现,过低的SA浓度会导致小球在实验48 h后出现破损,菌体暴露在溶液中[13]。该现象与本实验一致。因此,选择2%为SA的最佳投加量。
2.1.3 GAC投加量的影响 GAC投加量对固定化SRB颗粒去除Cr6+的效果见图3。
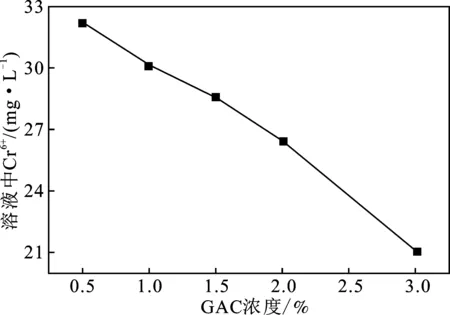
图3 GAC投加量对固定化SRB的性能影响Fig.3 Effect of GAC dosage on the performance of immobilized SRB
由图3可知,随着GAC投加量的增加,Cr6+浓度有一个明显的下降过程。初始Cr6+浓度为 50 mg/L,投加量为3%时,反应8 h后溶液浓度为(21.09±0.23)mg/L,去除率达57.82%。推测为活性炭具有良好的吸附性能和较大的比表面积,能够增强颗粒SRB的去除Cr6+的能力,同时也能快速减少Cr(Ⅵ)浓度,降低对颗粒内SRB的毒性。吴义诚等的实验发现,加入生物炭后,胶球中小球藻细胞密度是对照组的1.42倍[14]。因此,活性炭的空隙结构有利于SRB附着生长,选择3%为GAC的最佳投加量。
2.2 吸附等温线
称取10 g(湿重)固定颗粒于200 mL具塞锥形瓶中,加入100 mL不同浓度梯度的含Cr6+废水,反应2 h,平行取样3次,测定Cr6+的剩余浓度。采用Langmuir和Freundlich方程对数据进行拟合,结果见图4和表1。
其中Langmuir方程式(2)通过ce/qe对ce线性拟合求得参数qm和KL,Freundlich式(3)参数KF和n通过lnqe对lnce线性拟合得到。
(2)
(3)
式中qe——颗粒对Cr6+平衡吸附量,mg/g;
KL——常数,与吸附反应焓有关,L/mg;
ce——溶液Cr6+的平衡浓度,mg/L;
qm——颗粒对Cr6+的最大理论吸附量,mg/g;
KF——方程的吸附系数。
由图4可知,Langmuir、Freundlich拟合结果与实测值都比较贴合,说明该吸附过程既符合Langmuir方程,也符合Freundlich模型[15],而Freundlich模型R2值为0.98大于前者的0.93,说明固定化SRB颗粒属于多分子层吸附,在吸附过程中不仅是SRB对Cr6+的还原作用,也包含GAC的吸附作用。由Langmuir拟合结果可知,颗粒在该条件下的qm达到4.587 mg/g,说明颗粒对Cr6+的吸附效果显著,而Freundlich方程中1/n =0.593,说明颗粒不具备对Cr6+快速吸附的能力,这一结果与实验趋势一致,表明凝胶层对SRB起了保护作用,也削弱了菌体的传质性能。
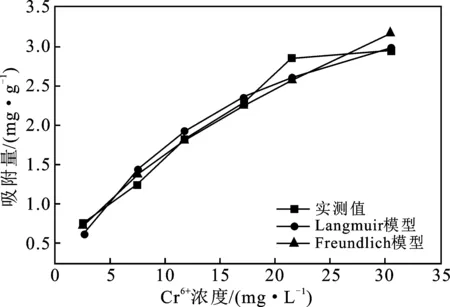
图4 固定化SRB颗粒吸附等温线拟合Fig.4 Adsorption isotherm fitting of immobilized SRB particles

表1 吸附等温线拟合参数Table 1 Adsorption isotherm fitting parameters
2.3 吸附动力学研究
吸附动力学采用拟一级动力学[16]和拟二级动力学[17]来拟合。
拟一级动力学qt=qe-qee-k1t
(4)
(5)
式中qt——t时刻时颗粒的吸附量,mg/g;
qe——平衡时吸附量,mg/g;
k1——拟一级动力学方程的速率常数,min-1;
k2——拟二级动力学方程的速率常数,g/(mg·min)。
称量10 g固定颗粒于200 mL具塞锥形瓶中,加入100 mL浓度为50 mg/L的Cr6+废水,设置培养箱温度为37 ℃,黑暗静置培养,设置3组平行样,于不同时间取样,测定Cr6+的剩余浓度。固定化SRB颗粒对Cr6+的吸附量变化见图5。
由图5可知,在实验开始的20 min内,Cr6+快速被吸附,0~24 h属于快速吸附阶段。随着颗粒表面吸附位点的饱和,Cr6+去除速率逐渐降低,进入慢速吸附阶段,在60 h达到吸附平衡,吸附量占总吸附量的29.6%。
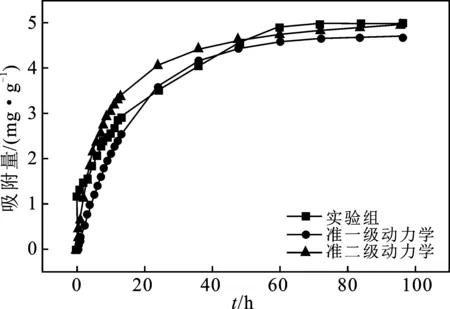
图5 固定化SRB颗粒动力学模型拟合曲线Fig.5 Fitting curve of kinetic model of immobilized SRB particles
分别采用准一级动力学和准二级动力学拟合颗粒吸附Cr6+的过程,结果见表2。

表2 吸附动力学模型拟合参数Table 2 Fitting parameters of adsorption kinetic model
由表2可知,准一级动力学和准二级动力学的R2分别为0.958和0.986,理论平衡吸附量(qe)分别为4.716 mg/g和5.345 mg/g,都十分接近实验平衡吸附量4.995 mg/g。这表明颗粒SRB吸附Cr6+的过程是多种吸附反应的复合效应,以表面化学吸附为主[2],准二级动力学模型更吻合颗粒对Cr6+的吸附动力学机制。
2.4 固定化SRB颗粒反应机理研究
2.4.1 SEM 图6为固定化SRB颗粒外表面和截面结构扫描电镜图。

图6 固定化SRB颗粒SEM分析Fig.6 SEM analysis of immobilize SRB particles
由图6b(颗粒20 μm表面)可知,由于小球经过干燥脱水,颗粒表面存在明显裂纹,凹凸不平较为粗糙。由图6a(5 μm)可知,局部表面布满细小微孔,便于微生物与外界的物质交换,但仍然有一些团聚物呈块状、圆球状分散在颗粒表面;切开截面观察,图6d(20 μm图)中可以看到颗粒内部更加粗糙,分布大大小小的各类形状的孔室和裂纹,这些构成了颗粒内部的物质运输通道和微生物生活空间。由图6c(5 μm)可知,在微生物附着在孔隙中生长,由于制备过程气泡没有完全去除,可以观察到大量规则的气孔。
2.4.2 FTIR 固定化SRB颗粒表面的FTIR见图7。
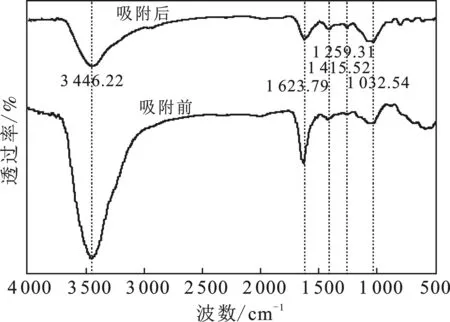
图7 固定化SRB颗粒FTIR分析Fig.7 FTIR analysis of immobilized SRB particles

2.4.3 XPS 为探讨颗粒SRB反应机理,采用XPS对材料进行表征。XPS全谱见图8a,Cr 2p光谱图见图8b。
由图8a可知,各元素信息表明,Cr被成功吸附到材料表面。随着反应的进行,颗粒粒径变小且强度降低,该实验现象与XPS全谱图中峰强减弱一致。Cr 2p3/2 和 Cr 2p1/2 的特征峰分别为 578.0 eV 和587.4 eV,与文献中峰范围一致[19]。结果表明,Cr 2p3/2在578.0 eV处的宽峰被拟合为两个峰,结合能分别为577.7 eV和581.2 eV,在587.4 eV处的Cr 2p1/2也拟合为 586.8 eV 和 589.0 eV 的两个峰,这些峰分别归属于Cr3+和Cr6+。Cr3+与Cr6+占比分别为70.7%和29.3%,该结果表明固定化SRB颗粒在反应中将Cr6+还原为毒性较小的Cr3+。
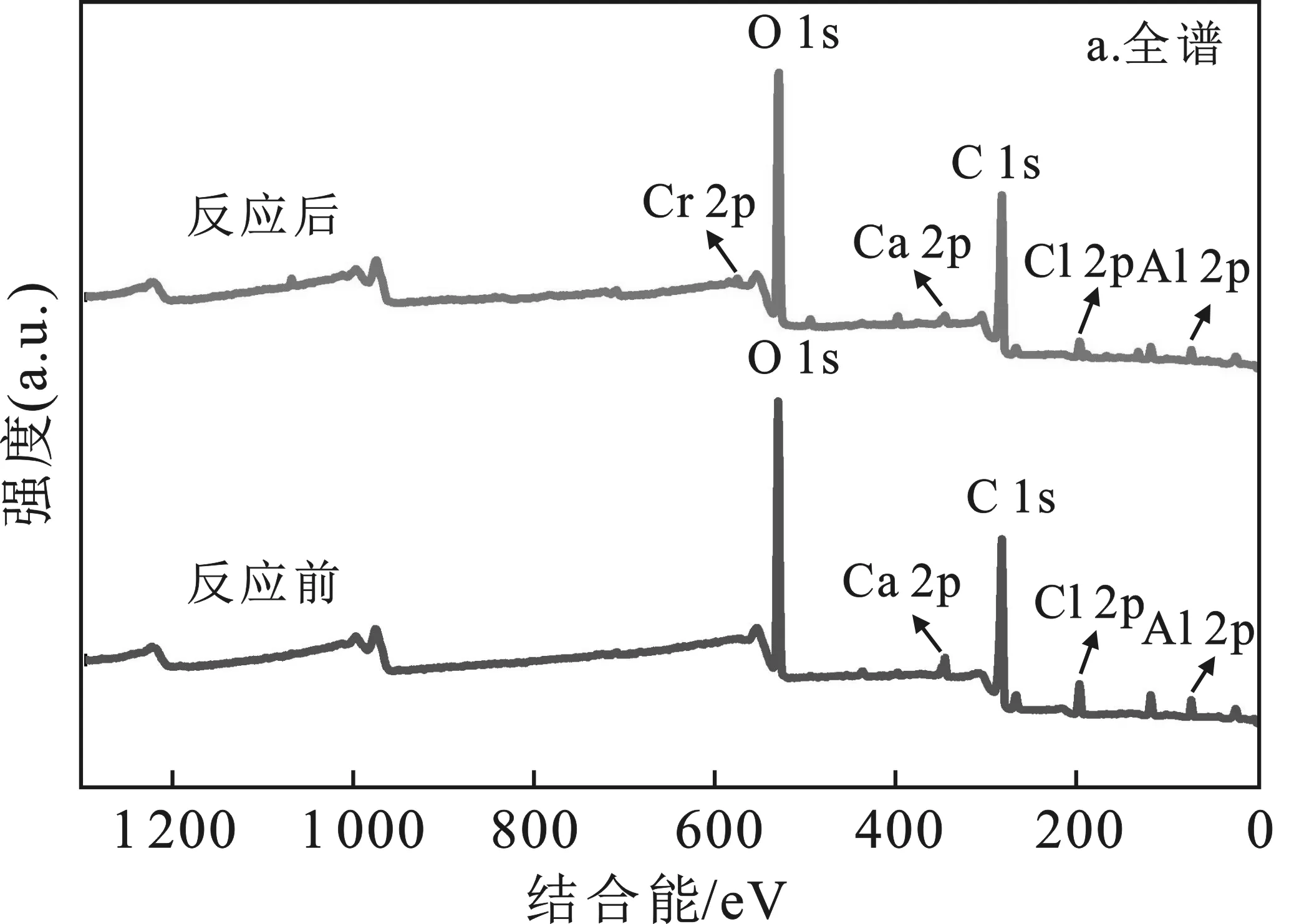
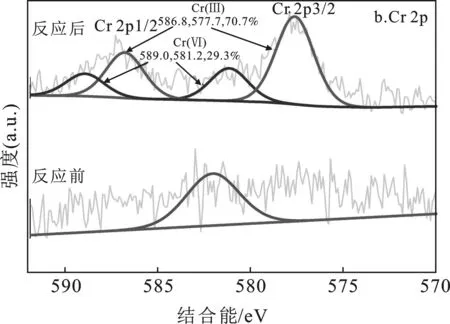
图8 固定化SRB颗粒XPS分析Fig.8 XPS analysis of immobilize SRB particlesa.反应前后XPS全谱图;b.反应前后Cr 2p-XPS光谱图
2.5 吸附-再循环实验
称量10 g(湿重)固定颗粒于200 mL具塞锥形瓶中,加入浓度为50 mg/L的Cr6+溶液,其他反应条件与动力学实验相同,完全反应48 h后将颗粒与液体分离,收集并测定溶液中Cr6+浓度。再重复上述步骤进行连续吸附实验,结果见图9。
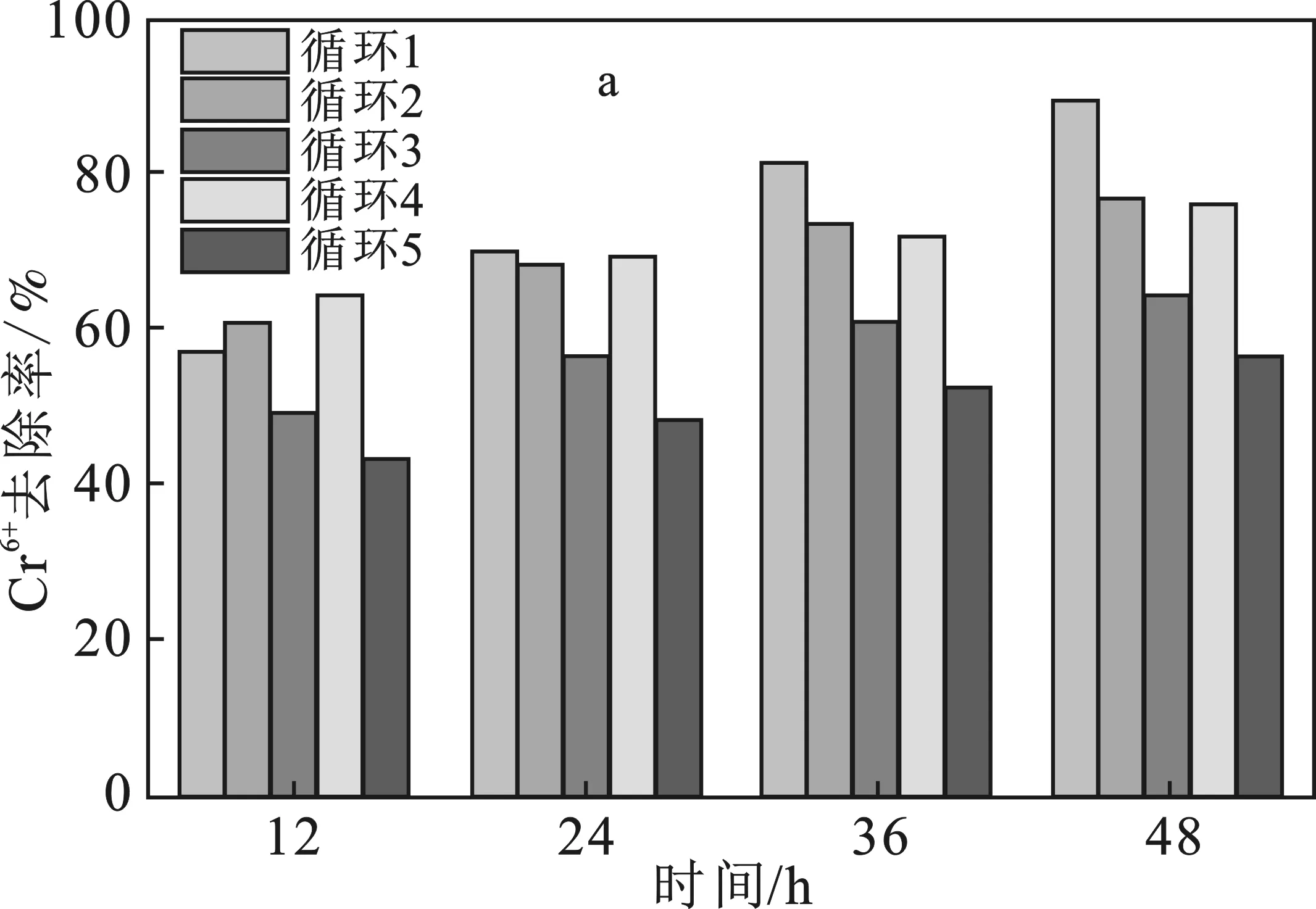
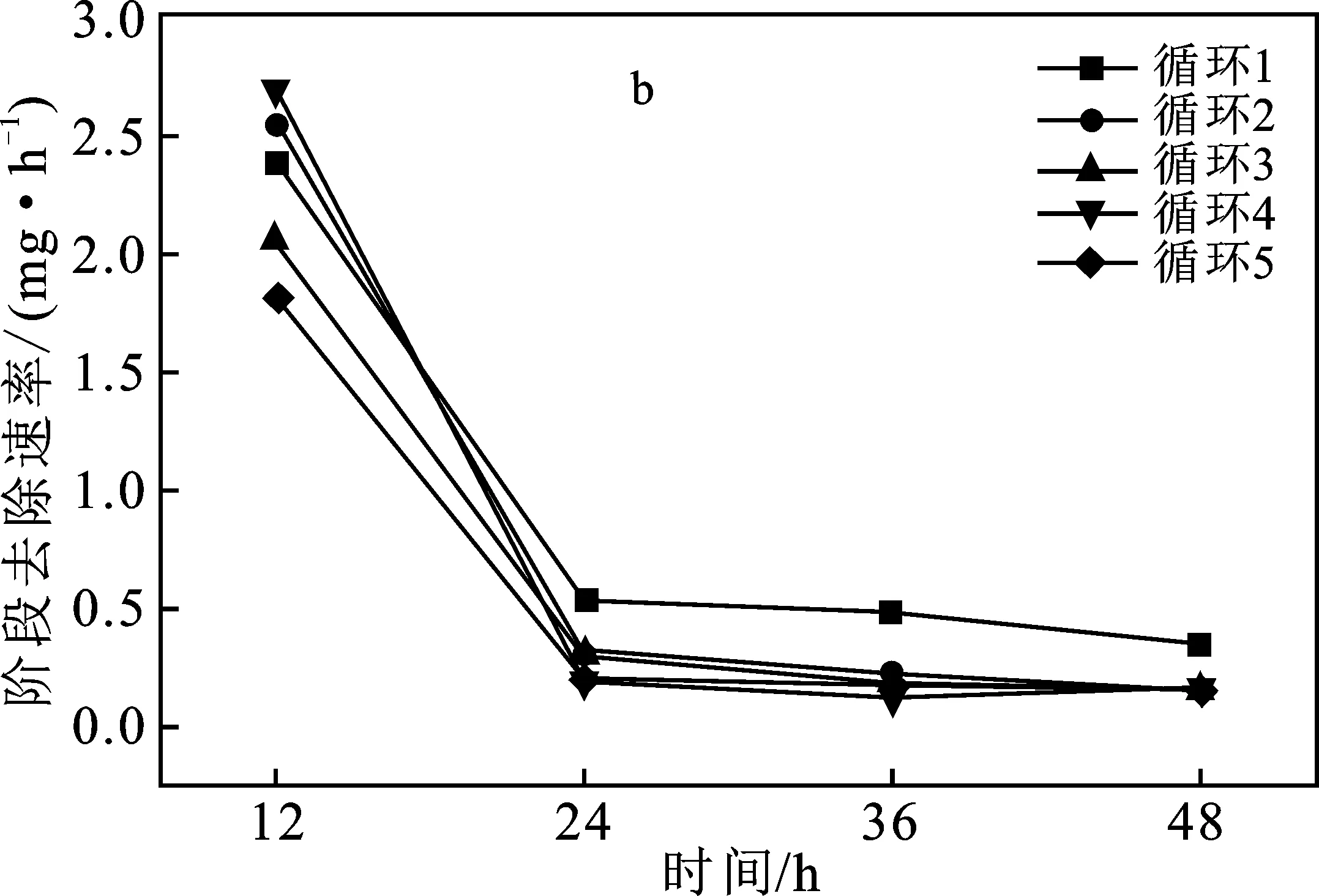
图9 固定化SRB颗粒吸附再循环Fig.9 Adsorption recycling of immobilized SRB particlesa.吸附再循环实验;b.阶段去除速率
由图9a可知,固定化SRB颗粒在第一次循环实验中去除率最高达89.44%,当循环次数不断增加,颗粒对Cr6+的去除率逐渐降低,并且在实验过程中发现颗粒表面凝胶溶解,粒径减小,出现细胞溶出现象。推测由于固定化时间短,导致材料交联程度差,机械强度较低。另外,连续多次的重复使用,也使得颗粒的吸附位点减少,同时,Cr6+被还原成硫化物沉淀包裹在颗粒表面使得颗粒去除效果减弱。由图9b可知,0~12 h阶段,颗粒经过12 h激活后,颗粒性能得到增强,随后出现骤降,该阶段5次循环的平均去除速率为0.31 mg/h,之后24~36 h和36~48 h两个阶段去除速率呈缓慢下降趋势,同时也可以看出5次循环实验中,各阶段的去除速率基本一致,颗粒对Cr6+的去除率仍高达 56.1%,这表明固定化SRB颗粒在处理含铬废水上具有较好的可重复利用率。
3 结论
(1)固定化SRB颗粒的最佳制备条件为:0.5% CMC,2%SA和3%GAC。
(2)固定化SRB颗粒吸附Cr6+符合准二级动力学方程,表明该过程以表面化学吸附为主,多种吸附反应的复合效应。吸附过程与Freundlich模型拟合结果贴合,是多分子层吸附,由于凝胶削弱了颗粒传质作用,颗粒SRB不具备对Cr6+的快速吸附能力。
(3)SEM、FTIR和XPS的表征结果表明,固定化颗粒通过大小不一的孔室对SRB起到保护作用和生长空间,同时颗粒含有多种官能团形成吸附位点,与SRB一同将Cr6+还原成毒性小的Cr3+。
(4)在吸附-再循环实验中,固定化SRB颗粒在5次循环实验后,对Cr6+的去除率仍有56.1%,在实验的各个阶段,去除速率基本保持不变。
