聚羟基烷酸酯缓释微球制备技术研究进展
2022-05-23梅鑫,白雪,张婵
梅 鑫,白 雪,张 婵
(太原科技大学 环境科学与工程学院,太原 030024)
缓释技术是通过某些措施,使药物在特定时间内以一定规律缓慢释放于环境中,并在较长时间内能够维持有效浓度。缓释载药微球是由药物分散于载体材料中或吸附于其表面而形成,常见载体材料可分为天然高分子材料、合成高分子材料和无机高分子材料等类型(表1)。近年来,已有文献报道利用缓释技术制备载农药微球的研究[1]。
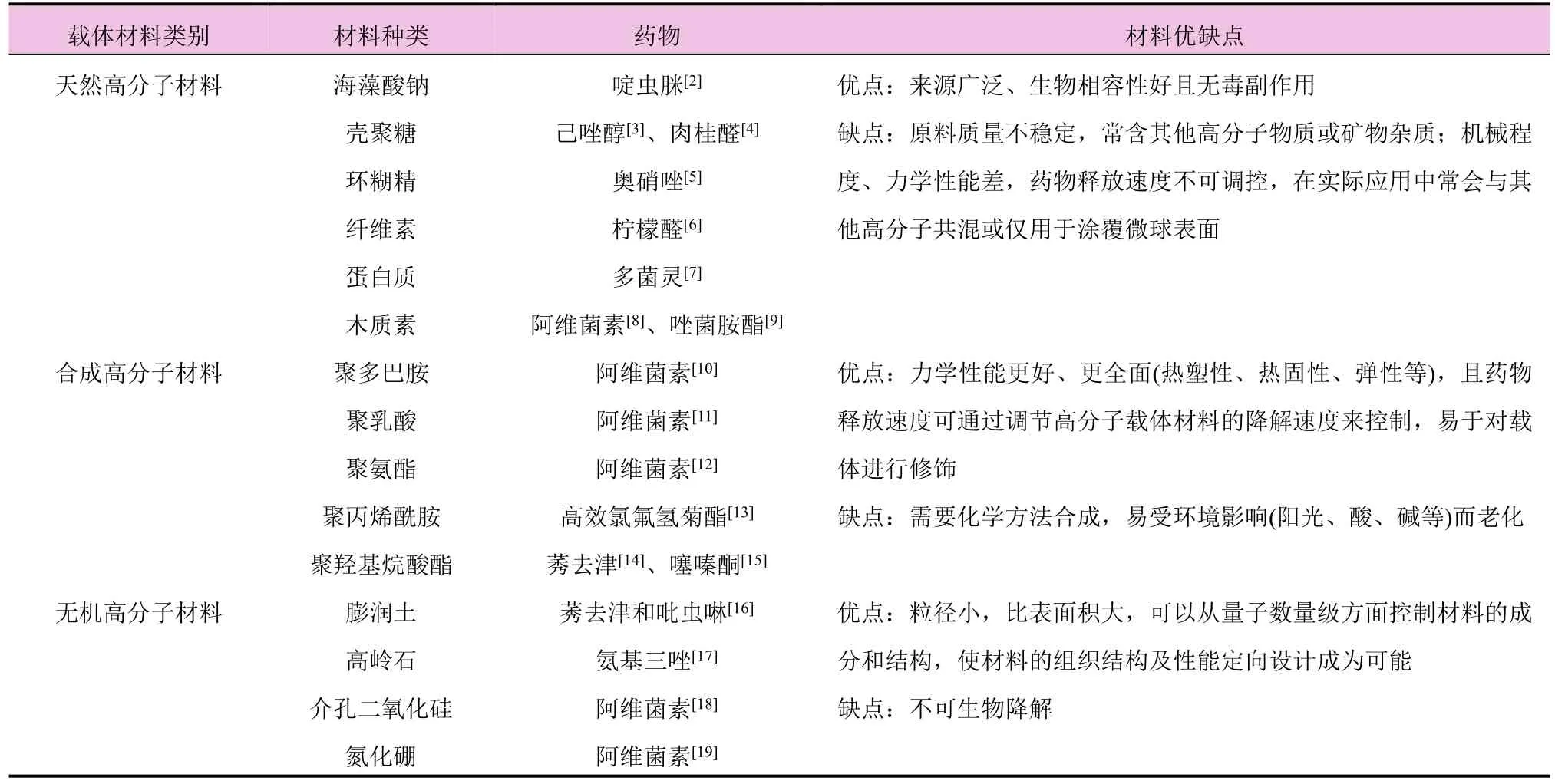
表1 常见载药微球载体材料
与难降解、污染环境的聚氯乙烯、聚乙烯、聚丙烯等[20]载体材料相比,聚羟基烷酸酯(PHAs)是一类由微生物发酵合成的高分子材料,可作为微生物体内的碳源与能源贮藏物[21],能直接被环境中的微生物降解,对环境无污染[22-25]。其具有优良的理化和生物特性,如热塑性、力学机械性能、生物相容性、表面可修饰性和抗紫外性能等。PHAs家族中常见的有聚羟基丁酸[PHB]、羟基丁酸与羟基戊酸共聚物[P(HB-HV)]、羟基丁酸与羟基己酸共聚物[P(HB-HH)]等。本文从PHAs的理化性质、载药微球的制备技术及应用等方面进行了综述,为更多PHAs载药缓释微球剂型的研制提供一定方法和技术参考。
1 PHAs的结构与性质
PHAs是由一个羟基脂肪酸的-COOH与另一个羟基脂肪酸的-OH脱水聚合而成[23],其通用分子结构如图1。依据PHAs单体中碳原子数目,可将其分为短链PHAs (SCL-PHAs)和中长链PHAs (MCL-PHAs C6~C16)。SCL-PHAs单体含有3~5个碳原子,如PHB;MCL-PHAs单体含有6~16个碳原子,如P (HB-HV)、P (HB-HH)等,多为共聚物。从性质角度而言,SCL-PHAs的结晶度较高,其硬度和脆性高于MCL-PHAs,而MCL-PHAs的柔韧性优于SCL-PHAs。此外,PHAs具有良好的生物降解性、生物相容性和表面可修饰性。以上特性均为PHAs用作载体材料奠定了基础。
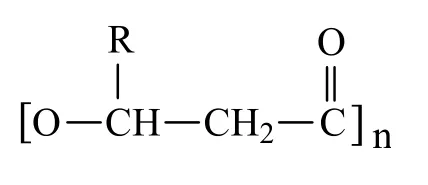
图1 PHAs的通用分子结构
2 PHAs载药缓释微球的制备方法
2.1 溶剂挥发法
溶剂挥发法是制备载药微球最常用的方法之一。采用此方法制备出的纳米粒分散均匀,呈球形,且包封率较高。但其制备过程中需要高速匀浆机,耗能大,仅适用于实验室中小剂量的制备,不利于工业化生产[26]。其一般步骤如下:首先将脂溶性载体材料溶于易挥发有机溶剂形成油相,再缓慢滴加到含乳化剂(分散剂)的水相中,机械搅拌形成乳状液,再低速搅拌从其中去除挥发性有机溶剂而形成微球。该法适用于多种聚合物载体,其制备工艺的影响因素主要包括聚合物理化性质、乳化剂浓度、有机相/水相体积比、搅拌速率等。水溶性的农药适于用油包水的方法,脂溶性的农药更适用于水包油的方法。Grillo等[14]采用油包水的方法制备了载除草剂莠去津的聚羟基丁酸-羟基戊酸酯微球。体外释药结果表明,与未包封的莠去津相比,微球中莠去津通过载体表面孔隙而缓慢释放,具有明显的缓释效果。Monnier[27]以PHBHV、PEG为载体材料,采用w/o/w复乳化溶剂挥发法制备了PHBHV/PEG载肝素微球,通过添加PEG降低了PHBHV载肝素微球中肝素的突释效应,可将其应用于组织再生领域。
2.2 喷雾干燥法
在载药微球的制备过程中,喷雾干燥法是将药物与载体材料溶解在适宜的溶剂中,通过雾化器在短时间内将上述溶剂雾化成粒径小、表面积大的小液滴,再与高温气流接触,液滴中的溶剂瞬间蒸发而固化形成微球。该法产量高,重现性好,广泛应用于制药、食品等领域。Anton等[28]采用纳米喷雾干燥仪制备了PHB载紫杉醇微球,大大延长紫杉醇的体外释药时间至2个月。该剂型可作为长效抗癌药物应用于临床癌症治疗中。
2.3 超临界流体法
超临界流体法的核心是超临界流体,这是一种优良的结晶溶剂,是由物质达到一定临界温度和压力以上形成的流体,兼具气体和液体的优点。超临界流体法用于微球制备的基本原理是将药物或有效成分溶解在适宜溶剂中形成一定浓度的溶液,然后与超临界状态下的介质(常用的为CO2)接触,二者发生快速的相互扩散,溶剂体积膨胀,密度下降,造成溶液对溶质的溶解能力降低,从而在短时间内形成极高的过饱和度,沉淀析出纯度高、粒径均匀的超细颗粒物[29,30]。该方法操作条件温和,对农药有效成分的破坏少,尤其适用于处理脂溶性农药,且CO2是无毒、廉价的溶剂,在使用过程中无毒无污染。但由于CO2是非极性物质,只能萃取极性较低的亲脂性物质及低分子量的脂肪烃,如醇、醚、醛及内酯等物质[31],对于极性较大的亲水性分子、金属离子及相对分子量较大的物质萃取效果不够理想。Machado Jr等[32]以PHBV为载体,二氯甲烷为有机溶剂,采用超临界流体增强分散技术(SEDS)研究了超临界CO2作为抗溶剂对虾青素的包封效果。共沉淀试验表明压力 100 bar时获得了粒径较小(0.128 μm)、包封率较高(48.25 %)的颗粒。Mendonça等[33]用超临界流体法将印楝籽油包埋在PHBV中,得到平均粒径为463 nm的乳状液液滴,液滴稳定时间至少为 90 min。SFE后的平均粒径为 228 nm,PHBV对印楝油的包封率为8.58%~12.79%。
2.4 纳米沉淀法
纳米沉淀法的原理如下:首先将疏水性聚合物高分子载体材料与药物溶于易挥发的有机溶剂中。然后在连续高速搅拌的状态下,将上述有机相滴入水相中,有机溶剂逐步向水相扩散。在此过程中,由于聚合物的疏水性导致其自组装形成载药颗粒。最后通过连续低速搅拌去除易挥发有机溶剂即得载药颗粒[34,35]。该方法本质上类似溶剂挥发法,但局限性在于只能选用疏水性的聚合物,一些性能更优的载体已被排除在外。Bini等[36]以PHB为载体材料,采用纳米沉淀法制备了载姜黄素纳米粒。该纳米粒的粒径分布较窄,平均粒径为216 nm。体外释药度试验结果表明,约80%姜黄素在4 d内从纳米粒中释放,具有较好的缓释性能。
2.5 冷压法
冷压法的过程是将药物与载体粉末置于冷却的容器内,然后装入金属模具,通过挤压得到一定形状的制剂。该方法简单,可大量制作样品,但需要特殊的仪器且需把载体磨成粉末,易破坏载体的结构。Volova等[37]以PHB和尿素粉为原料,采用压力机使用冷压法制备了直径为3 mm的包封肥料尿素的球团。在实验室条件下对多年生匍匐茎草和莴苣进行生长试验,研究表明所制备的尿素配方的使用有利于模型植物的生长,并大大减少了氮的流失。Boyandin等[38]以 PHB、聚乙二醇(PEG)、聚己内酯(PCL)、木粉(wood)为原料,冷压制备了包覆除草剂嗪草酮的控释球团。土壤试验表明:PHB/PEG样品中的嗪草酮释放最快(72%),PHB/wood、PHB/PCL和PHB样品释药速率基本一致,为59%~65%。
3 PHAs载药缓释微球的体外释药机理
PHAs载药缓释微球是众多微球中的一种,其体外释药机理的研究思路符合载药微球释放机制的常规方法。一般来说,载药微球的释放过程如下:⑴ 由于微球表面吸附药物,当微球进入水性介质时,其表面药物溶解在其中,因此药物最初的释放是在微球表面进行;⑵ 微球中药物均匀分散在载体基质中,随着载体材料的不断降解以及浓度差的存在,接近表层的药物被逐渐释放到介质中;⑶ 随着药物的释放,载体材料被大量溶蚀,载体分裂,高分子化合物化学链不断分裂变短最后溶解,大部分药物释放[39]。体外释药过程中,不同时间点累积释药率的比例与所包封的药物性质、载体材料性质以及所形成微球性质均相关。通过研究载药微球的释放机理,可以更好地筛选载体材料,对药物进行控制释放,提高药物的利用率。
Volova等[40]制备了PHB载嗪草酮微球,体外释药20 d时嗪草酮的累积释药率可达80%左右,其体外释药行为是通过聚合物层扩散引起的,符合Fickian扩散定律。Grillo等[41]制备了 PHB、PHBV载莠灭净微球,2种微球中莠灭净在水中的释放主要是由药物本身扩散和聚合物链松弛引起的,因而其释药行为符合non-Fickian扩散定律。本课题组采用溶剂挥发法制备了P (HB-HH)载噻嗪酮缓释微球[15],微球在pH7缓冲液中9 d体外释药率达80%以上,动力学分析表明噻嗪酮的释放表现为non-Fickian扩散方式(0.43<n<0.85),其释放机制是农药扩散和聚合物水解的综合作用。
4 总结与展望
PHAs是一类性质优良的可生物降解载体材料,可用于多种有效成分的包埋,已应用于医药、农业等不同领域。本文综述了 PHAs载药微球的几种制备方法(溶剂挥发法、喷雾干燥法、超临界流体法、纳米沉淀法和冷压法)。上述方法各有利弊,在实际应用中应根据有效成分的性质及缓释要求选择适宜的方法与载体材料。值得注意的是,溶剂挥发法、超临界流体法和纳米沉淀法在PHAs微球制备过程中会使用少量有机溶剂(如二氯甲烷、丙酮等),这些溶剂在挥发过程中会对环境存在一定危害。针对这一问题,活性炭吸附法[42]、吸收剂吸收法[43]等将有机溶剂回收再利用的措施已被证明可减少对大气的污染,但这种方法也仅局限于处理低浓度的有毒气体的源头排放,并且吸收后的有机溶剂和表面活性剂成为废液造成二次污染,会额外增加生产运营成本。为了从根本上解决上述问题,实现工业化生产,今后研究重点应集中于:⑴ 避免使用易挥发有机溶剂,重点开发PHAs良性溶剂;⑵ 目前PHAs剂型多为微球、纳米粒、微囊、悬浮剂等,可开发更多诸如可分散粒剂/片剂、颗粒剂等水基化制剂。
