伴有中/重度食管静脉曲张的慢加急性肝衰竭患者预后危险因素分析*
2022-05-16孙亚男曾庆环刘远志张世斌武永乐丁惠国
孙亚男,曾庆环,刘远志,张世斌,李 鹏,武永乐,丁惠国
慢加急性肝衰竭(acute-on-chronic liver failure,ACLF)是在慢性肝炎和肝硬化基础上由多种诱因促发的以急性黄疸加深和凝血功能障碍为主要表现的临床综合征,其慢性肝病基础包括各种肝炎、代偿期肝硬化和失代偿期肝硬化患者[1]。ACLF起病急骤,病情进展迅速,治疗难度大,是肝脏疾病患者死亡的主要原因之一[2]。ACLF临床分型的B型和C型均存在肝硬化基础[1],肝硬化会导致门静脉压力病理性持续升高,出现食管-胃静脉曲张、腹水、肝性脑病等多种并发症。约50%肝硬化患者存在食管-胃静脉曲张,约12%患者会出现急性曲张静脉破裂出血,这种并发症常常是致命性的[3]。近年来,研究ACLF患者预后危险因素的文献较多,但多数并未对患者的基础肝脏疾病进行区分。本文回顾性分析了58例伴有中/重度静脉曲张的ACLF患者影响其预后的危险因素,熟悉本文结果将有助于制定该类患者的治疗策略,进一步提高临床疗效。
1 资料与方法
1.1 研究对象 2017年11月1日~2020年3月31日我院住院的首次诊断为ACLF B型和C型患者58例,男性50例,平均年龄为46.91±11.43岁;女性8例,平均年龄为52.25±14.06岁。ACLF诊断符合我国《肝衰竭诊治指南》 (2018 年版 )[1]。肝性脑病及其分期符合《肝硬化肝性脑病诊疗指南》(2018年版)[4]。胃镜检查提示存在中/重度食管静脉曲张,伴或不伴有胃底静脉曲张,对其进行6个月的临床转归随访。排除标准:(1)接受过脾切除术、食管静脉曲张套扎或硬化剂治疗、胃静脉曲张组织胶治疗、经颈静脉肝内门体支架分流术(TIPS)及其他分流手术等;(2)合并恶性肿瘤或存在严重的心肺疾病;(3)曾经或目前正在服用β受体阻滞剂等降门脉压药物;(4)失访或随访期间行肝移植、脾切除或TIPS治疗;(5)伴有弥漫性血管内凝血或应用抗凝治疗者。
1.2 观察指标 收集患者的一般资料,包括性别、年龄、肝硬化病因、是否伴有糖尿病、肝性脑病分期、是否伴有门静脉血栓、是否有消化道出血病史、住院期间是否行食管静脉曲张硬化剂治疗术(esophageal vein sclerotherapy,EVS)、肝功能Child分级、门静脉主干直径和脾静脉直径(腹部增强CT检查测量)、胃镜下静脉曲张程度、肝衰竭临床分型。腹水量的判定标准:分为无腹水(腹部超声检查提示无腹水)、少量腹水(仅经超声检查可探及)、中或大量腹水(中度、对称的或明显的腹部膨隆)。
1.3 统计学方法 应用SPSS 24.0 统计学软件分析,计数资料以%表示,采用x2检验。采用多因素Logistic回归分析,当P<0.05时,表示差异具有统计学意义。
2 结果
2.1 一般资料 在本组58例ACLF患者中, B型18例(31.0%),C型40例(69.0%);住院期间行EVS治疗患者17例(34.5%)。
2.2 影响死亡的危险因素分析 在随访的6个月内,20例(34.5%)死亡,1例行肝移植,2例失访,35例(60.3%)生存。单因素分析结果显示,生存与死亡患者腹水量、住院期间是否行硬化剂治疗、肝性脑病、肝衰竭分型和静脉曲张程度等差异具有统计学意义(P<0.05,表1)。将上述差异有统计学意义的5个指标再行非条件Logistic回归分析,结果得出腹水量(OR=9.76)、住院期间是否行硬化剂治疗(OR=19.28)和肝性脑病(OR=5.98)均是影响患者6个月生存的独立危险因素(P<0.05,表2)。
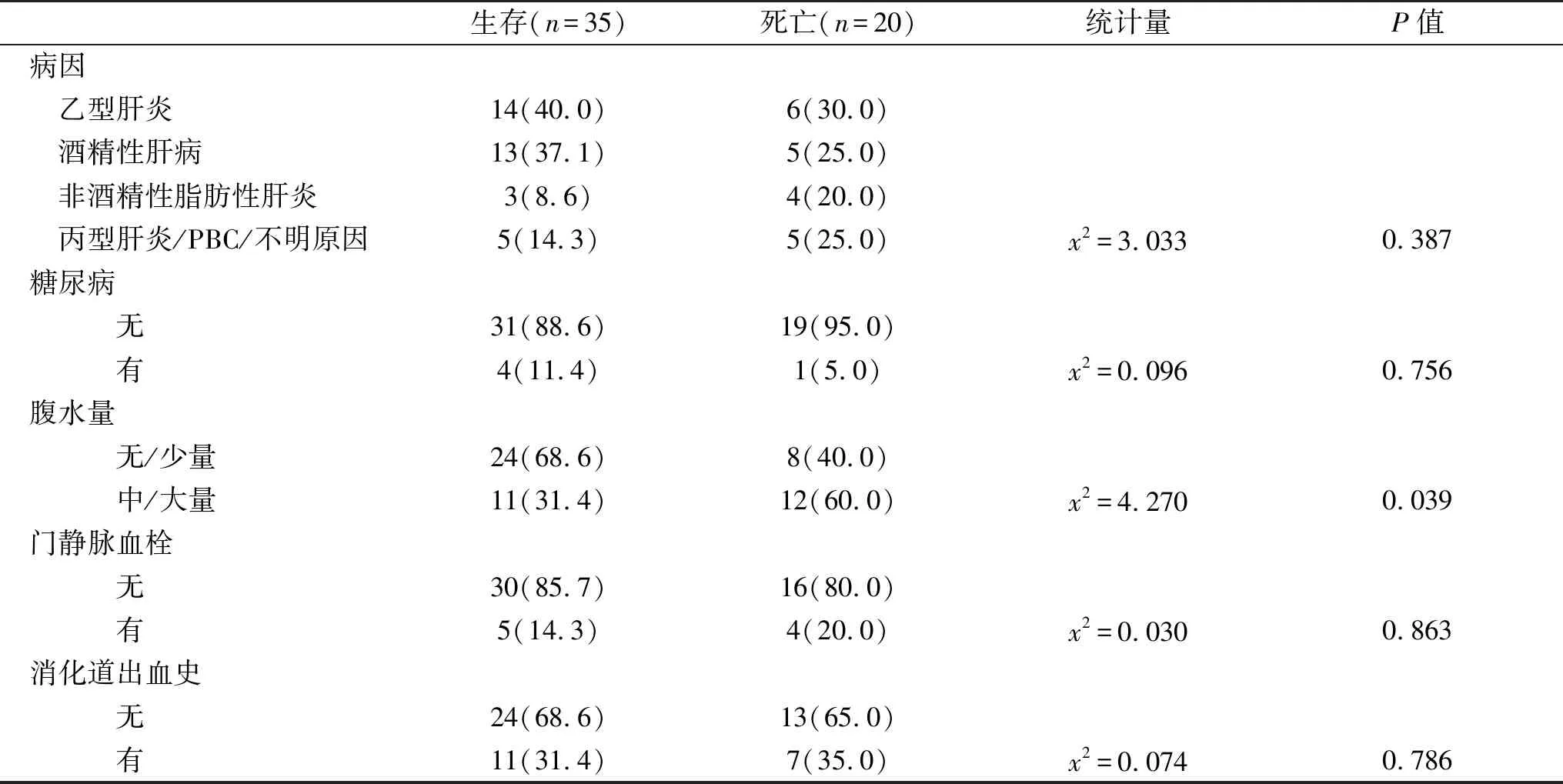
表1 影响6个月生存的单因素分析

续表1
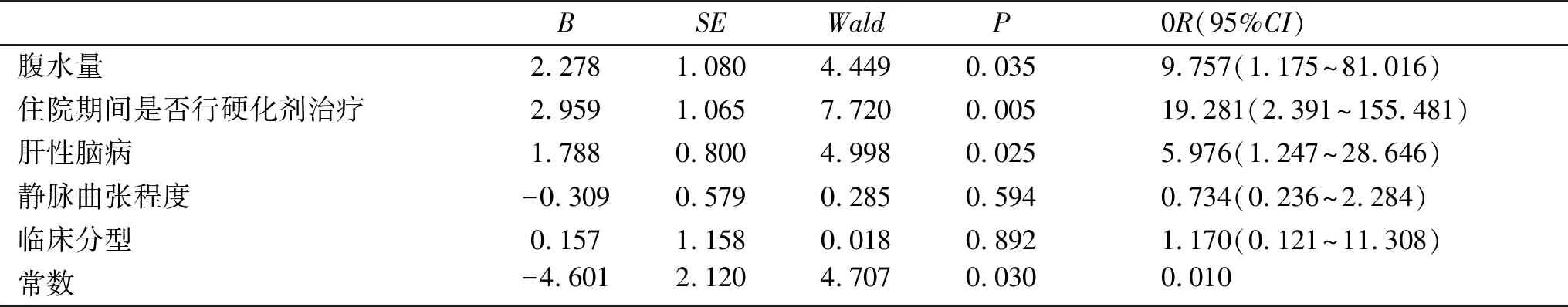
表2 影响6个月生存的多因素Logistic回归分析
3 讨论
慢加急性肝衰竭是指在慢性肝病基础上,由各种诱因引起的以急性黄疸加深、凝血功能障碍为主要表现的综合征,可合并肝性脑病、腹水、电解质紊乱、感染、肝肾综合征、肝肺综合征等,以及肝外器官功能衰竭[1],病死率达50%~70%[5]。按照慢性肝功能衰竭联盟器官功能衰竭评分(chronic liver failure consortium organ failure score,CLIF-COFs)诊断标准,在肝硬化患者,发生ACLF的比例约为24%~40%[6],多伴有严重的凝血功能障碍和不同程度的食管-胃静脉曲张,是发生消化道出血的重要原因[7]。本文以伴有肝硬化和中/重度食管静脉曲张的ACLF患者作为研究对象,探讨影响其6月生存率的危险因素,对及时、准确地评估该类患者病情、规避影响预后的危险因素具有非常重要的临床意义。
有研究表明,伴有肝性脑病的ACLF患者病死率明显升高[8-10]。北美终末期肝病研究联盟通过对1560例肝硬化患者的临床资料分析发现肝性脑病与肝硬化患者死亡具有独立相关性[11]。由此可见,终末期肝硬化和ACLF患者预后均与肝性脑病相关。已有研究[12]表明,在肝硬化急性失代偿和ACLF患者,肝性脑病的分期越高,病死率越高,与本研究的结论相同。在ACLF患者易发生全身性炎症反应[13,14],且在肝功能衰竭时,肝脏对毒素和毒物的代谢能力明显减退,造成血氨升高。多项研究表明,全身炎症反应、氧化应激和血氨升高均是发生肝性脑病的主要原因[15]。肝性脑病患者出现脑水肿是导致肝衰竭患者死亡的重要原因[16]。
腹水作为终末期肝病常见的并发症,也是不容忽视的。在对466例肝硬化患者进行随访显示,腹水、MELD评分、基线平均动脉压和基线血红蛋白是患者1 年内发生ACLF的独立预测因子,且与ACLF不良预后相关,3个月的无移植生存率仅为56%[17]。阮承兰[18]等研究亦发现,腹水、上消化道出血等是影响肝衰竭患者预后的独立危险因素。本研究结果提示除肝性脑病外,大量腹水患者预后较差。考虑腹水量大者提示患者门静脉压力较高,病情较重,易并发消化道出血等并发症,影响预后。大量腹水易合并自发性细菌性腹膜炎。有研究报道,自发性细菌性腹膜炎患者1 a生存率约为40%[19-21],其中分别有54%、60%和40%患者发生急性肾损伤、ACLF和死亡,病情进展快,病死率高,预后极差。
肝硬化患者常伴有门静脉高压,可合并不同程度的静脉曲张,食管静脉曲张破裂出血是肝硬化门静脉高压最严重和凶险的并发症之一,是肝硬化患者死亡的主要原因,故相对于A型ACLF患者,B型和C型ACLF患者具有更高的消化道出血风险。近年来,多项研究均显示内镜干预在食管静脉曲张破裂出血的防治方面具有重要的作用,其中EVS治疗急诊止血率达到81.6%~96.8%,明显提高了患者5 a和10 a生存率。EVS操作简单,疗效可靠,是我国治疗食管静脉曲张破裂出血的主要方法。本文在肝硬化并发中/重度食管静脉曲张的ACLF患者发现行EVS治疗不能提高短期生存率。本研究发现生存组与死亡组静脉曲张程度差异显著,死亡组静脉曲张程度较重,但多因素分析提示其并不是影响患者6月生存率的独立危险因素,而住院期间行EVS治疗明显增加了患者的死亡风险。ACLF患者凝血功能较差,在行EVS术后因注射点周围黏膜糜烂或溃疡形成,继发消化道出血的风险较高。EVS治疗并非无菌操作,有创操作可能增加了ACLF患者合并感染的概率。对于存在食管静脉曲张破裂出血的患者,应首先采用药物、三腔两囊管压迫止血等综合治疗策略,待肝脏功能恢复后评估治疗风险。若伴有不能控制的食管静脉曲张破裂出血或反复多次出血,可尝试行内镜下止血治疗,或评估行TIPS或手术治疗。
有文献显示,20%肝硬化患者在出现ACLF前并没有肝功能失代偿。一项针对415例ACLF患者28 d生存率的研究显示,无肝功能失代偿史的肝硬化患者比有失代偿史的患者病情更重、炎症反应更强、病死率更高。本研究显示C型ACLF患者较B型患者预后差,但临床分型并非短期生存的独立影响因素。可能与本研究纳入病例数较少有关。
