高强度玻璃组分的研究进展
2022-05-13李现梓王衍行杨鹏慧石晓飞祖成奎
李现梓,王衍行,韩 韬,杨鹏慧,石晓飞,何 坤,祖成奎
(中国建筑材料科学研究总院有限公司,建材行业特种玻璃制备与加工重点实验室,北京 100024)
0 引 言
玻璃作为一种重要的非晶无机非金属材料,具有高透光率、高强度、易加工和良好耐蚀耐热等特性,是光学元器件、电子显示零件和建筑装饰用品的主要材料[1-2]。随着其应用领域的不断扩大,玻璃材料的各种性能也亟需提高,尤其玻璃强度和硬度,对扩大应用场景和延长使用寿命至关重要。因此,通过有效的方法不断提高玻璃的强度和硬度是其未来发展的主要研究方向[3]。
目前,玻璃增强方法主要有两种:物理强化和化学强化。物理强化是先将玻璃加热接近玻璃软化温度,消除玻璃本身应力,之后迅速冷却使玻璃内外收缩速率不同,在玻璃表面产生压应力,内部产生张应力,获得强化效果;化学强化是通过离子交换来改变玻璃表面化学组分,形成表面应力,来提高玻璃强度的方法。两者都是在不改变玻璃材料成分的基础上进行的,且强化效果都具有一定的局限性[4]。
通过改善玻璃材料成分来提高基础玻璃的力学性能是解决强化局限性的一种有效方法,而影响氧化物能否作为改善玻璃材料性能制备原料的一个主要因素是解离能大小。解离能是指处于最低能态的一个分子分解为完全独立的原子时,从外界吸取的最小能量。含有高解离能化合物组分的玻璃,因其化学键能增强,使其网络结构强度更大,化学稳定性更高,从而在一定程度上提高了玻璃的硬度、弹性模量和抗断裂韧性等性能。
为满足在不同环境条件下的应用性能需求,玻璃体系不断丰富,已报道的高强度玻璃体系有钠钙硅(Na2O-CaO-SiO2)系统玻璃、钙铝硅(CaO-Al2O3-SiO2)系统玻璃、锂铝硅(Li2O-Al2O3-SiO2)系统玻璃、镁铝硅(MgO-Al2O3-SiO2)系统微晶玻璃等,不同体系玻璃组分之间存在明显区别,这导致玻璃性能也不尽相同。大量实验证明在玻璃成分一定的情况下,通过掺杂或者以其他成分元素替代主成分元素便可以实现玻璃性能的提升,例如在镁铝硅微晶玻璃中掺杂少量的TiO2可以增加玻璃网络连接程度,进而提高玻璃强度;在锂铝硅玻璃中掺杂进入不同质量分数的Y2O3可使玻璃体系中原子发生聚集,增加密度,改变玻璃介电性能等[5]。因此,研究通过改变玻璃成分来改善性能的方法十分必要。
1 组分设计对玻璃力学性能的影响
对高强度玻璃来说,按照成分的不同可以分为钠钙硅玻璃、无碱铝硅玻璃、高碱铝硅玻璃和锂铝硅玻璃体系等,如表1所示。
由表1可知,不同体系玻璃在组分和配比上存在明显差异,这是导致玻璃力学性能不同的主要原因。图1为氧化物的解离能、杨氏模量分布状况图,虚线为含有该氧化物的基础玻璃杨氏模量增长情况。表2为不同氧化物的解离能、密度、原子堆积密度和弹性模量系数,其中原子堆积密度为单位体积玻璃材料中原子本身所占体积分数。结合图1和表2可知通过掺杂高解离能的氧化物,能提高基础玻璃材料的杨氏模量[10-11]。但在实际应用中,具有高解离能的氧化物并不一定适合掺杂在玻璃组分中,如基础玻璃组分中加入BeO可以改善玻璃网络结构稳定性,大幅度提高玻璃的弹性模量,但因其本身具有毒性而限制了在实际生产中的使用;ZrO2具有高弹性模量系数,少量加入可提高玻璃材料的弹性模量等力学性能,但质量分数超过5%时易析晶;作为玻璃网络外体氧化物的K2O对于改善玻璃力学性能的作用很小,却可以起到降低玻璃黏度、助熔和减少析晶倾向作用,成为玻璃熔制过程中不可或缺的组分。

图1 基础玻璃中不同氧化物解离能与杨氏模量变化关系曲线[11]

表2 不同氧化物的解离能(G)、原子堆积密度(Cg)、密度(ρ)和弹性模量系数(E)[10]
玻璃材料的组分设计是提升玻璃力学性能的有效方法。作者根据氧化物解离能大小和对玻璃材料力学性能的影响程度,归纳了Al2O3、TiO2、ZrO2、Y2O3等氧化物掺杂引起的玻璃网络结构和性能变化,旨在探索出新型高强度玻璃组分。
1.1 Al2O3对玻璃力学性能的影响
Al2O3是典型的玻璃网络结构中间体氧化物,以铝氧四面体或铝氧八面体的形式存在于玻璃结构中。表3为当前常见手机盖板玻璃中Al2O3等成分含量及性能情况,从中可发现随着Al2O3含量增加,玻璃弹性模量和硬度提高,这说明Al2O3具有提高玻璃力学性能的作用。
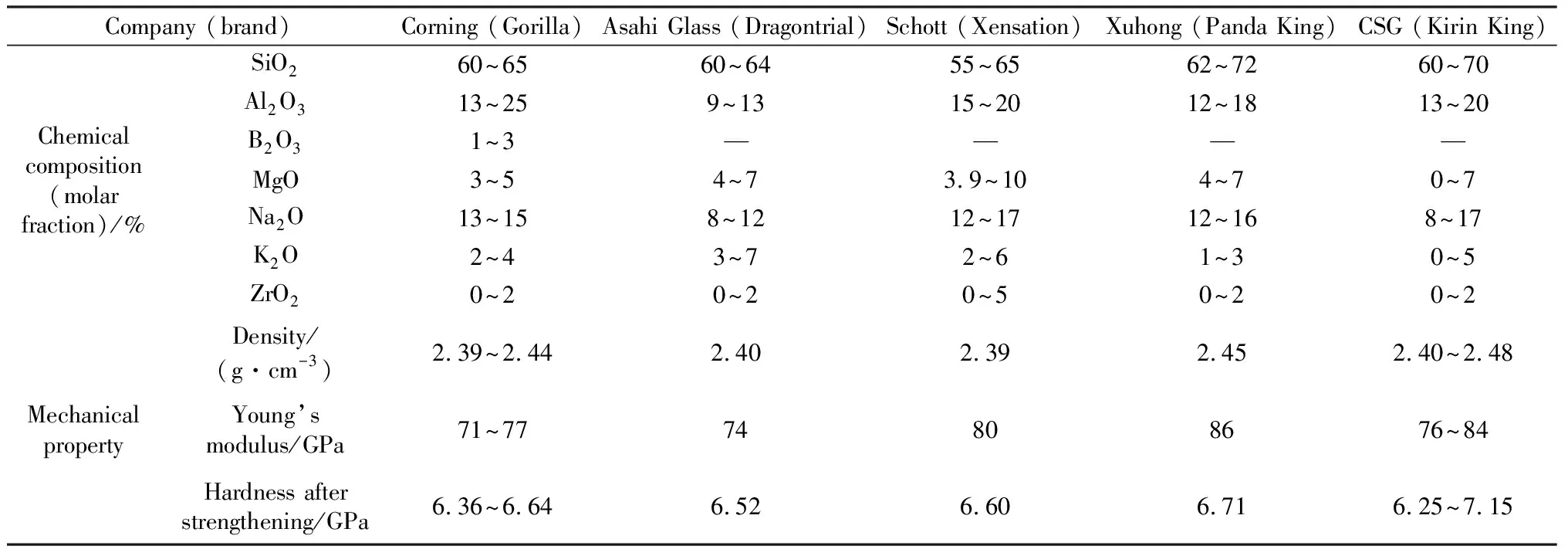
表3 当前市售手机盖板玻璃成分含量及力学性能
Al2O3对玻璃力学性能影响主要与Al3+的配位方式有关。当Al3+为[AlO4]四面体配位时可作为网络形成体,与玻璃结构中Si4+作用类似,可以增加玻璃的网络连接程度,强化玻璃的网络结构[12-14];而当Al3+为五配位或六配位时则具有电荷补偿的作用[12],这会使玻璃网络连结出现“断网”现象,降低玻璃强度。
郭宏伟等[15]利用X光电子能谱和红外光谱对有不同Al2O3含量的铝硼硅酸盐玻璃进行结构分析,发现玻璃的密度和硬度随着Al2O3含量的增加出现先增大后减小的现象,如图2所示。这是因为随着Al2O3含量的增加,更多的Al3+与游离氧离子结合形成[AlO4],与玻璃结构中的Si—O—Si键连接,修补了玻璃网络结构,将游离的玻璃网络外体离子更加紧密地包裹在网络中间,如图3所示。此外,半径较小的碱土金属离子被束缚于网络空隙之间,提高了玻璃的密度和介电性能;之后随着Al2O3继续增加,Al3+配位方式改变,[AlO6]的含量增加,且不参与玻璃网络形成,导致玻璃结构变得疏松,密度和硬度下降[16-17]。

图2 不同Al2O3含量的铝硼硅酸盐玻璃硬度和密度变化[15]

图3 铝硼硅酸盐玻璃网络结构变化示意图[15]
沈雪峰等[18]研究了Al2O3替代P2O5对P2O5-B2O3-Bi2O3系统玻璃结构、密度和硬度等性能影响。当Al2O3的摩尔含量由0%增加至2%时,玻璃硬度基本保持不变,这是因为Al3+可与游离氧结合形成[AlO4],连接断裂的玻璃网络,起到“补网”作用[19];另外P—O—P键断裂且形成了P—O—Al键,而P—O键比Al—O键的键能更强,使玻璃硬度减小。两者相互抵消,玻璃密度和硬度基本不发生变化[20-21]。继续增加Al2O3,促使[AlO4]结合更多游离氧形成[AlO6],玻璃网络结构断裂。同时六配位结构[AlO6]的增加引起[BO4]结构向[BO3]结构转变,导致玻璃网络结构疏松,力学性能下降。
由此可知,改变玻璃中Al2O3含量可改变Al3+配位方式,进而影响玻璃网络结构。四配位结构[AlO4]可提高玻璃网络结构交联度,而六配位结构[AlO6]会破坏玻璃网络结构,降低玻璃强度。因此,调控Al2O3含量成为改善玻璃性能的关键。
1.2 TiO2/ZrO2对玻璃力学性能的影响
TiO2在玻璃体系中常以[TiO4]或[TiO6]形式存在,可作为玻璃网络结构中间体来提高玻璃网络交联度,增大玻璃化学稳定性,减少玻璃中微裂纹缺陷。此外TiO2还能作为光学玻璃组分用以提高折射率,增强X射线和紫外线吸收能力。
Mukherjee等[8]研究了TiO2含量对钙铝硅微晶玻璃晶相和晶体结构变化的影响。当掺杂少量TiO2时,游离的Ti4+可进入到玻璃网络结构间隙,与游离氧结合形成四配位结构[TiO4],连接起断裂的硅氧网络,抑制玻璃中微裂纹扩展,提高玻璃力学性能。随着TiO2含量增加,微晶玻璃中晶体体积分数增加,具有微小树枝状结构的钛石晶体均匀地分布在玻璃基体中,使玻璃连接更加紧密[22-23],显微硬度值可达到6.63 GPa。
在玻璃组分中掺杂少量TiO2可以改善玻璃力学性能,主要与Ti4+具有较高场强有关。高任等[24]通过改变TiO2/SiO2-Al2O3-MgO系统玻璃中TiO2掺杂量研究了TiO2对玻璃力学性能的影响。研究发现随着TiO2含量增加,玻璃密度、抗弯强度和压缩模量出现“极大值”现象,其中弯曲强度随TiO2含量的变化如图4所示。当TiO2质量分数为1.5%时,玻璃的力学性能均取得最优值,其弯曲强度为110.36 MPa,压缩强度达到240.18 MPa,压缩模量达到115.03 GPa。这是因为掺杂少量TiO2可与玻璃中游离氧结合形成四配位结构[TiO4],与硅氧四面体形成良好的连接结构,提高玻璃网络交联度;Ti4+高场强的特点又增加了玻璃结构的内聚力,提高玻璃网络的密度和结构稳定性。过量掺杂TiO2导致玻璃网络中的四配位结构[TiO4]转变为六配位结构[TiO6],降低桥氧数量,破坏玻璃网络结构整体性,导致玻璃力学性能下降[25]。

图4 不同TiO2掺杂量SiO2-Al2O3-MgO系玻璃弯曲强度[24]
在玻璃组分中掺杂适量ZrO2,可改善玻璃硬度、弹性模量等力学性能。ZrO2含量对玻璃黏度和熔制温度影响很大,在质量分数超过5%时易出现析晶现象,常作为形核剂加入到微晶玻璃中。Zhang等[26]研究了以纳米ZrO2颗粒作为形核剂的CaO-Al2O3-MgO-SiO2系微晶玻璃的结晶行为和机理,纳米ZrO2颗粒可以降低微晶玻璃的转变温度,并且提高化学稳定性[27-28]。
具有高场强特点的Ti4+和Zr4+阳离子可以改变Al3+配位方式,提升玻璃硬度和弹性模量。Guo等[29]通过在铝硅酸盐玻璃中加入TiO2和ZrO2,将四配位结构的[AlO4]转变为五配位[AlO5]或六配位结构[AlO6],又因Ti4+和Zr4+比玻璃网络结构中其他离子的半径更小、场强更大,可提高玻璃网络结构原子填充密度,改善玻璃硬度和弹性模量[30-31]。
1.3 La2O3/Y2O3对玻璃力学性能的影响
关于稀土氧化物对玻璃力学性能影响的研究是在无规则网络理论和晶子学说基础上展开的,通过红外-拉曼光谱、核磁共振光谱、X-光电子能谱和X-射线衍射谱等测试方法来分析玻璃成分和网络结构中基团的化学键、配位方式以及表征玻璃微观网络结构。稀土氧化物以阳离子形式进入玻璃网络结构,与玻璃结构中游离的O2-结合,降低非桥氧数量,提高玻璃力学性能[27]。
韩建军等[32]研究了掺杂La2O3对SiO2-Al2O3-CaO-MgO系统玻璃密度和力学性能的影响,通过红外光谱振动峰强度变化探究玻璃网络结构的变化。研究发现,玻璃弹性模量随着La2O3的增加,出现“极大值”现象,当质量分数达到为3%时,弹性模量最大,达到93.6 GPa[32]。这是因为La2O3在玻璃网络结构中可做网络外体,La3+可以进入到玻璃网络结构空隙中,增大了玻璃体积密度和弹性模量;而La2O3中游离氧会增加非桥氧数量,降低玻璃网络交联度。La2O3对于提高玻璃网络紧密度作用有限,掺杂过量La2O3会大幅度增加游离氧数量,降低玻璃力学性能。
Kaur等[33]制备出xLa2O3(100-x)TeO2(摩尔分数x=5,7,10,12.5,15,20)和2TiO2-xLa2O3-(98-x)TeO2(摩尔分数x=5,7,10)两种体系玻璃以研究La2O3和TiO2对玻璃性能的影响。研究发现La2O3掺杂量x>10的玻璃具有较大的结晶倾向。此外,在La2O3-TeO2体系中加入TiO2可抑制玻璃中微晶的生长,提高了热稳定性和光透过性。进一步研究发现,随着La2O3和TiO2加入,玻璃结构中的[TeO4]结构基团转化为[TeO3]基团,夹杂物尺寸减小,热稳定性和力学性能得到改善。
Liu等[34]研究了不同含量Y2O3对B2O3-Al2O3-SiO2系统玻璃结构和性能的影响规律。由图5不同Y2O3含量B2O-Al2O3-SiO2玻璃强度变化曲线可知,玻璃的抗弯强度和抗压强度均出现先下降后升高的现象。结合图6红外光谱中振动峰变化情况可知,随着Y2O3掺杂量增加,在720 cm-1和1 500 cm-1附近吸收峰强度逐渐下降,这是因为硼酸含量降低导致玻璃网络中[BO3]结构减少,790 cm-1处振动强度的降低归因于Y2O3的掺杂破坏了[AlO4]结构,从而导致玻璃网络结构“断网”,非桥氧含量增加,力学性能下降。作者认为Y2O3在玻璃结构中作用与碱土金属氧化物相似,可作为一种玻璃网络修饰体。当Y2O3质量分数由4%增加到7%时,抗压强度和抗弯强度上升,这是因为玻璃密度增加,同时修补了玻璃网络结构,从而提高玻璃强度[35-37]。
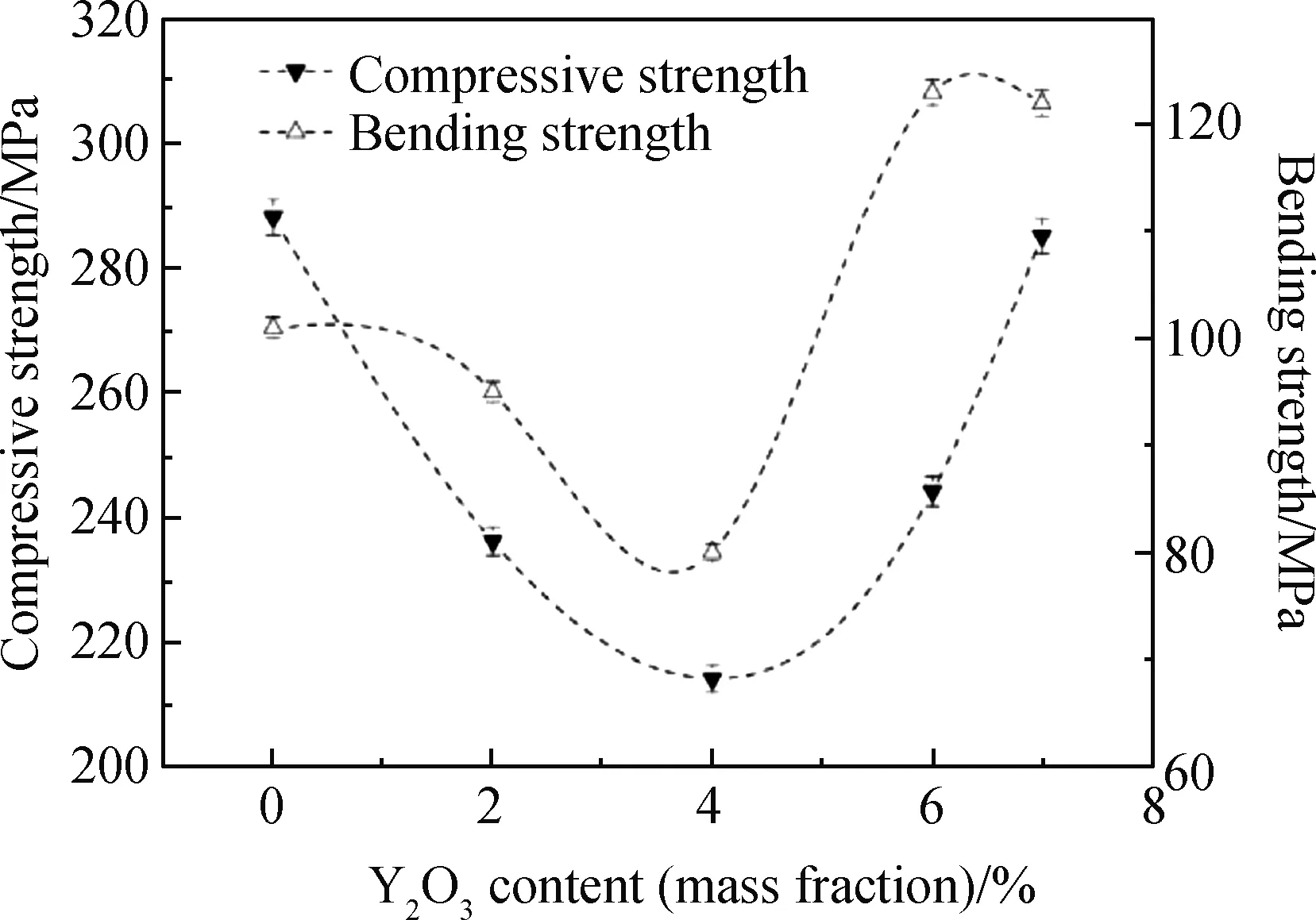
图5 不同Y2O3含量B2O-Al2O3-SiO2玻璃强度变化曲线[34]
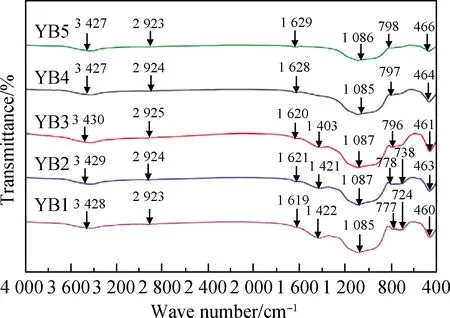
图6 硼铝硅玻璃红外光谱[34]
1.4 Nb2O5对玻璃力学性能的影响


图7 不同Nb2O5含量对钠钙硅玻璃抗弯强度的影响[6]


图8 不同Nb2O5含量的Li2O-Ta2O5-ZrO2-SiO2玻璃的维氏硬度[38]

图9 不同Nb2O5含量的Li2O-Ta2O5-ZrO2-SiO2玻璃的机械强度[38]
1.5 BeO对玻璃力学性能的影响
在玻璃网络结构中,Be2+可与游离氧结合形成铍氧四面体[BeO4],参与玻璃网络形成过程。Be2+具有较高场强,是碱土金属离子和碱金属离子中电负性最高的离子,其电子极化率低于形成玻璃结构网络的Si4+,可促进Si4+和O2-配位形成[SiO4]四面体[39]。此外,BeO可降低玻璃热膨胀系数,提高玻璃硬度和化学稳定性,改善玻璃折射率和X射线透过率[40]。但因BeO为有毒物质,会对环境和人体造成巨大伤害,在玻璃组分设计时尽量少用或不用。
Sen等[41]利用核磁共振技术研究了BeO摩尔分数为20%的BeO-SiO2系统玻璃的网络结构状态,作者发现BeO能以一种团簇体[BeO4/2]2-形态参与玻璃网络形成过程,其形成方式如式(1)所示。
BeO+BeO→[BeO4/2]Be2+
(1)
团簇体[BeO4/2]2-易与玻璃体系中的Na+结合,且团簇体的高极性使玻璃网络比之前更加紧密,增加了玻璃密度,提高了弹性性能。
1.6 其他组分对玻璃力学性能的影响
除了上述常用氧化物以外,玻璃中其他组分也可改善玻璃机械性能,它们往往是与其他的离子或基团结合或反应等,提高网络密集度,增加玻璃密度,从而提高玻璃材料的力学性能。
He等[42]在研究Li2O取代Na2O对Na2O-MgO-Al2O3-SiO2系统玻璃结构和性能影响时发现改变玻璃组分中Li2O含量可影响玻璃力学性能,如图10和图11所示,玻璃的密度出现先升高再降低的现象,而硬度和抗弯强度均为先降低后升高。这是因为与Li2O相比,Na2O可提供更多游离氧,破坏玻璃网络结构。随着Li2O含量增加,玻璃密度升高,游离的Li+破坏Si—O—Si键,使得玻璃硬度和抗弯强度大幅度降低;当Li2O摩尔分数由3%提高到5%时,低原子质量的Li+增加玻璃密度下降,且碱金属离子Na+含量降低,对Si—O—Si键混合碱效应减弱,提高了玻璃网络结构强度,促进了硬度和抗弯强度的提高[43-44]。

图10 不同Li2O含量的Na2O-MgO-Al2O3-SiO2玻璃的密度[42]

图11 不同Li2O含量的Na2O-MgO-Al2O3-SiO2玻璃的抗弯强度和维氏硬度[42]
Gui等[45]研究了ZnO替代MgO对MgO-Al2O3-SiO2-B2O3系统微晶玻璃晶体类型和尺寸的影响。如表4所示,随着ZnO含量增加,玻璃的硬度、抗弯强度和抗压强度均得到提高。作者认为加入ZnO可促进α-堇青石晶相的形成,帮助其均匀地分布在玻璃基体中,改善了玻璃微观结构。此外,ZnO含量提高引起的高结晶度增加了晶界数量,有效地抑制裂纹在玻璃中扩展,从而提高玻璃抗弯强度和抗压强度[46-47]。

表4 MgO-Al2O3-SiO2-B2O3系统玻璃的化学成分及其物理力学性能[45]
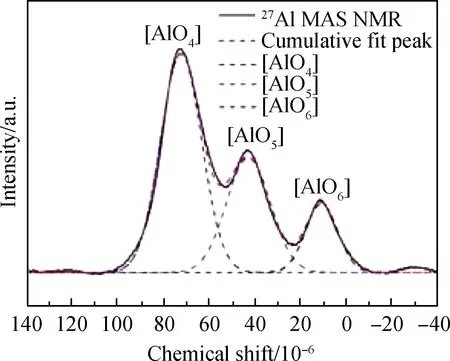
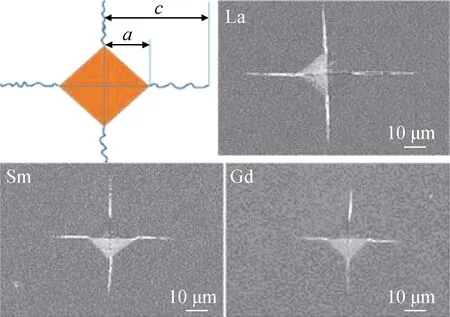
Guo等[29]利用悬浮熔制法制备了18.77R2O3-4.83Y2O3-28.22TiO2-8.75ZrO2-39.43Al2O3(R=La、Sm、Gd)高熵玻璃来研究镧系元素对玻璃硬度、杨氏模量和断裂韧性的影响。Guo等创新性地提出无硅玻璃组分制备高熵玻璃,其硬度、杨氏模量和断裂韧性最高分别达到12.58 GPa、177.9 GPa和1.52 MPa·m0.5(见表5),远超当前硅酸盐玻璃力学性能。结合27Al NMR光谱(见图12)峰面积分析,四配位([AlO4])、五配位([AlO5])和六配位([AlO6])结构占比分别为55.3%、31.0%和13.7%,这归因于高场强离子Ti4+和Zr4+的加入提高了Al3+的氧配位数,而高氧配位数也改变了玻璃原子填充密度,导致高熵玻璃密度提高[48]。由图13压痕的扫描电子显微照片可以看出,三种玻璃的裂纹扩展长度趋势为l(R=Gd) 表5 高熵玻璃的原子堆积密度(Cg)、密度(ρ)、杨氏模量(E)、维氏硬度(HV)和断裂韧性(KIC)[29] 图12 高熵玻璃核磁共振谱图[29] 图13 断裂韧性裂纹长度测量图[29] 随着玻璃材料应用领域的不断扩大,对其结构功能一体化要求不断提高,尤其是高强度玻璃的力学性能,它是玻璃服役安全性的保障。面对未来应用发展需要,高强度玻璃的研究和发展趋势主要有三个方面: (1)通过进一步完善玻璃体系的成分,设计力学性能更好的玻璃配方,如锂铝硅酸盐玻璃中提高Al2O3的含量,改善网络结构从而提高本体玻璃的机械性能;掺杂高场强离子,如Ti4+、Zr4+等可提高玻璃的原子填充密度,改善本体玻璃的硬度和弹性模量。 (2)探索新的可提升玻璃性能的元素,开发新型高强度玻璃体系,如镧系元素中的La、Gd和Lu均有提高玻璃强度的作用,在不断改善玻璃熔制条件的情况下深入研究其强化机理。 (3)突破固有的玻璃体系原料种类和配比的束缚,尝试新型概念玻璃,如高熵玻璃(R2O3-Y2O3-TiO2-ZrO2-Al2O3玻璃(R=La、Sm、Gd))体系,在不含有SiO2的前提下,制备得到了硬度和弹性模量均高于常规玻璃体系的新型玻璃材料,极大地扩展了人们对于新型玻璃未来发展的视野。 目前,关于高强度玻璃组分设计的研究主要是通过氧化物掺杂来改善玻璃网络结构,提高力学性能。用于提高玻璃强度的氧化物主要有Al2O3、Y2O3、La2O3和TiO2等,氧化物中阳离子可与玻璃中[SiO4]结构单元结合,提高玻璃骨架化学稳定性,并且能连接玻璃中游离的氧离子,提高玻璃机械强度;对于高场强的Ti4+、Zr4+,可进入到玻璃网络间隙,提高玻璃密度和弹性模量;掺杂Be2+氧化物不仅能够增加桥氧数量,还可形成极性团簇体参与到玻璃网络形成过程中,提高玻璃力学性能。此外,玻璃的强化方法还包括对基础玻璃的钢化、表面处理及复合强化等,例如化学强化是用原子半径较大的K+置换出玻璃中的原子半径较小的Na+,以形成表面压应力层,所以在玻璃组分设计时应考虑化学强化对基础玻璃中Na2O成分要求,以求达到“组分增强+化学强化”效果。因此在玻璃组分设计时要综合考虑各项性能要求,通过多种强化方法研制出新型高强度玻璃体系,以满足未来玻璃材料应用和发展需要。
2 高强度玻璃的发展趋势
3 结 语
