冬凌草甲素对急性哮喘小鼠气道重塑的影响
2022-05-11王兴兰张建勇
王兴兰,张建勇
1 遵义医药高等专科学校 贵州遵义 563006 2 遵义医科大学附属医院 贵州遵义 563000
支气管哮喘(Bronchial Asthma,简称哮喘)是由多种细胞和细胞因子共同参与的,以气道高反应性及气流受限为主要特征的慢性炎症性疾病[1]。作为全球最常见的慢性呼吸系统疾病之一,哮喘给患者、家庭、社会乃至整个国家带来了沉重的经济压力,已成为危害人类身体和身心健康的主要社会公共卫生问题之一[2]。哮喘的发病机制复杂,尚未完全明确,目前认为气道重塑和气道炎症是哮喘特征性病理改变[3]。1992年Koessler及Huber学者首次提出气道重塑学说[4],气道重塑是哮喘最为典型的病理学特点,涉及炎症细胞浸润、新生血管形成、上皮下胶原蛋白的沉积及纤维化以及气道平滑肌的增生、肥大等[5-7]。长期反复的气道炎症是导致哮喘气道重塑的重要原因,持续进展的气道重塑最终可导致气道阻塞的不可逆、肺功能的严重受损以及气道高反应性的持续存在[8]。“上皮-间充质营养单位学说”是至今较为认可的学说之一,是指由多种炎症细胞参与引起的炎症刺激。该学说认为,正常情况下促气道上皮细胞修复的生长因子与抑制上皮细胞修复、促进纤维增生的细胞因子处于动态平衡状态,当抑制上皮细胞修复、促进纤维细胞增生的细胞因子处于优势地位时,便会导致气道上皮细胞无法正常修复,进而导致气道纤维细胞发生活化、增生及纤维化,最终引起了气道重塑[9]。转化生长因子β(Transforming growth factor beta,TGF-β)是由上皮细胞、巨噬细胞、嗜酸性粒细胞及成纤维细胞等多种细胞产生,具有抑制气道上皮细胞的修复、促进纤维细胞增生的功能,是介导哮喘气道重塑的重要介质之一[10]。研究表明哮喘患者支气管上皮中存在TGF-β1和TGF-β3表达,TGF-β1由肺内成纤维细胞等多种细胞产生,在细胞生长、分化、免疫调节中发挥重要作用,并且是导致气道重塑的主要介质[11-12]。
冬凌草是香茶菜属植物,冬凌草甲素是从冬凌草中提取出的一种天然化合物,占冬凌有效成分的百分之九十以上,具有抗炎、抗肿瘤、免疫调节等多种功 能[13],有学者对冬凌草甲素在呼吸系统疾病中的作用进行研究,陈叶等对鸡卵蛋白(ovalbumin, OVA)诱导的哮喘小鼠模型进行研究,结果表明,冬凌草甲素可通过调节辅助性T细胞1型(Th1)/辅助性T细胞2型(Th2)平衡、抑制气道高反应性来减轻急性哮喘小鼠的炎症反应[14]。对于冬凌草甲素是否能减轻哮喘小鼠的气道重塑,国内外尚无相关文献报道,本实验旨在研究冬凌草甲素对急性哮喘小鼠气道重塑的影响及可能的机制,为哮喘的诊治提供新的思路。
材料与方法
1 材料
1.1 实验动物 清洁级6~8周龄BALB/C雌性小鼠,体重(16~20g)(18.11±0.66g),由重庆第三军医大学实验动物中心提供[SCXK(渝)2012-0005]。
1.2 药品与试剂 OVA(II级、V级,美国Sigma公司),氢氧化铝凝胶(美国Sigma公司),冬凌草甲素(上海士丰生物制品有限公司),二甲亚砜(北京中杉生物技术有限公司),实时荧光定量PCR(RT-PCR)引物(TGF-β1、β-actin,大连TaKaRa公司),小鼠抗小鼠-TGF-β1单克隆抗体(英国Abcam公司),二步法免疫组化检测试剂盒(北京中杉生物技术有限公司),RNAiso Reagent(大连TaKaRa公司),逆转录试剂盒(大连TaKaRa公司),SYBR® GREEN PCR Master Mix(大连TaKaRa公司),马森(Masson)染色试剂盒(北京索来宝生物科技有限公司),二氨基联苯胺(DAB)显色试剂盒(北京中杉生物技术有限公司),焦碳酸二乙酯(DEPC)(大连TaKaRa公司),多聚赖氨酸(北京中杉生物技术有限公司),4%多聚甲醛(庆川东化工有限公司),无水乙醇、二甲苯、盐酸(重庆川东化工有限公司)。
1.3 仪器 自制雾化箱(长27cm×宽24cm×高11cm),压缩式雾化器NE-C900(欧姆龙大连有限公司),核酸蛋白测量仪ND-1000(美国Nanodrop公司),ICycler iQ5荧光定量PCR仪(美国BIO-RAD公司),IPWin32采图系统DM4000B(德国Lecia公司),Image-Pro Plus 6.0图像分析软件(美国Media Cybernetics公司)。
2 试验方法
2.1 急性哮喘模型的建立 分别于实验第1天、第13天,腹腔(40ugOVA+1mg氢氧化铝)联合皮下注射(20ugOVA+1mg氢氧化铝)致敏。第19~23d,将小鼠放于自制雾化箱内,以超声雾化器进行雾化,10%OVA盐水气溶胶吸入激发,1次/d,每次30min,末次激发24h后处死小鼠。
2.2 分组给药 分组:将清洁级雌性BALB/c小鼠随机分为正常组、模型组、冬凌草甲素10mg/kg干预组(低剂量干预组)、冬凌草甲素20mg/kg干预组(高剂量干预组)。实验组:致敏过程同模型组,低剂量干预组及高剂量干预组分别于激发前30min腹腔注10mg/kg及20mg/kg冬凌草甲素。正常组:致敏过程以磷酸缓冲盐溶液(phosphate buffer saline,PBS)代替OVA腹腔联合皮下注射,激发过程以生理盐水雾化吸入,相关参数与模型组相同。
2.3 对支气管壁厚度进行测定 气道壁厚度测定参照加慧[15]等的方法,气道壁厚度计算公式:气道壁厚度(um)=(支气管总面积—气道内径面积)/支气管基底膜的周径。
2.4 马森染色(Masson染色)观察气道周围胶原纤维沉积 按照试剂盒说明书进行操作,应用IPWin60彩图系统及Image-proplus 6.0图像分析软件,定量分析气道胶原纤维阳性相对面积。
2.5 应用免疫组化检测气道TGF-β1表达 按照试剂盒说明书进行操作,以PBS代替一抗作空白对照,以小鼠大肠和脾脏分别作阳性和阴性对照,以PBS代替一抗作空白对照,以小鼠大肠和脾脏分别作阳性和阴性对照,以积分光密度(IOD)为指标对各组免疫组织化学染色进行定量分析。
2.6 应用荧光定量PCR检测肺组织内TGFβ1mRNA表达情况 先后完成总RNA的提取、RNA逆转录成cDNA、实时荧光定量PCR反应(SYBR Green Ⅱ嵌合荧光法)。TGF-β1引物序列上 游5,-GTGTGGAACATGTGGAACTCTA-3,下 游5,-TTGGTTCAGCCACTGCCGTA-3, β-actin引 物序列上游5,-GGCCAACCGTGAAAAGATGA-3,下游5,-CAGCCTGGATGGCTACGTCA -3。
3 统计学方法
使用SPSS17.0软件,根据资料属性对各组数据完成统计,以均数±标准差表示,两样本均数比较采用独立样本t检验;多样本均数比较采用单因素方差分析进行检验,方差齐者使用LSD检验,方差不齐者使用Dunnett’s T3检验。
结 果
1 各组小鼠气道壁厚度
正常组:肺组织的结构正常,气管平滑肌及基底层无增厚,表面光滑。模型组:杯状细胞、气道上皮细胞增生、官腔狭窄、管壁增厚,气道重塑显著。干预组:支气管壁的结构较完整,可见少量平滑肌以及基底层的增厚,且低剂量干预组平滑肌及基底层增厚更明显。测量气道壁厚度,干预组、模型组与正常组比较差异均具有统计学意义(P<0.01),干预组与模型组比较差异亦具有统计学意义(P<0.01),高剂量干预组与低剂量干预组比较,差异有统计学意义(P<0.01)。结果见表1。
表1 各组小鼠气道壁厚度(±s)
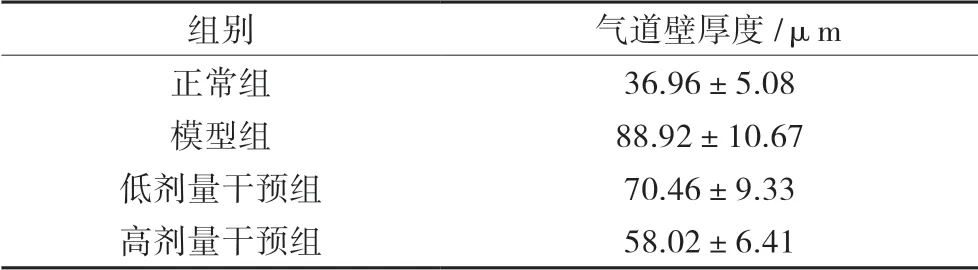
表1 各组小鼠气道壁厚度(±s)
注:与正常组组比较,模型组及干预组P均<0.01;与模型组组比较,干预组P均<0.01,与低剂量干预组组比较,高剂量干预组P<0.01。
组别 气道壁厚度/μm正常组 36.96±5.08模型组 88.92±10.67低剂量干预组 70.46±9.33高剂量干预组 58.02±6.41
2 Masson染色检测气道组织胶原纤维表达情况
模型组、干预组气道周围的胶原纤维沉积相对面积均较正常组明显增高(P<0.01)。干预组气道周围的胶原纤维沉积相对面积均较模型组明显减少(P<0.01)。高剂量干预组气道周围胶原纤维沉积相对面积均较低剂量干预组显著减少(P<0.01)。结果见表2,图1-图4。

图4 高剂量干预组气道组织胶原纤维表达
表2 各组小鼠气道周围胶原纤维阳性相对着色面积的变化(±s)
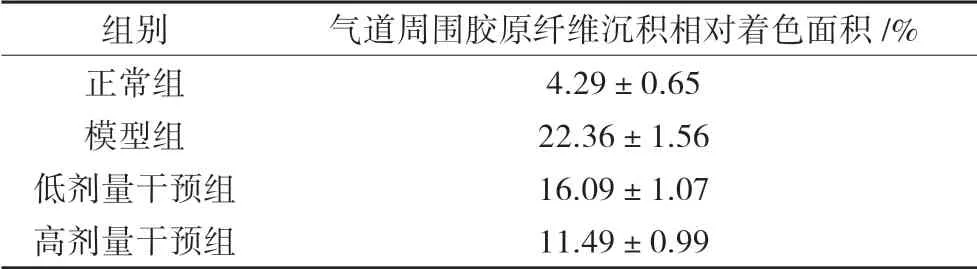
表2 各组小鼠气道周围胶原纤维阳性相对着色面积的变化(±s)
注:与正常组比较,模型组、干预P均<0.01;与模型组比较,干预组P均<0.01,与低剂量干预组比较,高剂量干预组P<0.01。
组别 气道周围胶原纤维沉积相对着色面积/%正常组 4.29±0.65模型组 22.36±1.56低剂量干预组 16.09±1.07高剂量干预组 11.49±0.99
3 免疫组化检测TGF-β1蛋白的表达情况
应用免疫组织化学染色方法进行检测TGF-β1在肺组织的表达,TGF-β1主要分布在肺泡巨噬细胞、炎症细胞、间质细胞以及气道黏膜上皮层。结果显示正常组中TGF-β1仅弱表达,而在模型组、干预组中TGF-β1呈阳性表达,测IOD值均较正常组增高,差异有统计学意义(P<0.01);模型组TGF-β1表达较干预组增加(P<0.01)。低剂量干预组的TGF-β1表达量较高剂量干预组增加(P<0.01)。结果见表3,图5-图8。
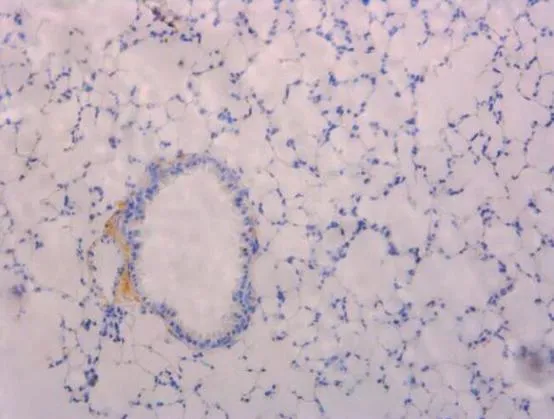
图5 正常组肺组织TGF-β1

图8 低剂量干预组肺组织TGF-β1表达
表3 各组小鼠肺组织TGF-β1蛋白表达(±s)

表3 各组小鼠肺组织TGF-β1蛋白表达(±s)
注:与正常组比较,模型组、干预P均<0.01;与模型组比较,干预组P均<0.01,与低剂量干预组比较,高剂量干预组P<0.01。
组别 TGF-β1蛋白阳性着色面积正常组 0.07±0.01模型组 0.33±0.02低剂量干预组 0.21±0.01高剂量干预组 0.14±0.01
4 RT-PCR检测小鼠气道TGF-β1mRNA的表达
RT-PCR检测TGF-β1 mRNA表达,模型组、干预组肺组织中TGF-β1 mRNA的表达量较正常组显著增加(P<0.01)。模型组肺组织中TGF-β1 mRNA表达量显著低于干预组(P<0.01);低剂量干预组肺组织中TGF-β1 mRNA的表达量较高剂量干预组显著增加(P<0.01)。结果见表4。图9-图12。
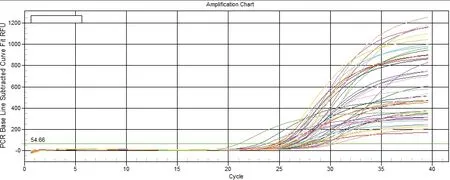
图9 肺组织TGF-β1扩增曲线图
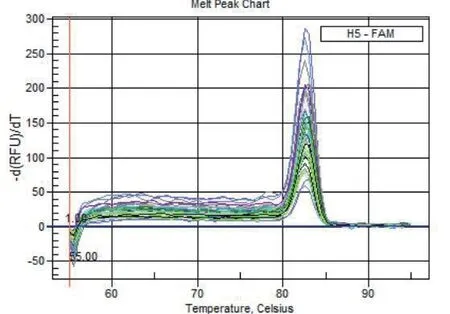
图12 肺组织β-actin融解曲线峰图
表4 各组小鼠肺组织TGF-β1 mRNA相对表达量(±s)

表4 各组小鼠肺组织TGF-β1 mRNA相对表达量(±s)
注:与正常组比较,模型组、干预P均<0.01;与模型组比较,干预组P均<0.01,与低剂量干预组比较,高剂量干预组P<0.01
组别 ΔCT ΔΔCT 2-ΔΔCT正常组 5.30±0.11 0±0.11 1.00±0.08模型组 3.71±0.13 -1.60±0.10 3.03±0.24低剂量干预组 3.96±0.13 -1.34±0.06 2.53±0.11高剂量干预组 4.25±0.12 -1.05±0.07 2.08±0.11
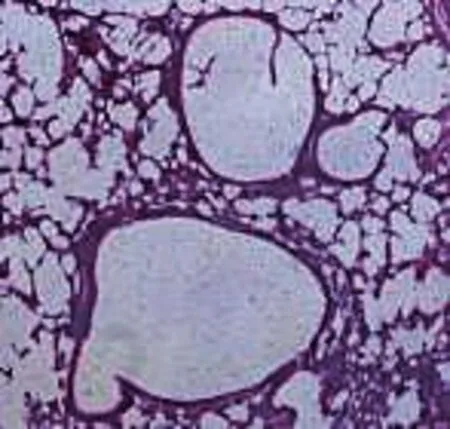
图1 正常组气道组织胶原纤维表达

图2 哮喘组气道组织胶原纤维表达
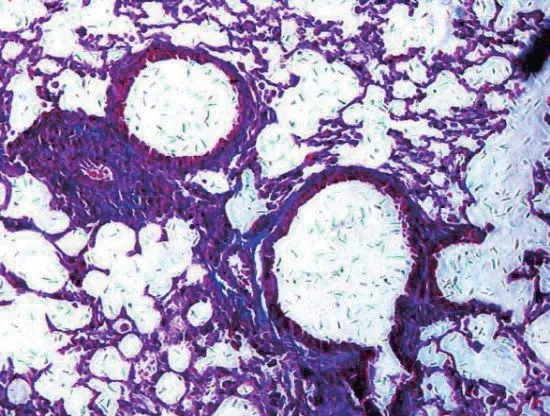
图3 低剂量干预组气道组织胶原纤维表达
讨 论
哮喘是全球最常见的慢性呼吸系统疾病之一,是一种以气道阻塞、气道高反应性及气道炎症为主要特征的异质性疾病[16]。气道重塑是哮喘的特征性病理改变,是气道在长期慢性炎症反应刺激下发生的气道壁结构改变,在哮喘的发生、发展中发挥重要作用,可加重哮喘患者的症状、降低肺功能[17]。TGF-β1可促进纤维细胞、肌层纤维细胞的增生,是气道重塑的主要调控因子之一,与哮喘的发生、发展密切相关[12]。
冬凌草甲素是从冬凌草中提取的贝壳烯二萜类天然有机化合物,既往研究显示冬凌草甲素具有抗肿瘤、抗增殖、抗炎和抗病毒等作用[18-19]。冬凌草甲素在我国治疗炎症性疾病已有数百年的历史,是我国临床使用最广泛的中草药之一。近年来有研究指出,冬凌草甲素可减轻哮喘小鼠气道炎症及气道高反应性[14],而冬凌草甲素是否能减轻支气管哮喘的气道重塑,目前国内外暂无相关文献报道。本实验通过研究不同剂量冬凌草甲素对OVA诱导的急性哮喘小鼠的影响,采用HE染色观察气道壁厚度;Masson染色观察气道周围胶原纤维沉积;免疫组化测定TGF-β1蛋白表达量,RT-PCR测定肺组织中TGFβ1mRNA表达水平。研究结果显示,不同剂量的冬凌草甲素均可减轻哮喘小鼠气道组织胶原纤维的增生、抑制TGF-β1的分泌,且高剂量冬凌草甲素干预组效果明显优于低剂量干预组,存在剂量-效应关系。TGF-β1作为支气管哮喘产生气道重塑的主要调控因子,能促进气道重塑的发生。由此推测冬凌草甲素可能通过抑制TGF-β1的分泌来减轻哮喘小鼠的气道重塑,这一研究结果或将为哮喘的治疗提供新的思路,发挥我国中医药的优势,值得进一步深入研究。
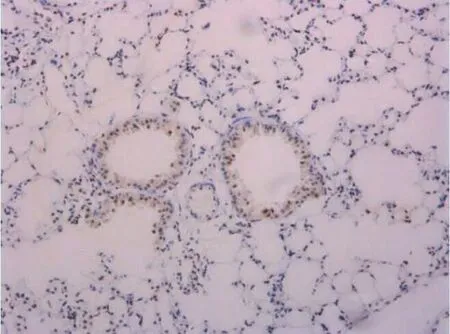
图6 模型组肺组织TGF-β1表达
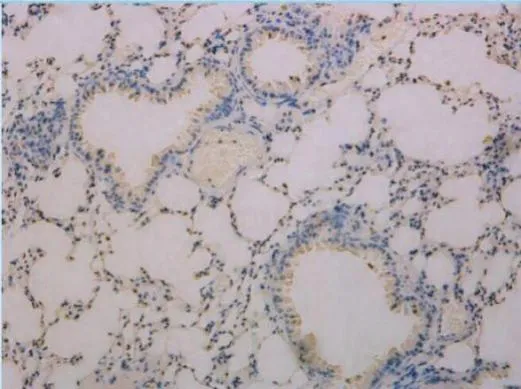
图7 低剂量干预组肺组织TGF-β1表达

图10 肺组织β-actin扩增曲线图
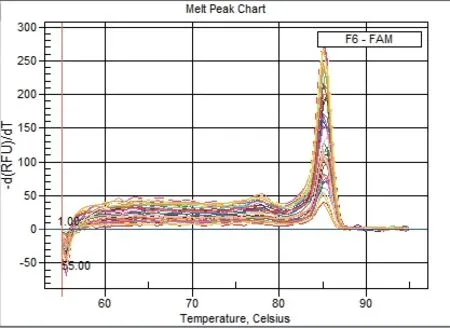
图11 肺组织TGF-β1融解曲线图
