ASCT2靶向抑制剂的合成及抗肿瘤活性研究*
2022-05-10覃双林
吴 娜,覃双林,任 平,吴 诗
(湖北科技学院医学部药学院,湖北 咸宁 437100)
异常活跃的谷氨酰胺代谢重排(glutamine metabolic reprogramming)是正常细胞区别于肿瘤细胞的本质特征之一[1-2]。丙氨酸-丝氨酸-半胱氨酸转运体2(alanine-serine-cysteine transport 2,ASCT2)是Na+依赖性谷氨酰胺转运蛋白,属于中性氨基酸转运系统system ASC家族成员之一[3],众多研究[4-6]显示多种肿瘤细胞,如乳腺癌、宫颈癌、肝癌、肺癌、黑色素瘤、结肠癌和前列腺癌等,其ASCT2的表达明显增加。反义RNA干扰ASCT2表达,明显抑制肿瘤细胞的生长,提示ASCT2过量表达可促进大量谷氨酰胺的吸收,为肿瘤细胞的生存提供有利条件。因而,以ASCT2为靶标筛选所得的先导化合物,很有可能成为有前景的新型靶向治疗药物。
本课题前期建立了ASCT2靶向抑制剂的高通量筛选模型,从靶向代谢通路的小分子化合物库中,已筛出ASCT2靶向抑制作用相对专一和有效的候选化合物。基于此,本课题采用分子对接技术,分析筛选出的候选化合物与ASCT2之间的相互作用,预测其结合的亲和力,同时合成目标化合物,研究其体外抗肿瘤活性,为研发新型ASCT2抑制剂提供一定的参考。
1 材料与方法
1.1 仪器与试剂
400M型核磁共振仪(德国布鲁克);LCMS8040型液质联用仪(日本岛津);酶标仪(Biotek),CCK-8试剂盒剂(碧云天试剂有限公司);其他试剂均为国产分析纯。
1.2 方法
1.2.1 目标化合物的合成
常温下,将3.02g(0.04mol)氯乙腈、27g(0.262mol)二氯二硫和15mL二氯乙烷一次性加入反应容器中搅拌反应,45min后通入氯化氢气体,反应16h后得大量的固体。抽滤、滤饼用10mL二氯甲烷洗涤,干燥后得7.09g产品,产率85%。测得化合物熔点为171.8℃~172.5℃,与文献[7]报道的172℃相符合,为目标产物4,5-二氯-1,2,3-二噻唑氯化物。然后将5mmol化合物1、10mL二氯甲烷和5mmol的2-氰基-4溴苯胺先后加入反应器中。在搅拌情况下将5mmol吡啶溶于20mL的二氯甲烷溶液并滴加到反应液中,反应8h后停止搅拌。再加入5mmol三乙胺搅拌得大量固体三乙胺盐酸盐,抽滤除去固体,滤液用水洗涤三次(20mL×3)后用无水硫酸钠干燥,过滤除去硫酸钠,所得滤液除去溶剂后得黄色固体。固体通过硅胶柱色谱分离纯化,产率90%。1H NMR(400MHz,CDCl3):δ 7.22(d,1H),7.78(dd,1H),7.87(d,1H).13C NMR(100MHz,CDCl3):δ 108.2,115.0,118.8,119.2,136.5,137.6,148.2,152.1,162.0。HRMS(ESI)m/zCalculated for [C9H3BrClN3S2+H]+:330.86,Found:330.86。图1为目标化合物的路线合成图。
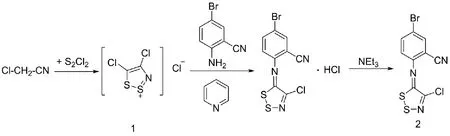
图1 目标化合物的路线合成图
1.2.2 CCK-8实验
MYCN扩增神经母细胞瘤kelly细胞、NLF细胞和胰腺癌BXPC3细胞在含有10%胎牛血清的RPMI-1640培养基中培养,结肠癌HCT116细胞和MYCN扩增神经母细胞瘤BE-2C细胞在含有10%胎牛血清的DMEM培养基中培养,所有细胞均置于5%CO2的37℃培养箱中,以1∶3的比例传代,每2d换液一次。待所有细胞生长至70%~80%消化处理,分别接种于96孔培养板中。当细胞生长到培养孔面积约80%时,分别给予0、5、15、45、135,405μmol/L的目标化合物处理48h。终止培养后,每孔加入10μL CCK-8,轻摇,37℃孵育1.5h,用酶标仪(λ=450nm)记录各孔的吸光度(OD)。取5孔OD值的平均数,按下列公式计算细胞存活率:细胞存活率(%)=处理组OD/对照组OD×100%,重复3次。
1.2.3 分子对接研究
从PDB数据库中提取ASCT2(PDB ID:6gct)蛋白文件。对接模拟前,用Pymol软件删去蛋白源文件中的配体化合物和水分子,得到一个干净的分子。采用Autodock vina软件将目标化合物与处理过的ASCT2蛋白分子进行对接,绘制结合模拟图,并评价对接结果。
2 结 果
2.1 目标化合物的合成与鉴定
合成的化合物是一种具有1,2,3-二噻唑结构的衍生物。合成反应中,通过自制的4,5-二氯-1,2,3-二噻唑与2-氰基-4溴苯胺反应制备,收率90%,此种方法步骤简单,原料便宜易得,产率高。从化合物的核磁共振氢谱可以看出,在谱图中除了目标化合物的氢和溶剂氢以外,没有其他氢,且谱图的基线平,说明产品较纯。
目前核磁共振技术(NMR)是用于化合物结构鉴定的重要方法之一[8],提供了有机化合物的结构信息,其谱图与化合物分子的结构密切相关,能反映出结构的细微差别,所以NMR可对药物进行定性鉴别[9]。因此,合成的目标化合物采用核磁共振波谱NMR表征。化合物的氢谱和碳谱分别见图2和图3。从氢谱图可以看出化合物有3个与芳香碳相连的氢,说明原料2-氰基-4溴苯胺在产物中。碳谱图在低场有9个碳,比原料2-氰基-4溴苯胺的碳原子数增加了2个,其来源于4,5-二氯-1,2,3-二噻唑的2个碳。再通过化合物谱氢图峰的化学位移和裂分分析可知,合成的化合物为目标化合物。目标化合物还经过了质谱表征,测得分子量为330.86,与理论计算值符合。

图2 目标化合物的1H NMR
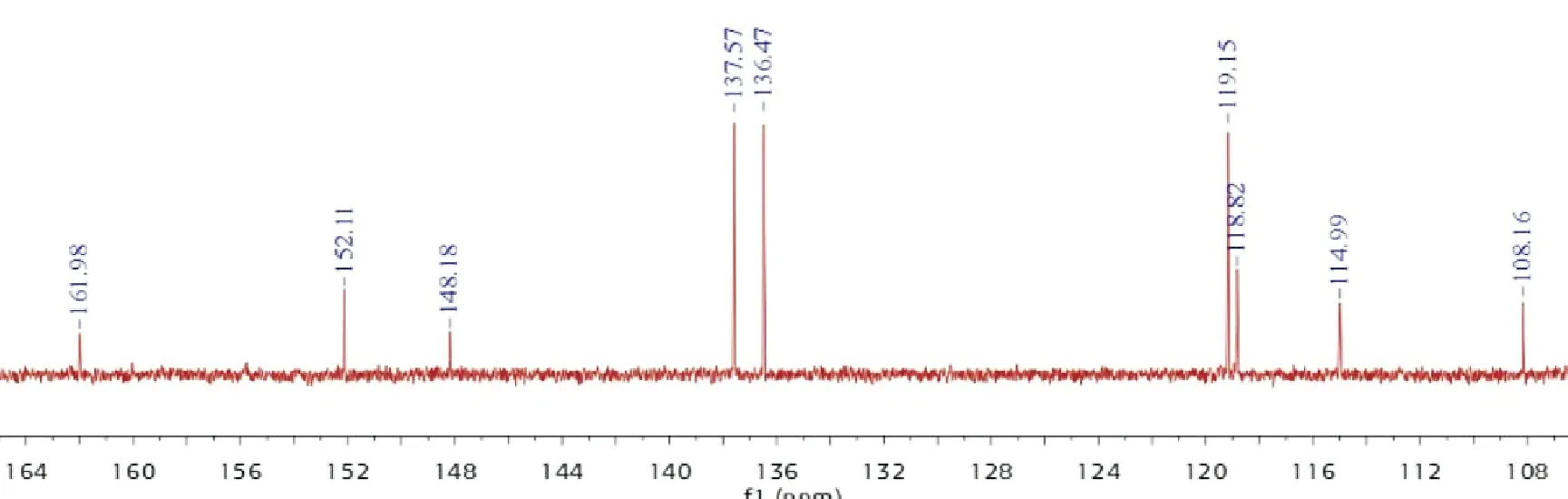
图3 目标化合物的13C NMR
2.2 计算机模拟目标化合物与ASCT2的相互作用
生物信息学和计算机模拟分子模型被广泛用于药物研发中[10]。通过计算模拟药物与蛋白靶点对接方法中最经典软件是AutoDock软件,常被用于小分子药物配体与大分子蛋白受体的对接和虚拟筛选[11]。多数情况下,小分子化合物与靶蛋白相互结合的主要部位是蛋白质上的氨基酸残基,这些氨基酸残基被认为是活性残基。氢键的形成有利于目标化合物更好地占据靶蛋白分子的活性口袋,提高与靶蛋白结合的紧密性[12]。疏水作用力也是小分子与蛋白质相互作用的一种重要方式[13]。我们的结果显示目标化合物与ASCT2蛋白的Ser354具有氢键作用,与Asn52、Ser352、Ala355、Ile431、Pro432具有疏水作用。见图4、图5。
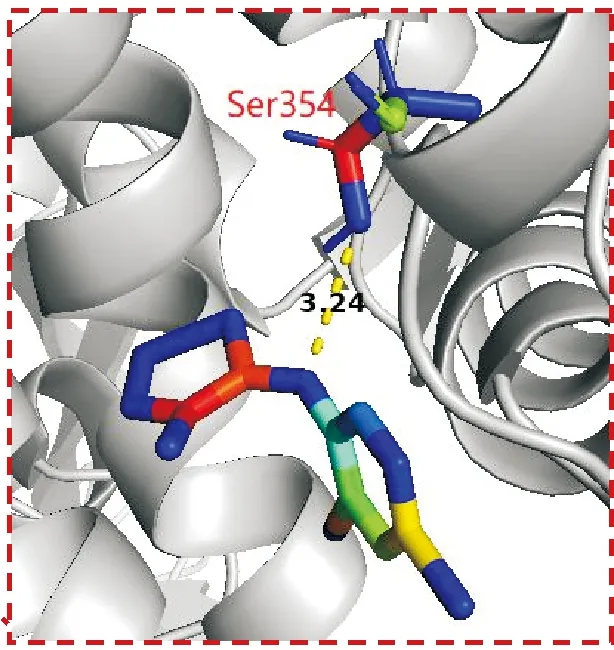
图4 目标化合物与ASCT2活性位点的立体对接图
2.3 目标化合物对肿瘤细胞增殖的抑制作用
采用CCK-8法评价目标化合物的抗肿瘤作用,结果显示目标化合物作用于MYCN扩增神经母细胞瘤kelly细胞48h,IC50值为176.4μmol/L;作用于BE-2C细胞48h,IC50值为421.1μmol/L;作用于NLF细胞48h,IC50值为270.3μmol/L;作用于结肠癌HCT116细胞48h的IC50值为78.2μmol/L;作用于胰腺癌BXPC3细胞48h,IC50值为60.33μmol/L,且随着化合物浓度的增加,细胞的活力逐渐下降,这种抑制作用呈现一定的剂量依赖关系(P均<0.05),见表1。结果表明目标化合物对不同类型的肿瘤抑制作用差异较大,对结肠癌和胰腺癌较强。
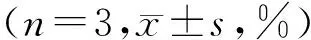
表1 不同浓度目标化合物作用肿瘤细胞后细胞存活率比较
3 讨 论
通过酮与伯胺结构化学物反应生成具有亚胺结构的目标化合物,其结构经过核磁氢谱和碳谱表征确证。进一步计算机模拟目标化合物与ASCT2的相互作用,结果表明,目标化合物能够深入到ASCT2蛋白的活性口袋中,并与活性口袋周围的氨基酸残基形成氢键,具有潜在ASCT2抑制活性;CCK-8结果显示目标化合物对肿瘤细胞具有一定的抑制作用。综上所述,目标化合物可能通过与ASCT2结合,抑制其谷氨酰胺的转运活性,发挥抗肿瘤作用,但是其抗肿瘤活性不高,可能与结合有关,因此,后续还需把合成的目标化合物结构进行优化,继续研究其靶向ASCT2的特异性和有效性。
