双腔微导管在颈内动脉慢性闭塞再通治疗中的应用
2022-05-09莫名陈忠军范铁平赵旭生胡腾李迪
莫名,陈忠军,范铁平,赵旭生,胡腾,李迪
颈内动脉闭塞是缺血性卒中的主要病因之一,通常将闭塞时间超过4周者称为慢性颈内动脉闭塞(chronic internal carotid artery occlusion,CICAO),其年发病率为6/10万[1],接受规范药物治疗后,每年仍有6%~20%的CICAO患者发生脑缺血事件[1]。闭塞动脉远端存在血流动力学改变的CICAO患者发生缺血性卒中的风险更高,每年达30%[2]。《慢性颈内动脉闭塞再通治疗中国专家共识》中推荐:对于存在明显血流动力学障碍、药物治疗无效的CICAO患者可能从血管再通治疗中获益[3]。长节段、长时间闭塞病变和钝型残端病变是目前CICAO血管内治疗的难点,成功开通率较低[4]。Kaneka双腔微导管(Kaneka dual lumen catheter,KDLC)目前已被广泛用于冠状动脉慢性完全闭塞病变的开通,其双管腔设计具备多种血管慢性完全闭塞辅助开通技术操作的空间[5]。有报道显示KDLC可提高冠状动脉慢性完全闭塞病变的开通率[6],但目前尚无KDLC应用于颈动脉慢性闭塞的报道。本研究主要观察KDLC在CICAO血管再通治疗中的应用价值。
1 对象与方法
1.1 研究对象 连续入组2020年1-12月大连市中心医院神经介入科应用KDLC进行血管再通治疗的CICAO患者。
入组标准:①年龄18~80岁;②CICAO符合《慢性颈内动脉闭塞再通治疗中国专家共识》中的定义标准[3],并经无创性血管成像或DSA证实;③具有血管内治疗的适应证:存在3个月内确定的与闭塞血管相关的症状性卒中或TIA;影像学上存在责任血管分布区的新发梗死(分水岭梗死或不超过1/3半球面积的脑叶梗死)或低灌注;经DSA检查确诊为颈内动脉节段性闭塞,闭塞远端大脑中动脉通过侧支循环代偿血管床正常;经规范的内科治疗,仍反复出现血管闭塞相关的缺血性卒中事件;④诊疗记录完整,资料齐全。排除标准:①颈内动脉急性闭塞;②术前已出现严重致残性卒中,mRS>2分;③已知的麻醉、血管再通治疗及术后规范药物治疗等相关禁忌证。
1.2 资料收集 一般资料:收集患者的年龄、性别等人口学信息,根据病历记录收集患者的血管危险因素,如高血压、冠心病、高脂血症、吸烟、酗酒等情况,记录患者发病症状、入院时NIHSS、mRS等临床特点。
影像学资料:患者术前均行头颈CTA或DSA检查,按照Lee[7]提出的CTA分型标准分类。A型:颈内动脉起始处闭塞一直向上延伸至C5段远端以上(长节段病变);B型:颈内动脉起始处闭塞一直向上延伸,终止于C5段近端或只涉及颈总动脉。颈内动脉分段方法参照Bouthillier[8]提出的分段标准。对于非急性或非责任血管卒中症状的CICAO患者行MRI PWI或CTP检查评估闭塞侧的脑血流量、脑血容量、平均通过时间及达峰时间。术中根据美国介入和治疗神经放射学学会/介入放射学学会侧支代偿分级系统评估脑动脉侧支循环[9],记录脑动脉DSA结果,观察并记录术后再通血管的前向血流mTICI分级。血管再通成功标准为术后病变处前向血流mTICI达到3级。术后依据北美症状性颈动脉内膜切除(North American symptomatic carotid endarterectomy,NASCET)研究的测量方法计算颈动脉残余狭窄率。计算公式:狭窄率=(1-颈内动脉最窄处内径/颈动脉膨大部以远正常处管腔内径)×100%[10]。
1.3 双腔微导管治疗
1.3.1 材料 KDLC(日本Kaneka Medix公司)有2个孔腔:1个端孔,是快速交换结构;1个侧孔,是同轴芯(over the wire,OTW)结构。端孔及侧孔可以分别置入直径0.014英寸(1英寸=2.54 cm)的微导丝。经侧孔走形的微导丝可以指向不同的方向,有利于寻找闭塞血管的残端(图1)。
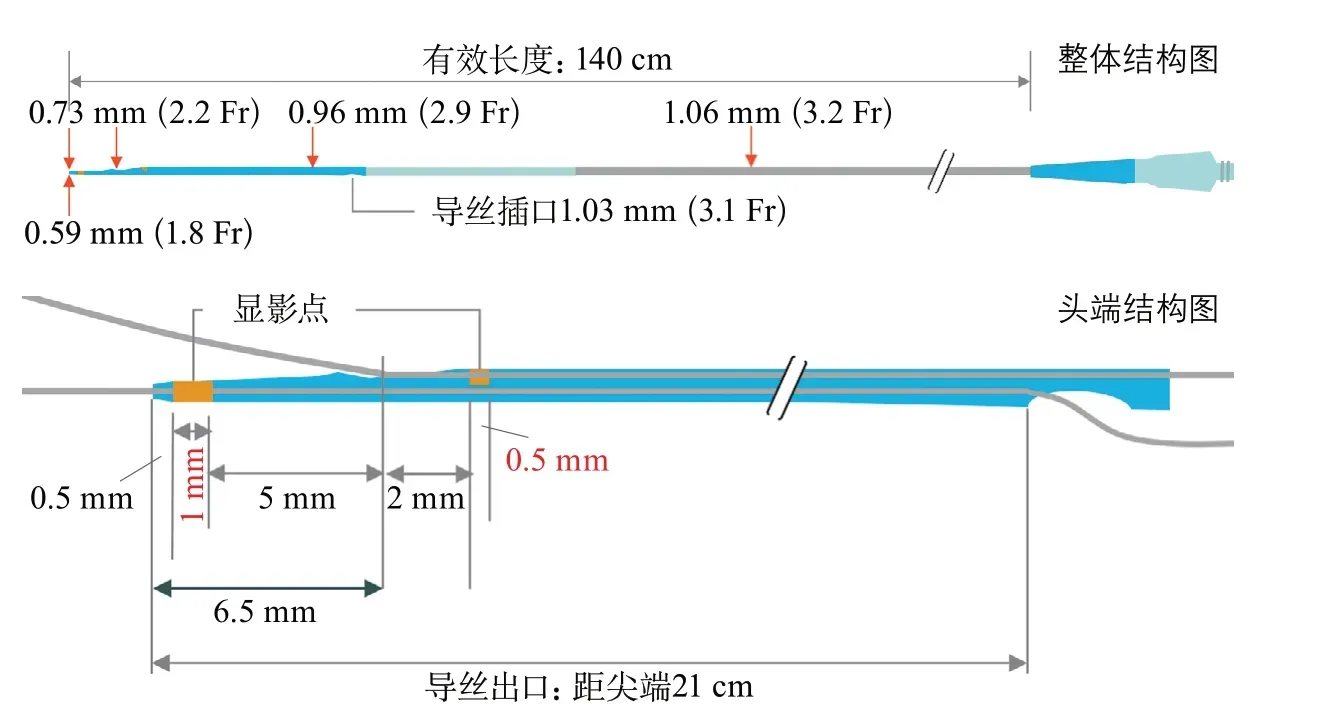
图1 Kaneka双腔微导管结构图
1.3.2 治疗方法 所有患者术前口服阿司匹林(100 mg/d)和氯吡格雷(75 mg/d),至少连续应用3 d。全身麻醉下,经右侧股动脉以Seldinger法穿刺,置入8F动脉鞘,并全身肝素化,8F导引导管(美国强生)在超滑导丝(日本Terumo Corporation)辅助下,将导引导管置于颈内动脉病变近端。沿导引导管送入5F 125 cm单弯导管及KDLC形成三轴系统(连接Y阀、三通连接管、肝素生理盐水)。根据闭塞残端形态选择不同类型的微导丝,首选Fielder XT-R或A配合KDLC轻柔突破闭塞近端的纤维帽后,小心通过闭塞的血管,经KDLC侧孔造影确认微导管远端位于正常管腔内。保留微导丝在闭塞远端正常管腔内,后撤KDLC由远及近行选择性节段性动脉造影评估闭塞段管腔全程情况。沿预留微导丝重新跟进KDLC越过闭塞远端后,沿KDLC侧孔送入第2根微导丝,撤出KDLC,沿第2根微导丝选用合适大小的球囊由远及近行预扩张后,常规行DSA评估血流情况以及是否存在血管夹层等并发症。选用合适大小的药物洗脱支架(Firebird 2代,上海微创公司)由远及近依次释放支架,根据颈内动脉闭塞近端钙化程度、与颈总动脉成角释放不同类型的颈动脉支架。根据闭塞节段及血栓机化程度如有必要置入保护伞(Spider,美国EV3公司)首先处理闭塞近端时,沿第2根导丝常规行颈动脉支架置入术,然后跟进导引导管置于颈内动脉近端,选用合适大小的药物洗脱支架(Firebird 2代,上海微创公司)由远及近依次释放支架处理闭塞远端病变。常规行DSA评估支架释放良好且远端血流通畅后结束手术。术后在抗血小板聚集治疗的同时应用低分子肝素皮下注射(4000 IU/12 h,连续3 d)。术后口服氯吡格雷(75 mg/d)至少12个月,终身口服拜阿司匹林(100 mg/d)。
1.4 随访 术后30 d、6~10个月随访,方式为门诊结合电话随访。记录术后30 d是否发生责任侧卒中事件(包括缺血性卒中和出血性卒中);3~6个月随访内容包括mRS评估功能预后,复查颈动脉超声和TCD评估支架内血流是否通畅,以及任何卒中(缺血性卒中和出血性卒中)或死亡事件。
1.5 统计学方法 本研究采用描述性方法,计量资料的离散程度用M(P25~P75)描述,计数资料以频数和率(%)描述。
2 结果
2.1 一般资料 共纳入6例患者,其中男性5例(83.3%),女性1例(16.7%),年龄43~83岁。临床表现为缺血性卒中5例(83.3%),症状为言语不清伴闭塞对侧肢体无力3例(50.0%),认知障碍1例(16.7%),眩晕伴四肢无力1例(16.7%);TIA 1例(16.7%),表现为反复左侧肢体无力。既往史:吸烟3例(50.0%),高血压2例(33.3%),糖尿病2例(33.3%),酗酒1例(16.7%),颈动脉闭塞1例(16.7%),心房颤动1例(16.7%)。DSA提示患者颈动脉慢性闭塞分型A型1例(16.7%),B型5例(83.3%)。4例进行了术前CTP或MRI PWI评估,均提示闭塞侧的脑血流量和脑血容量均有不同程度的下降,达峰时间及平均通过时间明显延长。DSA结果均显示颈内动脉慢性闭塞,2例(33.3%)可见软膜支或颈外动脉吻合支代偿颈内动脉,2例(33.3%)可见后交通动脉代偿,2例(33.3%)可见前交通动脉代偿(表1)。
2.2 手术结果和并发症 6例患者使用KDLC血管内治疗均再通成功,mTICI达到3级。术后2例(33.3%)残存狭窄<20%,4例(66.7%)残存狭窄<10%。无术后30 d责任侧卒中事件(表1)。
随访结果:6例患者术后6个月的mRS评分中位数为0.5(0~1.0)分。6例患者术后6个月内均复查了颈动脉超声或TCD,均显示支架内血流通畅,随访期内无新发卒中事件(表1)。
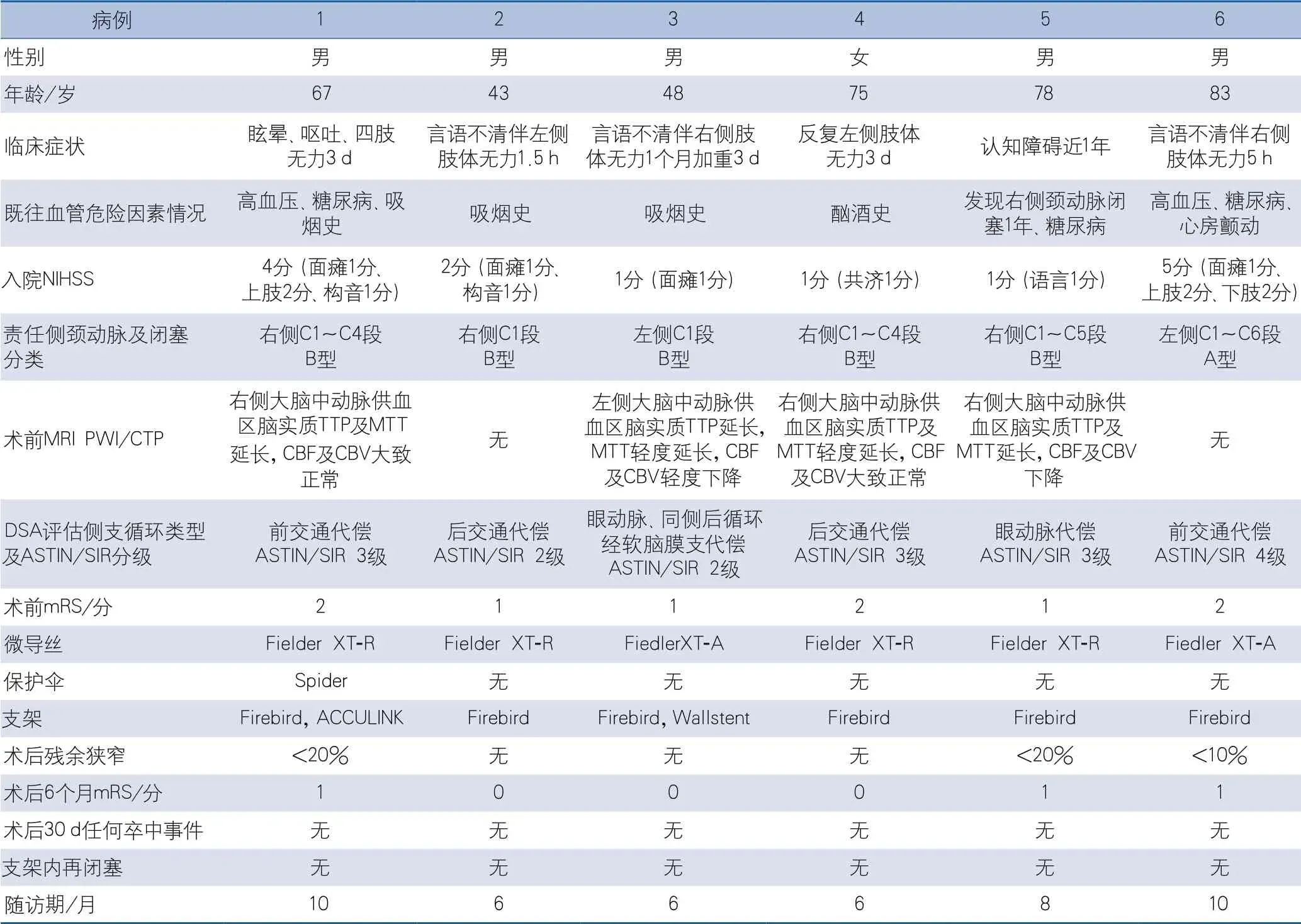
表1 患者临床资料及随访结果
2.3 典型病例介绍 3号病例,48岁,男性,临床表现为言语不清伴右侧肢体无力1个月,加重3 d,术前mRS 1分。术前MRI DWI显示左侧额颞顶叶及岛叶、侧脑室旁多发梗死灶。头颈部CTA及DSA证实左侧颈内动脉闭塞,闭塞类型B型,侧支循环代偿途径为眼动脉逆向代偿颈内动脉C4段。MRI灌注成像证实左侧大脑半球广泛低灌注。血管内治疗简要过程:将8F导引导管置于颈内动脉病变近端,选择Fielder XT-A微导丝配合SL-10微导管尝试通过左侧颈内动脉起始部闭塞段未成功,微导丝反复进入假腔。更换为KDLC,沿假腔内微导丝将KDLC送至闭塞段,通过其快速交换腔重新应用XT-A微导丝小心探索真腔,以假腔内微导丝为定位标志(平行导丝技术),操控XT-A微导丝反复尝试后于C2段近转弯处进入真腔,后经OTW腔造影确认微导管远端位于正常管腔内。撤出位于假腔的微导丝和KDLC,沿位于真腔的XT-A微导丝将SL-10微导管送至C3段,冒烟确认其在真腔内。路径图下,更换Synchro(0.014英寸×300 cm,美国史赛克公司),微导丝配合SL-10留置于大脑中动脉M2段远端,撤出SL-10交换为KDLC,缓慢后撤KDLC经OTW腔造影证实颈内动脉C1段至C3段闭塞。撤出KDLC后,沿微导丝送入Gateway(2.0×15 mm)球囊、Maverick(3.0×20 mm)由远及近预扩,复查造影见血管再通,但管腔内多处残余狭窄及机化血栓。在球囊辅助下将Guidezilla支撑导管送至C1段增加支撑力,沿微导丝由远及近置入Apollo(3.0×18 mm)、Apollo(3.0×18 mm)、Firebird(3.5×35 mm)、Firebird(4.0×35 mm)支架,复查造影提示前向血流通畅,mTICI 3级,远端分支无栓塞,观察30 min后复查造影同前并终止手术(图2)。术后规范药物治疗,出院前mRS 1分。术后随访6个月期间无新发缺血性卒中事件,术后第4个月复查颈动脉超声/TCD显示支架内血流通畅。
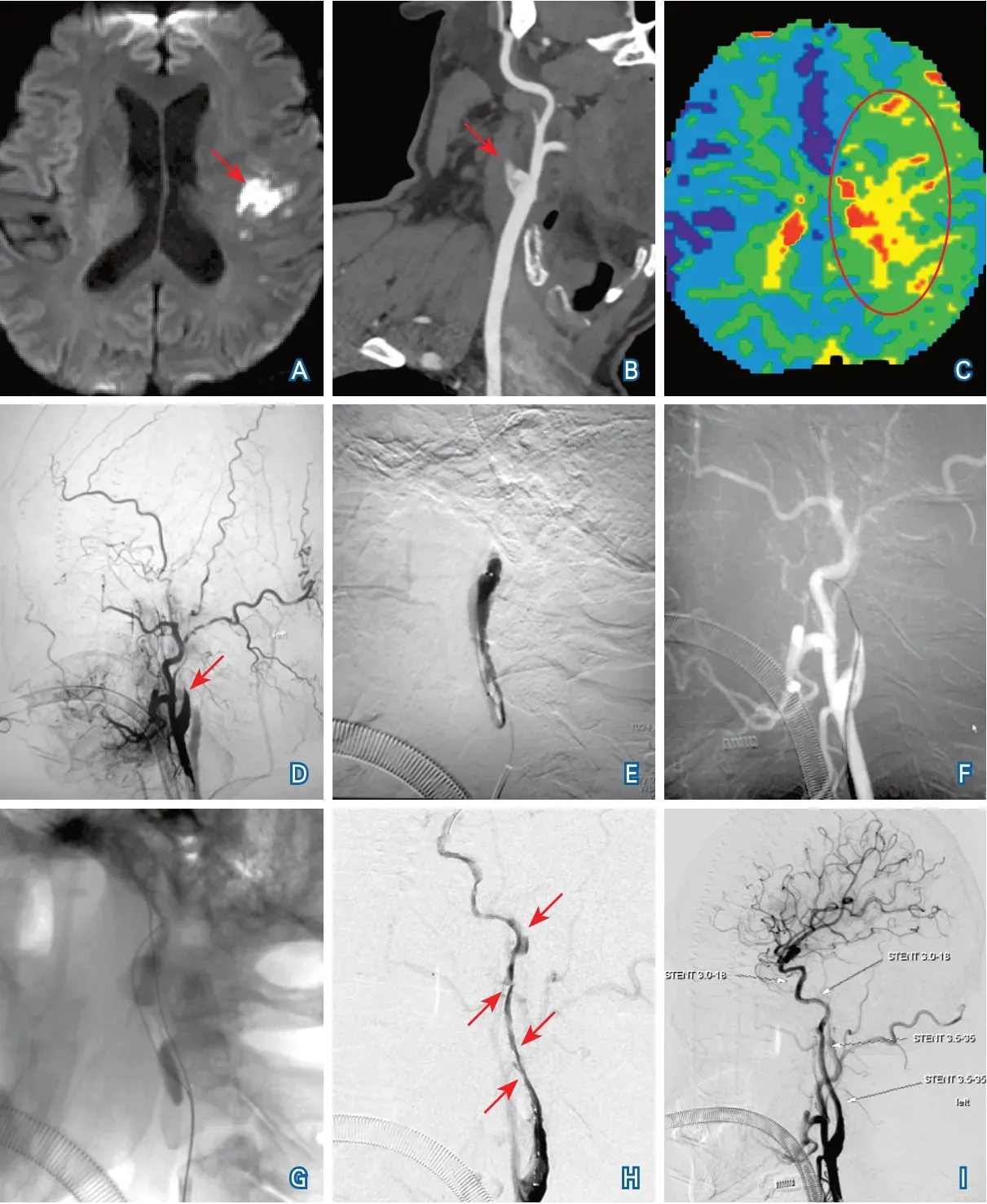
图2 左侧颈内动脉起始部慢性闭塞患者影像学资料
3 讨论
CICAO是引起缺血性卒中的主要原因之一,发病机制主要为脑组织低灌注、栓子清除能力下降及动脉-动脉栓塞[11]。血管内治疗具有创伤性小、手术并发症少、安全性和成功率高的优势,尤其适用于长节段闭塞病变。KDLC被广泛用于冠状动脉慢性闭塞的治疗中,本研究通过收集使用KDLC进行血管内治疗的CICAO患者的临床和影像资料,观察术中血管再通情况、术后30 d卒中事件发生情况以及术后随访期间支架再闭塞率等指标,对KDLC用于血管内治疗CICAO的安全性和有效性进行初步研究,并获得一定体会。
如何提高CICAO开通率以及降低术中栓塞事件风险是目前研究的热点问题。多角度投影、根据闭塞残端血管形态选择不同类型的微导丝、微导管低压节段性血管造影显示导丝路径等均可减少术中血管壁的损伤[12]。一项包含41例接受血管内治疗的CICAO患者的研究结果显示:术前CTA显示返流至床突段及以上的患者,其技术成功率、主要并发症发生率、1年血管再闭塞率分别是52%、22%和91%;而返流至床突段以下患者的技术成功率为89%,未出现主要并发症和1年血管再闭塞[7],表明长节段闭塞的手术难度及风险相应增加。在以往神经介入手术中,使用单腔微导管对目标血管行选择性造影时需由远及近逐渐将微导管头端撤出闭塞段以外,微导丝再次通过闭塞段增加了损伤血管壁及误入假腔的风险。本研究尝试利用KDLC解决开通长节段闭塞时导丝误入假腔问题,此方法尚无先例报道。在本研究中,全部6例患者术中均通过KDLC OTW导管腔缓慢注射造影剂评估闭塞管腔形态及走形,预留的微导丝可直接输送治疗器械,避免再次置入,简化了手术流程,也降低了操作相关的并发症发生风险。本研究全部6例患者术中未发生远端栓塞事件等并发症,可能与减少微导管反复穿过闭塞段次数有一定相关性。
CICAO血管再通治疗过程中,当闭塞远端血管有足够的区域时,可以放置滤网降低血栓碎片脱落导致远端栓塞的风险。目前常选用通过导丝引导的滤网,如Spider,但Spider滤网释放步骤要求外套导管到位后撤出微导丝,当C1段血栓负荷较大时,回收滤网过程中可能导致部分血栓外溢造成栓塞,但出现此类并发症需重复微导丝通过闭塞段的操作步骤,而应用KDLC能够预留1根微导丝在闭塞段远端真腔血管中,提高了处理突发栓塞事件的应变能力。CICAO血管再通治疗过程中当微导丝误入假腔时,常需使用平行导丝技术(图3)重回血管真腔,KDLC OTW导管腔出口端的凹凸结构使微导丝头端行进方向存在5 °的偏移,有助于第2根微导丝避开假腔破口寻找真腔,在本研究中3号病例治疗过程中,使用KDLC配合头端自带45 °成角的Gaia微导丝成功实现了血管再通,一定程度上展现了KDLC配合相关技术对动脉夹层等复杂病变的处理能力。
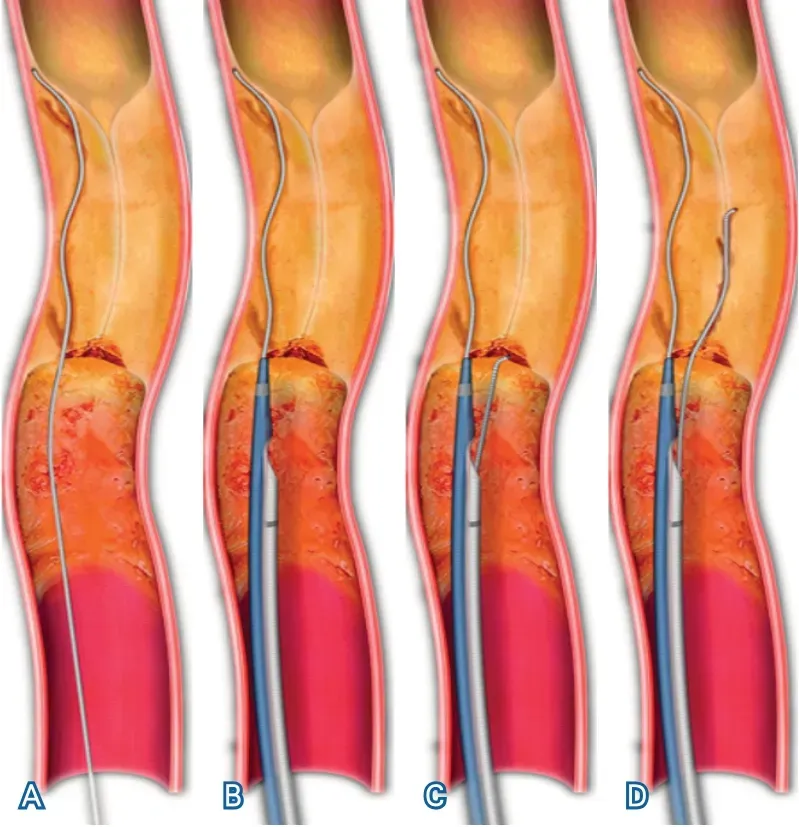
图3 平行微导丝技术图解
本研究中应用KDLC在CICAO血管再通治疗过程中的诊疗体会:①第1根微导丝通过闭塞段后可沿KDLC置入第2根微导丝,降低第2根微导丝通过闭塞段的难度以及误入假腔的风险;②可经KDLC OTW导管腔行选择性节段性动脉造影以便仔细评估闭塞段管腔全程情况;③可经KDLC OTW导管腔局部给药进行接触性动脉溶栓;④双微导丝可增强导引导管的支撑力,必要时可更换1根微导丝为支撑力更强的导丝,若支撑力仍然不足,可以应用Guidezilla延长导管增加整个系统的支撑力并提高支架通过性;⑤可经1根微导丝实施小球囊远端保护,沿另1根微导丝实施闭塞段球囊扩张及支架置入;⑥可经1根微导丝放置Spider滤网,即使滤网回收后,仍保留另1根微导丝在闭塞段远端正常血管中;⑦当使用平行导丝技术时,KDLC OTW导管腔出口端的凹凸结构有利于第2根微导丝避开假腔破口寻找真腔,而且经KDLC OTW导管腔行选择性节段性动脉造影有助于确定假腔破口位置。
本研究中,KDLC用于CICAO的血管内治疗可能是一种有效、操作简单、可靠的方法,一定程度上提高了闭塞血管的开通率(包括长节段病变),简化流程以降低操作相关的并发症的发生风险。但本研究样本量较小,所得出的结论在普适性方面尚有不足。整合不同领域开通慢性闭塞病变的经验、技术和器械是提高CICAO介入治疗成功率的关键因素之一,KDLC的应用还需要积累更多的经验。
【点睛】本研究首次对双腔微导管应用于颈内动脉慢性闭塞病变血管再通治疗的效果和安全性进行了描述,为此类患者的治疗提供了技术上的新思路。
