稀土离子在KMnF3 纳米晶复合玻璃中的微观分布机理*
2022-04-27李文豪谢玉清石海征芦鹏飞任晶
李文豪 谢玉清 石海征 芦鹏飞 任晶†
1) (哈尔滨工程大学物理与光电工程学院,哈尔滨 150001)
2) (北京邮电大学光电信息学院,北京 100876)
具有单(纯)色上转换荧光发射特性的发光材料,有望在三维显示、照明、生物成像、促进植物生长以及提高太阳能电池光电转换效率等领域得到应用,受到研究人员的广泛关注.本研究通过玻璃热处理析晶的方法,在稀土离子Yb3+/Er3+共掺的氟硅酸盐玻璃中原位生长出了钙钛矿型的KMnF3 氟化物纳米晶体,并观测到了显著增强的高单色性上转换红色发光.采用具有高分辨率的透射电子显微测试分析技术和第一性原理计算相结合,研究了稀土离子在KMnF3 纳米晶复合微晶玻璃中的掺杂机制,并讨论了稀土离子微观分布和能量传递效应对其上转换发光性能的影响.实验结果表明:稀土离子将通过优先取代KMnF3 晶体中K+格位的方式选择性富集在具有低声子能量的氟化物纳米晶体中,并由此获得显著增强的上转换发光强度.
1 引言
具有高效单(纯)色上转换发光特性的材料,特别是发光波段位于红色和近红外波段的上转换发光材料在三维全彩色显示、精确分子谱分析、高分辨率生物成像、促进植物生长以及提高太阳能电池光电转换效率等领域均具有潜在的应用价值[1].稀土离子(Er3+,Tm3+,Ho3+)掺杂的钙钛矿型氟化物晶体AXF3(A=Na,K,Rb,Cs;X=Mg,Zn,Mn,Cd),具有实现高效上转换发光所必须的低声子能量环境[2,3],特别是当X=Mn2+时,AMnF3晶体能通过能量传递的方式调控稀土离子上转换发光颜色,获得单色上转换发光,得到了各国研究人员的广泛关注[4−6].然而,AMnF3晶体难以光纤化或制成大型单片光学器件,极大地限制了其在光通信和集成光学等领域的应用[7].将化学合成的稀土离子掺杂AMnF3纳米晶体分散(镶嵌)在聚合物中可以制备有源光波导[7].但在高功率激光辐照时,由于聚合物光、热稳定性相对较差,导致基于聚合物的上转换发光材料性能发生难以逆转的退化,无法满足长期稳定使用的要求.
由于玻璃在热力学上处于亚稳状态,因此对玻璃进行热处理,即在稍高于玻璃化转变温度保温一定的时间,可以在玻璃基质中原位生长出纳米尺度的晶体[8,9].这种通过可控热处理析晶方式制备的纳米晶复合微晶玻璃,集晶体和玻璃的优势于一体,可广泛用于固态照明[10]、随机激光[11]、光学测温[12−14]和闪烁体[15−17]等领域,一直以来是光功能玻璃领域的研究热点.目前,已有研究证明了在氟硅酸盐玻璃体系中生长AXF3纳米晶的可行性,并发现在微晶玻璃中过渡(Mn2+,Ni2+)和稀土金属离子(Yb3+)的发光强度将显著增强[18−20].由于AXF3晶体中X2+格位与过渡金属离子在化学价态和离子半径方面匹配度较高,所以一般认为在热处理过程中,玻璃中掺杂的过渡金属离子会通过取代X2+的方式富集在晶体中,由此获得必需的晶体配位环境和发光增强.但稀土离子与X2+在价态和离子半径上差异较大,因此,对于稀土离子在AXF3纳米晶复合微晶玻璃中的分布倾向和掺杂机制尚存在较大的争议.对此,我们制备了稀土离子掺杂KMnF3纳米晶复合微晶玻璃,不但从实验角度直观给出了稀土离子在微晶玻璃中的微观分布情况,并通过第一性原理计算分析了稀土离子取代KMnF3晶体不同阳离子晶体格位的可能性.研究成果对于设计和开发具有高效单色上转换发光性能的材料具有一定的理论指导价值.
2 实验与测试
通过传统高温熔融淬冷法制备玻璃样品,组成为(摩尔百分数)70SiO2-15KF-15MnF2-1SnCl2-1YbF3-0.2ErF2,其中,还原剂SnCl2的引入可有效避免Mn2+被氧化成Mn3+而引起玻璃强烈着色.将高纯原材料(99.99%)按照组成配比精确称量后在玛瑙研钵中充分研磨混合,随后盛入高纯(99.9%)刚玉坩埚中,放入已经升温到1550 ℃的高温电炉中,在空气气氛下,融制35 min 后浇筑在300 ℃预热的铜板上淬冷.随即转移至精密退火炉中,在400 ℃保温3 h,得到前驱体玻璃(precursor glass,PG).最后,将前驱体玻璃在550 ℃下热处理10 h 得到微晶玻璃(glass ceramic,GC).将样品切割成1 cm×1 cm×0.2 cm 的薄片并进行表面抛光后备用后续测试.需要指出的是,我们研究了不同热处理温度下样品的析晶情况.结果发现样品在450 ℃和500 ℃下热处理不析晶,但若将热处理温度提高到600 ℃,则样品发生着色,可能是由于二价锰离子在高温下被氧化为三价锰离子.同时还发现600 ℃热处理的样品光学透过性较差,在玻璃表面出现析晶条纹,因而,考虑到实际应用中对玻璃光学质量的要求,没有对高温下热处理样品进行更深入的研究.
利用 X 射线衍射仪(Shimadzu,LabX XRD-6100)测试样品的X 射线衍射图;采用日本津岛公司的型号为UV-2450 的UV-VIS 分光光度计测试样品的透过光谱;采用PTI QuantaMasterTM 8000荧光光谱仪(Horiba,Canada)测试样品的光致发光(photoluminescence,PL)、荧光衰减和发光量子效率,在反射模式下进行光谱测量,入射光与样品表面法线夹角为45°.采用美国FEI 公司的FEI Talos F200x 型扫描透射电子显微镜(配备能谱仪,energy-dispersive spectrometer,EDS)测试微晶玻璃样品中纳米晶体的形貌及元素的分布情况.透射电镜测试的样品为特制的离子减薄后的样品,离子减薄所使用的仪器为美国GATAN 公司生产的型号为GATAN PIPS Ⅱ 695 的精密离子减薄仪,具体可参考课题组前期工作[21].
使用基于密度泛函的第一性原理计算方法仿真包Vienna Ab-initio Simulation Package (VASP)进行理论计算[22],其芯态用赝势缀加投影波(projector augmented wave,PAW)或超软赝势(ultrasoft pseudopotentials,USPP)来描述,电子波函数由一系列的平面波函数展开.采用局域态密度近似(local density approxiamtion,LDA)[23]或广义梯度近似(general gradient approximation,GGA)[24]来描述离子和电子的交换关联作用.在计算过程中,使用的赝势是赝势缀加投影波(projector augmented wave,PAW),离子和电子之间的交换关联作用采用Perdew and Wang 91 方案.平面波基矢的截断能设置为520 eV,结构优化采用准牛顿算法进行离子弛豫,力收敛标准设置为5 × 10–2eV/Å,总能计算中允许的能量误差设置为10–4eV,系统总能量和电荷密度在Brillouin 区的积分计算使用的k网格点为8 × 8 × 6.
3 结果与讨论
3.1 稀土离子微观分布与上转换发光性能
热处理前后玻璃样品的X 射线衍射图如图1(a)所示,其中,前驱体PG 样品为典型的馒头峰,意味着样品为非晶态;而热处理后微晶玻璃GC 样品衍射图中可以看到明显的衍射峰,这表明样品中有晶体析出.通过对比晶体的标准X 射线衍射卡片(卡片号:PDF#17-0116),可以判断析出的晶体为KMnF3.通过透射电镜测试发现微晶玻璃中析出均匀分布、平均粒径为20 nm 的纳米颗粒(图1(b)).一般减薄后样品厚度为50 nm,根据透射电子显微镜(TEM)照片晶体含量并假设晶体为边长为20 nm 的正方体,则估算样品晶化率为15%.从高分辨电镜图中可以清晰地看到晶格条纹(图1(c)),表明析出的纳米颗粒具有优良的结晶性,晶格条纹间距为0.3083 nm,与KMnF3晶体的d(1 1 0)晶面间距接近(0.2962 nm),进一步证实了微晶玻璃中析出了KMnF3纳米晶体.利用透射电镜配备的能谱仪(EDS)测试了稀土元素在微晶玻璃中的微观分布情况,结果如图1(e)和图1(f)所示,可以直观地看出稀土元素Er 和Yb 均优先富集在了纳米晶体所在的区域.
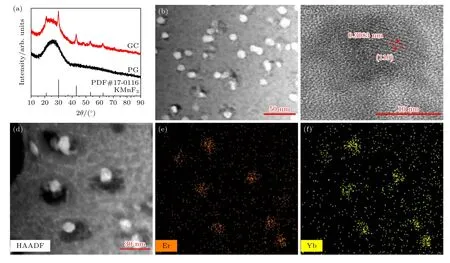
图1 (a) 前驱体玻璃PG 和微晶玻璃GC 样品以及KMnF3 晶体(PDF#17-0116)的X 射线衍射图;微晶玻璃样品的 (b) 暗场和(c) 高分辨TEM 图像;(d) 高角环形暗场电镜图像;能量仪测试GC 样品中稀土离子 (e) Er 和 (f) Yb 分布.不同颜色的深度与元素的浓度正相关Fig.1.(a) X-ray diffraction (XRD) patterns of the precursor glass (PG) and the glass ceramic (GC) samples.Also shown is the standard XRD pattern of the KMnF3 crystal (PDF#17-0116);(b) dark field and (c) high resolution TEM images of the GC sample;(d) high-angle-annular-dark-field (HAADF) TEM image of the GC sample,and the corresponding elemental mappings of (e) Er and(f) Yb,with their concentrations reflected by the brightness in colors.
考虑到实际应用中对发光材料透明度的要求,测试了样品的透过光谱,如图2(a)所示.从图2(a)可以看出,热处理前后玻璃样品均保持了良好的透过性能(图2(a)插图).与前驱体玻璃PG 样品相比,微晶玻璃GC 样品透过率略有下降,这主要源于晶体与玻璃基质折射率差引起的光散射.透过光谱中位于352 nm 和415 nm 的吸收峰源自Mn2+从6A1(6S) 基态到4T2(4D)和4A1-4E (4G)激发态的跃迁[25],位于520,650 和1530 nm 的吸收峰源于Er3+离子4I15/2基态到2H11/2,4F9/2和4I13/2激发态的跃迁,位于970 nm 的吸收峰源自Yb3+:2F7/2→2F5/2和Er3+:4I15/2→4I11/2电子跃迁[26].当用功率密度为1 W/cm2的976 nm 近红外激光作为激发光源时,可以观测到样品发出耀眼的红光(图2(c)中插图).相比于前驱体玻璃,微晶玻璃样品在658 nm 处的红光发射强度增强了6 倍.尽管在微晶玻璃的荧光光谱中还能观测到微弱的绿光,但由于红光和绿光强度比高达30,因此样品表现出了较为理想的上转换发光单色性.图2(c)左上角插图以log-log 方式给出了上转换发光强度随激光功率的变化趋势,通过线性拟合获得曲线斜率为1.92,表示上转换发光对应于双光子吸收.图2(b)显示了Mn2+如何通过能量传递的调制稀土离子上转换发光:首先Yb3+作为激活剂,电子从2F7/2基态吸收激发光能量后跃迁至2F5/2激发态,随后将能量传递给Er3+能量相近的4I11/2激发态,此时,Er3+能够再接受一份Yb3+传递的能量被进一步激发到能量更高的4F7/2激发态,然后通过多声子弛豫的方式回落到2H11/2和4S3/2能级,最后在向基态4I15/2跃迁的过程中产生上转换绿光发射.从图2(b)可以看到,由于Er3+的2H11/2和4S3/2能级位置与Mn2+的4T1能级匹配,因此,能量会由Er3+传递给Mn2+并通过交叉弛豫等方式被损失掉,从而起到淬灭Er3+上转换绿光发射的作用;另一方面,Er3+的4I11/2能级上的电子也可以通过多声子弛豫首先回落到4I13/2能级,并进一步吸收一份从Yb3+传递的能量跃迁至4F9/2能级,最后在向基态跃迁的过程中产生上转换红光发射[5].相比于SiO2玻璃基体声子能量为1100 cm–1[26],KMnF3晶体的声子能量仅为330 cm–1[27],因此,微晶玻璃上转换发光强度增强主要源自稀土离子选择性的富集在氟化物纳米晶体中,一方面由于间距的缩短有效提高了稀土离子之间的能量传递效率,另一方面氟化物晶体较低的声子能量有助于抑制多声子弛豫引起的发光淬灭[28].最后一点也能够从样品荧光寿命的测试中得到印证,如图2(d)所示,微晶玻璃的上转换红光发射衰减速率明显慢于前驱体玻璃,证明了稀土离子在微晶玻璃中具有更低的多声子弛豫速率.
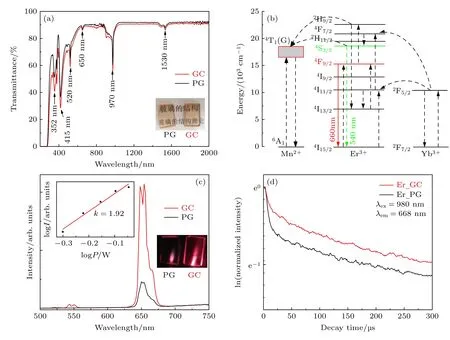
图2 (a) 前驱体玻璃PG 和微晶玻璃GC 的透过光谱;(b) Mn2+调制 Yb3+/Er3+上转化发光示意图;(c) 样品的上转换荧光发射光谱;(d) 样品的668 nm 荧光的衰减曲线.激发光源为功率密度为1 W/cm2 的976 nm 半导体激光器.(c)中插图为样品上转换发光照片以及上转换发光强度随泵浦激光功率变化,红线为对数据进行线性拟合Fig.2.(a) Transmission spectra of the PG and GC samples;(b) schematic energy-level diagram illustrating the energy transfer processes between Mn2+,Yb3+ and Er3+;(c) up-conversion luminescence (UCL) spectra of the samples.The excitation source is a 976 nm laser diode (LD) with a power density of 1 W∕cm2.Inset images:photos of the samples taken under the irradiation of a 976 nm LD and the log-log plot of UCL intensity vs.the excitation light intensity;(d) decay curves of the 658 nm red UCL emission of the samples.
上述内容从实验角度说明了KMnF3以纳米晶体的形式存在于玻璃中,且稀土离子选择性分布于KMnF3晶体中,但仅仅通过实验无法充分解释稀土离子与KMnF3晶体相互作用的关系,下面将利用第一性原理计算对稀土离子的掺杂机制进行分析.
3.2 第一性原理计算分析稀土离子掺杂机制
首先,进行KMnF3单晶胞电子结构计算,所用的晶体空间群为Pnma,构建2 × 2 × 2 超胞的理想模型如图3 所示;随后,构建稀土离子RE3+(Ho3+,Er3+,Tm3+,Yb3+)取代理论模型并设置边界条件完成晶体结构的优化;然后,用优化后的结构进行静态自洽计算,得到体系的掺杂形成能和结合能;最后,在保持电荷密度不变的情况下进行非自洽计算,得到体系的电子态密度(density of state,DOS)和分波态密度(partial density of state,P DOS).
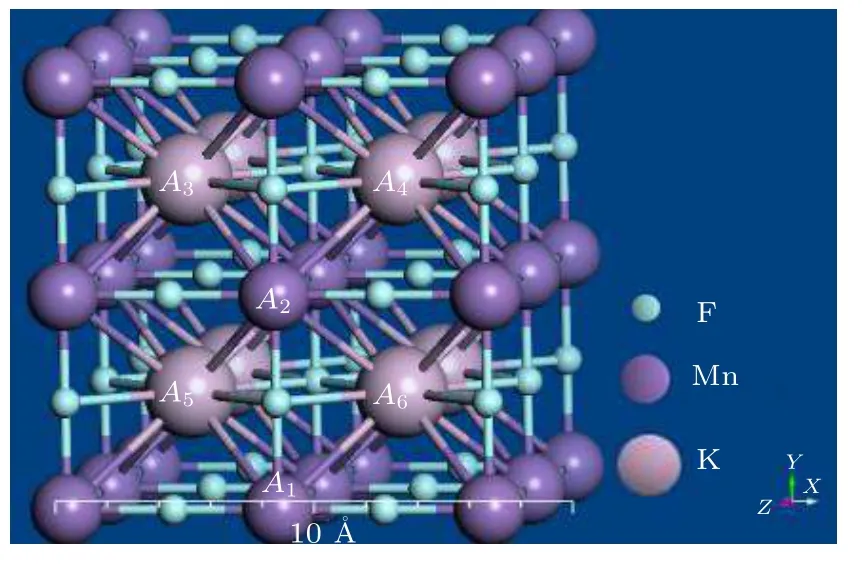
图3 计算采用的KMnF3 晶胞Fig.3.The crystal structure of KMnF3 used for the calculation.
从晶体结构可以看出(图3),K+为八配位,Mn2+为六配位,在晶胞中存在2 个Mn2+(A1,A2)和4 个K+(A3,A4,A5,A6)阳离子格位.由于稀土离子价态为+3,当取代晶胞中阳离子后,会产生电荷不匹配问题,考虑到KMnF3晶体在微晶玻璃中的生长环境为富F–环境,F–可以通过热扩散进入晶体中起到电荷补偿作用[29],即通过形成K(1–x)RExMnF(3+x)和KRExMn(1–x)F(3+2x)(x=0.25)结构实现电荷补偿[30].当用Er3+取代Mn2+的A1和A2格位后,计算获得的体系总能分别为–118.833 eV 和–118.845 eV;取代四个K+的格位后,得到的体系总能分别为–130.111 eV,–129.923 eV,–130.057 eV和–130.038 eV.不同取代位之间的体系总能差均在±0.188 eV 之间,因此,后续计算仅考虑RE3+选取Mn2+/K+的A1/A3格位的情况.掺杂结合能Eb(RE3+→ Mn2+)和Eb(RE3+→ K+)以及形成能Ef(RE3+→ Mn2+)和Ef(RE3+→ K+)的计算方法如下[31]:
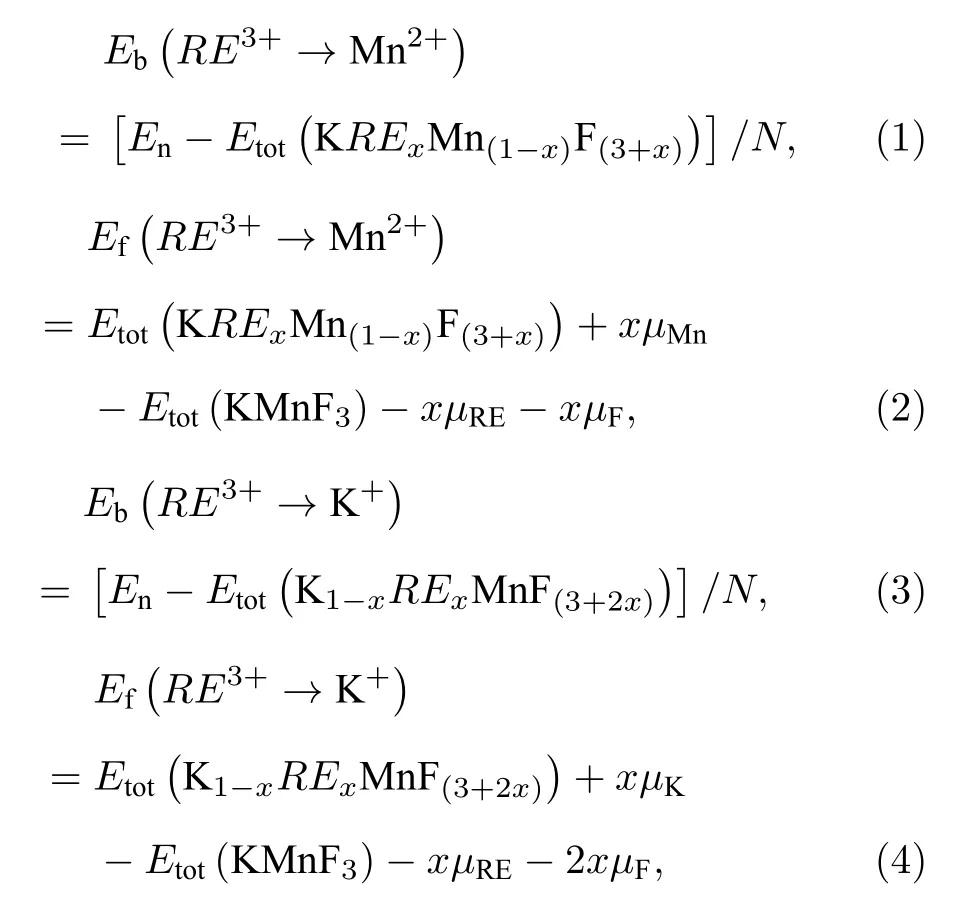
式中,En为体系所有原子的化学势能的总和;Etot(KMnF3),Etot(KRExMn(1–x)F(3+x))和Etot(K1–x RExMnF(3+2x))分别为纯KMnF3,RE3+取代Mn2+和K+后的体系总能,µMn,µK,µF和µRE分别为Mn,K,F 和稀土原子的化学势.
图4 是不同稀土离子取代KMnF3中Mn2+和K+的结合能和形成能.一般而言,晶体结合能越高则对应的晶体结构越稳定,稀土离子取代K+的结合能略高于取代Mn2+的情况(图4(a)和图4(b)),说明取代K+后可以形成更稳定的结构.从图4(c)和图4(d)可以看出,所有形成能均为负值,这说明取代后形成的结构很稳定,不会产生分相.稀土离子取代K+的形成能远低于取代Mn2+的情况,这主要是因为八配位K+离子半径(约为142 pm[32])大于六配位Mn2+离子半径(约为67 pm[32]),约为Mn2+离子半径的2.12 倍,较大的K+晶体格位更有利于稀土离子掺杂取代.比较不同稀土离子掺杂KMnF3晶体的形成能,可以发现,形成能与稀土离子的半径密切相关,Ho3+,Er3+,Tm3+,Yb3+在八配位环境下离子半径分别为101.5,100.4,99.4,98.5 pm[32],而稀土离子半径越小,取代倾向越强,其中Yb3+具有最低的形成能,说明其掺杂倾向最高.
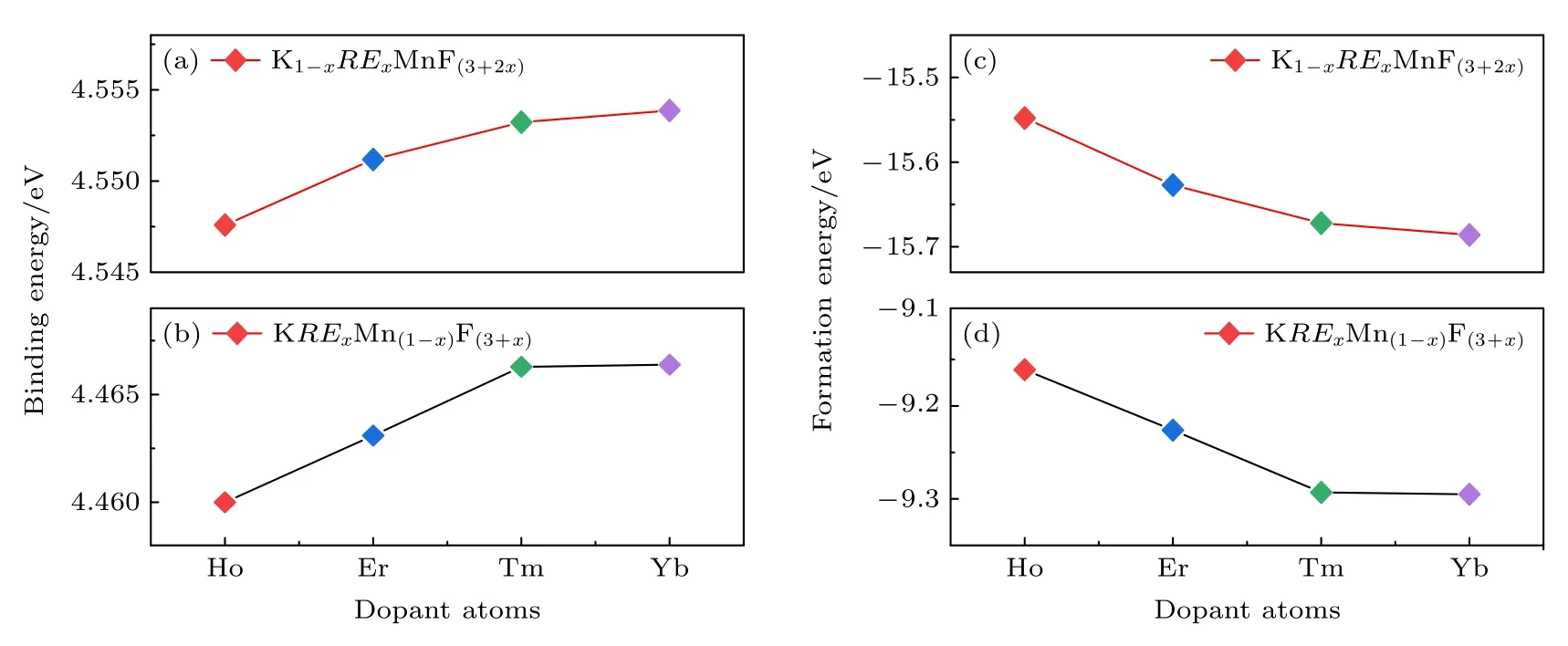
图4 稀土离子RE 3+取代KMnF3 晶体中Mn2+和K+晶体格位的(a),(b)结合能和(c),(d)形成能Fig.4.(a),(b) Binding and (c),(d) formation energies of rare earth ions RE 3+substituting for Mn2+ and K+ in the KMnF3 crystal.
通过非自洽计算可以得到稀土离子取代KMnF3中Mn2+和K+后的态密度图(以费米能级为能量零点),如图5 所示.从图5 可以看到:稀土离子取代晶体中Mn2+的A1位置后,价带顶和导带底处的电子态密度均有所增加,且导带底电子态密度增加更为明显(图5(a));当稀土离子取代晶体中K+的A3位置后,晶体价带顶和导带底处的电子态密度也有所增加,但与A1位置取代不同的是,A3位置取代使得价带顶的电子态密度增加更为显著(图5(b)).

图5 稀土离子RE 3+取代KMnF3 晶体中(a) Mn2+和(b) K+晶体格位后晶体的总电子态密度(TDOS)Fig.5.Total density of electronic states (TDOS) of rare earth ions RE 3+substituting for (a) Mn2+ and (b) K+ in the KMnF3 crystal.
从以上的讨论中可知,稀土离子倾向于通过取代KMnF3中K+晶体格位进行掺杂.下面以Er3+掺杂为例,说明不同元素对电子态密度的贡献.图6(a)为晶体的总电子态密度图,当Er3+取代K+后,晶胞导带底电子态密度主要由掺杂的Er3+贡献(图6(c)),而价带顶电子态密度主要由Mn2+贡献(图6(b)).从轨道的分波态密度可知,晶体价带顶处的贡献主要源自Mn2+的3d 轨道,而导带底处的贡献主要由Er3+的4d 轨道所提供.从Er3+轨道分波态密度可以看到,其4p 和5d 轨道的跨度较大,有较强的离域性,说明稀土离子在KMnF3中具有较强的成键倾向.对比F–的态密度(图6(d)),不难发现,在–8 —–6 eV 区间内,Er3+的4p 和5d 轨道与F–的2p 轨道有较高的态密度重叠.这三条轨道的杂化使得晶体总的电子态密度在–8.9 —–5.6 eV区间内出现了宽的共振峰(图6(a)),这也印证了F–与Er3+之间具有较强的成键性.
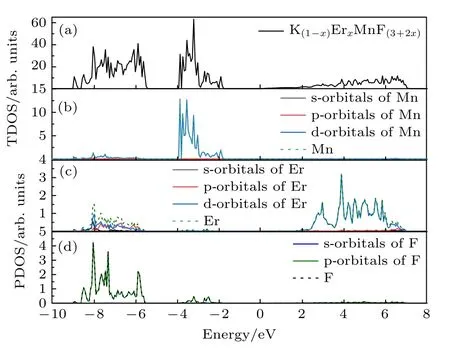
图6 (a) Er 3+取代KMnF3 中K+晶体格位后晶体的总电子态密度(TDOS);(b) Mn 电子态密度图与Mn 的3d,3p 和4s 轨道的分波态密度(PDOS);(c) Er 态密度图与Er 的4d,5p和6s 轨道的分波态密度;(d) F 态密度图与F 的2p 和2s 轨道的分波态密度Fig.6.(a) Total density of electronic states (TDOS) of Er 3+substituting for K+ in the KMnF3 crystal;(b) DOS of Mn(green dotted line) and partial density of states (PDOS) of the Mn 3d,3p,4s orbitals;(c) DOS of Er DOS and PDOS of the Er 4d,5p,6s orbitals;(d) DOS of F and PDOS of the F 2p and 2s orbitals.
4 结论
通过热处理原位析晶的方法制备了稀土离子掺杂KMnF3纳米晶复合透明微晶玻璃.采用纳米尺度高分辨率透射电子显微技术,直观地证明了稀土离子优先富集在KMnF3晶体中.由于氟化物晶体的声子能量远低于玻璃基体,因此稀土离子在氟化物晶体中无辐射弛豫速率大大降低,这也是引起微晶玻璃上转换发光强度显著增强的主要原因之一.同时,借助于稀土离子与Mn2+之间的能量传递作用,获得了具有高单色性的上转换红色发光.通过第一性原理计算发现稀土离子取代晶体中K+格位的形成能较低,这是由于八配位K+半径较大,更有助于稀土离子发生取代.此外,上述取代过程也与稀土离子的半径有关,小半径的稀土离子更容易发生取代.由轨道的分波态密度分布可知稀土离子与晶体中的配体F–具有较强的成键性.研究成果对于理解稀土离子在微晶玻璃中的掺杂机制以及设计和开发高效发光材料具有一定的理论指导价值.
