NASICON菱形结构材料的晶体结构与离子迁移行为
2022-04-26赵玉辉贺明辉韩松益汤卫平
赵玉辉,吴 洁,贺明辉,韩松益,2,汤卫平
(1.上海空间电源研究所空间电源技术国家重点实验室,上海 200245;2.陕西科技大学化学与化工学院,陕西西安 710021)
自Hong 等[1]报道了具有NASICON (Na super ion conductor)结构的材料以来,已有超过400 多种NASICON 结构材料被相继报道和研究,其中一些材料表现出≥10-4S/cm 的高离子电导率,可以满足全固态电池实用化对固体电解质离子电导率的要求,因此被研究作为固体电解质以发展全固态电池,解决电池安全性和能量密度不够高的问题。另外,由于结构稳定,晶体骨架中有大量空位可用于储存金属离子以及快速的离子扩散动力学,NASICON 结构材料也被探索用作电池的电极活性材料。NASICON 结构的NaTi2(PO4)3(NTP)可以作为锂/钠离子电池的负极材料,通过Ti4+↔Ti3+氧化还原反应储存/释放锂/钠离子,其理论比容量为133 mAh/g[2-4]。用Nb5+部分取代NTP 的Ti4+还可以提高钠离子嵌入/脱出过程中的离子扩散系数[5]。LiTi2(PO4)3也被大量研究作为电极材料[6-9]。Na3V2(PO4)3已被广泛用作锂/钠/锌离子电池的正极材料[10-13]。Zn2+的半径为0.074 nm,比Na+(0.099 nm)的要小[12],Zn2+嵌入Na3V2(PO4)3的放电产物NaV2(PO4)3,体积膨胀约为4.7%,比NaV2(PO4)3完全钠化为NVP 的体积膨胀(≈8.6%)要小,而且ZnNaV2(PO4)3的机械性能和电子电导率优于Na3V2(PO4)3[14]。但是NASICON 结构的电极材料电子电导率低,因此倍率性能和循环性能较差,往往需要通过降低颗粒尺寸和涂覆导电涂层来解决[5,8]。
NASICON 菱形结构是一种典型的NASICON 晶体结构,具有该结构的材料在固体电解质和电极活性材料两个领域被广泛研究。无论是作为固体电解质还是作为电极材料,离子在晶体骨架中的传输性质都受到大量的关注。由于结构决定了材料的性质,因此在NASICON 菱形结构材料的离子迁移问题的研究中,往往首先会对其晶体结构进行解析,然后再推断离子在晶体内部的传输行为特征。本文对三种常见的具有NASICON 菱形结构的材料的晶体结构及其离子迁移行为进行了总结。
1 晶体结构
Na1+xAlxTi2-x(PO4)3(NATP,0≤x≤0.9)、Li1+xAlxTi2-x(PO4)3(LATP,0≤x≤0.5) 和NaxV2(PO4)3(NVP,x=0,3) 的结构相似,同属NASICON 型化合物,均为菱形结构,空间群为R-3c。NATP、LATP 分别为NaTi2(PO4)3和LiTi2(PO4)3通过Al3+部分取代Ti4+得到的衍生物,Al 原子随机分布在Ti 原子位置,Al3+的掺杂能提高载流子浓度和移动性[15-17]。两个[Al/Ti]O6或者VO6八面体和三个PO4四面体共顶点连接形成被称为“灯笼”的基本单元结构,NATP、LATP 和NVP的刚性晶体骨架就是由多个这样的“灯笼”构成的[18-22](图1)。NATP、LATP 和NVP 均为六方晶系,三者的晶格常数如表1 所示。从组成上看,LATP 和NATP 仅存在一个元素(Li/Na)的差异,而且文献表明两者的结构相似,似乎两者结构随Al 掺杂程度的变化规律应该基本相同,但在Al 掺杂中两者晶轴a的变化略有差异。由于Al3+(0.053 5 nm)的半径比Ti4+(0.060 5 nm)的小以及掺杂引起的键角变化,随着取代程度的增加,LATP 的晶轴a和c逐渐减小,其中a的减小幅度比c的要小[15];同样,NATP 的c轴也逐渐减小,但x由0增加至0.2 时,a轴增大,之后随着Al 含量的增加a轴基本保持不变[21]。由于多出的钠离子进入结构中的空位点,Na3V2-(PO4)3的晶格常数比NaV2(PO4)3的要大。
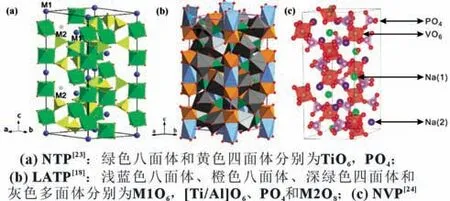
图1 晶体结构示意图
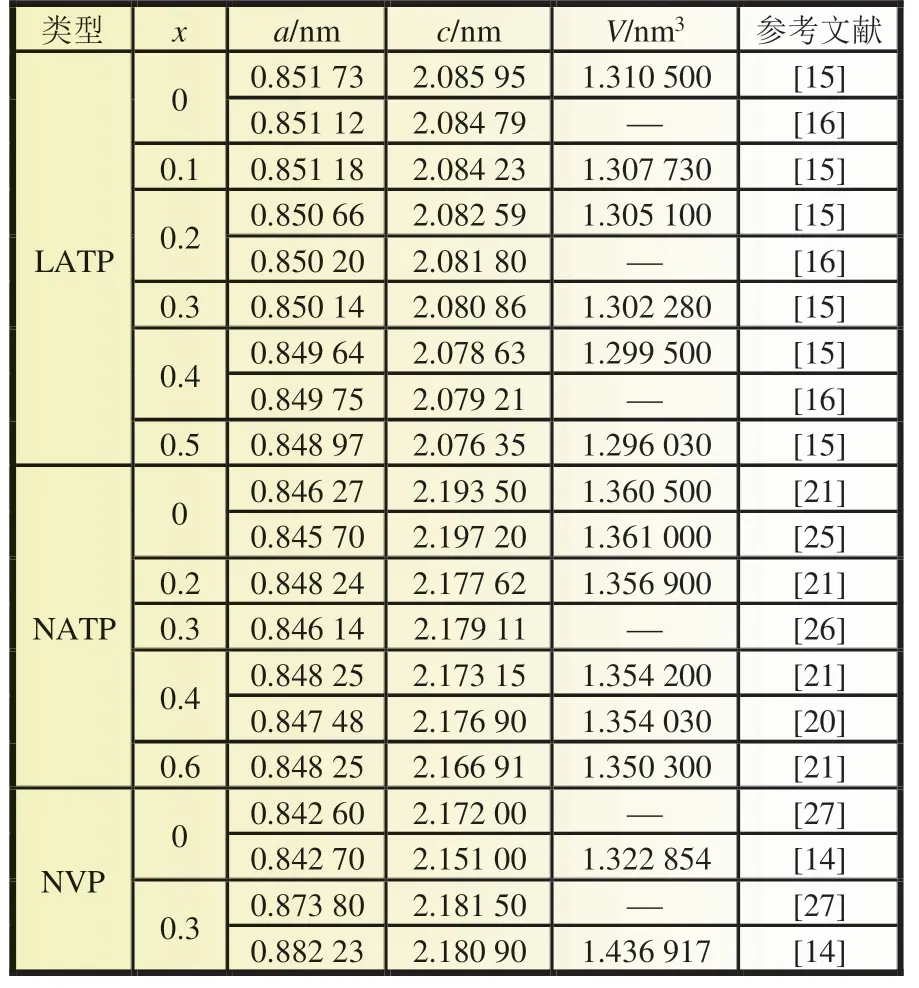
表1 LATP、NATP 和NVP 的晶格常数
在NASICON 型菱形结构中,每个单元结构中有1 个M1位点(6b,[0,0,0]),位于两个[Al/Ti]O6或者VO6八面体之间,与六个氧原子配位形成八面体,以及三个M2 位点(18e),位于两个平行排列的“灯笼”之间,与8 个氧原子配位形成不规则十二面体[22]。对于LATP 和NATP,M2 位点位于[m,0,0.25],在不同文献中,m的精修值会略有不同[20-21,28],这可能是受到材料合成和精修过程的影响,而Na3V2(PO4)3的M2 位点坐标为[0.633 37,0.003 20,0.250 00][27]。当x=0 时,由于势能较低,钠离子或锂离子倾向位于M1位点,当x>0时,额外引入的钠离子或锂离子位于M2 位点,但是对于LATP,有的研究表明,锂离子并非位于M2 位点,而是位于M3 位点(36f,[0.07,0.34,0.07]),与四或六个氧原子配位[15-16,19,28]。Na3V2(PO4)3骨架中的M1 和M2 位点的占有率分别为1 和2/3,另外M1 位点的Na-O平均键长比M2 位点的短得多,这表明M1 位点更加稳定,即M2位点活性更高[24,29-30]。LATP和NATP 的M1位点的Li/Na-O键长比M3/M2 位点的平均键长要短,随着x值增加,LATP 的M1 和M2 位点的平均Li-O 键长几乎不变。如图2 所示,NATP 和LATP 的XRD 图谱很相似,NATP 衍射峰的峰形甚至与NaV2(PO4)3的相同,峰位也相近。表2 为LATP 和NATP 中与两种Li+/Na+相关的原子间距。
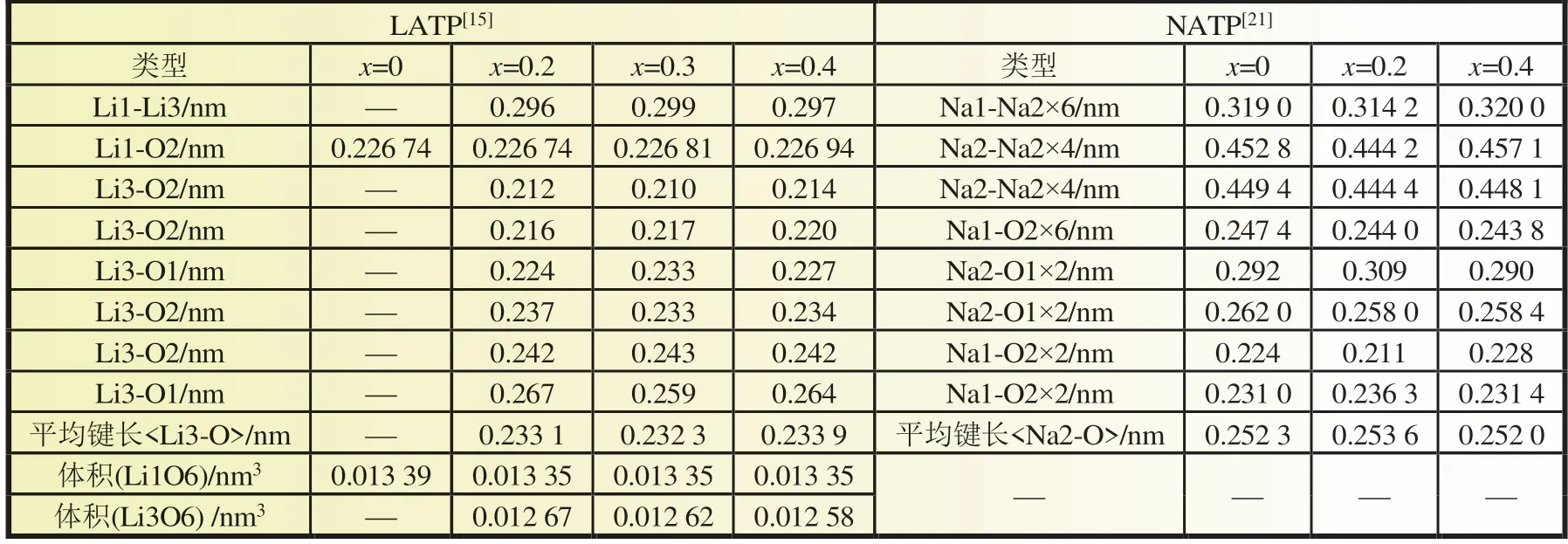
表2 LATP 和NATP 中与两种Li+/Na+相关的原子间距
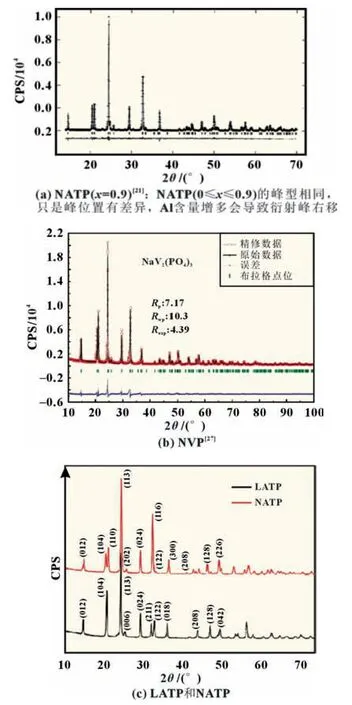
图2 XRD 图谱
2 离子迁移行为
在NASICON 结构的材料中,离子在晶体的晶格间隙中的迁移行为是最受关注的特性之一,它决定了固体电解质的离子电导率以及电极活性材料的电化学性能[24]。
在LATP 中,锂离子可能通过M1-M3-M3-M1 Z 字形路径或者M3-M1-M3 路径在晶体内进行迁移[15,28]。对于M3-M1-M3 迁移路径,M3 位点的一个Li+向前迁移时,由于库仑力,它必然推着M1 位点的另一个Li+跃迁至下一个M3 位点,因此Li+实际上是以协同迁移的方式在LATP 晶体内部进行跃迁的[15]。虽然具体的传输路径存在争议,但不少研究都表明,锂离子的迁移至少涉及到两个晶体学位点[16,18,23,31]。He 等[32]的研究揭示了LATP(x=0.3)的离子迁移机理为多离子协同迁移,而非单离子跃迁,因此LATP (x=0.3)具有较低的活化能(0.27 eV)。图3 是单离子跃迁和协同迁移的示意图,可见协同迁移的能垒较低。LATP (x=0.3)的典型协同迁移模式为,相邻的M1 和M2 位点的两个锂离子成对迁移——M1 位点的Li+跃迁到相邻未完全占据的M2 位点,与此同时,M2 位点的Li+则跃迁至下一个相邻的M1 位点。最后,He 等指出,Li+同时占据低能位点(M1)和高能位点(M2)以及两种Li+位点的强相互作用力是实现能垒较低的协同迁移的关键。
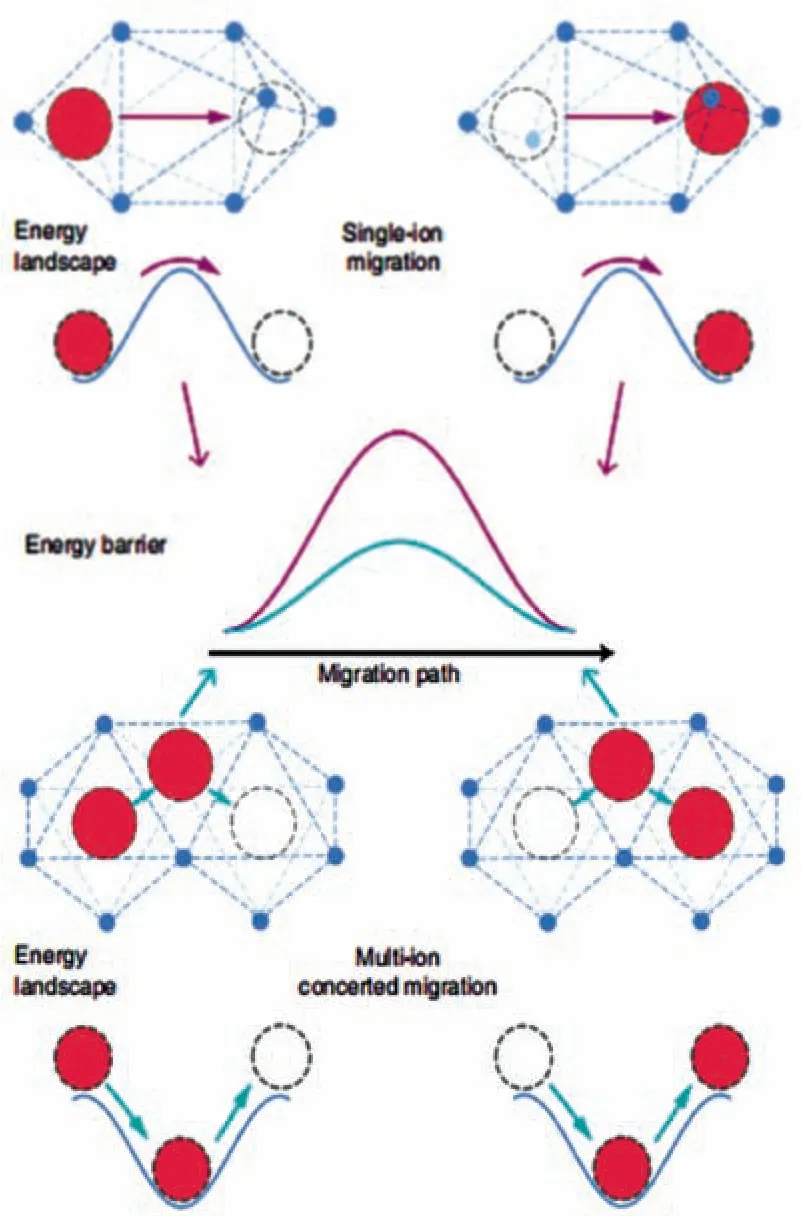
图3 单离子迁移和多离子协同迁移示意图[32]
与LATP 相比,关于NATP 晶体结构和离子迁移机理的研究相对较少。在Enrique 等[20]的研究中,在Na1.4Al0.4Ti1.6(PO4)3(NATP)的23Na MAS-NMR 谱上,除了M1 位点(6b,[0,0,0])的钠离子产生的信号峰,在~-9×10-6处还有一个M2 位点(18e,[0.658,0,0.25])的钠离子引起的小峰。考虑到钠离子的半径大小以及M2 和M2 之间的“瓶颈”尺寸较小,Enrique 等认为钠离子不可能通过M2-M2 路径进行迁移,因此NATP 晶体内钠离子可能的迁移路径为M1-M2-M1。Enrique 等计算了M1-M2-M1 迁移路径上任意一点的键价总数(Φ),所有键价总数最低的点的连线即为钠离子的运动轨迹。将键价总数对迁移距离d(nm)作图可得到图4,图中曲线的鞍点代表钠离子迁移的势垒(M1M2“瓶颈”)。NATP 的离子迁移活化能和离子电导率分别为0.53 eV,1.53×10-5S/cm(T=400 K)。Chen等[23]的研究表明,NaTi2(PO4)3的M1-M2-M1 迁移路径中最狭窄的位置(rmin)为0.079 nm,比钠离子半径(0.102 nm)小得多,这严重阻碍了钠离子的迁移,因此NaTi2(PO4)3更适合作为电极活性材料。
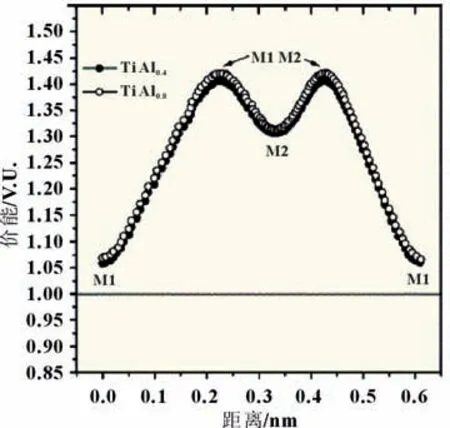
图4 M1-M2-M1迁移路径的Φ(d)曲线[20]
在被用作电极材料的研究过程中,NaxV2(PO4)3(NVP,x=0、3)的晶体内部的离子迁移行为逐渐地被揭示、理解。鉴于具有菱形结构的NASICON 型化合物的离子移动性比相应的单斜结构化合物更高,在2001 年Goodenough 等[35]希望以Na3V2(PO4)3为前驱体通过离子交换法制备具有菱形结构的Li3V2(PO4)3,但是只能得到Li2NaV2(PO4)3。Goodenough 等 认为,这表明位于M2 位点的钠离子具有移动性,因此能与锂离子发生交换,而M1 位点的钠离子没有移动性。另外,如果NVP 的钠离子迁移涉及到M1 和M2 位点,那么M1 位点的钠离子同样能发生交换,但是这种情况并没有发生,因此他们推测Na3V2(PO4)3的离子迁移路径为M2-M2。为了确认M1 位点的钠离子是否确实是不能移动的,Goodenough 等对Li2NaV2-(PO4)3进行了电化学Li+嵌入/脱出实验,在100 次循环后,仅剩下25%的Na+,说明在循环过程中部分Na+从Li2NaV2(PO4)3正极脱出。他们认为,这可能是循环过程中V3+的氧化及其离子半径的收缩导致了LixNaV2(PO4)3(0 2014 年,Chen 等[27]通过XRD 精修和像差校正的扫描透射电子显微镜(Aberration-Corrected STEM)证明了Na3V2-(PO4)3转变为NaV2(PO4)3的过程中,钠离子只能从Na3V2(PO4)3的M2 位点脱出,原先M1 位点的钠离子则仍然位于M1 位点。23Na MAS-NMR 谱的半高宽(Δυ)可以描述为:υ0Δυ=25CQ2/192,υ0为Larmor频率,CQ为四极耦合常数。钠离子的热运动会旋转或释放Na-O 键,因此CQ减小。如图5(a)所示,在295 K≤T≤375 K 的温度区间里,NaV2(PO4)3的M1 位点的钠离子引起的核磁信号峰的半高宽(Δυ)几乎不随温度变化,而Na3V2(PO4)3的M2 位点的钠离子信号峰的半高宽(Δυ)随温度升高而减小,即CQ减小。这些结果表明,Na3V2(PO4)3/NaV2-(PO4)3的M2 位点的钠离子可以移动,而M1 位点的不能,这暗示了在Na3V2(PO4)3中,钠离子的迁移路径为M2-M2。2016年,Huang 等[12]第一次将Na3V2(PO4)3用作锌离子电池的正极活性材料,在对锌化ZnxNaV2(PO4)3正极的精修过程中,当假设嵌入的Zn2+仅占据在M2 位点时,精修未成功,而当假设嵌入的Zn2+同时占据在M1 和M2 位点时,精修结果变得更为合理[图5(b)]。Huang 等认为这种离子占位的变化可能发生在Zn2+嵌入结构的过程中。 图5 核磁图谱和XRD 图谱 不同于Goodenough[35]和Chen[27]等的研究结果,Wang等[24]通过NEB (nudged-elastic-band)计算表明,在Na3V2(PO4)3中,两个位点的钠离子沿着M1-M2-M1 路径以协同迁移的方式跃迁时,活化能比钠离子直接沿着M2-M2 路径迁移更小,是最为可行的离子迁移方式。这也表明了离子导体中离子迁移行为的复杂性,不同的研究可能得到不同的结果。 晶体的离子迁移可能涉及到多个方面,如“瓶颈”大小、离子的配位环境、结构稳定性的维持等,是一个动态的过程,这可能导致了其迁移机理十分复杂,加上研究方法和研究手段的限制,以致于不能够被清晰地揭示,甚至出现不一致的研究结果。NATP 和LATP 的组成、结构相似,但是离子移动性差异巨大。LATP 的室温离子电导率高达10-4S/cm,而NATP 在400 K 下离子电导率仅为1.53 × 10-5S/ cm。Goodenough 和Chen 的研究表明Na3V2(PO4)3和NaV2(PO4)3的M1 位点没有移动性,而且Na2TiM(PO4)3的钠离子只能部分被锂离子交换,这说明NASICON 菱形结构化合物的离子不一定都具有移动性,这些非活性的位点会阻碍离子的迁移。由于NATP 和NaV2(PO4)3的结构很相似,NATP(x=0.4)的离子电导率低、活化能高很可能是因为M1 位点是非活性的,这阻碍了离子的迁移。详细研究NATP 的结构和离子迁移机理并与LATP 进行比较,以及对NVP(x=0,3)的部分钠离子被“困住”现象的研究,或许有助于加深对离子导体的离子迁移行为的理解,从而设计出离子电导率更高的固体电解质和电化学性能更佳的电极材料。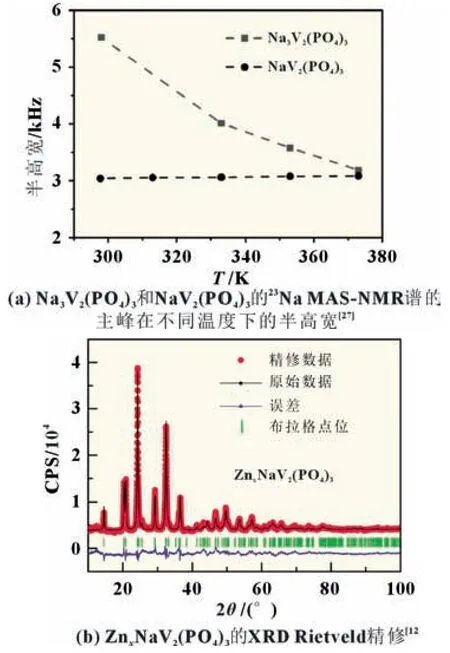
3 总结
