氮掺杂石墨烯对水中微量磺胺甲恶唑的吸附特性
2022-04-26李彦娟王三反
吴 楠,张 雪,李彦娟,王三反
(1. 兰州交通大学 甘肃省黄河水环境重点实验室,兰州 730070,2. 兰州交通大学 环境与市政工程学院,兰州 730070,3. 兰州交通大学 寒旱地区水资源综合利用教育部工程研究中心,兰州 730070,4. 兰州石化职业技术大学 石油化学工程学院,兰州 730060,5. 兰州理工大学 土木工程学院,兰州 730050)
抗生素为人类健康与社会发展做出了独特贡献,然而其过度使用所造成的危害(如耐药性、持久性污染、难降解等)已引起人们关注,其中水生态系统成为抗生素污染的第一个也是最严重的环境介质.磺胺甲恶唑(SMZ)在天然水环境中检出频次多、浓度大,其中白洋淀中浓度高达940 mg/L.抗生素可能导致抗生素耐药基因(ARGs)和抗生素耐药细菌(ARBs)的产生增大了其危害性,而且一些净水工艺(如生物活性炭、氯消毒)和配水系统可能会丰富和促进ARGs与ARBs的产生.目前常规水处理技术对抗生素去除效率不高,这是因为其设计目的并不是用来处理抗生素等新型污染物的[1-6].
均相Co(Ⅱ)/过硫酸氢钾(PMS)体系已被证明是一种高效氧化体系,但存在金属浸出污染的可能,因此无机非金属催化剂因其无二次污染、稳定性好、催化性能优越而受到人们的青睐[7-8].石墨烯具有大比表面积、超强电子转移能力等特性,自2012年发现还原氧化石墨烯可以激活PMS以来,研究表明石墨烯有望成为极具前途的催化新材料,且氮掺杂的方式已被证实可以有效的提高其催化效率[9-10].多数的研究着眼于提高其催化性能,而忽视了石墨烯的本质特征——强大的吸附能力.对于水中微量污染物,吸附是一种简单、有效的富集及去除方法,目前已有较多研究证实石墨烯在吸收不同种类抗生素方面具有很大的潜力,但其实验浓度范围与天然水中抗生素的含量相差甚远,导致研究与实际应用存在一定的脱节.同时石墨烯只是作为吸附剂存在某种意义上的功能浪费,可以将石墨烯类材料的吸附、催化等性能结合以发挥更大作用[11-13].因此本课题组在研究石墨烯催化PMS时结合其吸附性能,突破现有研究的局限,通过构建“吸附-催化氧化”体系提高其处理能力,尤其针对水中微量存在的抗生素,希望通过吸附作用促进高级氧化处理微量污染物的反应进程[14-15].
综上所述,本文通过制备氮掺杂石墨烯(N-rGO)研究其对水中微量抗生素的吸附能力,为构建“吸附-催化氧化”体系提供物质条件.考察温度、SMZ初始浓度、N-rGO投加量、pH值对吸附效果的影响,分析吸附过程中的动力学及等温线,同时结合表征分析推断吸附机制.本文通过研究N-rGO对微量抗生素的吸附行为考察其应用前景,并模拟天然水基质中无机离子、NOMs对其吸附微量抗生素的效能影响[16-17].以上工作可为构建“吸附-催化氧化”体系提供现实支撑,更为重要的是为下一步研究“吸附-催化氧化”体系中主导反应及作用机制的分析夯实了基础,为水中微量抗生素的处理提供一种新的理论选择.
1 材料与方法
1.1 实验材料、仪器
1) 原料及药品:石墨粉(AR,粒径<30 μm,天津大茂)、浓硫酸(98%,AR,天津大茂)、高锰酸钾(AR,汕头西陇)、双氧水(30%,天津大茂)、氨水(AR,),尿素(25%,AR,天津大茂)、盐酸(AR,汕头西陇)、氢氧化钠(AR,天津大茂)、碳酸氢钠(AR,天津大茂)、氯化钙(AR,广东光华)、碳酸钠(AR,天津大茂)、磺胺甲恶唑(98%,AR,麦克林)、腐殖酸钠(AR,麦克林)、冰醋酸(AR,广东光华)、磷酸二氢钾(AR,广东光华)、乙腈(AR,广东光华)、磷酸(AR,天津大茂)、甲醇(AR,广东光华).
2) 实验仪器:水浴锅(HH-S,江苏正基)、离心机(80-2,常州金坛)、超声仪(KH2200,昆山禾创)、鼓风干燥箱(SPX-250B,上海琅玕)、pH计(PHS-3C,上海雷磁)、恒温振荡器(SHAZ,江苏正基)、扫描电镜(ZEISS GeminiSEM 500,德国蔡司)、高效液相色谱(Waters Acquity UPLC I-Class,美国沃特世)、傅里叶红外光谱仪(VERTEX 70、德国布鲁克)、透射电镜(GEMINI 500、德国蔡司).
1.2 氮掺杂石墨烯的制备
使用浓硝酸(20 mL)、过硫酸钾(8 g)及五氧化二磷(8 g)在80 ℃条件下对石墨粉(10 g)进行预氧化6 h.然后室温条件下冷却,加入去离子水稀释、过滤、洗涤数遍后60 ℃干燥12 h,研磨过100目筛,得到预氧化石墨粉.将10 g预氧化石墨粉放入含有180 mL浓硫酸、20 mL浓磷酸的烧杯中(冰浴)搅拌30 min,少量多次加入60 g高锰酸钾.然后将烧杯移至水浴锅中,35 ℃恒温搅拌1 h.然后调节温度至60 ℃,连续滴加490 mL去离子水使温度上升至98 ℃反应30 min,再加入30%双氧水25 mL后终止反应.趁热直接过滤,用0.1 mol/L盐酸进行洗脱离心.随后置于去离子水中进行超声剥离30 min,功率100 W.离心浓缩后在60 ℃条件下干燥12 h,干燥完成后研磨过100目筛,得到氧化石墨烯粉末[18].
将氧化石墨烯分散在水中,浓度为2 mg/L,超声1 h.取60 mL加入2 mL氨水搅拌10 min后转移到高压反应釜中,180 ℃反应24 h.离心收集后去离子水洗涤,60 ℃干燥12 h后研磨过100目筛,得到氮掺杂氧化石墨烯粉末(N-rGO)[19].
1.3 吸附实验条件
1.4 抗生素浓度测试
采用HPLC方法测定SMZ浓度,色谱柱为C18,流动相为水(799)、乙腈(200)、三乙胺(1),使用氢氧化钠或冰醋酸调节pH值为5.9,流速1 mL/min,波长240 nm.
生命体征监测设备通过调用Bluetooth 接口,获取自带的蓝牙适配器,并开启蓝牙功能。通过调用蓝牙设备搜索接口函数,对周边的蓝牙设备终端进行扫描,当搜索到匹配的蓝牙适配器时,则进行设备注册、建立连接并停止扫描,至此蓝牙扫描工作完成。扫描并匹配成功的设备名称和设备MAC 地址将分别储存在蓝牙搜索的公有成员变量中,当扫描结束后,会向生命体征监测设备蓝牙适配器发送一个类型为0x01 的句柄消息。同时handleMessage 接口函数也会收到类型为0x01 的消息,扫描程序通过设备遍历对周边的设备进行逐个匹配直到找到符合要求的蓝牙终端设备。
1.5 表征方法
通过电镜图像表征石墨烯的形貌特征,傅里叶红外谱图(FT-IR)可以分析石墨烯材料的官能团分布情况,Zeta电位测试石墨烯在水相及吸附过程中的电位变化,为吸附机理分析提供佐证.
2 结果与讨论
2.1 SMZ初始浓度及N-rGO投加量对吸附效果的影响
SMZ初始浓度及N-rGO投加量对吸附效果的影响,如图1所示,SMZ初始浓度不变时增加N-rGO的投加量可以提高去除率,说明N-rGO的增加提供了更多的吸附点位.当达到平衡后继续增加N-rGO的投加量则不会改变对SMZ的吸附效果,可能是过多的N-rGO产生了重叠或堆叠现象,导致有效表面积及活性吸附点位减少,同时也会导致吸附剂内部吸附点位竞争增强,这些都不利于吸附效果的提升.吸附剂量较少时增大SMZ浓度其去除率显著降低,这是由于污染物浓度增加会导致少量存在的N-rGO吸附位点的数量减少所引起的,从图中可以看出,增加N-rGO的投加量即可克服并提高去除率.在低浓度条件下,N-rGO对SMZ的去除率超过了87.5%,可以说明N-rGO对水中微量存在的SMZ有较好的吸附效果.

图1 SMZ初始浓度及N-rGO投加量对吸附去除效果 的影响Fig.1 Effect of initial concentration and dosage on adsorption removal
2.2 pH值对吸附效果的影响
溶液pH值会影响SMZ的存在形态及N-rGO的表面荷电状态,从而影响吸附剂与吸附质之间的相互作用,如图2所示.pH值的变化改变了SMZ的溶解度和电离官能团,SMZ的pKa值为2.3、7.4,即当pH<2.3时SMZ表现为正电荷,在pH=2.3~7.4时表现为两性物质同时存在,在pH>7.4时则表现为负电荷[20].同时从图2可以看出,N-rGO在pH=3时Zeta电位为-0.65 mV,因此在整个pH范围内都带负电荷.当pH值由酸性变化至中性的过程中,N-rGO发生表面质子化,对SMZ静电吸引作用增强,吸附量增大;在中性附近时,质子化的SMZ比去质子化的SMZ疏水性更强,同时中性的SMZ吸引π电子数量增加,导致石墨碳结构中π电子与去电离基团的π-π EDA相互作用增强,吸附能力达到最大;在碱性增强时,静电作用由吸引转变为互斥,抑制了N-rGO的吸附作用.

图2 pH对吸附去除效果和Zeta电位的影响Fig.2 Effect of pH on adsorption removal and Zeta potential
2.3 温度对吸附效果的影响
在吸附的诸多影响因素中,温度影响的重要性不言而喻.如图3所示,随着温度的升高,N-rGO对SMZ的吸附效果呈下降趋势,说明升温不利于吸附过程的进行,N-rGO对SMZ的吸附是放热反应.升高温度虽然有利于抗生素分子或离子在吸附剂表面的活动,增大了其与吸附剂接触的机会,这是有利于吸附的发生的,但是温度升高同样会导致抗生素与吸附剂之间的作用力减弱,从而影响吸附效率.
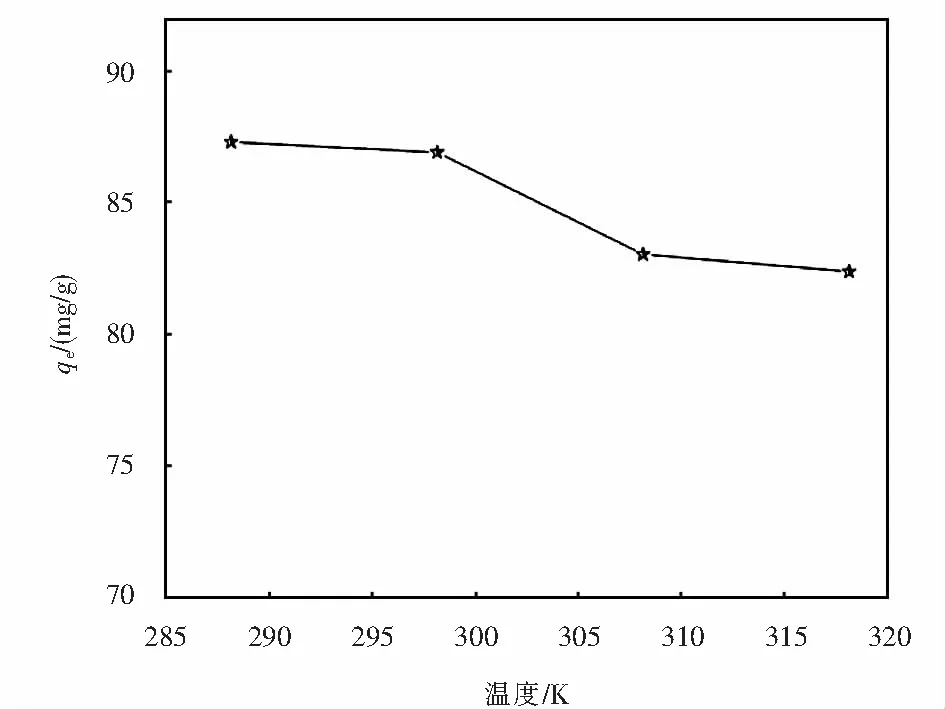
图3 温度对吸附去除效果的影响Fig.3 Effect of temperature on adsorption removal
2.4 吸附动力学分析
吸附效果与时间的影响关系,如图4所示,N-rGO在60 min内即可完成对SMZ的吸附.为进一步研究N-rGO对SMZ的吸附过程,采用准一级动力学及准二级动力学方程对吸附过程进行拟合,其中准一级动力学方程如式(1)所示:
ln(qe-qt)=lnqe-k1t,
(1)
式中:qe为平衡吸附量,mg/g;qt为反应t时刻对应吸附量,mg/g;k1为一级动力学方程反应速率常数,min-1.
准二级动力学方程如式(2)所示:
(2)
式中:k2为二级动力学方程反应速率常数,g/(mg·min);其余参数与式(1)相同.

图4 吸附效果随时间变化的关系(C0=10 ug/L,T= 288.15 K)Fig.4 Effect of time on adsorption removal(C0=10 ug/L, T=288.15 K)
相关动力学拟合的结果见图5,相关动力学参数见表1.从图5和表1可以看出,准一级动力学及准二级动力学方程均能够很好的描述氮掺杂石墨烯对磺胺甲恶唑的吸附过程,其R2值均大于0.98.经过计算得到的吸附容量分别为85.49 mg/g、89.50 mg/g,而实验所得吸附容量为87.30 mg/g,相差不到3%,非常接近.从拟合结果分析,吸附剂对吸附质的吸附作用除化学吸附(如静电作用、π-π相互作用等),范德华力也对N-rGO吸附SMZ起到了重要作用.吸附过程中单分子层吸附、多分子层吸附均有表现,这种物理吸附与化学吸附的共同作用会引起吸附速率的提升,比单纯的化学吸附要快得多.
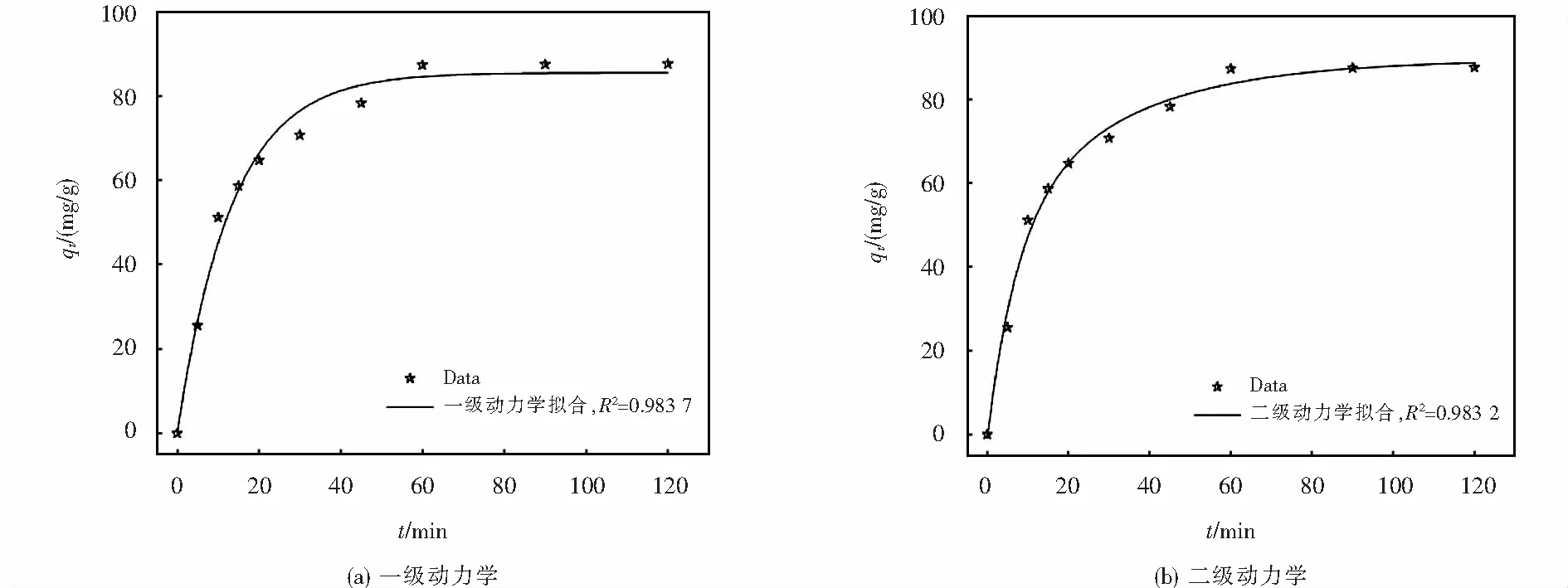
图5 动力学拟合结果Fig.5 Fitting results of first order dynamics and second order dynamics
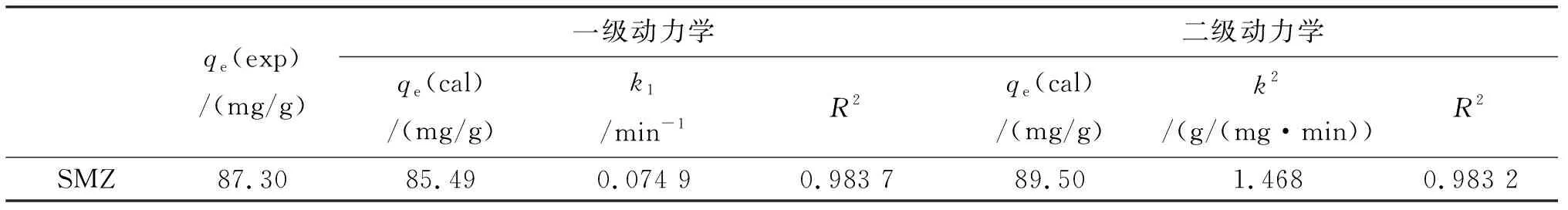
表1 一级动力学及二级动力学拟合参数(C0=10 ug/L,T=288.15 K)
2.5 吸附等温线分析
磺胺甲恶唑在N-rGO上的吸附等温线,如图6所示,从图中的变化趋势可以看出吸附平衡浓度增大吸附量也在增大,而等温线的斜率逐渐减小,图形符合Giles吸附等温线理论中的L型吸附,表明在N-rGO吸附SMZ的过程中存在单分子层吸附.通过一些吸附模型对N-rGO吸附SMZ平衡状态进行描述可以进一步探究其吸附机制,Langmuir与Freundlich等温模型是最为常见也是应用性较好的两种模型,其公式分别如式(3)、(4)所示,拟合结果及参数见图7和表2.
(3)
(4)
式中:qe为平衡吸附量,mg/g;qm为饱和吸附量,mg/g;ce为平衡浓度,mg/L;KL为Langmuir吸附等温常数;KF为Freundlich吸附等温常数.
从拟合结果来看,N-rGO对SMZ的吸附实验更符合Langmiur吸附等温线,其R2>0.999,这表明了N-rGO对SMZ的吸附过程中单分子层吸附占据了比较重要的地位,可能由于N-rGO活性位点比较均匀的分布在其边缘及两侧.该拟合结果与结构表征结果相符,N-rGO结构中存在重叠的形式.而Freundlich等温线与吸附剂表面的不均匀性有较大关联,这种不均匀性会在吸附过程中形成多层吸附,而N-rGO的结构特点会限制这种多层膜的形成,虽拟合结果不如Langmiur吸附等温线,但R2>0.97,在一定程度上说明了多层吸附在N-rGO吸附SMZ中的作用.Langmiur吸附等温线计算得到的N-rGO理论最大吸附容量为574.71 mg/g,高于之前报道的石墨烯基吸附剂,显示了强大的吸附能力,对构建“吸附-催化氧化”体系具有重要的意义[21-22].
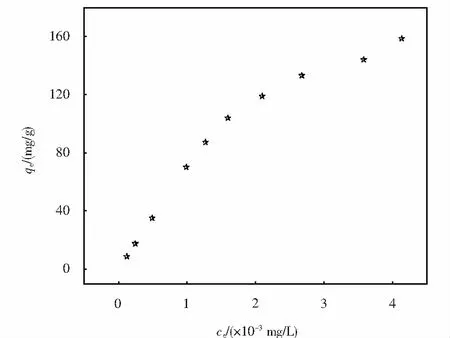
图6 磺胺甲恶唑在N-rGO上的吸附等温线(C0= 10 ug/L,T=288.15 K)Fig.6 Adsorption isotherms of SMZ on N-rGO(C0= 10 ug/L,T=288.15 K)
2.6 热力学分析
通过计算吉布斯自由能、焓变及熵变可以从更
深层次的角度分析N-rGO吸附SMZ的过程,标准态下标准吉布斯自由能变化与标准平衡常数的关系及与焓变、熵变的计算公式如式(5)~(8)所示,计算结果及热力学参数见表3.
ΔG=-RTlnKd,
(5)
(6)
(7)
ΔG=ΔH-TΔS.
(8)
式中:ΔG为吸附自由能,kJ/mol;R为气体常数,8.314 J/(mol·K);T为温度,K;Kd为热力学平衡常数;ΔS为熵变,J/(mol·K);ΔH为焓变,kJ/mol;a为吸附剂用量,g/L.

图7 吸附等温线拟合结果Fig.7 Results of adsorption isotherm fitting

表2 不同吸附等温模型拟合参数(C0=10 ug/L,T=288.15 K)
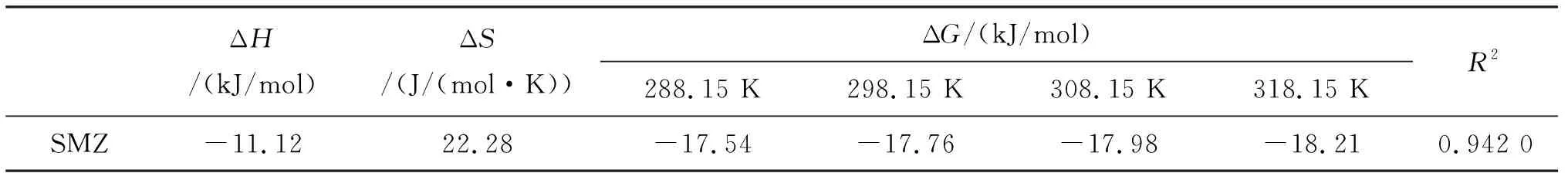
表3 吸附热力学参数(C0=10 ug/L)
从计算结果可以看出,N-rGO吸附SMZ的过程为焓变为负值,说明反应为放热反应,与升高温度去除效果下降的实验现象一致.且ΔH的值小于一般化学吸附的焓变值,与单分子层作用的体现是相一致的.ΔG值均为负值,表明N-rGO对SMZ的吸附可以自发进行.而ΔS为正值,说明了系统趋向于一种混乱、无序的状态,可能引发N-rGO与SMZ的接触几率增大,吸附效果增强.
2.7 循环吸附实验
循环次数对N-rGO吸附SMZ效果的影响如图8所示,从图中可以看出,随着循环次数的增多,N-rGO的平衡吸附容量出现了下降,与第一次平衡吸附容量相比,经过4次循环其吸附容量可达到初始吸附容量的90%,经过8次循环后仍可达到初始吸附容量的80%以上.在循环再生过程中,有可能引起N-rGO的层间结构发生变化,增大了团聚的发生倾向,从而导致用于吸附的活性位点减少,进而引发吸附量下降.虽然再生后吸附容量减少,但多次循环后减小幅度小于20%,可以认为N-rGO具有较好的再生利用性能.
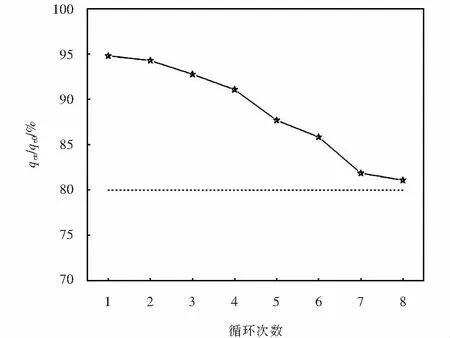
图8 循环次数对N-rGO吸附SMZ效果的影响Fig.8 Influence of cycle number on SMZ adsorption effect of N-rGO
2.8 共存离子对吸附效果的影响

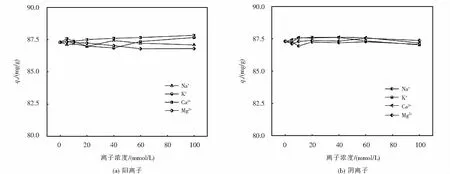
图9 共存离子对N-rGO吸附SMZ效果的影响Fig.9 Influence of co-existing ion on SMZ adsorption effect of N-rGO
2.9 NOMs对吸附效果的影响
腐殖酸的存在会影响N-rGO对SMZ的吸附效果(见图10),且这种影响随着腐殖酸浓度的增大而增强.这是由于腐殖酸中含有大量的酚羟基、羧酸盐等官能团,容易形成负电荷,可能会与水中的SMZ形成可溶的络合物,增强了静电斥力,同时这些负电荷与SMZ竞争吸附剂的活性位点,从而减弱吸附效果[23].
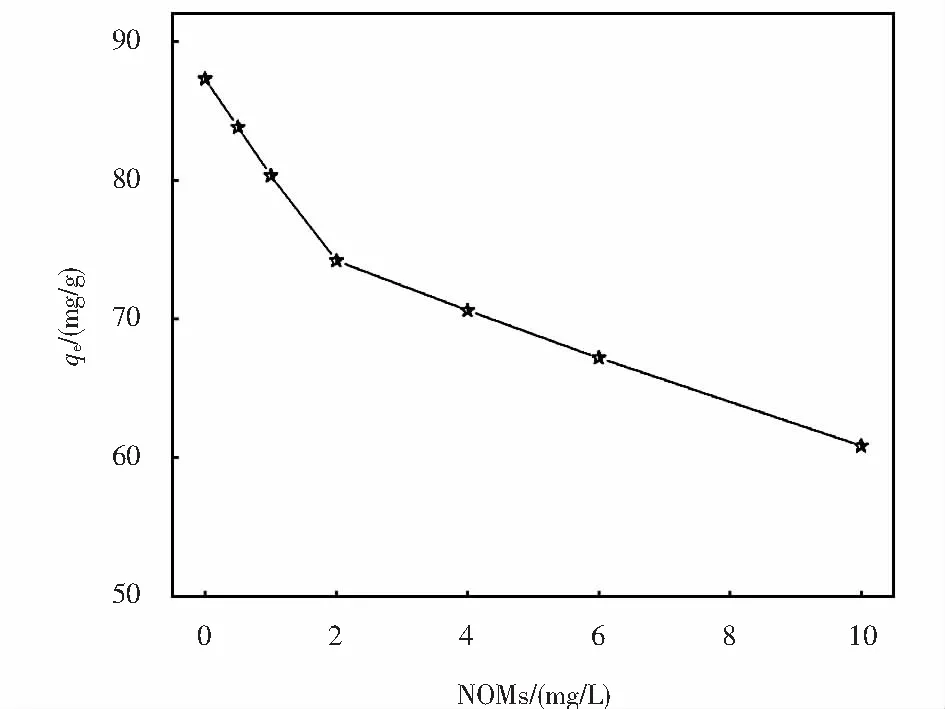
图10 NOMs对吸附效果的影响Fig.10 Effect of NOMs on adsorption effect
2.10 表征分析
N-rGO的形貌如图11所示,表面具有典型的波纹,片层呈现透明状态,有微聚集的倾向,褶皱大量分布在石墨烯的基面上,形成了较多的沟壑区域,这些褶皱与平面结构可提供较多的吸附位点.N-rGO的基本性质列于表4.从表4可以看出,N-rGO中含氧量为34.75%,可能存在较多的含氧官能团,这可能与其表面粗糙度较高有关.

图11 N-rGO的SEM与TEM图Fig.11 SEM and TEM images of N-rGO
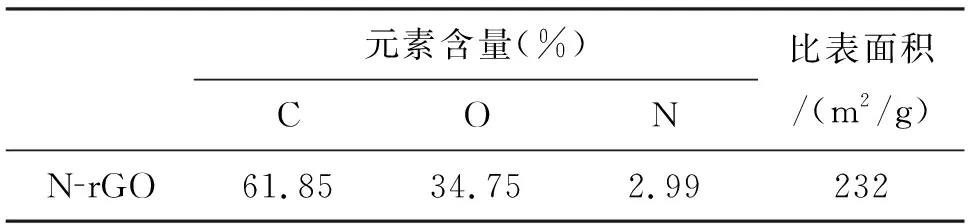
表4 N-rGO的基本性质
通过红外光谱可以判断N-rGO中官能团的类型,如图12所示,N-rGO在3 390 cm-1处有一个非常明显的吸收峰,归属为OH、COOH的伸缩振动,在1 627 cm-1处出现一个吸收峰,归属为C=C的吸收峰,而1 032 cm-1处的吸收峰归属为C-O-C振动吸收峰,1 397 cm-1处归属为-OH吸收峰,而2 920 cm-1处的微弱吸收峰为C-H[14].以上结果表明N-rGO中含有不同种类的含氧官能团,与元素分析中氧含量非常高相吻合.
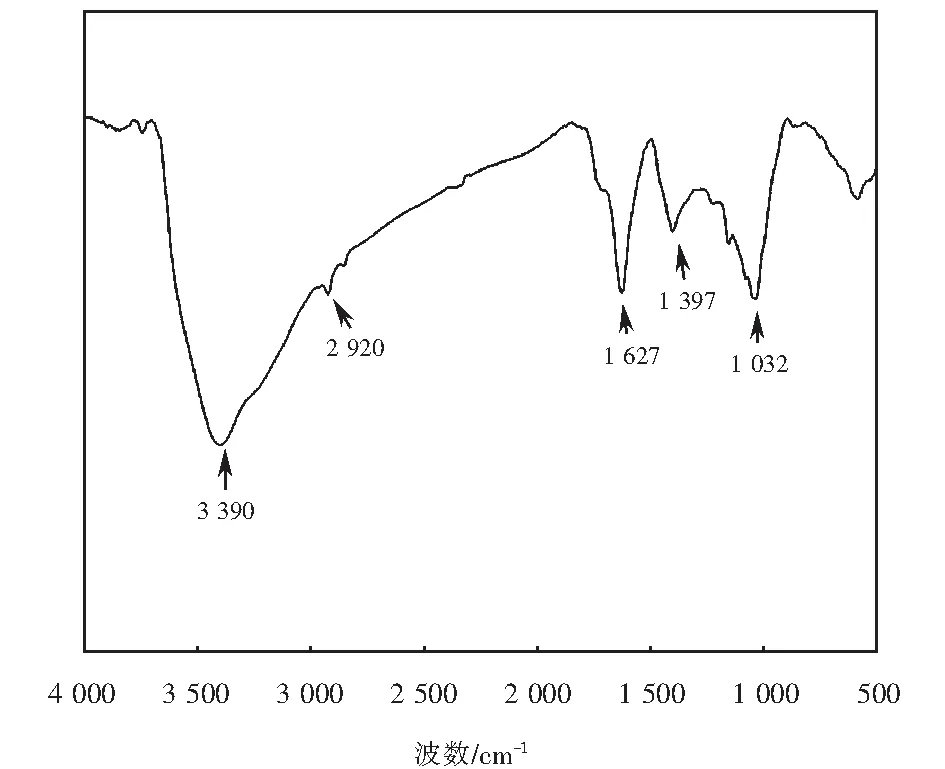
图12 N-rGO的红外光谱图Fig.12 FT-IR spectra of N-rGO
2.11 吸附机理分析
由于磺酰胺基团具有很强的吸电子能力,所以两个芳香环的系统会缺乏电子,因此磺酰胺可以作为强π受体.在SMX中,由于O原子的高电负性导致电子共振稳定,杂芳基的π电子密度进一步降低.氨基官能团也表现为π受体,因为它们能将N的孤电子对提供给芳香环.由于胺基的质子化和异芳香族N能进一步提高其π接受能力,SMZ在低pH下成为更强的π受体.因此,π- π电子给体受体(EDA)与N-rGO表面上的给体芳烃的相互作用是很重要的,是N-rGO与SMZ之间显著的相互作用之一.在中性时π-π EDA与N-rGO表面的π给体芳烃相互作用表现强烈,此时吸附效果最佳.此外,π-π电子受体-受体(EAA)的相互作用也可以发生在与表面芳香环和质子化羧基的正SMZ位点上,但是由于电荷排斥EAA相互作用可能不稳定.这与实验现象中吸附效果受pH值影响较大相符合,低pH值条件下SMZ表现为正离子吸附效果好于高pH值时.同时,质子化的羧基和羟基在中性SMZ中能够与O和N原子形成氢键.另外在足够高的pH(大约比各自的pKa值高两个单位)下,SMZ的碱基与碳质表面的芳香羧基和羟基之间可以发生较强的Lewis酸碱相互作用.也有研究表明非特异性范德华力也是吸附相互作用的一个因素,而在低溶质浓度和吸附剂显著的孔隙效存在的情况下,微孔填充或尺寸排斥相互作用也会发生.综上所述,在N-rGO吸附SMZ的过程中,π- π相互作用可能是吸附的主要作用力[24-26].
3 结论
研究结果表明N-rGO吸附SMZ在60 min内达到平衡,去除率为87.3%,动力学拟合表明吸附过程更加符合一级动力学方程.温度升高不利于N-rGO对SMZ的吸附,吸附等温线分析显示与Langmiur等温吸附模型拟合性更好,单分子层吸附在吸附过程中起重要作用,计算得到的最大吸附容量为574.71 mg/g,吸附潜力巨大,通过热力学分析结果表明吸附过程为自发进行的放热反应.N-rGO对SMZ吸附受pH值影响较大,最佳吸附范围为中性.无机阴、阳离子的存在不会影响N-rGO对SMZ的吸附效果,而在腐殖酸存在的情况下,N-rGO对SMZ的吸附能力出现了下降.表征结果表明N-rGO表面褶皱较多,同时含有丰富多样的含氧官能团,这些结构特征为高效吸附的进行提供了条件.以上结果与分析说明N-rGO能够对水中微量存在的磺胺甲恶唑进行快速有效的吸附,为“吸附-催化氧化”体系的构建与调控提供了基础,有利于下一步研究的继续进行.
