高氯酸掺杂聚苯胺复合阴极的制备及性能研究
2022-04-25周富威佘家璇罗伍庆赵云鹏夏恩杰方文强邓姝皓
周富威,佘家璇,罗伍庆,赵云鹏,夏恩杰,方文强,邓姝皓,b
高氯酸掺杂聚苯胺复合阴极的制备及性能研究
周富威a,佘家璇a,罗伍庆a,赵云鹏a,夏恩杰a,方文强a,邓姝皓a,b
(中南大学 a.材料科学与工程学院 b.有色金属材料科学与工程教育部重点实验室,长沙 410083)
为提高聚苯胺海水电池正极的导电性和放电性能,研究各种制备工艺条件对电极性能的影响。采用电化学的方法,以石墨纸为载体,在高氯酸体系中制备聚苯胺(PANI)/二氧化锰(MnO2)/氧化石墨烯(GO)复合电极,研究复合电极制备的最优条件。采用X射线衍射仪、红外光谱仪和扫描电镜表征复合电极,采用交流阻抗法、循环伏安法和极化曲线研究电极的电化学性能。石墨纸在室温下经30 mA/cm2的电流密度氧化60 min后,在磺基水杨酸(SSA)质量浓度为15 g/L,硫酸锰浓度为0.2 mol/L的苯胺-高氯酸溶液里以电流密度18 mA/cm2聚合20 min,可制备出较优的PMGO复合电极,它与镁合金组成海水电池,以200 mA/g恒流放电至1 V,其比能量可达600 W·h/kg。PMGO复合电极的表面微观形貌是由纳米线组成的三维立体网状结构,聚苯胺与二氧化锰成功复合到氧化石墨烯表面。高氯酸体系掺杂的聚苯胺导电性增强,氧化使石墨纸表面形成大量的氧化石墨烯,为苯胺聚合、复合提供大量活性点,复合后电极比表面积增大,与电解液充分接触,使电极活性物质利用率提高,并降低了电极的极化,电化学性能也远优于AgCl电极。
氧化石墨烯;导电聚苯胺;复合阴极;海水电池;电化学性能
海水电池是一种特别的一次电池,泛指以海水作为电解质的电池,在海上救生设备、海洋标志、海洋应急灯、鱼雷等海上运输、海洋作业和国防领域中有较多的应用。常用的海水电池中金属氧化物阴极(PbO、MnO2)或金属盐阴极(Cu2Cl2、AgCl)材料比能量为90~130 W·h/kg[1-2],存在成本高、密度大、重金属污染严重等缺点,限制了海水电池在民用领域的应用。导电聚苯胺具有质轻、价廉易得、稳定等特点,主要用于超级电容器[3-4]、电池[5-7]、传感器[8]、防腐材料[9]、电磁屏蔽材料[10]、防静电材料[11]等。另外,聚苯胺在海水中的稳定性好,理论比能量超过500 W·h/kg[12],在电池领域有较好的研究潜力和应用前景。目前,采用导电聚苯胺做海水电池阴极已在笔者课题组进行了一段时间的研究[12-14]。
导电聚苯胺电极有压制成型[13-15]、模板(如聚四氟乙烯微孔膜)聚合[16]等方式。由于电极的比表面积小、载体导电性较差,因此在电极工作时,与电解液先接触的外层导电聚苯胺脱掺杂后变为导电性差的本征态聚苯胺,使电极内层工作时的电阻增大,极化增加,活性物质的利用率降低,放电性能受到限制。
本征态聚苯胺不导电,需要掺杂质子酸来导电,故聚苯胺常通过筛选掺杂的质子酸来提高其导电性。报道采用的掺杂酸体系有硫酸[12,17]、盐酸[18-19]、高氯酸[20-21]、硝酸[22]、磷酸[23]等无机酸体系,苯磺酸[9,24]、樟脑磺酸[25]等有机酸体系,以及硫酸和磺基水杨酸等复合酸体系[14,25]等。其中,有机和无机复合酸掺杂体系的导电性优异。在质子酸掺杂聚合聚苯胺过程中,与二氧化锰复合,会减小电极极化,起到稳定剂的作用[14,26]。有研究报道表明,对石墨纸进行氧化处理可形成表面有羟基、羰基、羧基和环氧基等大量含氧官能团[27-28]的氧化石墨烯。石墨纸基体对电极结构有支撑和导流的作用,同时氧化形成的表面活性位点便于聚苯胺附着,从而利用这个结构扩大电极表面积和增强电极导电性。文中希望将上述几种方法进行优化和有机结合,利用电氧化石墨纸在其表面形成丰富的氧化石墨烯(GO),随后将其与高氯酸和磺基水杨酸复合掺杂的聚苯胺以及二氧化锰进行复合,以期提高聚苯胺电极的导电性,从而提高活性物质的利用率和电池放电性能。
1 实验
1.1 电极制备
配制浓度为1 mol/L的硝酸作为氧化的电解液(分析纯,株洲市星空化玻有限责任公司),置于20 ℃恒温水浴槽中。以石墨纸(分析纯,北京晶龙特碳石墨厂)为阳极,不锈钢为阴极,以电流密度30 mA/cm2氧化60 min,氧化后取出浸入清水中,漂洗掉残余的硝酸溶液。
采用正交设计实验,考察硫酸锰浓度、5-磺基水杨酸(SSA)浓度和聚合-复合电流密度等3个因素,确定在高氯酸体系中制备复合酸掺杂聚苯胺复合电极(PMGO)的最优条件,正交实验的因素和水平如表1所示。在含0.5 mol/L苯胺、1 mol/L高氯酸体系中,加入一定量的硫酸锰和SSA配成溶液,置于50 ℃恒温水浴中。以氧化后的石墨纸为阳极,不锈钢为阴极,聚合20 min,获得电极(PMGO)。以同样制备的条件在不锈钢上制备聚合物,经烘干称量,利用获得的电极质量计算比能量。再以相同条件制备出电解液中不含硫酸锰的聚苯胺复合电极,作为对比样品(PGO)。
在室温下,将聚苯胺复合正极(4 cm×4 cm)和镁合金负极(6 cm×6 cm)组成简易的海水单电池,电极间距为5 mm左右,浸入300 mL 质量分数为3.5%的氯化钠溶液中,进行恒电流放电测试(采用ZTE Technology生产的单通道电池检测仪),以3.125 mA/cm2恒流放电到1.0 V,得到电池的放电时间、容量和能量等数据,计算得出电池的比能量,同时结合电极放电时间评估结果,确定聚苯胺复合电极的最优制备条件。
表1 正交设计和因素水平

Tab.1 Factors and levels of orthogonal test
1.2 表征与测试
取复合电极表面的粉末,采用日本Rigaku公司D/max 2500PC型X射线衍射仪,测试条件:Cu靶,扫描速率为8 (°)/min,扫描范围为5°~80°,分析复合电极材料的物相。采用美国Quanta-200扫描电子显微镜观察氧化石墨纸和PMGO的表面形貌,并利用配置的能谱仪(EDS)分析复合电极材料的元素。利用美国Nicolet公司6700型傅里叶变换红外光谱仪,采用KBr压片法,在400~4 000 cm−1内测试,并分析复合电极材料的分子结构。
在室温下,在质量分数为3.5%的氯化钠溶液中,采用Multi-autolab M204电化学工作站,以铂电极为辅助电极,以饱和甘汞电极为参比电极,制备最优复合电极为工作电极的三电极体系,对制备的复合电极进行电化学性能研究。在不同温度下,测量复合电极的极化曲线,扫描速度为5 mV/s,由此计算反应的活化能。循环伏安曲线的扫描速度为50 mV/s,交流阻抗测试的频率为0.1~106Hz,分析电极的电化学性能。
2 结果及分析
2.1 复合电极的最优制备工艺条件
在高氯酸体系下,PMGO复合电极制备工艺条件的结果与分析如表2所示。通过对放电比能量、时间的均值和极差进行综合分析发现,影响电池比能量和放电时间的因素由高到低均为锰离子浓度、聚合电流密度、磺基水杨酸(SSA)浓度。硫酸锰经电化学氧化后会形成二氧化锰,二氧化锰与聚苯胺复合,有稳定电位的去极化作用,因此二氧化锰含量增大,电极比能量增加。由于二氧化锰含量过多时,电极质量增大,会引起电池比能量降低,放电时间缩短,因此硫酸锰适宜的浓度为0.2 mol/L。此外,苯胺聚合、硫酸锰氧化及两者的复合是一个电化学过程,较大的电流才能使两者更好地氧化聚合-复合。由于过大的电流会造成电活性的中间氧化态聚苯胺含量降低,没有电活性的完全氧化态聚苯胺含量增大,并且复合物中二氧化锰含量增加,导致电池比能量降低,放电时间缩短,所以最佳聚合电流密度为18 mA/cm2。在实验中,SSA浓度对比能量和放电时间的影响都较小,表明在复合酸掺杂中,体系本身所含高氯酸的掺杂量对电极性能的影响较SSA更为明显。从比能量的角度分析,SSA的最佳质量浓度应为35 g/L。从放电时间分析,SSA的质量浓度为15 g/L即可。考虑到溶解SSA需要较高液温,且SSA的影响没有高氯酸明显,因此确定SSA的最优质量浓度为15 g/L。综上所述,正交最优复合电极制备条件为:硫酸锰0.2 mol/L,聚合电流密度18 mA/cm2,SSA的质量浓度为15 g/L,即正交表4号数据,其在200 mA/g下放电,比能量达到600 W·h/kg,放电时间达到112 min。最优正交实验比能量数据比聚苯胺的理论能量高,推测是几种因素的综合作用造成的,首先是石墨纸处理的氧化电流较大,其表面形成的含氧基团较多,为苯胺聚合、复合提供了更多的活性位点;其次,掺杂酸的体积较大,使得聚苯胺分子间作用力减弱,分子链上离域增强,因而导电性增强;再者由于聚苯胺具有优异的电化学性能,并且聚合时形成了纳米结构,有利于扩大电极表面,吸附了更多的电荷,并利于电子在其上传递,从而提高了电极材料的利用率;由于电极复合了一定量的二氧化锰,二氧化锰起到了抑制氢析出、减弱极化的作用。这几种因素的协同作用使得整个电极比能量得到比较大的提升。
表2 正交实验结果及分析

Tab.2 Results and analysis of the orthogonal test
Note:1se,2se,seandserepresent the average specific energy and the range of the specific energy under different factors, respectively.1t,2t,tandtrepresent the average discharge time and the range of the discharge time under different factors, respectively.
2.2 表征分析
2.2.1 红外光谱分析
电化学聚合的PMGO的红外谱见图1。PMGO谱图中波数为1 115.84、1 384.38、1 656 cm−1分别对应的是C—O—C、C—O、C—OH和C==O的伸缩振动峰,说明样品表面含氧基团的种类丰富,也说明石墨纸的表面经氧化处理后可成功获得氧化石墨烯。波数为1 240 cm−1和799 cm−1附近分别为苯式结构N—B—N中的C—N和C—C伸缩振动特征峰;醌环结构和苯环结构的伸缩振动吸收峰分别为1 561.83、1 473.82 cm−1,这些都表明聚苯胺的分子结构为苯环和醌环交替出现的骨架;波数1 300 cm−1对应的是C—N+的伸缩振动特征峰,799.26 cm−1处的峰为苯环的C—C键特征峰,在623 cm−1和1 090 cm−1处的吸收峰对应的是高氯酸根的特征峰,说明了高氯酸掺杂的有效性。1 115.84 cm−1是S—O基团的不对称伸缩振动峰,表明SSA也被成功掺杂到聚苯胺上。511 cm−1处的峰对应的是Mn—O键的特征峰,表明二氧化锰与掺杂的聚苯胺复合良好。
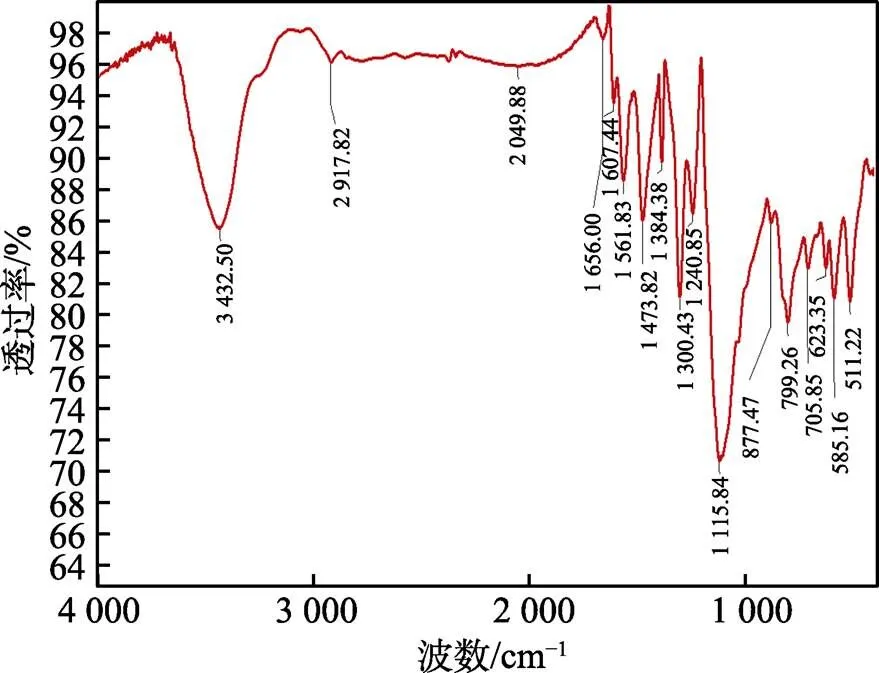
图1 PMGO电极的红外谱
2.2.2 X射线衍射分析
电化学聚合PMGO的XRD图谱见图2,图谱中氧化石墨烯的特征峰2=11°[29]不明显,说明PANI和较大的MnO2粒子联接氧化石墨烯层状结构,引起石墨烯层间距离增加,掩盖了本身氧化石墨烯的特征峰。谱图中最尖锐和强烈的27°附近的峰是石墨纸的特征峰,这是因为样品附着在石墨纸表面未完全剥离,因此包含一部分石墨背景峰。在2为20°和22°附近出现了一定峰宽化的特征峰,说明具有一定结晶度的PANI被成功合成到氧化石墨烯表面,这主要是复合酸掺杂的贡献;2为35.56°、37.06°、55.2°的峰是MnO2的特征峰,PDF卡片对应65-1298,说明硫酸锰已通过电化学氧化的方式转变为二氧化锰,并与一定结晶度的聚苯胺一起复合到石墨纸上。二氧化锰的峰强度远远小于聚苯胺,说明复合材料中二氧化锰晶体含量远少于聚苯胺,或者部分二氧化锰被聚苯胺包裹。经计算,复合电极材料的结晶度为59.28%,这种较高的结晶度有利于电子的传导,因此材料的导电性优异。另外,材料的平均晶粒尺寸为14.7 nm,晶体粒度小而比表面积大,有利于电解液与之充分接触,促进电池反应进行完全。

图2 PMGO电极的XRD谱
2.2.3 表面形貌分析
PMGO电极的表面微观形貌如图3所示,其中经电化学氧化后石墨纸得到的GO如图3a所示,电化学聚合的PMGO电极微观形貌如图3b—d所示。图3a显示石墨纸经氧化后的微观形貌为多层片状结构,层与层的堆叠不太规整,距离增大,宏观表现为氧化后石墨纸厚度增大,表面粗糙,褶皱突起很多。在较低倍率下观察到的PMGO形貌见图3b,显示出明暗相间的区域,明亮区域略微凸起,呈堆叠的圆球状。较暗的区域经高倍率观察(图3c),其微观形貌为纳米纤维状物质交错连接形成的三维立体网状结构。纤维的直径为100 nm左右,长度为2~ 3 μm。三维纳米网状结构使得材料比表面积增大,有利于电解液的渗入和吸附,且不会因为表层聚苯胺脱掺杂反应而使整个电极绝缘,阻碍电极继续反应。图3d是图3b PMGO中明亮区域的高倍率扫描形貌。对图3d区域中明亮球形区域进行EDS分析,分析结果如表3所示。电极主要含有C、O、N、S、Cl、Mn元素。其中C、O、N元素是聚苯胺的主要构成元素,因此含量很高,表明了聚苯胺的骨架组成。S、Cl元素是聚苯胺的掺杂酸元素,分别代表掺杂酸为SSA和高氯酸。虽然掺杂溶液体系中高氯酸含量占比很大,但有机酸SSA的掺杂并不比其少,两者原子比接近1,这也说明复合体系中的有机酸含量不需要太高就可以满足掺杂要求。电极中锰元素含量较少(原子数分数<1%),主要集中在图3b中所示的明亮球形区域,说明MnO2以结晶形式存在于氧化石墨烯之间。同时,过亮区域也证实了MnO2的导电性不如聚苯胺,含量过多会导致电池的比容量下降。这里研究电极中二氧化锰含量比硫酸体系的二氧化锰含量要低很多[26],推断应是高氯酸体系氧化性较强,溶液中的二价锰离子可能在反应前就有部分被化学氧化,因此实际经电化学复合生成的二氧化锰含量不高。此电极的放电性能较硫酸体系电极的性能差别不大,这是由于石墨纸氧化电流较大,因此表面形成了大量含氧基团的氧化石墨烯,复合的活性位点也更多。聚苯胺-二氧化锰更容易在氧化石墨烯表面聚合、复合,提高了材料的比表面积,加快了电极的反应速度,提高了材料的导电性能。另外,二氧化锰作为电极的稳定剂和氧催化还原剂,虽然复合后的含量少,但所起的作用不可忽略。有报道称,电化学氧化制备的二氧化锰存在的氧空位可以改变MnO2的电子结构和质子嵌入,从而提高复合电极的导电性和电极催化氧还原的能力[30-31]。此外,研究表明电化学制备的电极立体结构有着相对合适的比表面积和平均孔径,既能形成较多的有效活性位,也有利于反应物与产物的传递,颗粒更小,分散更均匀。同时,体积较大的复合酸(高氯酸和SSA)掺杂、较大的孔径有利于活性位点的充分利用,促进反应物向活性位点的运输和反应,因此电极表现为极化减弱,放电性能较为优异。

图3 GO(a)、PMGO电极(b、c)的扫描电镜照片和能谱照片(d)
表3 图3d中区域各元素的能谱分析
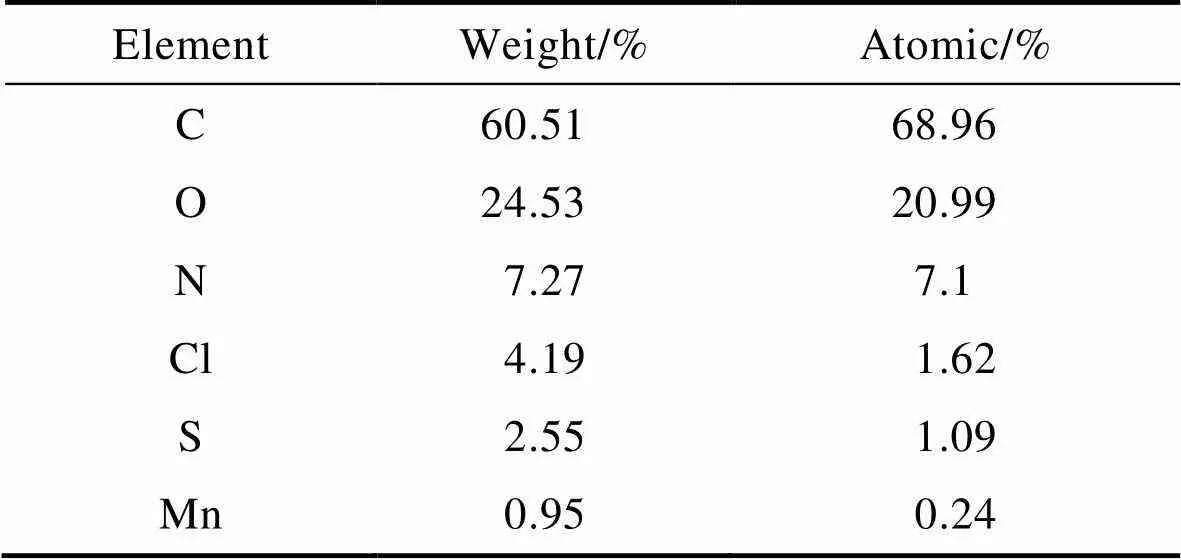
Tab.3 EDS analysis of elements in zone A of Fig.3d
2.2.4 电极的电化学性能
利用不同温度的阴极Tafel曲线求得稳定电位下反应电流(lg)与温度(1/)数据线性拟合,见图4。计算出电极反应在此条件下的活化能为70.27 kJ/mol。由于电极反应活化能较高,由此可知电池反应主要速度控制步骤为氧的还原,而非掺杂酸的脱掺杂。PMGO电极上氧还原的活化能还是低于一般氧还原反应所需要的活化能(90 kJ/mol左右),这说明PMGO复合电极对氧还原有一定的催化活性,较常用的氧阴极性能高。PMGO复合电极之所以催化氧性能较高,是因为电极中含有一定量的二氧化锰。二氧化锰是常见的氧还原催化剂,而电化学氧化制备的二氧化锰会产生许多氧的空位和缺陷,这有利于促进氧还原速控步骤的进行[30-31]。同时,复合电极还具有很大的比表面积和微观上的三维立体纳米网状结构,都有利于促进氧的还原。活化能数据表明,PMGO复合电极有催化氧还原反应和降低极化的能力,可通过降低电极反应活化能来提高反应速度。

图4 lg i和1/T的线性拟合曲线
采用最优条件制备出PMGO复合电极,其循环伏安曲线如图5所示,箭头所指向的循环伏安曲线峰代表自然条件下溶氧的还原反应峰。循环伏安曲线形状类似于平行四边形,表明复合电极具有一定赝电容的特性[32-33],这应该是电极的纳米线三维结构所致,可以吸附较多的电荷用于提升能量。由于曲线所包围的面积较小,表明氧在其上还原时的极化还是较大。虽然MnO2具有减小极化的作用,但EDS的结果显示其含量远低于硫酸体系制备的PMGO复合电极上二氧化锰的含量[26],表明极化的增大与GO上复合的MnO2的量减少有关。这可能由于高氯酸氧化性太强,硫酸锰在反应前有部分已被高氯酸化学氧化,因此经电氧化复合到聚苯胺电极中的MnO2量大大降低,还原催化氧的能力不如硫酸体系的电极。由于整个PMGO阴极反应包括掺杂酸的脱掺杂反应,而这个反应阻力小,另外电极的质量也有所减少,因此整个电极所释放的能量并不低。
PMGO电极在开路电位下的交流阻抗图和等效电路见图6,其谱图由第1象限高中频区的前小后大、2个圆心不在轴上的圆弧与低频区斜率约为45°的直线组成,谱图最后段的数据点波动性较大是由于频率较低所致。第1象限的2个半圆弧表明存在2个界面电子转移过程。结合CV曲线分析结果可知,电荷转移的半圆所代表的反应为聚苯胺的质子酸脱掺杂以及聚苯胺复合阴极上氧的还原。高频区半圆弧的直径代表电荷传输电阻,故分析可知前一个圆弧对应的半圆直径小(1<2 Ω),即反应阻抗较小,表明阴极上聚苯胺质子酸的脱掺杂还原反应的阻力较小。后面的大圆反应的阻力大(2约为6 Ω),表明聚苯胺复合阴极上吸附氧的还原反应阻力较大。低频区的直线斜率与电解质扩散/迁移到电极界面有关[34-35],代表了氧气在电解液和复合电极中的扩散速度。直线斜率在开始阶段偏离45°,在最后段又接近45°,说明存在浓度极化阻抗使得氧的扩散速度变慢,也可能是由于电极表面粗糙或者表面不均一的微孔引起感抗,反映了氧的扩散对整个电极反应起到了重要影响。
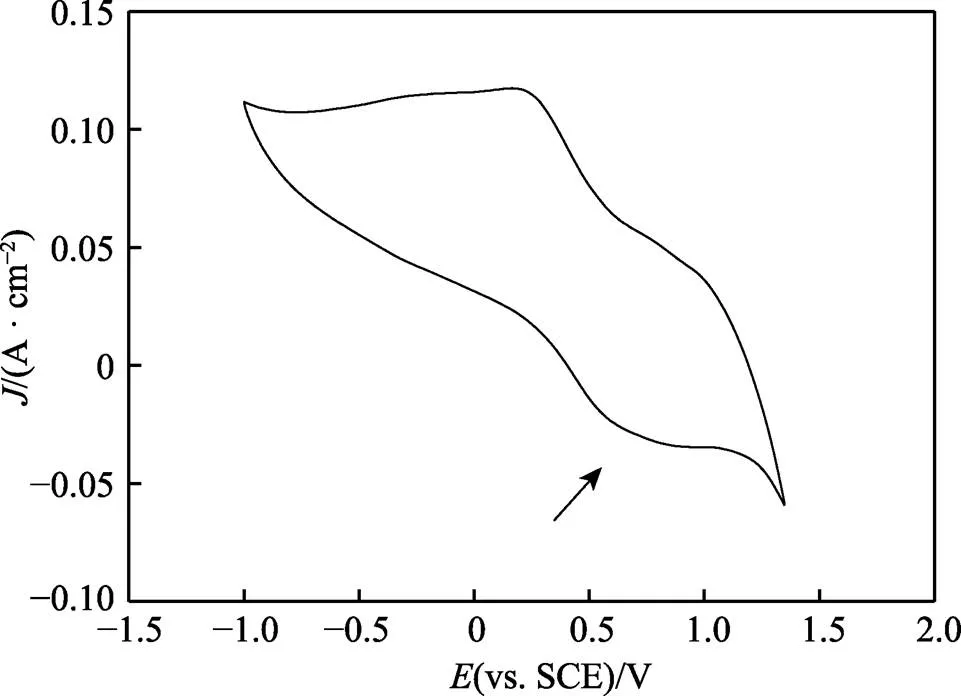
图5 PMGO电极的循环伏安曲线
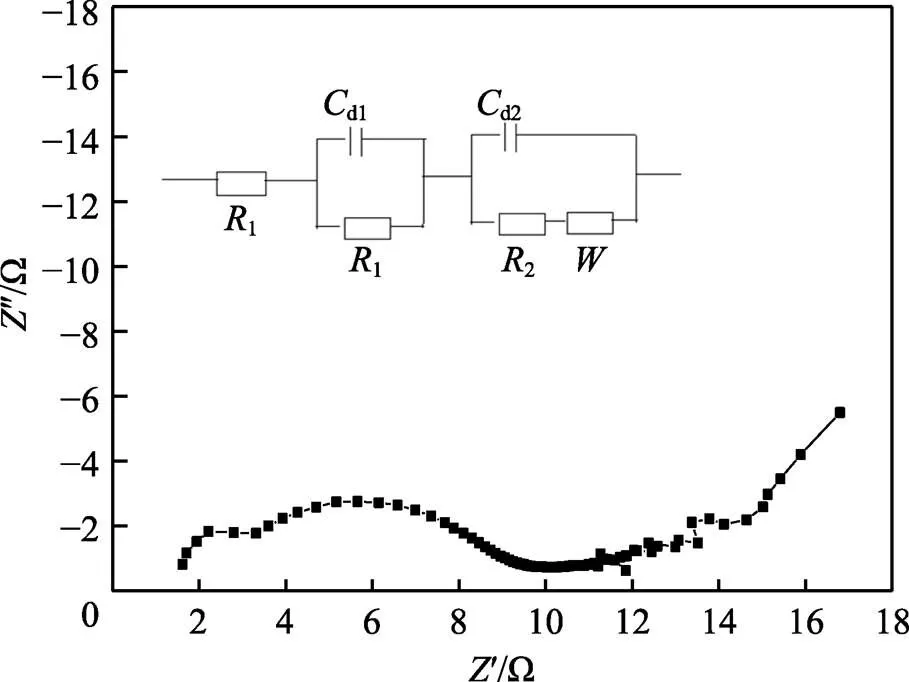
图6 PMGO电极的交流阻抗谱
高氯酸体系掺杂PMGO电极的阻抗谱图与硫酸体系掺杂PMGO电极体系的阻抗谱图有一定的区别[15]。硫酸体系的PMGO电极阻抗谱图只由一个半圆弧和斜线组成,半圆代表质子酸脱掺杂反应,它是一个电荷转移过程,而直线代表氧还原的电化学过程受浓度影响明显,因此正极反应为混合控制。高氯酸体系制备的PMGO电极对氧还原的影响更明显,不仅部分反应是扩散控制,受氧浓度的影响,也有部分反应是电化学控制,因而材料的真实表面积和表面状态对反应速度有更为显著的影响,能有效降低活化能,提高反应速率。
2.3 镁/PGO、镁/PMGO海水电池的性能
采用最优工艺条件制备PMGO复合电极和PGO复合电极,分别与镁合金负极组装成海水电池,研究了其在质量分数为3.5%的氯化钠溶液中恒电流的放电情况,结果如图7所示。由于制备PGO复合电极的聚合溶液体系中没有MnSO4,故PGO电极中不含MnO2。比较2条放电曲线,PMGO的起始放电电压高于PGO,这是由于PMGO电极中含有MnO2,使得其电极电位较PGO更正。放电时,PMGO曲线的斜率较PGO小得多,因此电压下降速度比PGO小,这表明PMGO 复合电极发生反应时的极化阻力明显比PGO复合电极小,也说明MnO2具有显著降低极化阻力的作用,使得PMGO电极的放电性能进一步提高。对比AgCl电极和硫酸体系制备的PMGO复合电极的放电测试数据[26],结果如表4所示。PMGO复合电极的各项放电数据远远优于AgCl电极。可见最优工艺条件制备的PMGO电极进一步拓宽了传统镁海水电池正极的应用范围。另外,高氯酸体系的PMGO复合电极比硫酸体系的PMGO复合电极的比容量和比能量都高,这是由于前者所述复合电极中二氧化锰的含量远小于后者。说明虽然二氧化锰可以稳定电位,但是也会增大复合电极质量,降低电池的比能量。另外,2种电极制备工艺对石墨纸的表面处理也有明显差别,高氯酸体系的石墨纸表面氧化处理时间为60 min,但氧化电流密度为30 mA/cm2;硫酸体系的表面氧化处理时间为100 min,氧化电流密度只有15 mA/cm2,这表明石墨纸表面处理对PMGO复合电极/镁海水电池的放电性能也有较大的影响,氧化电流较大有利于在石墨表面形成更多的氧化石墨烯,也为复合提供更多的活性位点,PMGO复合电极性能得到优化,展现出优异的电化学性能。
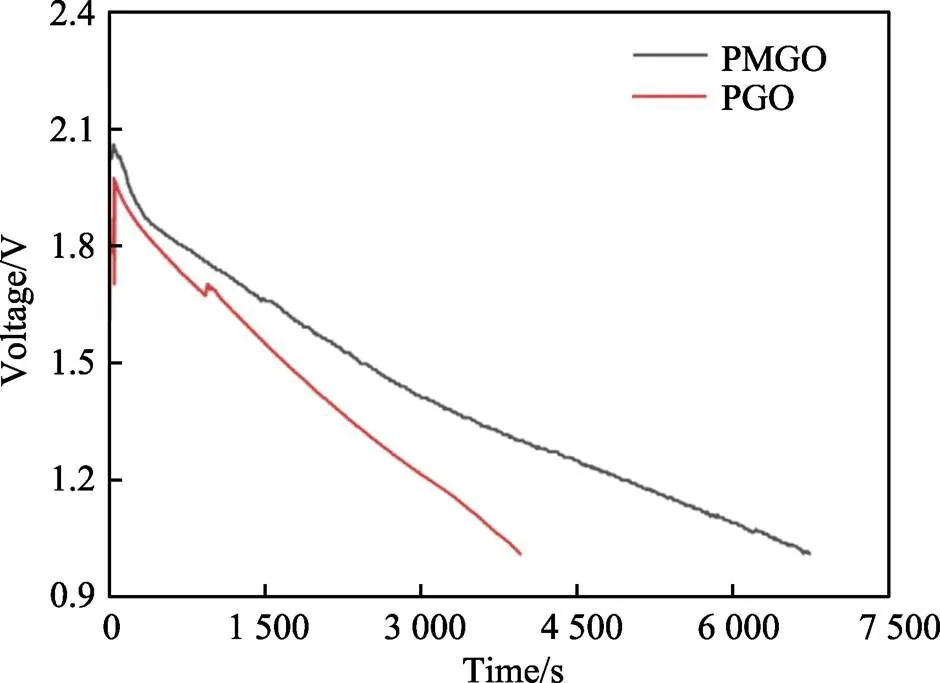
图7 PGO和PMGO电极的放电曲线
表4 4种电极的放电结果比较

Tab.4 Comparison of discharge results of 4 types of electrodes
3 结论
高氯酸复合体系掺杂聚苯胺电极的最佳制备工艺条件:石墨纸在室温下经30 mA/cm2的电流密度氧化60 min后,在硫酸锰浓度为0.2 mol/L、磺基水杨酸(SSA)质量浓度为15 g/L的苯胺-高氯酸体系中,以电流密度18 mA/cm2聚合20 min,获得的PMGO复合电极与镁合金组成的海水电池以200 mA/g恒流放电1 V,其比能量可达600 W·h/kg。
在高氯酸体系下制备PMGO复合电极的三维纳米线结构更利于提高电极的导电性和降低极化。虽然MnO2含量较低,但是其电极质量降低明显,因此电极比能量高于硫酸体系制备的PMGO复合电极和AgCl电极。
石墨纸表面处理工艺对PMGO复合电极/镁海水电池的放电性能影响很大,氧化电流大有利于在石墨表面形成更多的氧化石墨烯,为苯胺聚合和与MnO2复合提供更多的活性位点,提高了电极的电化学性能。
[1] 宋玉苏, 王树宗. 海水电池研究及应用[J]. 鱼雷技术, 2004, 12(2): 4-8.
SONG Yu-su, WANG Shu-zong. Research and Application of Seawater Battery[J]. Torpedo Technology, 2004, 12(2): 4-8.
[2] 蔡年生. 加速发展电雷满足海军需求[J]. 船电技术, 2000, 20(2): 15-19.
CAI Nian-sheng. Accelerated Development of Electric mines to Meet Naval Needs[J]. Marine Electric & Electric Technology, 2000, 20(2): 15-19.
[3] SONG Yang, LIU Sai-er, WANG Bao-yi, et al. Continuous and Controllable Preparation of Polyaniline with Different Reaction Media in Microreactors for Supercapacitor Applications[J]. Chemical Engineering Science, 2019, 207: 820-828.
[4] YILMAZ ERDOGAN P, ZENGIN H, YAVUZ A. Growth and Cycling of Polyaniline Electrode in a Deep Eutectic Solvent: A New Electrolyte for Supercapacitor Applications[J]. Solid State Ionics, 2020, 352: 115362.
[5] 郝彦忠, 武文俊, 康志敏. 导电聚合物在纳米太阳能电池中的应用研究[J]. 高分子材料科学与工程, 2004, 20(6): 46-50.
HAO Yan-zhong, WU Wen-jun, KANG Zhi-min. A Review on Research of Conducting Polymer Application in Nanostructured Solar Cells[J]. Polymeric Materials Science & Engineering, 2004, 20(6): 46-50.
[6] 盖新璐. 导电聚苯胺的合成及其在锂硫电池中的应用研究[D]. 长沙: 国防科学技术大学, 2016: 4-8.
GAI Xin-lu. Study on the Preparation of Conductive Polyaniline and Its Application for Lithium/Sulfur Battery[D]. Changsha: National University of Defense Technology, 2016: 4-8.
[7] KUMAR G, SIVASHANMUGAM A, MUNIYANDI N, et al. Polyaniline as an Electrode Material for Magnesium Reserve Battery[J]. Synthetic Metals, 1996, 80(3): 279- 282.
[8] CHEN Guo-zhen, ZHENG Jian-bin. Non-Enzymatic Electrochemical Sensor for Nitrite Based on a Graphene Oxide-Polyaniline-Au Nanoparticles Nanocomposite[J]. Microchemical Journal, 2021, 164: 106034.
[9] 王霞, 侯丽, 张代雄, 等. 聚苯胺在防腐方面的研究及应用现状[J]. 表面技术, 2019, 48(1): 208-215.
WANG Xia, HOU Li, ZHANG Dai-xiong, et al. Research and Application of Polyaniline in Anti-Corrosion[J]. Surface Technology, 2019, 48(1): 208-215.
[10] RMOHAN R, VARMA S J, JAYALEKSHMI S. Effective Electromagnetic Shield Using Conductive Polyaniline Films[J]. Materials Today: Proceedings, 2019, 8: 371-378.
[11] 张洪锋, 杨锦锦, 吴壮壮, 等. 抗静电聚苯胺改性羊毛纤维的制备[J]. 天津科技大学学报, 2019, 34(4): 42-44.
ZHANG Hong-feng, YANG Jin-jin, WU Zhuang-zhuang, et al. Preparation of Wool/Polyaniline Antistatic Composite Fibers[J]. Journal of Tianjin University of Science & Technology, 2019, 34(4): 42-44.
[12] 邓姝皓, 袁莉君, 徐杨明, 等. 海水电池用硫酸/磺基水杨酸掺杂聚苯胺正极的制备及性能[J]. 高分子材料科学与工程, 2019, 35(7): 141-146.
DENG Shu-hao, YUAN Li-jun, XU Yang-ming, et al. Preparation and Performance of Sulfuric/Sulfosalicylic Acid Doped Conductive Polyaniline Cathode Materials for Sea-Water Battery[J]. Polymer Materials Science & Engineering, 2019, 35(7): 141-146.
[13] 邓姝皓, 易丹青, 刘娟, 等. 硫酸掺杂导电聚苯胺正极材料的电化学制备及性能[J]. 电池, 2007, 37(3): 208-211.
DENG Shu-hao, YI Dan-qing, LIU Juan, et al. Electrochemical Preparation and Performance of Sulfuric Acid Doped Conductive Polyaniline for Cathode Material[J]. Battery Bimonthly, 2007, 37(3): 208-211.
[14] 邓姝皓, 易丹青, 郑康丽, 等. 新型Mg/导电PANI海水激活电池性能研究[J]. 船电技术, 2007, 27(6): 334-338.
DENG Shu-hao, YI Dan-qing, ZHENG Kang-li, et al. Study on the Performance of a Novel Mg/Conducting Polyaniline Seawater Battery[J]. Marine Electric & Electronic Engineering, 2007, 27(6): 334-338.
[15] 徐杨明, 王亚琴, 袁莉君, 等. 复合酸掺杂聚苯胺正极材料的制备及性能[J]. 电源技术, 2020, 44(1): 80-82.
XU Yang-ming, WANG Ya-qin, YUAN Li-jun, et al. Preparation and Performance of Sulfuric/Sulfosalicylic Acid Doped Conductive Polyaniline for Cathode Material[J]. Chinese Journal of Power Sources, 2020, 44(1): 80-82.
[16] 邓姝皓, 王玉. 聚苯胺/聚四氟乙烯导电复合膜的电化学制备和表征分析[J]. 材料导报, 2012, 26(2): 34-39.
DENG Shu-hao, WANG Yu. Electrochemical Synthesis and Characterization of Polyaniline/Polytetrafluoroethylene Conductive Composite Films[J]. Materials Review, 2012, 26(2): 34-39.
[17] GIZDAVIC-NIKOLAIDIS M R, JEVREMOVIC M M, MILENKOVIC M, et al. High Yield and Facile Microwave-Assisted Synthesis of Conductive H2SO4Doped Polyanilines[J]. Materials Chemistry and Physics, 2016, 173: 255-261.
[18] 李居衡. 导电聚苯胺的化学合成及其结构与性能的研究[D]. 昆明: 昆明理工大学, 2014: 15-31.
LI Ju-heng. Study on Chemical Synthesis, Structure and Properties of Conductive Polyaniline[D]. Kunming: Kunming University of Science and Technology, 2014: 15-31.
[19] 金恺. 聚苯胺电极的制备及其在电化学合成苯甲酸中的应用[D]. 大庆: 东北石油大学, 2018: 15-32.
JIN Kai. Preparation of Polyaniline Electrode and Its Application in Electrochemical Synthesis of Benzoic Acid [D]. Daqing: Northeast Petroleum University, 2018: 15-32.
[20] 朱超. 导电聚苯胺作为电池正极材料的性能研究[D]. 哈尔滨: 哈尔滨工业大学, 2010: 23-28.
ZHU Chao. A Study on Performance of Conductive Polyaniline Used as a Positive Electrode of Battery[D]. Harbin: Harbin Institute of Technology, 2010: 23-28.
[21] 高兴斌. 聚苯胺的合成方法及应用[J]. 化工新型材料, 2015, 43(7): 218-219.
GAO Xing-bin. Synthetic Method and Application of the Polyaniline[J]. New Chemical Materials, 2015, 43(7): 218-21.
[22] 周海晖. 聚苯胺及其衍生物的电化学制备和应用研究[D]. 长沙: 湖南大学, 2005: 14-20.
ZHOU Hai-hui. Studies on Electrochemical Synthesis of Polyaniline and Its Derivative and Their Applications[D]. Changsha: Hunan University, 2005: 14-20.
[23] WANG Chun-lei, SUN Li, ZHOU Ying, et al. P/N Co- Doped Microporous Carbons from H3PO4-Doped Polyaniline by in Situ Activation for Supercapacitors[J]. Carbon, 2013, 59: 537-546.
[24] KARAOĞLAN N, BINDAL C. Synthesis and Optical Characterization of Benzene Sulfonic Acid Doped Polyaniline[J]. Engineering Science and Technology, an International Journal, 2018, 21(6): 1152-1158.
[25] KOZIK T, ŚNIECHOWSKI M, ŁUŻNY W, et al. Neutron Diffraction Study of Conducting Polyaniline Doped with (±) Camphorsulfonic Acid[J]. Polymer, 2017, 111: 148-155.
[26] 邓姝皓, 袁莉君, 徐杨明, 等. 聚苯胺/二氧化锰/氧化石墨烯复合电极的制备及性能[J]. 高分子材料科学与工程, 2020, 36(9): 150-156.
DENG Shu-hao, YUAN Li-jun, XU Yang-ming, et al. Preparation and Properties of Polyaniline/Manganese Dioxide/Graphene Oxide Composite Cathode[J]. Polymer Materials Science & Engineering, 2020, 36(9): 150-156.
[27] HUANG Y F, LIN C W. Facile Synthesis and Morphology Control of Graphene Oxide/Polyaniline Nanocomposites via In-Situ Polymerization Process[J]. Polymer, 2012, 53(13): 2574-2582.
[28] SUN Yu-bing, SHAO Da-dong, CHEN Chang-lun, et al. Highly Efficient Enrichment of Radionuclides on Graphene Oxide-Supported Polyaniline[J]. Environmental Science & Technology, 2013, 47(17): 9904-9910.
[29] SUN Yi-ge, TANG Jie, ZHANG Kun, et al. Comparison of Reduction Products from Graphite Oxide and Graphene Oxide for Anode Applications in Lithium-Ion Batteries and Sodium-Ion Batteries[J]. Nanoscale, 2017, 9(7): 2585-2595.
[30] STOERZINGER K A, RISCH M, HAN Bing-hong, et al. Recent Insights into Manganese Oxides in Catalyzing Oxygen Reduction Kinetics[J]. ACS Catalysis, 2015, 5(10): 6021-6031.
[31] SUNTIVICH J, GASTEIGER H A, YABUUCHI N, et al. Design Principles for Oxygen-Reduction Activity on Perovskite Oxide Catalysts for Fuel Cells and Metal–Air Batteries[J]. Nature Chemistry, 2011, 3: 546-550.
[32] BROUSSE T, BÉLANGER D, LONG J W. To Be or not to Be Pseudocapacitive? [J]. Journal of the Electrochemical Society, 2015, 162(5): A5185-A5189.
[33] AUGUSTYN V, SIMON P, DUNN B. Pseudocapacitive Oxide Materials for High-Rate Electrochemical Energy Storage[J]. Energy & Environmental Science, 2014, 7(5): 1597.
[34] HE Xin-yi, LIU Qi, LIU Jing-yuan, et al. High-Performance All-Solid-State Asymmetrical Supercapacitors Based on Petal-Like NiCo2S4/Polyaniline Nanosheets[J]. Chemical Engineering Journal, 2017, 325: 134-143.
[35] DIRICAN M, YANILMAZ M, ASIRI A M, et al. Polyaniline/MnO2/Porous Carbon Nanofiber Electrodes for Supercapacitors[J]. Journal of Electroanalytical Chemistry, 2020, 861: 113995.
Preparation and Properties of Perchloric Acid Doped Polyaniline Composite Cathode
a,a,a,a,a,a,a,b
(a. School of Materials Science and Engineering b. Key Laboratory of Nonferrous Metal Materials Science and Engineering Ministry of Education, Central South University, Changsha 410083, China)
The work aims to study the effect of various preparation technologies on properties of electrode so as to improve the conductivity and discharge property of positive electrode of polyaniline seawater battery. The polyaniline (PANI)/manganese dioxide (MnO2)/graphene oxide (GO) composite electrode was synthesized by electrochemical method on graphite paper and the optimum synthesis condition of the composite electrode was studied. The XRD, SEM and FT-IR were used to characterize the composite electrode. The electrochemical property of the composite electrode was measured by the AC impedance method, cyclic voltammetry and polarization curve. After the graphite paper was oxidized at room temperature for 60 minutes under the oxidation current density of 30 mA/cm2, the optimal PMGO composite electrode was synthesized at the polymerization current density of 18 mA/cm2in HClO4-aniline solution containing sulfosalicylic acid (SSA) of 15 g/Land 0.2 mol/L MnSO4for 20 minutes of polymerization. The seawater battery composed of composite electrode and magnesium alloy discharged to 1 V at a constant current of 200 mA/g, and the specific energy reached 600 W·h/kg. The surface microstructure of the PMGO composite electrode showed a complex 3D network structure constructed by nanowires on graphite paper. Polyaniline and manganese dioxide were successfully compounded on the surface of graphene oxide. The conductivity of polyaniline doped with perchloric acid has been enhanced. A large amount of GO is formed on the surface of graphite paper by oxidation, providing numerous active sites for the polymerization of PANI. Thus, specific surface area of electrode prepared increases and fully contacts electrolyte, which improves the utilization of active material and reduces the composite electrode polarization. The electrochemical property of PMGO is much better than that of AgCl electrode.
graphene oxide; conductive polyaniline; composite cathode; sea water battery; electrochemical property
TQ152
A
1001-3660(2022)04-0348-08
10.16490/j.cnki.issn.1001-3660.2022.04.037
2021-04-11;
2022-02-12
2021-04-11;
2022-02-12
邓姝皓(1973—),女,博士,副教授,主要研究方向为材料电化学。
DENG Shu-hao (1973—), Female, Doctor, Associate professor, Research focus: electrochemistry of materials.
周富威, 佘家璇, 罗伍庆, 等. 高氯酸掺杂聚苯胺复合阴极的制备及性能研究[J]. 表面技术, 2022, 51(4): 348-355.
ZHOU Fu-wei, SHE Jia-xuan, LUO Wu-qing, et al. Preparation and Properties of Perchloric Acid Doped Polyaniline Composite Cathode[J]. Surface Technology, 2022, 51(4): 348-355.
责任编辑:彭颋
