超声治疗动脉粥样硬化性心血管疾病研究进展*
2022-04-24李正革徐礼胜许家林郭丽婷崔慧颖姚育东
李正革 徐礼胜 许家林 郭丽婷 崔慧颖 姚育东
(1)东北大学医学与生物信息工程学院,沈阳110169;2)Faculty of Physical Engineering,Kim Chaek University of Technology,Pyongyang,DPR of Korea;3)沈阳东软智能医疗科技研究院有限公司,沈阳 110015;4)东北大学生命科学与健康学院,沈阳 110169)
动脉粥样硬化(atherosclerosis,AS)是一种全身性心血管疾病;其中脂肪、炎症、细胞和组织疤痕在动脉壁内堆积形成斑块及栓子,是引起大多数临床心血管疾病(cardiovascular disease,CVD)的根本原因[1]。AS 通常可以在不同类型的动脉(心脏、大脑、肾脏和四肢的大动脉或者小动脉)中形成,从而导致多种临床动脉粥样硬化性心血管疾病,如冠心病(coronary heart disease,CHD)、中 风(stroke) 和 慢 性 肾 病(chronic kidney disease,CKD)[1-2]。心血管疾病是目前世界最受关注的疾病之一。自1950 年代以来,在美国每年有超过80 万人死于心血管疾病[2]。另一方面,在西方国家,中风在所有死亡原因中排名第3[1,3];在所有中风疾病中,有87%是缺血性疾病[4]。Dilic等[3]发现,这种脑血管疾病(cerebrovascular disease) 中65%~70% 的 病 例 是 由AS 引 起 的。《2018年中国心血管疾病报告》指出,在中国,心血管疾病导致的死亡率超过40%,高于癌症或其他疾病的死亡率,AS仍然是血管疾病的主要原因[5]。综上所述,AS成为引起心血管疾病如CHD和中风等的主要因素,因此在治疗心血管疾病的过程中清除AS斑块是最受关注的治疗靶点之一。
超声(ultrasound,US)设备是在临床诊疗中应用最广泛的仪器之一,其应用范围越来越广。除了超声成像诊断方面的应用,目前,超声干预多被应用于各种疾病的无创治疗中,为保障人类的生命健康做出重大贡献。一般超声波在身体组织中传播时会产生热作用及机械作用,这些作用会引起病灶组织热凝集坏死、促进生化反应、细胞膜上形成小孔来促进透药等[6-7]。由于超声波的这些特殊作用,它可以应用于很多方面的疾病治疗,例如改善血管疾病[6,8]、促进肿瘤坏死[9]、击碎肾或尿结石破裂[10]、促进透药[7,11]、缓解关节痛[12]及肌筋膜疼痛[13]、改善神经功能[14]等。超声干预治疗动脉粥样硬化性心血管疾病是其中受关注的无创治疗技术之一。
超声干预治疗动脉粥样硬化性心血管疾病包含两种疗法,分别为高强度超声的热疗法和低强度超声的理疗法。在热疗法中,通常使用高强度聚集超声(high intensity focused ultrasound,HIFU)系统(图1a)[6],超声产生的热量可使斑块热坏死。HIFU(普通聚集区域直径1 mm、深度10 mm、超声强度I=100~10 000 W/cm2)暴露在组织中会引起局部组织温度上升至60℃以上,保持这种状态通常会导致大多数组织发生不可逆的凝集性坏死,立即导致细胞凋亡[7]。但在热疗法中,由于斑块与血管壁非常接近,可能对血管中的组织产生严重热损伤。理疗法通过低强度超声(I≤30 W/cm2)的机械、空化和生化作用可以有效地清除AS 斑块[15-16]。在理疗法中,有将装备微小或线型超声探头的导管通过血管插入到病灶发生超声消除斑块的导管系统(图1b)[15-17]和非聚焦超声探头放在病灶外面刺激组织来消除病灶的无创方式非聚焦超声(noninvasive unfocused ultrasound) 系 统 ( 图1c)[18]。有报道将诊断超声作为非聚焦型超声用于治疗,从而实现诊疗一体化[8]。导管式超声(catheter-delivered ultrasound)系统是一种侵入性疗法,由于难避免创伤,因此,其应用存在争论。

Fig.1 HIFU(a)[6],catheter-delivered(b)[17]and unfocused(c)[18]ultrasound system for therapy,and their therapy图1 HIFU(a)[6]、导管式(b)[17]和非聚焦(c)[18]超声治疗系统的外观及其治疗形式
非聚焦超声系统是一种基于无创方式去除血管内斑块或者血栓,减少组织损伤的系统,因此,目前越来越多的研究关注研发这种治疗技术,积极地进行人体、动物和体外模型实验。本文基于超声治疗技术的发展状况,聚焦超声理疗法,比较分析了各种超声干预治疗方法的效果,并在分析疗效和安全性的过程中讨论了治疗参数的影响。最后,讨论了将该超声疗法应用于临床治疗中存在的一些挑战及解决方案。本文综述的目的是针对当前手术治疗心血管疾病中常出现的创伤问题,采用无创方式的新超声疗法,并优化其策略,改善治疗效果,减少创伤带来的风险。为未来超声治疗心血管疾病的应用与推广提供新的技术支持及理论依据。
1 超声治疗技术的发展状况
表1显示超声干预治疗动脉粥样硬化性心血管疾病技术领域的发展状况。超声治疗心血管疾病技术的发展是自1970 年代日本中山氏用超声波治疗实验性心肌梗塞取得疗效[19],且Trübestein 等[20]用线型超声在动物血管中清除血栓为基础开始。其后,1988 年,Siegel 等[21-22]开发了更高适应性的导管式超声治疗设备进行临床实验。1989 年,Kudo等[23-24]开创了无创方式非聚焦超声疗法,并显示出其加速药物纤溶作用,很多研究者开始关注该无创方式的超声疗法发展。从此,导管式超声[15-16,25-29]和无创方式超声疗法[19,30-32]分别通过离体、动物及临床实验发展起来了。其发展过程中引入超声造影剂类型的微泡(microbubble,MB)[33-35]来提高疗效是该技术发展的一次创新。2012 年Wright 等[36]将HIFU 技术应用于治疗心血管疾病,从此开创了新的超声疗法。目前,该项超声治疗技术包括导管式[37-38]和无创非聚焦超声疗法[18],且已取得了较大进展,后续有待进行临床实验研究。但是,超声治疗中常出现的出血[39-40]、对组织[41]及血管产生副作用[42]且斑块碎片导致的远端栓塞[43]等不良后果是阻碍该项技术发展的主要障碍。由于该原因,超声干预治疗动脉粥样硬化性心血管疾病技术尚未广泛应用于临床治疗,在提高疗效的同时亟需解决其治疗的安全性问题。我国研究者自1975 年以来开始关注超声治疗技术[19,32],陆续取得了不少成果[44-46],目前部分成果已经达到开展临床实验的水平[47-49]。

Table 1 Development of ultrasound technology for ASCVD therapy表1 超声治疗动脉粥样硬化性心血管疾病技术发展状况
2 超声理疗法机制
2.1 机械作用
机械振动是超声最基本的作用。当缺乏胶原蛋白并且有弹性的斑块或血栓时,振动作用才有效。超声振动可以增加血液和淋巴循环、改善组织营养、增加细胞膜渗透性、促进高分子化合物的分离、并释放出活性生物物质。因此,它可以清除异常的大分子,例如AS斑块中的脂质[18]。这些机械作用(粒子移动和应力)促进药物浸入到纤维之间的空间,从而提高药物作用[50]。
2.2 空化作用
超声空化(ultrasonic cavitation)作用是在超声消除AS斑块中最重要的机制。超声产生的空化运动在超声传播介质中产生微流和辐射力,这可以清除血块和AS 斑块[51-55]。超声空化是一种现象,在该现象中,暴露于超声场的充满气体的小腔体(称为微泡,MB)会生长、振荡、破裂[7,56],从而在液体介质中施加多种物理应力。根据试验测定,MB振动和其在声场中迅速破裂时,泡核内温度可高达1 000 K,局部压力可高达2.02×109Pa[56-57]。根据空化的运动特性,空化分为稳定空化(stable cavitation)和不稳定空化(unstable cavitation)两种类型。稳定空化(非惯性空化,non-inertial cavitation)是指其在超声场中不被破坏并且保持稳定振动的气泡运动[7,56]。稳定的空化会在周围介质中产生溶液的微流和高剪切压力[57]。不稳定的空化(惯性空化,inertial cavitaion)是指在超声波传播某些周期中充气的气泡膨胀和收缩重复,最后破裂,从而瞬时产生局部高温、高压(冲击波/高速射流)区域的气泡运动[7,56-59]。当空化气泡破裂时发生的大量动量、局部高温、高压、发光、放电和其他现象不仅会增加化学反应,例如局部自由基的发生和碘的释放,还会引起生物效应包括裂解泡沫细胞和破坏大分子[18]。在其机械作用方面,斑块附近的空化作用很容易在细胞膜上形成小孔,从而将药物等活性物质传递到斑块内以溶解斑块[7,56],并机械分离斑块成小块[43,59]。
2.3 生化作用
在超声干预治疗中,上述作用之后的生化作用也很重要。对内皮细胞进行超声刺激可以改善一氧化氮(nitric oxide,NO)的产生并增强其活性[60],其中包括血管舒张作用[61-62]、微循环的改善、血小板聚集的抑制、减少内皮细胞黏附分子的产生、限制平滑肌细胞(smooth muscle cell,SMC)的增殖和迁移、抑制脂质氧化、抗炎、抗氧化、抗凋亡作用、并促进血管内皮生长因子和其他细胞因子的产生[18]。所有这些生物学活性都可以提高超声干预治疗动脉粥样硬化性心血管疾病的疗效。
3 超声干预治疗
本文聚焦超声理疗法,从谷歌学术搜索网络(https://ac. scmor. com) 上 使 用 关 键 词“atherosclerosis, ultrasound therapy/treatment,plaque”检索了100 多篇与超声干预治疗动脉粥样硬化性心血管疾病有关的文献,仔细研读后选择相关度最高的21 篇文献,在此论文中对超声干预治疗方面进行了综述。
3.1 治疗对象及病变
已有学者对人体、动物和体外模型进行了超声干预治疗动脉粥样硬化性心血管疾病的实验研究,这些实验处理的病变如表2 所示。7 项人体临床实验涉及的病变包括中风[39-41,63]、CHD[42,64]和颈部动脉AS[18]。这些疾病都是由AS 或血栓导致的病变,对于治疗靶点,可以选择消除AS斑块或血栓。10 项动物(兔子和小鼠)实验涉及的病变包括由饮食高胆固醇而导致的AS[65-67,70-71]、将自体血凝块注射在颈动脉中而造成的血栓栓塞[43,68-69,72]和将硅胶涂层的尼龙缝合线插入到大脑前动脉阻塞血流的右侧脑中动脉细丝栓塞[73]。表中还列出了使用不同超声干预方法消除AS 斑块及血栓的5 项体外模型实验[29,43,50,74-75]。

Table 2 Lesions of ASCVD and ultrasound intervention therapies表2 动脉粥样硬化性心血管疾病的病变和超声干预治疗方法
3.2 治疗方法
表2的治疗方法栏表明,对于不同病变,使用各种超声干预治疗方法包括超声干预及其与超声造影剂类型的MB 或多种药物配合的方法。对于MB的应用,有研究[43,64-66,69-74]直接将MB注射到血液中,此后超声刺激使实现空化作用。多种常规药物(conventional drug,CD)、纤溶酶原和抗凝剂,例如重组组织型纤溶酶原激活剂(recombinant tissuetype plasminogen activator,rtPA)、阿 托 伐 他 汀(atorvastatin,AV) 钙片、通心络(tongxinluo,TXL)胶囊、血管生成抑制剂(endorstar,ES)、链激酶(streptokinase,SK)和尿激酶(urokinase,UK),作为药物直接口服[18,41,63]或者直接通过静脉注射到病变[39,40,43,69-70,72-73](在体外模型实验中,其药物与血液或血块一起混合装进实验系统中[29,43,50,74])。另外,药物被载在MB 中[70],通过超声干预传递到斑块。这种超声干预与多种常规药物或MB结合的治疗方法在表2中使用符号“+”表示,例如US+rtPA、US+AV、US+MB、US+MB+rtPA 标记分别表示US 与rtPA 结合、US 与AV结合、US 与MB 结合、US 与MB 和rtPA 结合的疗法。支架+US表示结合超声干预消除放置支架后脱落的微栓子;激光+US表示超声与激光结合的治疗技术。标记US 和rtPA 分别表示US 或rtPA 单独使用的疗法。
应用药物或MB后,再对病变部位施加超声干预。大多数用于此类治疗的超声有两种,非聚焦及诊断超声,只有文献[29]使用线型探头。用于此类超声干预治疗的超声、MB和药物应用参数资料在下文中进行详细展示。
4 治疗方法及参数的影响
表3展示了部分研究[18,29,39-43,50,63-75]中的超声干预治疗动脉粥样硬化性心血管疾病结果。结果包括与各种治疗方法相比,斑块消除率、溶栓率、血管再通率、斑块内新生血管的减少和梗塞体积变化等。此外,还有一些超声刺激导致的副作用、出血和温度上升之类的损伤以及碎片信息。本文在对疗效和创伤症状的分析中同时讨论了超声干预治疗方法和参数的作用。
4.1 不同治疗方法的疗效分析
在超声干预治疗中,超声常常与MB或各种溶栓药物配合。将人造MB 注入到血管或者试验管中,可在超声刺激下获得空化作用[43,64-66,69-74]。但是,有些研究[18,29,41,50,67-68]并未在血液或水溶液中另外注入MB,而是用超声单独刺激得到空化作用,这是利用了血液中原本存在的少量气泡。多种常规药物,例如rtPA、AV、TXL、ES、SK和UK,通过动脉注射或口服的方式与超声结合用于治疗[18,29,39-41,43,50,63,67-70,72-74]。超声刺激在血液中把药物传到病变位置以提高药物作用,促进溶解血栓。另外,药物也可以被载在MB 中[70],通过超声作用被传递到病变位置。
通过观察表3的治疗结果可知,超声干预和药物治疗配合的方法比药物单独服用的方法,疗效更好((US+rtPA)>rtPA)[18,40-41,50,63,68-69],表明超声干预对治疗动脉粥样硬化性心血管疾病有效。就超声和MB 结合而言,US+MB 组的疗效高于rtPA 组((US+MB)>rtPA)[43,69-70,72,74]。Culp 等[69]研究发现,US+MB 组对治疗梗塞比US+rtPA 组更好((US+MB)>(US+rtPA))。另外,有研究对比了US+MB 和rtPA 两种方法在脑缺血治疗[39,72]和红色血栓溶栓治疗[43]中的效果,两种方法效果相近。这是因为他们使用了相对低强度的超声[39,72]。另外,绝大多数研究[43,50,71,74-75](包括消除斑块内新生血管、肠系膜栓塞的再通率、脑梗塞率和溶栓率等方面的数据)表明,超声单独使用的疗效不高于所有的结合治疗组,即(US+MB+rtPA、US+MB、US+UK、UK、rtPA)>US,而单独超声治疗组其疗效好于无治疗的对照组,即US>Ctrl。这些结果表明,未与MB结合的超声单独使用产生的机械作用和生化作用对治疗动脉粥样硬化性心血管疾病的影响很小。当单独使用超声时,在血液或水溶液中已存在的微量气泡引起空化作用,但是这不如通过人工MB 注射产生的空化有效。最后,US+MB+rtPA组的疗效比其他各治疗组都更高[43,73-74],即(US+MB+rtPA)>(US+MB、rtPA、US)。这是因为超声空化作用加强了药物的溶栓作用。

Table 3 Results of treating ASCVDs by ultrasound intervention表3 超声干预治疗动脉粥样硬化性心血管疾病结果
4.2 治疗参数的影响
4.2.1 超声参数的影响
治疗参数(包括超声、MB 和药物应用参数)对疗效和安全性有影响,其中最受关注的是超声参数,主要包括超声频率f、强度I、脉冲重复频率(pulse repetation frequency,PRF)、占空比(duty factor,DF)和刺激时间。
超声频率与超声波的衰减、空化作用、辐射力及发热等有关,是决定疗效和安全性的关键因素。通常用于治疗的超声波频率在20 kHz~2 MHz 范围。超声波在较低的频率下可产生更高的功率,从而在其通过的介质中产生剧烈的空化现象,并且可能引起化学变化[57]。因此,早期将低频超声(f<50 kHz)用于超声治疗动脉血栓,并一直被当作传统的超声频率[29,50,54,76-77]。空化过程中产生的MB大小与超声频率成反比关系,低频超声产生大气泡,相反高频超声产生小气泡[56-57]。与高频超声产生的小气泡相比,低频超声产生的大气泡在振动和内爆过程中产生的力更大。过大气泡的内暴力会破坏血管壁组织,从而引起出血。增加超声频率可以减少血液中气泡产生的辐射力,从而使血管的力学损伤减少。因此,近年高频超声(f=0.8~1.6 MHz,表4)在超声干预治疗动脉粥样硬化性心血管疾病中得到了广泛应用[18,41-42,63-64]。在频率高于1 MHz时,MB破裂力的强度大大减小,在频率高于2.5 MHz 时,超声根本不会产生空化现象[57],这会降低治疗效果。Ammi 等[78]在超声干预人类颅骨的实验中显示,在频率为0.12 MHz 时,声压衰减率为22.5%,而在频率为1.03 MHz、2 MHz时,其声压衰减很严重,最高达到96.6%。所以,频率过大(f>3 MHz)不能带来良好的疗效。并且,增加频率会导致对生物体组织的严重摩擦及热损伤。在超声传播方面,低频超声(f<300 kHz)在超声传播的介质中容易产生驻波[79],引起由于负声压增加而导致高出血率。有研究[39]发现,当频率为300 kHz时,超声刺激人类颅骨治疗中风中出现较大的颅内出血(表3和表4),这是由低频超声产生的驻波导致[80]。另外,Ammi等[78]的研究显示,由于低频超声波束宽度较大,0.12 MHz 颅骨内波束形状的畸变比1.03 MHz 和2 MHz 时的更大。这种较大的声速宽度可能会降低疗效,而且对血管造成不利影响的面积也较大。基于以上多种原因,目前被公认适合的治疗超声频率在在0.8~2 MHz范围内(表4)。
检索的文献中超声强度在0.03~30 W/cm2的范围内,特别高的强度(20~30 W/cm2)通常对应着高频率(5.3 MHz)[65,75]。随着超声波频率的增加,声压衰减很大,需要更大的功率,因此,有研究表明[65,75],在高频率情况下使用了较高强度的超声。还有研究[65,71,74-75]显示,随着超声强度或压力的增加,斑块或斑块内新生血管的消除率也在增加(表3)。这是因为随着超声强度的增加,MB 发生不稳定空化,产生更大的辐射力。其实,当声压高于0.6 MPa时,MB破裂,发生不稳定空化[74]。超声强度及空化作用过大会引起血管内皮的机械性损伤或出血并发症及热损伤等不良后果[43,50,75]。所以,超声强度不宜过大。实际上,为了避免机械性损伤及空化的副作用,超声强度(I)、机械指数(MI)分别被限制在0.7~1.25 W/cm2[18,39,41,63]和1.9以下[43,64,73]。为了防止超声波在生物体组织中传播时的发热现象,通常使用脉冲并调控脉冲参数包括PRF和DF。Damianou等[65]对兔子的实验显示,在I=30 W/cm2、f=5.3 MHz、PRF=100 Hz 的 条 件下,DF 每增加10%,组织温度就增加1℃,最后DF 为40% 时,温度可上升4℃。这种现象在Damianou等[75]的另一份研究中也显示了出来。由此可知,脉冲参数在防止组织热损伤中起着重要作用。不同的研究使用不同的脉冲参数,这样脉冲参数可能与其使用的强度和频率有关。检索的所有文献在设定的超声参数条件下,都没有出现热损伤的事件。不同文献中超声刺激时间不同,但是,大多数临床治疗中[18,39,41,63]单次超声刺激的时间为30 min。超声刺激时间越长,斑块消除率越高。Leeman等[74]在超声干预溶栓的实验显示,随着超声刺激时间的增加,溶栓率呈现指数级增长。但是,Roos等[42]指出,超声长时间刺激会破坏血管内皮细胞形成小孔,这样钙就通过小孔流入到SMC,这些现象引起血管收缩,从而产生副作用,这种现象说明超声刺激时间需合理设定,以确保治疗的安全性。
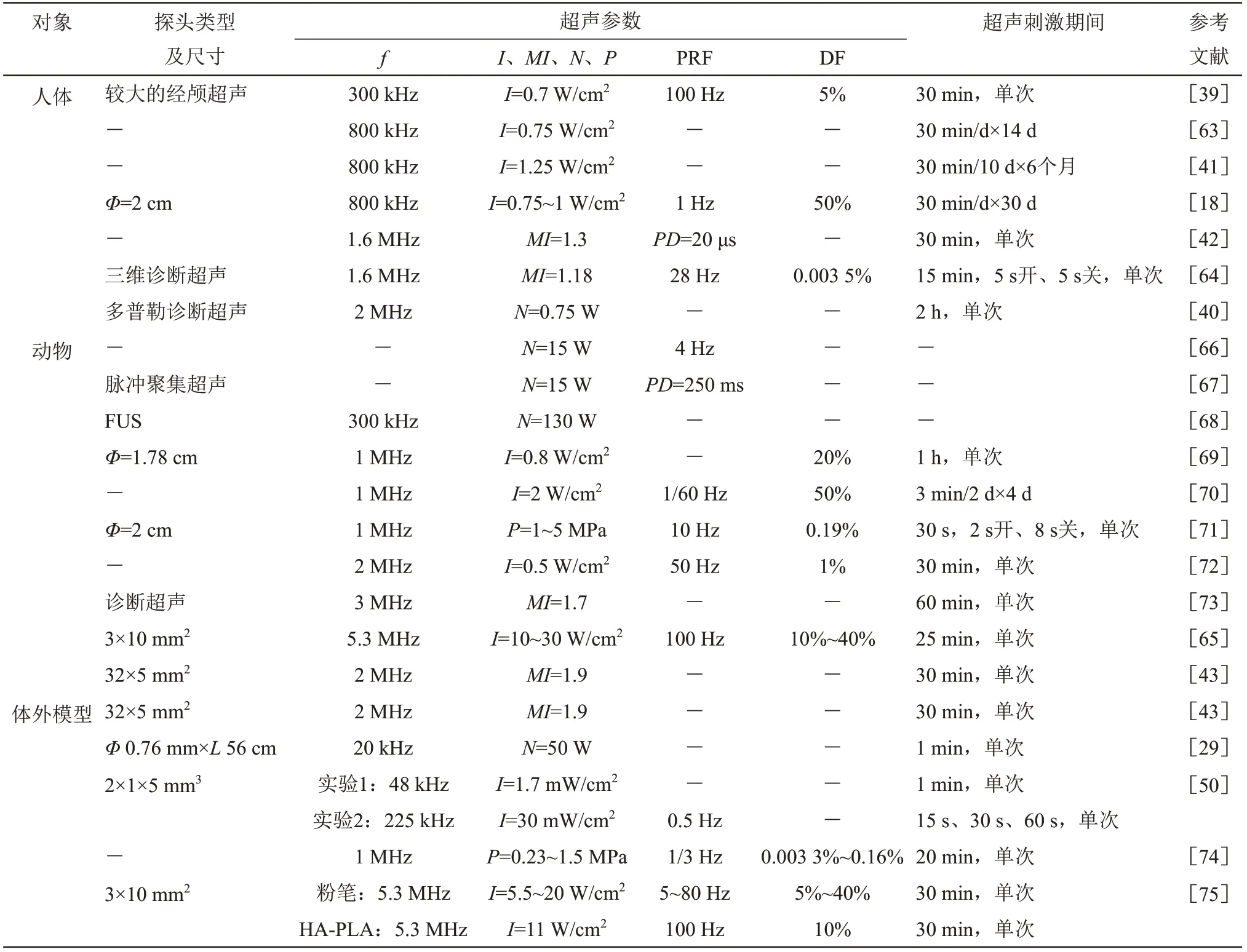
Table 4 Parameters of ultrasound used in treatment表4 用于治疗的超声参数
4.2.2 MB和药物参数的影响
用于超声干预治疗的人造MB和药物也是影响疗效和安全性的因素之一。注射到病变位置的MB直径通常分布在3 μm 范围内[43,69-70,73-74](表5)。但是,用于治疗的MB浓度和应用剂量并未得到统一。它们是既影响疗效,又影响安全性的重要参数。事实上,临床经颅超声溶栓实验[81]表明,MB 浓度与脑出血率之间可能存在关联。MB 浓度及剂量对疗效和创伤的影响是仍需解决的课题。在常规药物与超声干预结合治疗动脉粥样硬化性心血管疾病方面,表6列举了使用不同药物、不同剂量及服用方式的研究文献。rtPA在临床应用中的标准剂量是0.9 mg/kg[40]。但是,应用标准剂量rtPA 也会导致一些出血的现象[39-40](表3)。因此,rtPA临床应用中应该在考虑出血不良反应的基础上限制剂量。除了rtPA 应用组以外,其他药物应用组未发现不良症状。

Table 5 Parameters of MB used in treatment表5 用于治疗的MB参数

Table 6 Parameters of drug used in treatment表6 用于治疗的药物参数
5 安全性分析
5.1 出血和热损伤的实时评估
超声干预导致的创伤和预后副作用是超声应用于临床治疗动脉粥样硬化性心血管疾病中一定要解决的重要问题。超声波在生体组织中传播时产生的机械性振动和空化现象会导致出血[39]、发热[65]和其他副作用[41-42]。为了解决创伤问题,应对各种病变,合理选择治疗参数的同时,在治疗中实时评估创伤程度以避免创伤在确保安全性中具有重要意义。 磁 共 振 成 像(MRI, magnetic resonace imaging) 或计算机断层扫描(CT,computed tomography)可用于观察出血症状[39-40]。一般使用组织学分析(histology analysis)如苏木素和伊红(H&E,hematoxylin and eosin)染色[6,82-83]来评估热损伤。可是,用这种方法不可能在治疗中得出损伤程度。基于热损伤程度与组织温度及受热时间有关的概念,很多治疗通过测量组织温度来实时预测热损伤。测量组织内温度可以将热电偶插入到血管[65,84]或肌肉组织[85-86]中进行。也可以使用基于观测声速变化的超声成像[87-88]或红外热成像方法[89-90]计算组织内或测量体表温度分布。Burtnyk等[91]在超声治疗过程中获取了基于水质子共振频移的实时MRI 测温法[92],以无创伤方式测量组织温度变化。
5.2 碎片的处理
超声干预治疗动脉粥样硬化性心血管疾病的过程中如何安全处理因消除而掉落的碎片是一个重要问题。这些碎片可能通过血液达到远端的小血管或毛细血管,引起严重的血管闭塞。Lu 等[43]和Hong等[29]指出,超声干预治疗产生的碎片绝大多数(99%以上)小于10 μm(表3),充分小于血细胞,所以不会引起严重的远端栓塞。另外,Zhang等[18]指出这些很小的碎片会被网状内皮系统消除。但是,Damianou等[65,75]认为,应重点关注碎片的收集处理,可以使用抽吸技术来收集碎片并且收集设备的尺寸应小于1 mm。碎片处理方面目前有两种大致的研究方向,即用吸收技术收集碎片,或者使用不会引起远端栓塞的超声技术击碎斑块,使得碎片直径小于毛细血管直径。碎片处理是今后将超声干预临床应用的挑战,有待深入研究。
6 总结与展望
动脉粥样硬化性心血管疾病是AS 的发展及变化过程当中产生的一种心血管疾病,如CHD、中风和CKD 等。在这种心血管疾病治疗中,基本治疗方法是消除AS斑块或血栓。近年来,在动脉粥样硬化性心血管疾病的治疗中,超声干预疗法作为非介入方法,与介入方法一起被广泛使用。超声干预治疗动脉粥样硬化性心血管疾病的方法中有两种方法,第一个是使用HIFU热作用的热疗法,第二个是使用低强度超声的机械作用、空化作用及生化作用的理疗法。理疗法中把超声、微泡和药物相互组合起来用于治疗,疗效显著高于常规药物疗法。超声单独刺激不如与微泡或药物结合治疗有效,超声、MB和药物三者结合治疗的疗效最高。
超声参数是影响疗效和安全性的重要因素。以前,临床治疗中常使用低频段(f<50 kHz)的超声,但近年来,高频段(f=0.8~2 MHz)的超声开始用于临床治疗。高频超声产生的小气泡能够减少血管的力学性损伤。但频率过高会导致更大的衰减,而且会对生体组织产生严重摩擦及热损伤。超声疗法中更高的出血率与近300 kHz下产生的驻波有关,应避免使用该频段的超声。低频段超声波速的宽度较大会降低疗效,而且对血管造成不良影响的面积也较大。在查阅的文献中,用于治疗的超声强度在0.03~30 W/cm2范围内。更高强度超声具有更好的疗效,但是,过大的强度会引起组织损伤及温度上升等不良后果。临床治疗中常用强度I=0.7~1.25 W/cm2及机械指数MI≤1.9的超声。考虑到疗效和安全性,脉冲参数和超声刺激时间可根据病变和超声强度及频率设置为不同值。对各种病变要合理调控超声参数从而确保安全性。用于治疗的人造MB平均大小在3 μm左右,随着实验MB浓度和应用剂量的不同,可能影响出血率,这些参数的选择需要慎重考虑。各种用于治疗的常规药物如rtPA、AV、TXL、ES、SK 和UK,其应用剂量和应用方式不同。除了rtPA 发生出血症状以外,其他药物并未引起副作用。
为确保超声干预治疗的安全性,在治疗过程中实时评估创伤程度是必要的。临床中通常使用MRI和CT观察出血症状。此外,可用热电偶、超声成像、红外热成像和MRI 测量组织温度来实时预测热损伤程度。安全处理被超声刺激产生的碎片也是确保安全性的另一重要问题。可以使用两种技术来处理碎片,即抽吸技术或超声刺激使碎片比毛细血管小(<10 μm)的技术。
超声干预治疗方法前景广阔,有望在动脉粥样硬化性心血管疾病临床治疗中发挥重要作用。发展该疗法的过程中,在合理的超声参数选择、提高疗效、碎片处理及安全性保证等方面仍然有不少问题需要解决,有待进一步深入研究。