艾迪注射液联合化疗治疗晚期非小细胞肺癌临床疗效及对患者免疫功能的影响
2022-04-23申文明那兴邦
申文明 那兴邦
肺癌中约85%为非小细胞肺癌[1](non-small cell lung cancer,NSCLC)。药物治疗主要以含铂类药物为主的基础化疗,针对明确致癌驱动基因靶向治疗,如EGFR-络氨酸激酶抑制剂,间变性淋巴瘤激酶(ALK)、受体酪氨酸激酶(ROS1)等重排基因为靶点的药物,以及免疫治疗。治疗目标以缩小肿瘤体积,延缓病情进展,提高生活质量等为主[2]。艾迪注射液由传统中药斑蝥、人参、黄芪、刺五加等经过现代工艺提取、加工制备而成,具有清热解毒,消瘀散结功效[3]。其能抑制肿瘤新生血管形成,诱导肿瘤细胞凋亡,抑制肿瘤细胞增殖等。对肝癌、肺癌、直肠癌等恶性肿瘤有很好临床疗效,能明显延长患者的生存期,改善患者免疫功能[4]。本研究基于肺癌化疗方案联合艾迪注射液治疗对患者炎症指标、血清因子水平,以及免疫功能指标进行比较,报道如下。
1 资料与方法
1.1 一般资料 选取浙江省宁波市鄞州区第二医院2015 年4 月至2019 年10 月收治的120 例晚期非小细胞肺癌患者,男68 例,女52 例,年龄51~75(54.2±6.3)岁。采用随机数字法随机分为对照组和观察组,每组60 例。本研究方案经医院医学伦理委员会审核通过(伦理批件号:NBYZ-2020-018),患者在知情、自愿的前提下同意参加本次临床观察研究,并签订知情同意书。
1.2 纳入及排除标准 纳入标准:(1)符合《中国常见恶性肿瘤诊治规范》中NSCLC 诊断标准[5];(2)功能状态评分(performance status,PS)[6]0~2 分,预计生存期>3 个月,至少1 个病灶直径≥1cm,无重要器官功能障碍,血常规、肝肾功能指标基本正常;(3)患者无化疗的禁忌证。排除标准:(1)合并感染类疾病、大咳血、胸腹水的患者且未得到控制者;(2)合并有其他恶性肿瘤、肺癌脑转移和骨转移患者;(3)合并严重的心、脑血管疾病,伴有肝肾功能不全的患者;(4)孕妇或哺乳期妇女;(5)伴有精神类疾病和智力障碍的患者。
1.3 治疗方法 两组患者在治疗前均给与保肝、保护胃黏膜、止呕、止吐、升白细胞、营养支持等对症治疗。对照组给与常规的化疗方案,多西他赛(上海创诺制药有限公司,批号20160218)60mg/m2+0.9%生理盐水250mL,静脉滴注,每周期第1 天静滴;顺铂(江苏豪森药业集团有限公司,国药准字H20010743,批号20180325)25mg/m2+0.9%生理盐水250mL,静脉滴注,d1~d5。观察组在对照组的基础上,给予艾迪注射液(贵州益佰制药股份有限公司,批号20180117)50mL,加入0.9%生理盐水500mL 中,1 次/d,静脉滴注。两组患者均治疗21d 为1 个疗程。患者在接受治疗过程中每周对其血常规进行监测,每个周期结束前后对患者肝肾功能进行复查,CT 和MRI 评价临床疗效。治疗中根据两组患者治疗情况给予增减用药。
1.4 观察指标(1)免疫指标:对两组患者治疗前后T 细胞亚群进行检查,以评价免疫功能状况。分别在治疗前后抽取外周静脉血,用流式细胞仪检测CD3+、CD4+、CD8+细胞率,以及CD4+/CD8+比例进行分析。(2)血液指标检测:患者在治疗前后采空腹静脉血5mL,采用冷冻离心机3000rpm,离心10min。根据试剂盒(南京生物工程研究所)上操作,采用酶联免疫吸附法(ELISA)分别检测基质金属蛋白酶(MMP-9)、组织蛋白酶抑制剂-1(TIMP-1)、血管内皮生长因子(VEGF)、肿瘤坏死因子-α(TNF-α)水平,采用透射免疫比浊法测定C-反应蛋白(CRP)含量。(3)生活质量评分:分别对两组患者从个体生理、心理、社会功能三方面状态进行评估[7]。(4)不良反应:参照WHO公布抗癌药物不良反应分度为评价标准和分级,评价等级分为0~Ⅳ级,级别越高表明不良反应越严重[8]。观察两组患者在治疗过程中出现骨髓抑制、肝肾功能损伤、贫血、恶心呕吐等不良反应事件,并对出现的不良反应随时进行监测、记录。
1.5 疗效标准[9]完全缓解(CR):肿瘤完全消失,维持时间大于4 周,且未出现新病灶;部分缓解(PR):肿瘤体积缩小50%以上,至少维持4 周,未出现新病灶。疾病稳定(SD):肿瘤体积缩小小于50%或增大未超过25%;疾病进展(PD):靶病灶最大径之和至少增加≥20%,或出现新病灶。总有效率(RR)=(CR+PR)例数/总例数×100%。
1.6 统计学方法 应用SPSS 18.0 软件进行统计分析,符合正态分布的计量资料以均数±标准差()表示,采用计数资料以百分率(%)表示,采用χ2检验,以P<0.05 认为差异有统计学意义。
2 结果
2.1 两组晚期非小细胞肺癌患者一般资料比较 对照组男35 例,女25 例,年龄(55.8±8.5)岁;病理类型:鳞癌41 例,腺癌13 例,鳞腺癌6 例;TNM 分期[5]:ⅢA 期16 例,ⅢB 期30 例,Ⅳ期14 例。观察组男33例,女27 例,年龄(51.5±4.6)岁;病理类型:其中鳞癌38 例,腺癌15 例,鳞腺癌7 例;TNM 分期:ⅢA 期14例,ⅢB 期32 例,Ⅳ期14 例。两组患者年龄、性别、病理类型及临床分期等一般资料比较,差异无统计学意义(P>0.05),具有可比性。
2.2 两组晚期非小细胞肺癌患者近期疗效比较 对照 组PR 26 例,SD 25 例,PD 9 例,总有效率43.33%(26/60);观察组CR 1 例,PR 36 例,SD 16例,PD 7 例,总有效率61.67%(37/60)。两组近期疗效比较,差异有统计学意义(χ2=0.651,P=0.038)。
2.3 两组晚期非小细胞肺癌患者免疫功能指标比较两组患者治疗前CD3+、CD4+、CD8+细胞率,以及CD4+/CD8+比例比较,差异无统计学意义(P>0.05)。与对照组治疗后比较,观察组CD3+和CD4+水平无明显差异(P>0.05);CD8+水平明显降低(P<0.05);CD4+/CD8+比例明显升高(P<0.05)。见表1。
表1 两组晚期非小细胞肺癌患者治疗前后T 细胞亚群比较(%,)
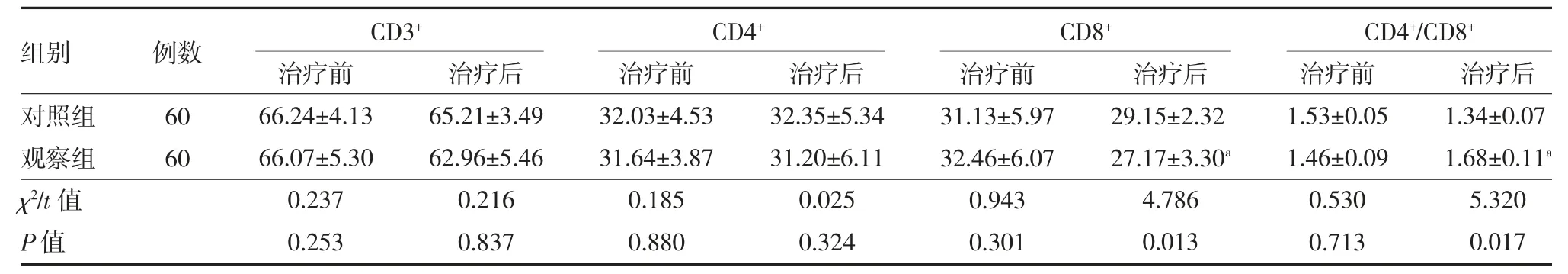
表1 两组晚期非小细胞肺癌患者治疗前后T 细胞亚群比较(%,)
注:对照组给予多西他赛+顺铂;观察组在对照组基础上加用艾迪注射液
2.4 两组晚期非小细胞肺癌患者生活质量评分比较两组患者在治疗前生活质量评分比较,差异无统计学意义(P>0.05)。治疗后两组患者生活质量均有所提高。与对照组比较,观察组生活质量评分明显提高(P<0.05)。见表2。
表2 两组晚期非小细胞肺癌患者生活质量评分比较(分,)

表2 两组晚期非小细胞肺癌患者生活质量评分比较(分,)
注:对照组给予多西他赛+顺铂;观察组在对照组基础上加用艾迪注射液
2.5 两组晚期非小细胞肺癌患者血清VEGF、MMP-9、TIMP-1 水平比较 两组患者治疗前血清VEGF、MMP-9、TIMP-1 比较,差异无统计学意义(P>0.05)。治疗后,两组上述指标均明显低于治疗前(P 均<0.05)。与对照组治疗后比较,观察组VEGF、MMP-9、TIMP-1 水平明显降低(P 均<0.05)。见表3。
表3 两组晚期非小细胞肺癌患者血清VEGF、MMP-9、TIMP-1 水平比较(pg/mL,)

表3 两组晚期非小细胞肺癌患者血清VEGF、MMP-9、TIMP-1 水平比较(pg/mL,)
注:对照组给予多西他赛+顺铂;观察组在对照组基础上加用艾迪注射液;VEGF 为血管内皮生长因子;MMP-9 为基质金属蛋白酶;TIMP-1 为组织蛋白酶抑制剂-1;与本组治疗前比较,aP<0.05
2.6 两组晚期非小细胞肺癌患者血清TNF-α 和CRP 水平比较 两组患者治疗前血清TNF-α 和CRP 水平比较,差异无统计学意义(P>0.05)。治疗后,两组上述指标均明显低于治疗前(P 均<0.05)。与对照组治疗后比较,观察组TNF-α 和CRP 水平明显降低(P 均<0.05)。见表4。
表4 两组晚期非小细胞肺癌患者TNF-α 和CRP比较(pg/mL,)

表4 两组晚期非小细胞肺癌患者TNF-α 和CRP比较(pg/mL,)
注:对照组给予多西他赛+顺铂;观察组在对照组基础上加用艾迪注射液;TNF-α 为肿瘤坏死因子-α;CRP 为C-反应蛋白;与本组治疗前比较,aP<0.05
2.7 两组晚期非小细胞肺癌患者不良反应比较 两组患者在治疗过程中常见的不良反应为骨髓抑制,贫血,肝肾功能损伤及消化道反应,消化道反应为恶心、呕吐、腹泻及食欲减退等,无治疗相关性死亡。贫血、恶心呕吐、腹泻及消化道反应均为轻度。与对照组比较,观察组的骨髓抑制、贫血、肝肾功能损伤、恶心呕吐、乏力发生率明显低于对照组(P<0.05)。两组脱发、腹泻发生率比较,差异无统计学意义(P>0.05)。
3 讨论
NSCLC 治疗重在早发现、早诊断、早治疗,其预后与肿瘤分期和患者治疗效果密切相关。艾迪注射液是天然药用植物提取组方而成,斑蝥性辛、热,具有破血逐瘀、攻毒蚀疮的功效,其含有斑蝥素能阻滞肿瘤细胞有丝分裂,减少氧化应激反应,预防多药耐药[10]。人参性平、味甘,能恢复心脏功能,改善身体衰弱,增强机体免疫力[11]。黄芪味甘,性微温,具有补气固表、生津、利水消肿的功效,是抗肿瘤药物中常见辅助药。研究发现,其能抑制P21 蛋白和细胞周期蛋白表达,抗氧化应激,抑制肿瘤细胞增殖[12]。刺五加味辛,性温,具有祛湿止痛、强筋骨、补肾安神等功效。研究发现,其能通过调节Bax 和P53 蛋白表达,抑制肿瘤细胞的增殖[13]。本研究结果显示,联合用药近期疗效观察组总有效率为51.67%,明显高于对照组的43.33%,提示联合用药能明显提高NSCLC 患者近期疗效。
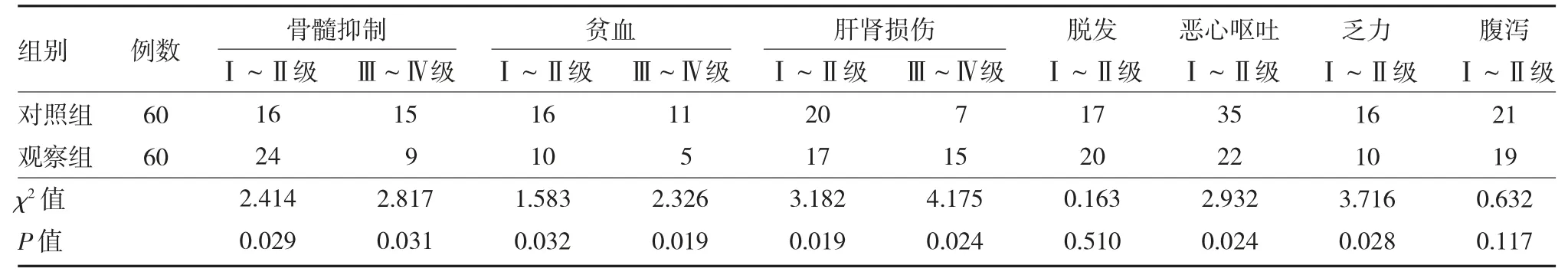
表5 两组晚期非小细胞肺癌患者不良反应发生率比较(例)
VEGF 为一种高度特异性的促血管内皮因子,VEGF 的过度表达与恶性肿瘤病程,转移情况,肿瘤分期等有关[14]。MMP-9 可以通过释放VEGF 以参与血管生成,可重塑细胞外基质动态平衡[15]。TIMP-1 能抑制类蛋白酶,又不使蛋白酶变性,其水平与肺癌的发生发展有密切的关系[16]。本研究显示,与对照组比较,治疗后观察组VEGF、MMP-9、TIMP-1 水平明显降低。提示联合用药能明显预防肿瘤远处转移,有效抑制肿瘤侵袭。T 细胞亚群和NK 细胞在体液免疫调节中发挥重要作用,是衡量机体免疫功能的重要指标。本研究显示,与对照组比较,观察组CD8+水平明显、CD4+/CD8+比例明显升高。提示中药对外周血淋巴T 细胞亚群水平有显著影响,能够促进机体免疫能力的恢复。本研究显示,治疗后观察组在骨髓抑制、贫血、肝肾功能损伤、乏力等不良反应发生率方面明显低于对照组,提示化疗药物联合艾迪注射液能降低化疗药物所带来的毒副作用,并且安全性高。
综上可知,艾迪注射液联合化疗对晚期NSCLC近期疗效确切,协调增强化疗药物疗效,能改善患者生存质量,提高机体免疫功能,降低化疗药物不良反应,患者耐受性好。
