25例转移性Xp11.2/TFE3易位相关性肾细胞癌临床分析
2022-04-21王博文一乔保平苗腾飞洪星磊冯一鸣陈跃帅
王博文一,乔保平,李 攀,苗腾飞,洪星磊,冯一鸣,陈跃帅,张 超,高 远
(郑州大学第一附属医院泌尿外科,河南 郑州 450052)
Xp11.2/TFE3易位性肾细胞癌属于罕见的小眼畸形相关转录因子(microphtalmia-associated transcriptional factor, MiTF)家族易位性肾细胞癌[1]。2004年WHO首次将Xp11.2 易位性肾细胞癌作为肾细胞癌的一个单独分类[2]。本文回顾性分析郑州大学第一附属医院25例转移性Xp11.2/TFE3易位性肾细胞癌,探讨总结其临床表现、影像学特征、诊断方法、治疗及预后等,并复习相关文献,旨在提高对转移性Xp11.2/TFE3易位性肾细胞癌的认识。
1 资料与方法
1.1 研究对象收集于2013年1月至2021年6月郑州大学第一附属医院收治并经病理学确诊为转移性Xp11.2/TFE3易位性肾细胞癌的所有病例。
纳入标准:1)经病理学检查免疫组化技术检测出TFE3融合蛋白或荧光原位杂交技术(fluorescence in situ hybridization, FISH)检测出TFE3融合基因,目前分子遗传学检测(如FISH)是诊断Xp11.2/TFE3家族易位性肾细胞癌的最佳标准[3];2)确诊时已发生区域淋巴结转移或远处转移的Xp11.2/TFE3易位性肾细胞癌;3)通过复诊及随访发现区域淋巴结转移或远处转移的Xp11.2/TFE3易位性肾细胞癌。
排除标准:1)同时合并有其他系统的原发性恶性肿瘤的Xp11.2/TFE3易位性肾细胞癌患者;2)患有其他严重影响术后正常康复的疾病或患有其他难治性疾病的Xp11.2/TFE3易位性肾细胞癌患者;3)拒绝随访的Xp11.2/TFE3易位性肾细胞癌患者。
1.2 方法记录本次研究纳入的25例Xp11.2/TFE3易位性肾细胞癌患者的临床资料,包括临床表现、体格检查、影像学检查结果、手术方式、病理学结果(免疫组化、FISH)、辅助治疗方案、随访时间以及疾病的转归预后情况等。
1.3 随访检索、查阅郑州大学第一附属医院数据库的初诊病例、复诊记录,通过电话联系等方式进行随访记录,截止时间为2021年12月31日或患者因Xp11.2/TFE3易位性肾细胞癌转移而死亡。总生存时间定义为确诊Xp11.2/TFE3易位性肾细胞癌至死亡或随访截止的时间。
1.4 统计学处理采用SPSS 22.0进行统计学分析,选择Kaplan-Meier法计算转移性Xp11.2/TFE3易位性肾细胞癌患者的中位生存时间,绘制生存曲线,应用log rank检验比较生存曲线组间差异,并进行单因素生存分析,检验水准α=0.05。
2 结果
2.1 临床资料25例转移性Xp11.2/TFE3易位性肾细胞癌患者中,男18例,女7例,男女比例为2.571.00。患者年龄12~63岁,中位年龄32岁。19例(76.0%)患者表现出临床症状,余6例(24.0%)患者均无明显临床症状,体检发现患肾占位而就诊。1例患者有2型糖尿病病史2 a,1例患者有慢性阻塞性肺疾病病史30 a余,2例患者有肿瘤家族史(分别为母亲患乳腺癌、父亲患食管癌)。见表1。
2.2 辅助检查1例患者仅行彩超检查,19例患者行计算机断层扫描(computed tomography,CT)检查,7例患者行磁共振成像(magnetic resonance imaging,MRI)检查,其中2例患者行CT和MRI检查。1例患者表现为双肾占位,24例患者CT表现为单侧单发病灶,其中左肾占位13例,右肾占位11例。瘤体最大直径为2.8~18.0(7.53±3.70)cm。彩超检查示:1例患者经彩超检查发现肾占位性病变及淋巴结转移。CT检查示:19例转移性Xp11.2/TFE3易位性肾细胞癌患者术前行CT平扫及增强检查,1例患者CT表现为双肾占位,余18例患者CT表现均为患肾占位。CT平扫表现为稍高密度或等密度实性或囊实性团块,多数为圆形或类圆形,少数呈不规则分叶状;肿块皮质期增强不明显,髓质期明显强化;肿块内部多为不均质成分组成,6例病灶内部可见钙化灶。4例可见患侧肾静脉或腔静脉充盈缺损,疑为瘤栓。8例患者可见淋巴结转移,4例患者可见一处或多发远处转移。MRI检查示:7例转移性Xp11.2/TFE3易位性肾细胞癌患者初诊行MRI平扫加动态增强检查。转移性Xp11.2/TFE3易位性肾细胞癌患者泌尿系统MRI均表现为T2加权图像上呈异质低信号,弥散加权成像呈稍高信号。MRI结果均考虑患肾占位,恶性可能。可疑瘤栓2例,其中1例患者可见淋巴结转移,1例患者可见一处或多发远处转移。病理检查示:25例患者经免疫组化确诊为Xp11.2/TFE3易位性肾细胞癌。肿瘤切面可见出血坏死25例,可见钙化6例。分子检查示:8例患者经FISH检测TFE3融合基因阳性。见表2。

表1 25例转移性Xp11.2/TFE3易位性肾细胞癌患者的临床资料
2.3 TNM分期根据术前影像学结果及术后病理学结果,应用2017年美国癌症联合会制定的肾癌TNM分期对25例Xp11.2/TFE3易位性肾细胞癌患者进行分期。原发肿瘤T分期:T1期10例(40.0%),T2期7例(28.0%),T3期7例(28.0%),T4期1例(4.0%)。区域淋巴结N分期:N0期15例(60.0%),N1期10例(40.0%)。远处转移M分期:M0期20例(80.0%),M1期5例(20.0%)。TNM分期:Ⅰ期患者5例(20.0%),Ⅱ期患者6例(24.0%),Ⅲ期患者9例(36.0%),Ⅳ期患者5例(20.0%)。
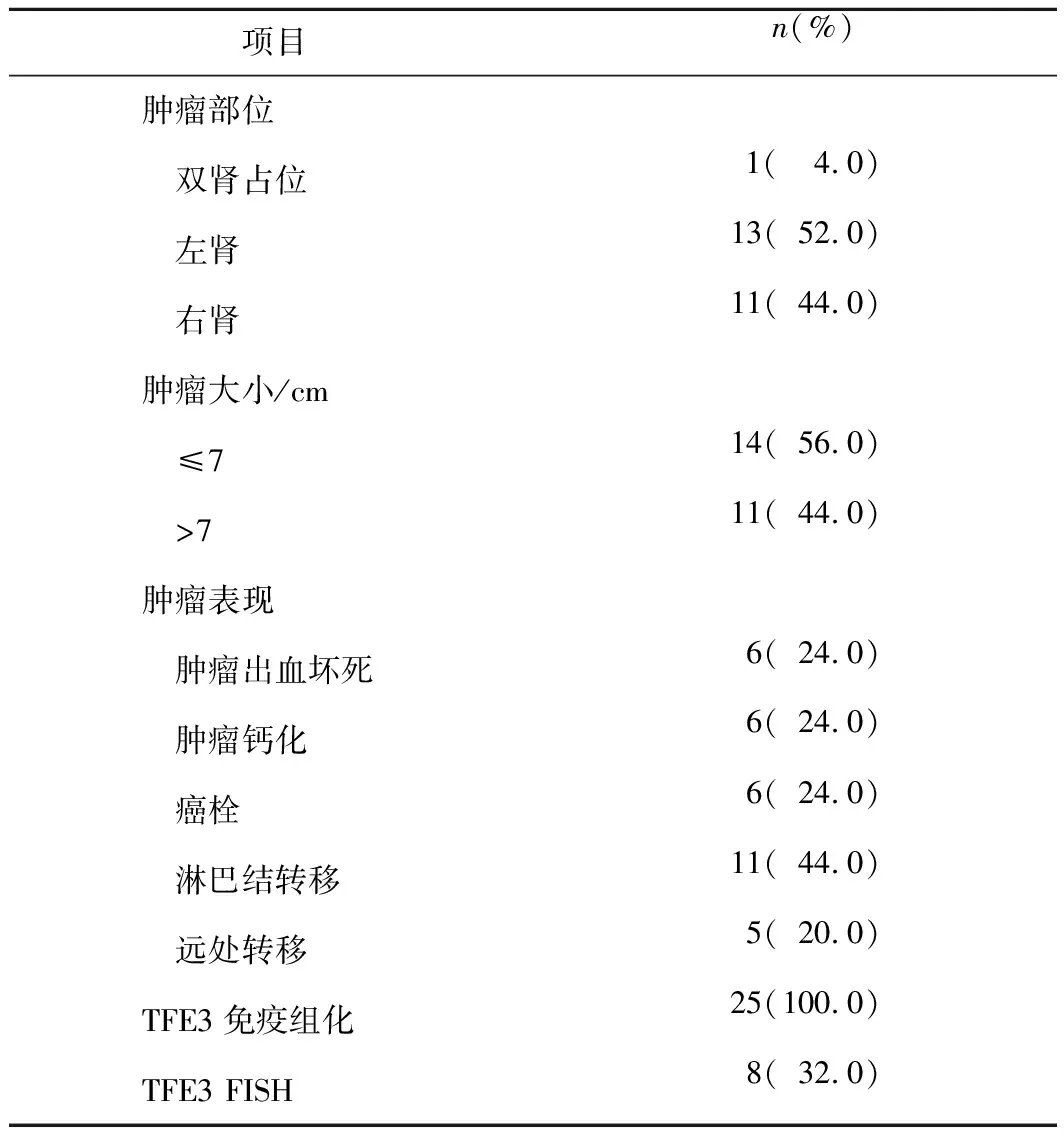
表2 25例转移性Xp11.2/TFE3易位性肾细胞癌患者的辅助检查资料
2.4 治疗方案手术方式:25例转移性Xp11.2/TFE3易位性肾细胞癌患者主要采取以手术为主的治疗方案,其中1例患者采用CT引导下肾肿瘤射频消融,其余24例患者均行手术治疗,包括。腹腔镜根治性切除术10例(40.0%)、腹腔镜下根治性切除+输尿管切除+膀胱部分切除术1例(4.0%)、后腹腔镜根治性切除术2例(8.0%)、机器人辅助部分切除术2例(8.0%)、机器人辅助根治性切除术1例(4.0%)、机器人辅助根治性切除术+淋巴结清扫术1例(4.0%)、机器人辅助根治性切除术+腔静脉癌栓取出术1例(4.0%)、机器人辅助根治性切除术+腔静脉癌栓取出术1例(4.0%)、开放根治2例(8.0%)、开放根治+腔静脉癌栓取出术1例(4.0%)、开放根治+肾静脉癌栓取出术1例(4.0%)、开放根治+腔静脉癌栓取出术1例(4.0%)。
辅助治疗方案:5例患者失访且无复诊记录,20例转移性Xp11.2/TFE3易位性肾细胞癌患者中有12例(60.0%)采用靶向药物治疗,2例(10.0%)化疗,1例(5.0%)放疗,5例(25.0%)患者无辅助治疗。12例靶向药物治疗中,应用阿昔替尼1例,阿帕替尼1例,培咗帕尼3例,舒尼替尼2例,索拉非尼1例,1例患者先后应用了舒尼替尼、培咗帕尼、安罗替尼,余3例具体靶向药物应用不详。
2.5 随访结果随访时间截止至2021年12月31日,25例转移性Xp11.2/TFE3易位性肾细胞癌患者初诊出院后获得随访20例(80.0%),失访5例(20.0%)。本研究中有15例患者初诊时已发生淋巴结转移或远处转移,10例患者初诊后出现病情进展(疾病进展定义为初诊治疗后Xp11.2/TFE3易位性肾细胞癌出现复发、新发转移灶等情况)。
2.6 生存情况纳入研究的25例Xp11.2/TFE3易位性肾细胞癌患者中有5例(20.0%)失访,9例(45.0%)至2021年12月31日随访结束仍生存,11例(55.0%)患者因Xp11.2/TFE3易位性肾细胞癌转移而死亡。20例转移性Xp11.2/TFE3易位性肾细胞癌总生存时间为5~65个月,中位总生存时间42.0个月。Xp11.2/TFE3易位性肾细胞癌患者1、2、5 a疾病特异性生存率分别为70.0%、60.0%、50.0%。见图1。

图1 25例Xp11.2/TFE3易位性肾细胞癌患者总生存曲线
2.6 单因素分析转移性Xp11.2/TFE3易位性肾细胞癌患者的预后影响因素25例患者中5例患者确诊为转移性Xp11.2/TFE3易位性肾细胞癌后,郑州大学第一附属医院数据库中无复查记录且失访,无法统计其生存时间及生存情况。因此,本研究对剩余20例转移性Xp11.2/TFE3易位性肾细胞癌患者生存结果影响因素进行单因素生存分析。结果显示,瘤体最长直径>7 cm是转移性Xp11.2/TFE3易位性肾细胞癌患者的预后危险因素(χ2=4.078,P=0.043)。见表3。
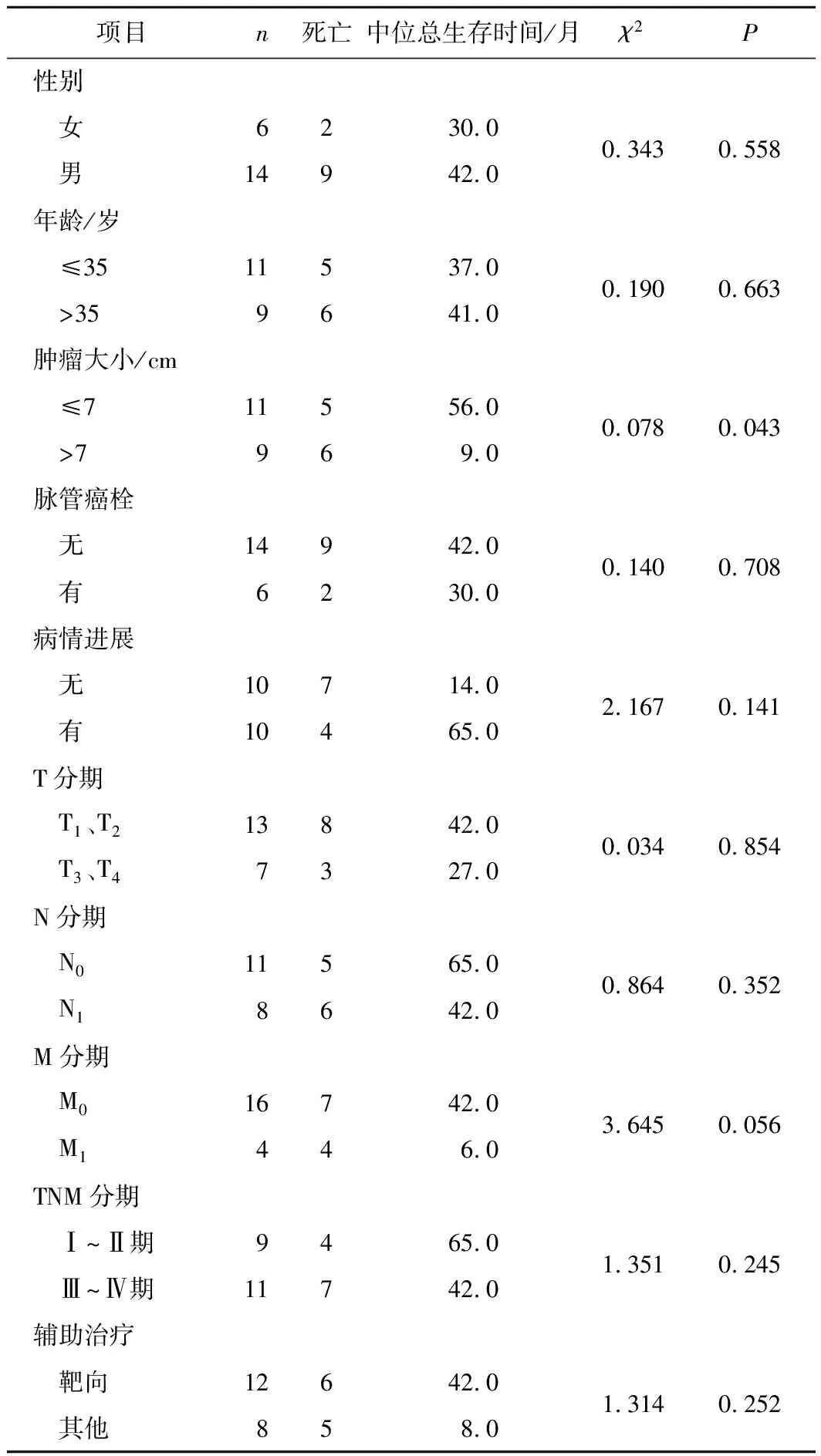
表3 20例转移性Xp11.2/TFE3易位性肾细胞癌患者的单因素生存分析结果
3 讨论
Xp11.2/TFE3易位性肾细胞癌具有显著的基因改变特征,即TFE3基因发生断裂并与相应的基因发生平衡易位从而形成新的TFE3融合基因[4],即Xp11.2/TFE3易位性肾细胞癌。目前Xp11.2/TFE3易位性肾细胞癌明确的基因易位形成的融合基因有5种,分别为PSF-TFE3融合基因、NonO-TFE3融合基因、ASPL-TFE3融合基因、PRCC-TFE3融合基因及CLTC-TFE3融合基因[5-8]。
Xp11.2/TFE3易位性肾细胞癌是一种具有独特基因类型改变的,新分类的肾癌独立亚型,在儿童和青少年患者中多见,由40.0%儿童肾细胞癌和1.6%~4.0%的成人肾细胞癌组成[9]。Xp11.2易位性肾细胞癌占MiTF家族易位性肾细胞癌的90%以上[10]。Xp11.2/TFE3易位性肾细胞癌预后与透明细胞癌患者相似,但相比乳头状细胞癌患者差距较大,伴有远处转移和年轻患者的预后通常较差[11]。由于Xp11.2/TFE3易位性肾细胞癌发病率极低,影像学检查、免疫组化及FISH等诊断体系尚不完善,存在漏诊可能性极大,在成年人中Xp11.2/TFE3易位性肾细胞癌的发病率可能被严重低估。
Xp11.2/TFE3易位性肾细胞癌术前诊断主要依靠CT、MRI等影像学检查,影像学表现与其他常见类型的肾细胞癌极易混淆,但仍具有一定的参考价值,例如CT平扫可出现典型的肿块内环形钙化影;其确诊主要依靠经病理学免疫组织化学技术(免疫组化)检测出TFE3融合蛋白或荧光原位杂交技术FISH检测出TFE3融合基因。
Xp11.2/TFE3易位性肾细胞癌的相关研究尚不深入,其治疗方法没有形成指南性的建议,根治性切除手术为主要治疗方式。对于泌尿外科和肿瘤科医生来说,面对儿童及青少年等肾脏肿瘤患者,术前应考虑到Xp11.2/TFE3易位性肾细胞癌的可能性,并熟悉其临床特性。目前报道预后良好的Xp11.2/TFE3易位性肾细胞癌患者,都是在未发生淋巴结或者远处转移前进行根治性肾切除术,这提示根治性手术是目前最有可能获得良好预后的方式,患肾根治性切除术是Xp11.2/TFE3易位性肾细胞癌患者首选的手术方式[12],但也有Xp11.2/TFE3易位性肾细胞癌患者行射频消融辅助肾肿瘤剜除术且随访良好的病例报道[13]。部分Xp11.2/TFE3易位性肾细胞癌患者在诊断初期已发生淋巴结转移或远处转移,手术无法完全阻断肿瘤的进展,已经发生转移的Xp11.2/TFE3易位性肾细胞癌患者需要术后辅助治疗,延长生存时间。Damayanti等[14]提出雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)信号通路在Xp11.2/TFE3易位性肾细胞癌中被激活,由此基因向下调控mTOR信号通路,因此临床上可采用mTOR抑制剂、靶向血管内皮生长因子受体疗法、免疫疗法或靶向上皮间质转化信号通路疗法等作为其辅助治疗方案。其中,靶向药物治疗是目前较为有效的辅助治疗选择,舒尼替尼、索拉非尼,西罗莫司等药物能部分延长Xp11.2/TFE3易位性肾细胞癌患者疾病无进展生存时间及总生存时间[15-16],但预后较其他常见肾癌亚型差,因此术后密切长期随访十分必要[17]。
总之,Xp11.2/TFE3易位性肾细胞癌是一种临床罕见的肾细胞癌亚型,多发生于儿童及青少年,绝大多数为单侧、单发病灶,双侧发病罕见;临床表现同其他肾细胞癌类似,通常表现为肉眼血尿,腰腹部疼痛、腰腹部肿块等,且出现典型的肾癌三联征并不多见,出现肉眼血尿的概率明显高于肾透明细胞癌和乳头状肾细胞癌。影像学检查为Xp11.2/TFE3易位性肾细胞癌术前诊断的主要依据,其确诊依赖病理学检查,包括免疫组织化学检査TFE3融合蛋白和FISH检测TFE3融合基因。转移性Xp11.2/TFE3易位性肾细胞癌同大多数肾恶性肿瘤一样,晚期患者生存率低,预后差,目前主要治疗手段为根治性手术治疗及术后辅助治疗,靶向药物治疗优于其他辅助治疗方案。本研究虽具有一定局限性,但也为以后转移性Xp11.2/TFE3易位性肾细胞癌的研究和患者的管理提供了参考依据,我们迫切期望多中心、大样本、长随访周期的相关研究来进一步研究该疾病。
