程序性死亡受体1抑制剂联合奥沙利铂、替吉奥和阿帕替尼治疗晚期胃癌的临床疗效和安全性
2022-04-21黄小玉李颖霞姜利彬周明霞何益信温洪涛
黄小玉,李颖霞,姜利彬,周明霞,何益信,温洪涛
(郑州大学第一附属医院消化内科,河南 郑州 450052)
胃癌是一种重要的全球性疾病,据不完全统计,每年有超过100万的新发病例,其中近一半的胃癌新发病例发生在中国[1-2]。虽然通过早期发现、内镜和手术治疗,胃癌的死亡率在逐年下降,但是从总体来看晚期胃癌预后很差,手术无法切除的病例和复发病例几乎不能够被治愈,这严重危害了人类的生命和健康,同时也加重整个社会的医疗负担[3]。
手术切除被认为是恶性肿瘤的唯一根治性治疗方法。然而,由于胃癌术后复发率高,且许多患者手术已进入晚期,所以全身化疗是其替代手术的主要治疗方法[4]。目前,被广泛用于人表皮生长因子受体2阴性转移性胃癌的标准一线化疗为双重细胞毒性方案,是包括氟嘧啶+铂或两种药物联合表柔比星或多西他赛的三联方案[5]。但是部分患者在一线化疗治疗后仍会复发,在此情况下主要推荐紫杉醇联合雷莫芦单抗的二线方案[6]。晚期胃癌或转移性胃癌患者常接受一线和二线细胞毒药物化疗,然而,这些患者的预后不好,很少能够被治愈。如果在接受二线化疗后,这些患者的总生存期、疾病无进展生存期在治疗后仍然达不到预期水平,就没有其他更好的治疗方法可以选择[7]。因此,为了尽可能提高晚期胃癌患者的治愈率、降低死亡率,寻找一种对于晚期胃癌患者更好的治疗方案势在必行。
随着医学的进步和研究的深入,联合治疗逐渐进入了人们的视野。阿帕替尼靶向治疗联合两种或两种以上化疗药物治疗晚期胃癌患者的效果已经得到证实[8-10],可以提高患者的总生存期和疾病无进展生存期。另外,化疗联合PD-1免疫治疗也已得到证实效果优于单独治疗[11-13]。此外,2020年,已有学者发表了卡瑞利珠单抗联合奥沙利铂、替吉奥和阿帕替尼作为可切除、局部晚期胃或胃食管交界处腺癌围手术期治疗的疗效和安全性的研究[14],这项前瞻性的研究结果显示了PD-1抑制剂联合奥沙利铂、替吉奥和阿帕替尼SOXAP方案在中国可切除、局部进展期胃腺癌或胃食管交界处腺癌患者围手术期的治疗潜力。本研究对PD-1抑制剂联合奥沙利铂、替吉奥和阿帕替尼治疗晚期胃腺癌患者的临床疗效和安全性进行了研究,现将结果报道如下。
1 资料与方法
1.1 一般资料收集2019年10月至2021年3月在郑州大学第一附属医院治疗的60例晚期胃癌患者,按照治疗方案分为PD-1抑制剂联合奥沙利铂、替吉奥组(SOXP组,30例)和PD-1抑制剂联合奥沙利铂、替吉奥和阿帕替尼组(SOXAP组,30例)。本研究已通过郑州大学第一附属医院伦理委员会批准。2组患者详细资料比较见表1。
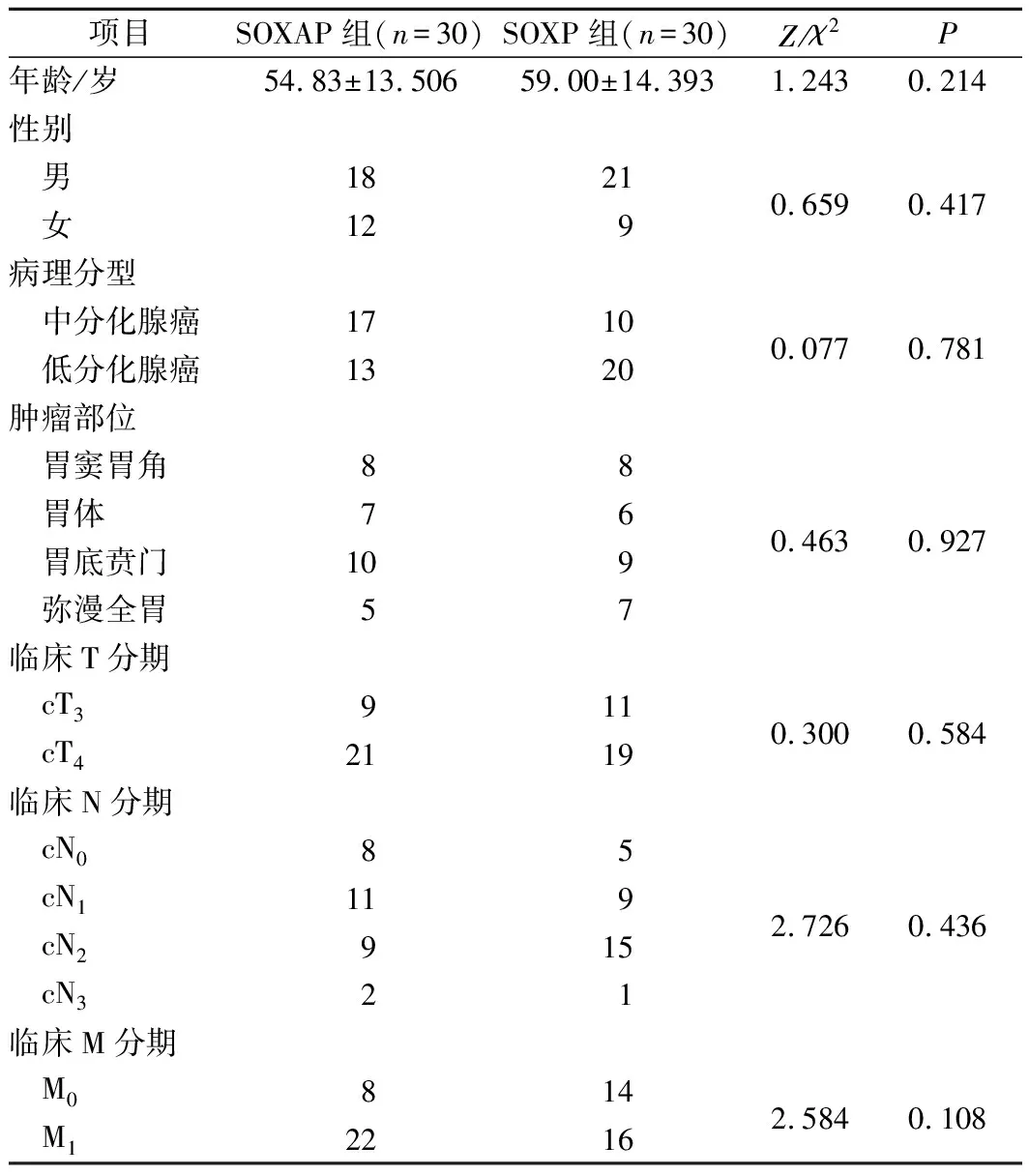
表1 2组患者一般资料比较
1.2 纳入和排除标准纳入标准:1)年龄>18~<75岁;2)经病理学确诊为胃癌;3)接受过规范化治疗包括手术、化疗;4)末次治疗至开始接受此方案治疗的间隔时间为3~4 周;5)KPS评分≥60分;6)至少具有一个可客观测量或评价的病灶;7)无化疗、靶向治疗和免疫治疗的禁忌证;7)临床预期生存期≥3个月。排除标准:1)大手术伤口未完全愈合者;2)同时存在其他恶性肿瘤及传染性疾病;3)排除重要脏器功能障碍的患者;4)妊娠期或哺乳期妇女;5)合并其他肿瘤的患者;6)对奥沙利铂、替吉奥、阿帕替尼、PD-1药物及其辅料过敏者;7)具有影响口服药物的多种因素。
1.3 治疗方案SOXP组给予替吉奥40~60 mg/次,每天2次,第1~14天;奥沙利铂130 mg/m2,静滴大于2 h,第1天;PD-1抑制剂200 mg/次,第1天;21 d为1个周期。SOXAP组在SOXP组基础上联合阿帕替尼500 mg,每天1次,第1~21天。
1.4 近期疗效评价方法近期疗效根据实体瘤疗效评价标准1.1分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD),以CR+PR计算总有效率,CR+PR+SD计算总疾病控制率。
1.5 不良反应评价方法治疗相关不良反应有骨髓抑制、消化道反应、高血压、手足综合征、乏力、血管瘤等,每个周期行血常规检查及血压监测,根据WHO抗肿瘤药物不良反应评价标准分为0~Ⅳ度
2 结果
2.1 2组患者近期疗效比较60例患者均可进行近期疗效评价。SOXP组患者CR 0例、PR 5例、SD 16例、PD 9例,总有效率为16.7%,总疾病控制率70.0%。SOXAP组患者CR 0例、PR 12例、SD 16例、PD 2例,总有效率为40.0%,总疾病控制率93.3%。SOXAP组患者总有效率、总疾病控制率明显高于SOXP组,差异均有统计学意义(χ2=4.022,P=0.045;χ2=4.007,P=0.045)。
2.2 2组患者生存分析比较SOXAP组疾病无进展生存期明显长于SOXP组(P=0.038)。见图1。
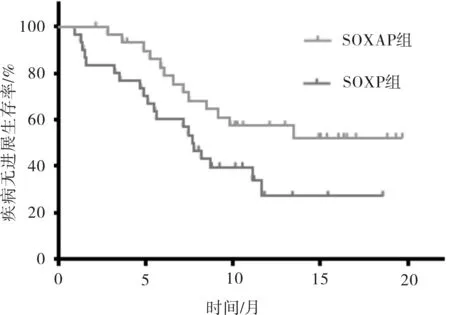
图1 2组患者疾病无进展生存比较
2.3 2组患者不良反应比较SOXAP组和SOXP组不良反应均可耐受,未影响治疗的顺利进行。SOXAP组血管瘤总发生1例(3.3%),SOXP组8例(26.67%),SOXAP组总发生率低于SOXP组(χ2=4.706,P=0.030)。SOXAP组骨髓抑制、消化道反应、高血压、手足综合征、乏力总发生20例(66.67%)、7例(33.33%)、5例(16.67%)、3例(10.00%)、1例(3.33%),其中Ⅲ、Ⅳ度分别为2(6.67%)、1例(3.33%)、1例(3.33%)、1例(3.33%)、0例(0.00%);SOXP组总发生分别为21例(70.00%)、14例(46.67%)、0例(0.00%)、3例(10.00%)、2例(6.67%),其中Ⅲ、Ⅳ度分别为3例(10.00%)、2例(6.67%)、0例(0.00%)、1例(3.33%)、0例(0.00%);SOXAP组和SOXP组骨髓抑制、消化道反应、高血压、手足综合征、乏力总发生率比较差异无统计学意义(χ2=0.077,P=0.781;χ2=3.590,P=0.058;χ2=3.491,P=0.062;χ2<0.001,P>0.999;χ2<0.001,P>0.999)。
2.4 2组患者生活质量比较SOXAP组治疗后KPS评分明显高于SOXP组(t=10.095,P<0.001)。见表2。
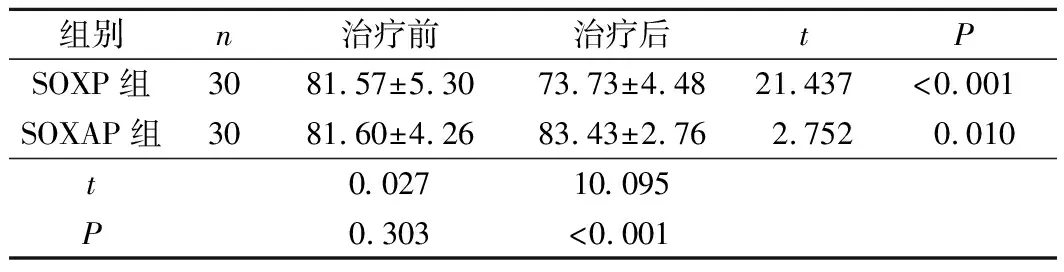
表2 2组患者KPS评分比较 分
3 讨论
胃癌作为一种恶性程度极高的肿瘤,预后极差,已经成为我国最常见的肿瘤之一。胃癌的确诊通常较晚,发现时常进展至中晚期。手术、化疗、放疗和营养支持治疗是治疗胃癌的传统方法。然而,晚期胃癌手术疗效极差,能获取外科手术机会者不足20%。化疗在晚期胃癌中作为一线治疗方案,但临床治疗效果有限,不能很好阻止或延缓病程。一项日本的Ⅲ期临床试验研究[15]显示,奥沙利铂联合替吉奥一线治疗胃癌的总有效率为56%~59%,疾病无进展生存期为5.5~6.5个月。在靶向治疗方面,我国研发的阿帕替尼表现出一定程度的生存获益,抑制肿瘤生成和进展,且已有学者证明,SOX联合阿帕替尼临床疗效明显优于SOX[16-19]。
近几年来,肿瘤的治疗已经进入了免疫治疗时代,免疫治疗在晚期胃癌中具有相当大的潜在价值,幽门螺旋杆菌或EB病毒感染导致的慢性炎性改变是促进胃癌发生、发展的重要因素[20]。在炎性因子和趋化因子的介导下,多种免疫细胞,如巨噬细胞、T细胞、中性粒细胞和髓源抑制性细胞等迁移至肿瘤微环境。免疫细胞分泌的一些细胞因子,如IFN-γ和IL-1等,可上调免疫检查点的表达,抑制免疫反应的程度,因此胃癌是免疫治疗潜在人群。在Keynote-012研究中,给予程序性死亡配体1阳性晚期胃癌患者程序性死亡配体1抑制剂治疗,可达到22.2%的有效率。因此,靶向免疫检查点治疗是相当有前景的治疗模式。随着靶向治疗、生物治疗药物的发展,越来越多的治疗方案被应用于临床。免疫治疗与化疗联合靶向治疗是值得探索的治疗模式,当然更全面深入研究肿瘤微环境中复杂的相互作用机制是一切免疫治疗的基础。胃癌化疗联合靶向及免疫治疗尚处于起步阶段,Ⅲ期临床试验结果显示PD-1抑制剂联合奥沙利铂、替吉奥和阿帕替尼方案疗效优于PD-1抑制剂联合奥沙利铂、替吉奥方案。因此开展PD-1抑制剂联合奥沙利铂替吉奥和阿帕替尼在晚期胃癌的临床疗效和安全性研究十分必要。
本研究为单中心的回顾性研究,结果发现,SOXAP组患者总有效率、总疾病控制率、KPS评分明显高于SOXP组,SOXAP组发生血管瘤发生率较SOXP组明显降低,且SOXAP组疾病无进展生存期明显长于SOXP组。这进一步证实了PD-1抑制剂联合奥沙利铂、替吉奥和阿帕替尼方案用于晚期胃癌治疗的优势。
综上所述,PD-1抑制剂联合奥沙利铂、替吉奥和阿帕替尼方案临床疗效显著,安全性高,明显提高患者生活质量,并能改善患者生存,有望成为一种有效治疗晚期胃癌的新方案。
