黄栀祛伤水质量标准研究*
2022-04-20谢宏赞罗纯清
朱 芹 ,赵 娟 △,谢宏赞 ,王 兴 ,罗纯清
(1. 湖南省湘潭市食品药品检验所,湖南 湘潭 411000; 2. 湖南省湘潭市中医医院,湖南 湘潭 411000)
黄栀祛伤水为湖南省湘潭市中医医院的医院制剂,由黄连、黄柏、大黄、栀子、牡丹皮、红花、乳香、没药、薄荷、白矾10 味中药组方,具有清热解毒、活血化瘀、消肿止痛功效,主治肢体损伤、肿胀疼痛伴灼热、红肿者。方中大黄、黄连、黄柏、栀子清热燥湿、泻火解毒,为君药[1-3];牡丹皮清热凉血,乳香、没药活血消肿、化瘀止痛,红花活血化瘀,共为臣药[4-5];薄荷、白矾疏散解表、透疹行气、燥湿止痒、解毒杀虫,为佐药[6-7]。该方参考清代吴鞠通的《温病条辨》拟订,经多年临床实践验证,目前正在申报医院制剂批准文号,但尚无质量标准。为了全面、有效地控制黄栀祛伤水的质量,本研究中采用薄层色谱(TLC)法对方中黄连、黄柏、大黄进行定性鉴别,采用高效液相色谱(HPLC)法测定方中盐酸小檗碱、栀子苷、丹皮酚的含量。现报道如下。
1 仪器与试药
1.1 仪器
E2695型高效液相色谱仪(美国Waters 公司),配有2998型二极管阵列检测器、2695型自动进样器、Empower3色谱工作站;ABS-135S 型电子天平(瑞士梅特勒-托利多公司,精度为0.01 mg);KQ-250DB型数控超声波清洗器(昆山市超声仪器有限公司,功率为500 W,频率为40 kHz);明澈-D24UV纯水/超纯水一体化系统(德国默克密理博公司);硅胶G薄层板(青岛海洋化工有限公司)。
1.2 试药
黄栀祛伤水(湖南省湘潭市中医医院制剂室,批号分别为 20210106,20210211,20210325,规格为每瓶500 mL);栀子苷、丹皮酚、盐酸小檗碱对照品(批号分别 为 110749 - 201919,110708 - 201908,110713 -202015,纯度分别为97.1%,99.8%,85.9%),黄连、黄柏、大黄对照药材(批号分别为120913 - 201310,121510 - 201807,120902 - 201912),均购自中国食品药品检定研究院;甲醇、乙腈为色谱纯,其他试剂均为分析纯。
2 方法与结果
2.1 TLC 鉴别
黄连[8]:取样品 20 mL,加甲醇100 mL,超声提取(功率为500 W,频率为40 kHz)30 min,滤过,取续滤液,作为供试品溶液。另取黄连对照药材0.25 g,同法制成对照药材溶液。按黄栀祛伤水处方工艺制备缺黄连的阴性样品,取5 mL,同法制成缺黄连药材的阴性对照品溶液。照2020 年版《中国药典(四部)》通则0502 TLC 法试验,吸取上述3 种溶液各2 μL,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-异丙醇-甲醇-水-三乙胺(30∶35∶10∶15∶5∶10,V/V/V/V/V/V)为展开剂,置浓氨试液预饱和20 min 的展开缸内,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照药材溶液色谱相应位置显相同颜色的荧光斑点,且阴性对照无干扰。详见图1 A。
黄柏[9]:取样品30 mL,加1%醋酸甲醇溶液200 mL,于60 ℃温度条件下超声提取(功率为400 W,频率为40 kHz)40 min,滤过,滤液浓缩至5 mL,作为供试品溶液。另取黄柏对照药材0.5 g,加1%醋酸甲醇溶液50 mL,同法制成对照药材溶液。按黄栀祛伤水处方工艺制备缺黄柏药材的阴性样品,同法制备阴性对照品溶液。照2020 年版《中国药典(四部)》通则0502 TLC 法试验,吸取上述3 种溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷 - 甲醇 - 水(30∶15∶4,V/V/V)的下层溶液为展开剂,置氨蒸气饱和的展开缸内,展开,取出,晾干,日光下检视。供试品溶液色谱中,在与对照药材溶液色谱相应位置显相同颜色的斑点,且阴性对照无干扰。详见图1 B。

图1 薄层色谱图1.Reference medicinal material solution 2-4.Test solution 5.Negative reference solutionA.Coptidis Rhizoma(365 nm) B.Phellodendri Chinensis Cortex(sunlight) C.Rhei Radix et Rhizoma(365 nm)Fig.1 TLC chromatograms
大黄[10]:取样品20 mL,加甲醇100 mL,超声提取(功率为400 W,频率为40 kHz)40 min,滤过,取滤液10 mL,蒸干,残渣加水10 mL 使溶解,再加盐酸1 mL,加热回流30 min,立即冷却,用乙醚分2 次振摇提取,每次20 mL,合并乙醚液,蒸干,残渣加三氯甲烷1 mL使溶解,作为供试品溶液。另取大黄对照药材1.0 g,同法制成对照药材溶液。按黄栀祛伤水处方工艺制备缺大黄药材的阴性样品,同法制备阴性对照品溶液。照2020 年版《中国药典(四部)》通则0502 TLC 法试验,吸取上述3 种溶液各5 μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶H 薄层板上,以石油醚(30~60 ℃)- 甲酸乙酯 - 甲酸(15∶5∶1,V/V/V)的上层溶液为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照药材溶液色谱相应位置显相同的橙黄色荧光斑点,且阴性对照无干扰。详见图1 C。
2.2 含量测定
2.2.1 色谱条件与系统适用性试验
色谱柱:Waters Xterra C18柱(250 mm × 4.6 mm,5 μm);流动相:乙腈(A)-0.25%磷酸溶液(B),梯度洗脱[11-14](程序见表1);流速:1.0 mL/ min;检测波长:238 nm(栀子苷)和274 nm(盐酸小檗碱和丹皮酚);柱温:30 ℃;进样量:10 μL。在此色谱条件下的色谱图见图2。理论板数以栀子苷峰计大于5 000,各待测成分与前后峰分离度均大于1.5。

图2 高效液相色谱图1.Geniposide 2.Berberine hydrochloride 3.PaeonolA.Mixed reference solution B.Test solution C-E.Negative control solution(lacking of Coptidis Rhizoma,Gardeniae Fructus and Moutan Cortex,respectively)Fig.2 HPLC chromatograms
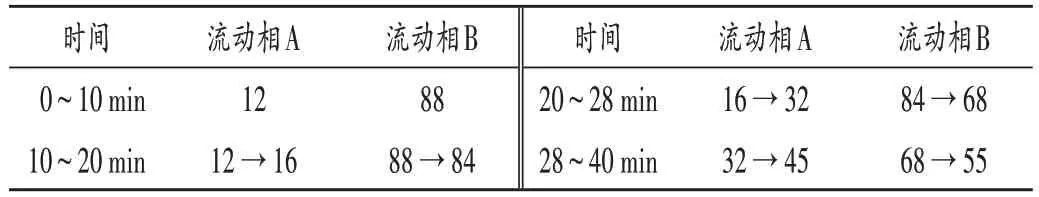
表1 流动相梯度洗脱程序(%)Tab.1 Gradient elution program of the mobile phase(%)
2.2.2 溶液制备
取盐酸小檗碱对照品24.29 mg、栀子苷对照品12.65 mg 及丹皮酚对照品20.07 mg,精密称定,置同一50 mL 棕色容量瓶中,加甲醇超声溶解并定容,即得混合对照品溶液(室温避光保存,备用)。取装量差异项下样品,混匀,精密量取20 mL,置100 mL 棕色容量瓶中,加甲醇适量,超声处理(功率为400 W,频率为50 kHz)40 min,放冷,再加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得供试品溶液。按处方工艺,分别制备缺黄连、栀子、丹皮的阴性样品,并按供试品溶液制备方法分别制备阴性对照品溶液。
2.2.3 方法学考察
线性关系考察、检测限与定量限确定:分别精密吸取 2.2.2 项下混合对照品溶液 4.0,6.0,8.0,10.0,12.0,15.0 mL,置同一20 mL 棕色容量瓶中,加甲醇稀释至刻度,摇匀,得盐酸小檗碱、栀子苷及丹皮酚质量浓度分别为0.485 8,0.253 0,0.401 4 mg/mL的系列对照品溶液。精密吸取上述系列对照品溶液,按2.2.1项下色谱条件进样测定,记录色谱图。以质量浓度(X,μg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归。将对照品溶液逐级稀释,以信噪比(S/N)为3.0时的质量浓度为各成分的检测限,以S/N为10.0 时的质量浓度为各成分的定量限。结果见表2。

表2 线性关系考察、检测限与定量限确定结果(n=6)Tab.2 Results of linear relationship test,LOD and LOQ(n=6)
精密度试验:精密吸取2.2.2项下混合对照品溶液10 μL,按2.2.1 项下色谱条件连续进样测定6 次,记录峰面积。结果盐酸小檗碱、栀子苷及丹皮酚峰面积的RSD分别为0.55%,0.62%,0.71%(n=6),表明仪器精密度良好。
稳定性试验:取同一批(批号为20210106)样品,按2.2.2项下方法制备供试品溶液,分别于常温下放置0,3,6,9,15,20,24 h 时按2.2.1 项下色谱条件进样测定,记录峰面积。结果盐酸小檗碱、栀子苷及丹皮酚峰面积的RSD分别为1.25%,0.94%,1.03%(n=7),表明供试品溶液在常温下24 h内稳定性良好。
重复性试验:取同一批(批号为20210106)样品6份,按2.2.2 项下方法制备供试品溶液,按2.2.1 项下色谱条件进样测定,记录峰面积,并计算质量浓度。结果盐酸小檗碱、栀子苷及丹皮酚的平均质量浓度分别为1.187 0,0.674 1,0.820 7 mg/ mL,RSD分别 1.24%,0.96%,0.89%(n=6),表明方法重复性良好。
加样回收试验:取已知含量的样品(批号为20210106)9 份,分为 3 组,各 3 份,每份精密量取 10 mL,每组按供试品中盐酸小檗碱、栀子苷及丹皮酚含量的80%,100%,120%精密加入相应对照品,按2.2.2 项下方法制备供试品溶液,再按2.2.1 项下色谱条件进样测定,记录色谱图,并计算加样回收率。结果见表3。

表3 加样回收试验结果(n=9)Tab.3 Results of recovery test(n=9)
2.2.4 样品含量测定
取3 批样品,按2.2.2 项下方法制备供试品溶液,再按2.2.1项下色谱条件进样测定,采用外标法计算样品中盐酸小檗碱、栀子苷及丹皮酚的含量。结果见表4。

表4 3批样品含量测定结果(mg/mL,n=3)Tab.4 Results of content determination of ingredients in the three bacthes of samples(mg/mL,n=3)
3 讨论
3.1 TLC 条件选择
对黄连、黄柏、大黄进行定性鉴别时,分别考察了不同品牌(青岛海洋、上海邦凯)的薄层板、不同温度(室温、2~10 ℃)、相对湿度(40%,50%~60%,75%)条件下展开的效果,以及不同检视方式(日光、紫外光灯)的显色效果,最终确定为2.1项下TLC条件。
3.2 色谱条件选择
为保证各成分在各自最佳吸收波长处被检测到,并达到同时检测3种有效成分的目的,采用二极管阵列检测器于190~400 nm 波长范围内测定混合对照品溶液和供试品溶液,最终确定采用分段变换波长检测,在238 nm 波长处检测栀子苷,在274 nm 波长处检测盐酸小檗碱及丹皮酚。分别考察了不同洗脱体系(乙腈-水、乙腈- 磷酸溶液、甲醇- 水、甲醇- 磷酸溶液),以及不同梯度、不同比例的洗脱条件,不同柱温(25,30,35 ℃),不同品牌色谱柱(Waters Xterra C18柱、Agilent Zorbax C18柱、Ultimate XB-C18柱),不同浓度提取溶剂(甲醇、50%甲醇、80%甲醇),不同提取时间(35,40,45 min)的提取效果,最终确定为2.2.1项下色谱条件。
3.3 指标性成分选择
参照2020 年版《中国药典(一部)》[15]中单味中药的质量标准,黄连和黄柏、栀子、牡丹皮的指标性成分分别为盐酸小檗碱、栀子苷、丹皮酚,故确定采用高效液相色谱法同时测定3种化学成分,以控制黄栀祛伤水的质量。由表4 可知,3 批样中盐酸小檗碱、栀子苷及丹皮酚的平均含量分别为1.180 7,0.675 6,0.823 2 mg/mL,将其平均值的70%作为含量测定下限值,初步拟订黄栀祛伤水中盐酸小檗碱、栀子苷及丹皮酚的含量限度分别为0.83,0.47,0.58 mg/mL。
3.4 方法评价
本研究中建立的方法操作简便,结果准确,灵敏度高,重复性好,拟订的质量标准为控制黄栀祛伤水的质量提供了参考。
