高效液相色谱法测定杞菊地黄制剂中毛蕊花糖苷含量
2022-04-20南荣华康小风
南荣华 ,吴 芳 ,康小风 ,黄 艳 ,李 翠 ,2,戴 涌 ,2△
(1. 陕西省食品药品检验研究院,陕西 西安 710065; 2. 国家药品监督管理局药品微生物检验技术重点实验室,陕西 西安 710065)
杞菊地黄制剂主要由枸杞子、菊花、熟地黄、山茱萸(制)、牡丹皮、山药、茯苓、泽泻等中药材经提取加工制成,用于治疗肝肾阴亏、头晕耳鸣、明畏光、迎风流泪、视物昏花[1]。熟地黄采取酒炖蒸煮的炮制方法,药性微温,味道甘甜,有益精填髓、补血滋阴功效。熟地黄富含氨基酸、地黄素、糖类、梓醇等多种微量元素[2],具有抗衰老、抗氧化、促进造血、增强免疫力的药理学作用[3-5]。毛蕊花糖苷为常用于熟地黄质量评价的指标性成分,但2020 年版《中国药典(一部)》仅对杞菊地黄制剂中芍药苷、马钱苷进行含量测定[6-7]。本研究中建立了测定杞菊地黄制剂(片剂和口服液)中毛蕊花糖苷含量的高效液相色谱法,为系统评价其质量提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Agilent 1260 Infinity Ⅱ型高效液相色谱仪(美国Agilent公司),配有G7115A型紫外检测器、Waters Empower工作站;P211D 型分析天平(精度为0.01/ 0.1 mg),BS224S 型分析天平(精度为0.000 1 mg),均购自德国赛多利斯公司;HH - S8A 型恒温水浴锅(北京科伟公司);UPH - 11 - 10T 型超纯水机(优普科技股份有限公司)。
1.2 试药
毛蕊花糖苷对照品(中国食品药品检定研究院,批号为111530 - 201411,含量为94.4%);杞菊地黄制剂(2018 年国家评价性抽验样品);乙腈(色谱纯,德国默克公司);其余试剂均为分析纯(国药集团化学试剂有限公司);水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:Shiseido Spolar C18柱(250 mm × 4.6 mm,5 μm);流动相:乙腈 - 0.1%甲酸溶液(15∶85,V/V);流速:1.0 mL/min;柱温:30 ℃;检测波长:330 nm;进样量:10 μL。理论板数以毛蕊花糖苷峰计应不低于4 000。
2.2 溶液制备
取毛蕊花糖苷对照品7.18 mg,精密称定,加甲醇定容至100 mL 容量瓶中,摇匀,精密量取2 mL,定容至10 mL 容量瓶中,即得每1 mL 含毛蕊花糖苷14.36 μg的对照品溶液。精密量取杞菊地黄口服液5 mL,置10 mL容量瓶中,加甲醇定容,摇匀,滤过,取续滤液,即得口服液供试品溶液。取杞菊地黄片,除去包衣,研磨均匀,取3.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇100 mL,称定质量,于80 ℃水浴加热30 min[6],放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,精密量取续滤液50 mL,蒸干,用甲醇转移至10 mL容量瓶中并定容,摇匀,滤过,取续滤液,即得片剂供试品溶液。按处方工艺制备不含熟地黄的阴性样品,按供试品溶液制备方法制备阴性对照品溶液。
2.3 方法学考察
专属性试验:吸取 2.2 项下 5 种溶液各 10 μL,按2.1 项下色谱条件进样测定。供试品溶液色谱中,在与对照品溶液色谱相同保留时间处有相应色谱峰出现,且阴性对照无干扰,表明方法专属性良好。色谱图见图1。
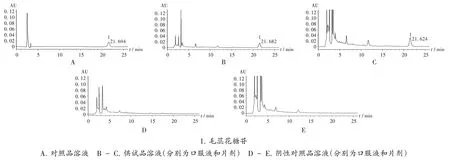
图1 高效液相色谱图1.VerbascosideA.Reference solution B-C.Test solution(oral liquid and tablets,respectively) D- E.Negative reference solution(oral liquid and tablets,respectively)Fig.1 HPLC chromatograms
线性关系考察:考察口服液时,精密吸取质量浓度为14.36 μg/ mL 的对照品溶液1,2,4,6,8,10,15 μL;考察片剂时,精密吸取质量浓度为71.8 μg/mL 的对照品溶液1,2,4,6,8,10,15,20 μL,分别按2.1 项下色谱条件进样测定,以进样量(X,μg)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程Y口= 1.22 ×106X口+ 1 730(r= 0.999 0,n= 7)和Y片= 1.21 ×106X片+60 200(r=0.995 0,n=8)。结果表明,口服液和片剂中毛蕊花糖苷的进样量分别在0.013 6~0.203 4 μg和0.067 8~1.355 7 μg范围内与峰面积线性关系良好。
精密度试验:精密吸取毛蕊花糖苷对照品溶液(质量浓度为14.36 μg/mL)10 μL,按2.1项下色谱条件重复进样测定6 次,记录峰面积。结果的RSD为1.21%(n=6),表明仪器精密度良好。
稳定性试验:精密吸取2.2 项下供试品溶液(口服液、片剂)各 20 μL,分别于0,4,8,12,16,20,24 h 时按2.1 项下色谱条件进样测定,记录峰面积。结果口服液和片剂的RSD分别为1.12%和1.27%(n= 7),表明供试品溶液在24 h内稳定性良好。
重复性试验:精密量取同一批口服液,取同一批片剂,精密称定,分别依法平行制备供试品溶液6 份,按2.1 项下色谱条件进样测定,计算含量。结果口服液和片剂中毛蕊花糖苷的平均含量分别为10.90 μg/mL 和113.74 μg/ g,RSD分别为0.99%和1.94%(n= 6),表明方法重复性良好。
加样回收试验:考察口服液时,精密量取已知含量的供试品溶液(含毛蕊花糖苷10.90 μg/ mL)6 份,各3 mL,置10 mL容量瓶中;考察片剂时,取已知含量的供试品溶液(含毛蕊花糖苷113.74 μg/ g)6 份,各1.5 g,精密称定,分别精密加入质量浓度为35.9 μg/mL 的毛蕊花糖苷对照品溶液1 mL 和5 mL,依法制备供试品溶液,按2.1项下色谱条件进样测定,记录色谱图,并计算回收率。结果见表1。

表1 毛蕊花糖苷加样回收试验结果(n=6)Tab.1 Results of recovery test of verbascoside(n=6)
耐用性试验:分别采用不同品牌及型号的高效液相色谱仪(岛津2030C-3D型、Agilent 1260 Infinity Ⅱ型),以及不同品牌的色谱柱[Agilent 5TC - C18柱、Shiseido Spolar C18柱(250 mm × 4.6 mm,5 μm)],按2.1 项下色谱条件进样测定。结果样品中的待测定峰均分离完全,表明方法耐用性良好。
2.4 样品含量测定
共抽取4 个省份、8 家不同生产企业的样品(65 批口服液、5批片剂),按2.1项下色谱条件进样测定,计算毛蕊花糖苷的含量。结果5批片剂中毛蕊花糖苷的含量为0.11~0.27 mg/ g,平均为0.22 mg/ g;口服液中含量测定结果见表2。可见,不同生产企业的样品中毛蕊花糖苷含量有不同程度的差异,部分生产企业含量高,但集散程度较大,产品批间差异大,说明该生产企业在原料药和生产工艺的控制方面的水平不稳定。
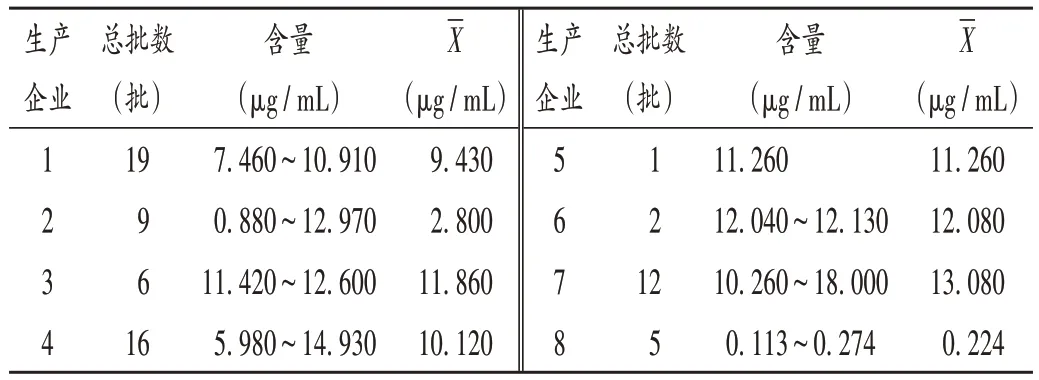
表2 8家生产企业的杞菊地黄口服液中毛蕊花糖苷含量测定结果Tab.2 Results of content determination of verbascoside in Qiju Dihuang Oral Liquid of eight manufacturing enterprises
3 讨论
3.1 提取条件选择
在供试品溶液的制备中分别以乙醇、50%甲醇、甲醇为溶剂,结果以甲醇为溶剂时测定的含量最高;考察了片剂加热回流提取及超声提取2种提取方法,结果采用加热回流提取时测定的含量最高。
3.2 色谱条件选择[8-15]
以甲醇(乙腈)-水、甲醇(乙腈)-0.1%甲酸按一定比例混合作为流动相,结果以乙腈-0.1%甲酸溶液(15∶85,V/V)为流动相时杂质峰较少,基线平稳,分离度较好;在其余条件不改变的前提下,改变柱温(25,30,35,40 ℃),结果柱温为30 ℃时目标峰与相邻峰间分离度最佳。故最终确定2.1 项下色谱条件,供试品溶液的峰形较好,分离度符合要求。
3.3 指标性成分选择
熟地黄为玄参科植物地黄的炮制加工品,味甘,微温,归肝、肾经,具有填精补肾、滋养阴血功效,通过配伍可实现真精与气、血、阴、阳的互化,视为五脏六腑之药,熟地黄及其活性成分在血液、内分泌、心血管、免疫、神经系统均有广泛的药理学作用[16-17],在杞菊地黄制剂中为处方量最大的一味药。取生地黄药材,照《中国药典》方法自行炮制熟地黄,分析炮制过程中不同阶段地黄的含量,结果毛蕊花糖苷的含量在炮制过程中并未发生明显变化,故其可作为评价熟地黄饮片及含熟地黄成分的制剂质量优劣的指标性成分之一。
3.4 方法评价
本方法操作简单,结果准确,重复性好,可用于测定杞菊地黄制剂中毛蕊花糖苷的含量。
