婴幼儿配方乳粉中泛酸检测国家标准微生物法与试剂盒法比对探究
2022-04-19孙丛丛李玉平张天博
◎ 孙丛丛,李 鹏,李玉平,张天博
(河北三元食品有限公司,河北 石家庄 050700)
泛酸又称维生素B5,是一种水溶性维生素,化学式为C9H17NO5,因以辅酶A(CoA)和酰基载体蛋白(ACP)这种结合态形式广泛存在于动植物中而得“泛酸”之名[1]。泛酸纯品为淡黄色油状物,具有酸性,易溶于水及乙醇,不溶于脂溶剂;在酸性溶液中易分解,在中性溶液中较为稳定[2-4]。
经文献报道,泛酸的检测方法有间接竞争酶联免疫法、液相色谱-质谱联用法、超高效液相色谱-同位素稀释质谱法、毛细管等速电泳法以及气相色谱-质谱联用法等[5-9]。目前,《食品安全国家标准 食品中泛酸的测定》(GB 5009.210—2016)中规定,食品中泛酸的检测方法有微生物法和高效液相色谱法,各企业使用微生物法检测泛酸还可分为国家标准微生物法和试剂盒法。
高效液相色谱法利用泛酸的化学性质,即泛酸易溶于水,在弱酸性至中性条件下(pH为5.0~7.0)稳定,样品经超声提取后,经C18反相色谱柱分离,在紫外检测器200 nm波长处测定,通过对色谱峰的保留时间和紫外光谱图定性,利用外标法定量,可计算样品中泛酸的含量。但该方法不适于含水解蛋白乳粉样品检测,而且需要的仪器成本和维护成本投入较大[10]。传统微生物法是利用植物乳杆菌生长需要泛酸,泛酸含量与植物乳杆菌生长吸光度成线性关系,通过对植物乳杆菌吸光度的测定,可计算出待测样品中泛酸的含量。此检测方法需要提前活化菌株,洗菌制备接种菌悬液,样品前处理提取过程至少4 h,接种前需要对标准系列管和试样管进行高压灭菌,检测过程比较复杂,对人员和环境设施要求高,检测周期长。试剂盒法与传统微生物法原理相同,但其采用了一种新型的微孔板反应体系,使用方便,不需要活化菌株,标准溶液配制简单,可实现快速检测,而且灵敏度高,特异性好,重复性好,可在各企业内广泛使用。
《婴幼儿配方乳粉生产许可审查细则(2013版)》中明确规定,企业可以使用快速检验设备,但应保持检测结果准确。企业使用的快速检测方法及设备应定期与食品安全国家标准规定的检验方法进行比对或验证。因此,本文采用国家标准微生物法与试剂盒法检测婴幼儿配方乳粉中的泛酸含量,并对两种方法进行比对,以期为相关研究提供参考。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
5种婴幼儿配方乳粉,均购自河北三元食品有限公司;质控样品QC-IP-705(2021),购于中国检验检疫科学研究院;试剂盒,购于北京陆桥技术股份有限公司。
1.1.2 标准菌株
植物乳杆菌(ATCC 8014),美国Microbiologics公司。
1.1.3 培养基及试剂
(1)培养基。乳杆菌肉汤培养基、菌株储存用琼脂培养基、泛酸测定培养基,购于北京陆桥技术股份有限公司。
(2)试剂。冰乙酸(天津市河东区红岩试剂厂)、三水合乙酸钠(天津市永大化学试剂有限公司)、乙醇(天津市光复科技发展有限公司)。
(3)标准品。D-酸钙(C18H32CaN2O10),纯度99.8%,美国Sigma公司。
1.2 仪器与设备
ME204分析天平(梅特勒托利多有限公司);KQ5200DE超声振荡器(昆山市超声仪器公司);SW-CJ-2FD超净工作台(上海新苗医疗器械公司);DNP-9272BS-Ⅲ电热恒温培养箱(上海新苗医疗器械公司);YXQ-LS-100A压力蒸汽灭菌器(上海博讯实业有限公司);Vortex Genie2涡旋混匀器(美国Vortex);TD5M-WS离心机(上海卢湘仪仪器有限公司);T9S紫外分光光度计(北京普析通用仪器公司);Multiskan FC酶标仪、移液器(美国热电)。
1.3 方法
1.3.1 样品前处理
国家标准微生物法参照《食品安全国家标准 食品中泛酸的测定》(GB 5009.210—2016),称取样品后加入80 mL 20%乙醇溶液,具塞,超声振摇提取4 h以上至试样完全溶解,用水定容至100 mL,适当稀释。试剂盒法是加入20 mL样品提取稀释液后,95 ℃水浴加热30 min,迅速冷却,无菌滤膜过滤,再进行适当稀释。
1.3.2 标准溶液配制
根据《食品安全国家标准 食品中泛酸的测定》(GB 5009.210—2016)和试剂盒说明书分别制备标准溶液。具体见表1、表2。为保证标准曲线的线性关系,应制备2~3套标准系列管,绘制标准曲线时,以每个标准点的均值计算。
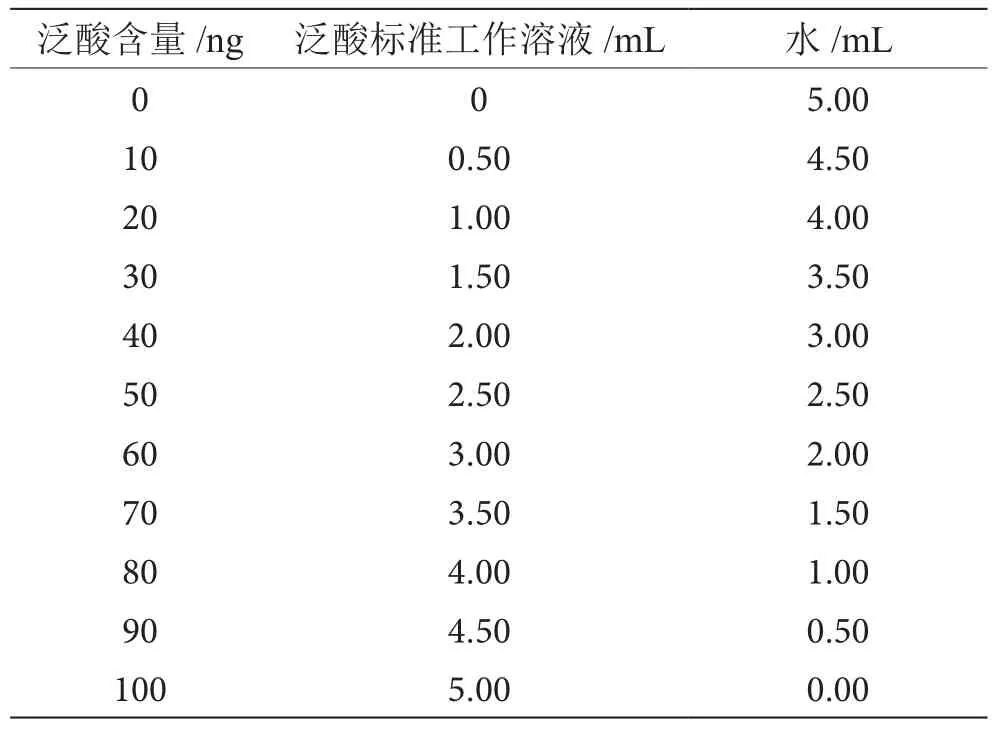
表1 国家标准微生物法标准溶液制备表
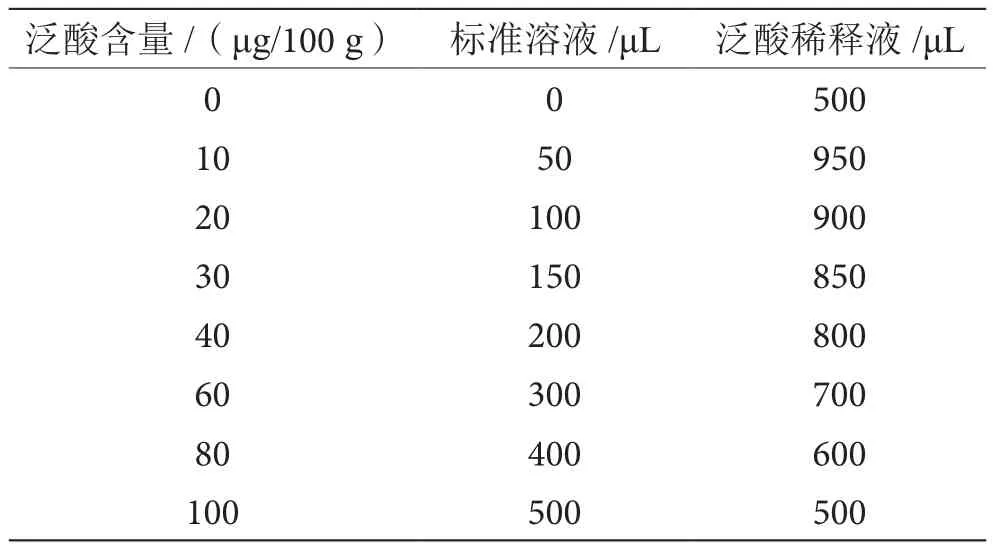
表2 试剂盒法标准溶液制备表
1.3.3 菌悬液制备
国家标准微生物法需要活化菌株,挑取单菌落至种子培养液,(37±1)℃培养20~24 h后,3 000 r·min-1,离心10 min,弃去上清液,用0.9%无菌生理盐水重复洗菌2次(3 000 r·min-1,离心10 min)后,弃去上清液,复溶,制成接种液。试剂盒法直接使用套装菌球即可。
1.3.4 标准系列管及样品管制备
国家标准微生物法标准系列管按照表1制备,最后每管加入5 mL泛酸测定用培养基。样品系列管制备见表3。

表3 样品系列管制备表
各系列管制备完成后,需要于121 ℃灭菌15 min,之后迅速冷却至室温。无菌条件下,每管加入50 μL接种液,另准备一支标准0管(含0 ng泛酸)不接种,作为0对照管。
1.3.5 接种与培养
试剂盒法采用点板操作,套装内干粉培养基与10 mL无菌水混合后,于95 ℃水浴加热10 min,迅速冷却,经无菌滤膜过滤,加入标准菌球,混匀。微孔板内先点培养基,每孔100 μL,再点标准品溶液/样品稀释液,每孔100 μL。
国家标准微生物法培养条件为(37±1)℃恒温培养箱中培养16~20 h。试剂盒法为(36±1)℃,避光培养44~48 h。
1.3.6 吸光度测定
国家标准微生物法使用紫外分光光度计,于550 nm处,以未接种的0对照管调节吸光度值为0,依次测定标准系列管、试样系列管的吸光度值。试剂盒法使用酶标仪,于550 nm处,测定标准溶液和各样品溶液吸光度值。
1.3.7 泛酸含量计算
国家标准微生物法试样稀释液中泛酸浓度按式(1)计算:

式中:ρ为试样稀释液中泛酸浓度,ng·mL-1;ρx为从标准曲线上查得测定系列管中泛酸含量,ng;Vx为制备试样系列管时吸取的试样稀释液体积,mL。
国家标准微生物法待测液中泛酸含量按式(2)计算:

式中:X为试样中泛酸含量,固态试样,mg/100 g;为试样稀释液泛酸浓度平均值,ng·mL-1;V1为试样提取液的定容体积,mL;F为试样提取液稀释倍数;m为试样质量,g;为换算系数。
试剂盒法待测液中泛酸含量按式(3)计算:

式中:X为样品中泛酸浓度, μg/100 g( μg/100 mL);C为标准曲线上读取的浓度,μg/100 g;F为稀释倍数(不考虑热提取时稀释的20倍);m为样品质量,g。
2 结果与分析
2.1 标准曲线制作
以标准系列管泛酸含量为横坐标,每个标准点吸光度值均值为纵坐标,使用ELISA专业统计分析软件中4-Parameyer绘制标准曲线。国家标准微生物法和试剂盒法标准曲线如图1、图2所示。国家标准微生物法标准曲线相关系数为0.992 8,试剂盒法标准曲线相关系数为0.994 3,两种方法线性关系均良好。
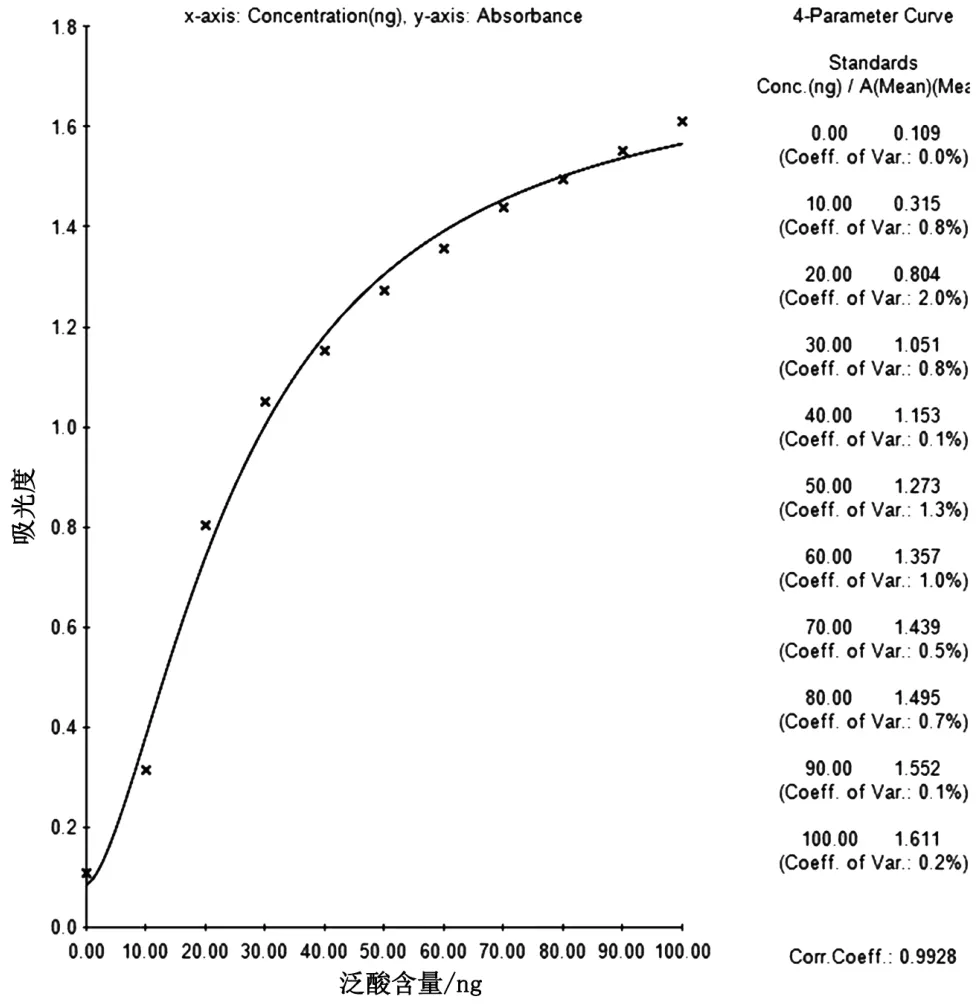
图1 国家标准微生物法泛酸测定标准曲线图

图2 试剂盒法泛酸测定标准曲线图
2.2 重复性实验结果
国家标准微生物法和试剂盒法分别对6个样品测定,每个样品重复测定6次,检测结果见表4、表5。国家标准微生物法重复性测定RSD值为1.16%~2.43%,试剂盒法重复性测定RSD值为1.14%~2.29%,两种方法重复性均良好,且质控样品检测数据与理论真值(3.955 mg/100 g)接近,准确度较高。
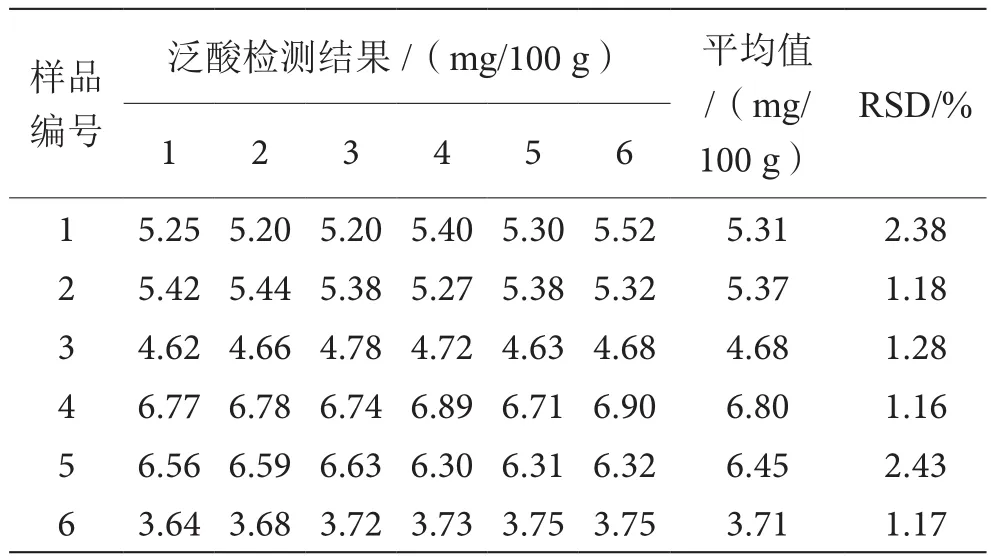
表4 国家标准微生物法重复性测定结果表
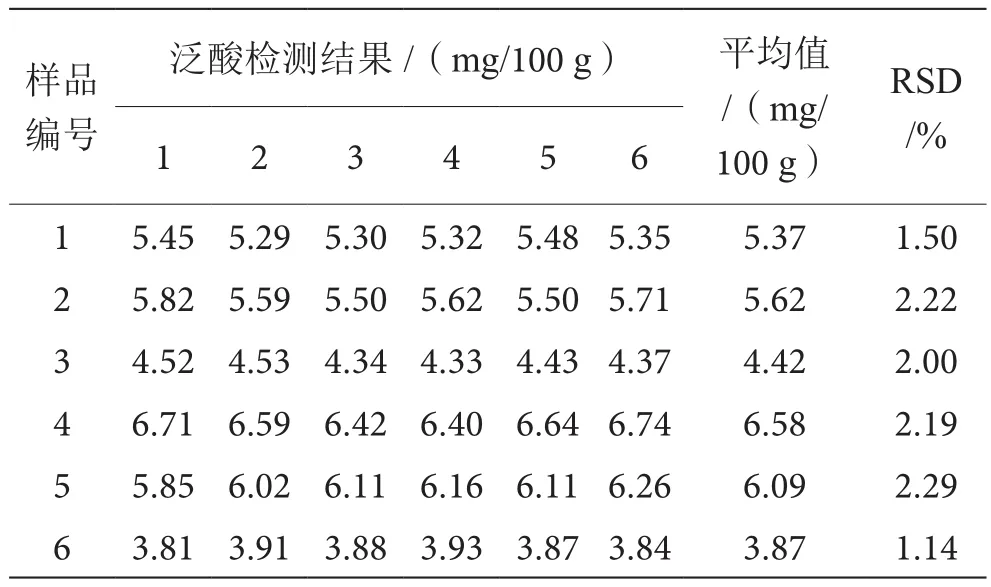
表5 试剂盒法重复性测定结果表
2.3 方法差异比较
采用配对样品t检验,对两种检测方法的结果进行分析,t值为0.602,sig值为0.573(p>0.05),表明国家标准微生物法和试剂盒法检测泛酸含量无显著差异,因此试剂盒法可以应用于婴幼儿食品中泛酸的测定。
3 讨论
与国家标准微生物法相比,试剂盒法主要有以下优势。①菌株活化方面,不需要提前活化菌株,缩短了检测周期。②耗材使用方面,不需要大量试管、三角瓶、容量瓶等玻璃器皿,可省去清洗、沸水浴煮、高温干燥灭菌等处理工序。③标准溶液配制直接配制工作液即可,线性范围更宽,适于高含量泛酸样品检测。④样品前处理时间短,方便快捷。⑤样品吸光度值测定采用96孔板,使用酶标仪测定,一次性读取数据,快速、高效。因此,试剂盒法更适于企业实验室大量实验样本的检测。
4 展望
实验室可通过探究冻干菌球复溶菌悬液浓度,配制不同浓度泛酸标准溶液,使用96微孔板,对泛酸进行测定,这样可省去试剂盒检测费用,为企业节约检测成本。另外,通过调试菌悬液浓度与样品稀释液稀释度,通过优化其最佳配比,有可能缩短微孔板培养时间,进而缩短检测周期。
