恩替卡韦联用3种中药治疗慢性乙肝纤维化效益风险评价
2022-04-19袁楚桥邓君竹黄倩倩邹文俊
袁楚桥,邓君竹,黄倩倩,王 涛,李 薇,蒋 淼,邹文俊
恩替卡韦联用3种中药治疗慢性乙肝纤维化效益风险评价
袁楚桥,邓君竹,黄倩倩,王 涛,李 薇,蒋 淼*,邹文俊*
成都中医药大学药学院,四川 成都 611137
评估恩替卡韦联用扶正化瘀胶囊(Fuzheng Huayu Capsules,FHC)、复方鳖甲软肝片(Fufang Biejia Ruangan Tablets,BRT)及安络化纤丸(Anluo Huaxian Pills,AHP)治疗慢性乙型肝炎(chronic hepatitis B,CHB)肝纤维化的效益与风险,指导临床合理用药。应用多准则决策分析模型,确定效益风险指标,建立价值树。检索筛选随机对照试验(andomized controlled trials,RCTs)与半随机对照试验(quasi-randomized controlled trials,qRCTs)。通过Meta分析生成合并值,并根据摆动权重法为各指标进行赋权,采用Hiview 3软件计算恩替卡韦联用中药的效益值、风险值和效益风险总值,利用蒙特卡洛模拟优化研究结果。应用敏感性分析检验结果稳定性。恩替卡韦联用FHC、BRT、AHP的效益值分别为32、27、31,风险值分别为70、56、63,效益风险总值分别为51、41、47,恩替卡韦联用FHC作为最优用药方案与BRT、AHP联用方案的差异分别为10 [95% CI (3,154)],4 [95% CI (−121,137)],差异大于0的概率为98.37%和54.35%。恩替卡韦联用3种中药治疗CHB肝纤维化的疗效显著,安全性较好;其中,联用FHC临床应用优先级最高。因此,恩替卡韦联用FHC方案值得进一步推广。
中成药;扶正化瘀胶囊;复方鳖甲软肝片;安络化纤丸;慢性乙型肝炎;肝纤维化;多准则决策分析;效益风险评价
慢性乙型肝炎(chronic hepatitis B,CHB)是由乙型肝炎病毒(hepatitis B virus,HBV)引起的传染性疾病。HBV是全球性的卫生问题,每年约88万人死于HBV,且患病人数呈逐年上升趋势[1-2],其5年的累计生存率最低仅为14%[3]。纤维化作为CHB恶化的病理基础[3],目前临床用药以核苷(酸)类为主[4],其中,恩替卡韦因其疗效显著,已经成为我国治疗CHB肝纤维化的一线药物之一[5]。但其长期使用带来的胃肠道反应[6-8]及耐药性[9],限制了其临床使用。
中医药具有整体优势,可以多靶点、多途径抑制肝纤维化发展,且不良反应较小[10]。其中,扶正化瘀胶囊(Fuzheng Huayu Capsule,FHC)、复方鳖甲软肝片(Biejia Ruangan Tablets,BRT)以及安络化纤丸(Anluo Huaxian Pills,AHP)等肝纤维化常用治疗药物已收载于《中国药典》2020年版[11]。临床研究显示,中西药联用治疗CHB肝纤维化的效果优于单用中药或化学药[12],但尚未有研究对恩替卡韦联用上述中药的有效性与安全性进行整合评价。因此选择安全、有效的抗CHB肝纤维化药物治疗方案是目前亟待解决的问题。
效益风险评价方法为药品监管部门及医药企业权衡多药物效益风险,对其进行决策的有效手段。多准则决策分析(multi-criteria decision analysis,MCDA)是灵活性最好、运用最多的效益风险辅助决策模型,目前已经广泛应用于医药领域[13]。MCDA通过权衡各指标的重要性赋予其相应权重,以此在结果中体现指标间的差异性,并据此干预备选方案中包含的冲突准则并将方案进行排名,使决策者能够以直观,全面的方式对决策问题进行处理[14]。本研究拟采用MCDA模型,评估恩替卡韦联用3种中药治疗CHB肝纤维化的效益风险情况,以期为临床用药及利益相关者决策提供合理化建议。
1 资料与方法
1.1 效益风险评价指标的确定及价值树的建立
参照中华医学会肝病学分会和中华医学会感染病学分会联合制定的《慢性乙型肝炎防治指南》中肝纤维化诊断指标及相关文献报道[15]确定效益指标;根据《慢性乙型肝炎防治指南》报道的不良反应及CHB肝纤维化临床随机对照试验(andomized controlled trials,RCTs)中反映用药安全性的指标确定风险指标。最终,纳入MCDA模型的效益风险指标见图1。

图1 恩替卡韦联用3种中药治疗CHB肝纤维化效益风险评价指标决策树
1.2 数据收集与处理
1.2.1 数据库文献检索 计算机检索中国知网、维普、万方、Web of Science、Embase、Cochrane Library和PubMed数据库中收录的恩替卡韦联用FHC、BRT及AHP 3种中药治疗CHB肝纤维化的RCT与半随机对照试验(quasi-randomized control trial,qRCT)。检索时间截至2021年11月1日。以“中药”“安络化纤丸”“扶正化瘀胶囊”“复方鳖甲软肝片”“恩替卡韦”“慢性乙型肝炎肝纤维化”“慢性乙型肝炎”“肝纤维化”“Chinese medicine”“Anluo Huaxian Pills”“Fuzheng Huayu Capsule”“Biejia Ruangan Tablets”“Entecavir”“chronic hepatitis B liver fibrosis”“chronic hepatitis B”“liver fibrosis”为检索词。检索方式采用主题检索结合全文检索进行。
1.2.2 纳入和排除标准
(1)纳入标准:①研究类型为RCT和qRCT。②研究对象:根据《慢性乙型肝炎防治指南(2010版)》和《肝纤维化中西医结合诊疗指南》诊断为CHB肝纤维化的任意性别、年龄、病程的患者,且在治疗前6个月,所有患者均未接受核苷(酸)类药物的治疗。③干预措施:研究中仅包括恩替卡韦分别联合FHC、BRT、AHP 3种中药的联用组和单用恩替卡韦的对照组,不含安慰剂。④结局指标:效益结局指标为透明质酸(hyaluronic acid,HA)、层黏连蛋白(laminin,LN)、Ⅲ型前胶原(procollagen type III,PC-Ⅲ)、Ⅳ型胶原(collage type Ⅳ,Ⅳ-C);丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)和HBV-DNA转阴率;风险结局指标为胃肠道反应、疲劳乏力、头痛眩晕。
(2)排除标准:①重复发表的文献;②数据不完整或前后不一致的研究;③在治疗期间对照组联用其他药物的研究;④动物实验和综述文献。
1.2.3 数据处理 使用RevMan 5.3软件对效益风险指标进行Meta分析,设置数据分析的置信区间(confidence interval,CI)为95%,连续性变量的效应量为均数差(mean difference,MD),二分类变量采用相对风险差(relative risk,RR)作为效应量,并根据纳入文献的异质性选择合适的分析模型。
1.3 指标的评分及尺度的确定
为消除各指标量纲的差异,采用摆动权重法将Meta分析合并值转化为分值0~100的偏好值。通常利用线性价值函数进行转化,它可以综合各个方案在不同指标下的表现,将其转化为偏好值[16]。偏好值100对应最优值,偏好值0则对应最差值。对于效益指标,偏好值越高代表药物方案在该指标上效益越好,风险指标的偏好值越高则代表药物方案风险越低。本研究通过RevMan 5.3软件处理不同指标Meta分析合并值极值,确定最优值及最差值,见表1。
1.4 指标的赋权
由于所选指标在临床重要性上有所不同,药物在不同指标上的评分对应的临床价值会产生差异,即重要指标的分值可能更高。为了量化这一差异,本研究采用摆动权重法对各效益、风险指标赋予权重。首先,将3项方案治疗CHB肝纤维化的一级指标效益与风险视作同样重要,各赋予50%权重。其次,二级指标中HA作为肝纤维化诊断的最重要指标,赋权100%,并据此权衡比较其余效益指标,赋予相应权重。风险指标中,胃肠道反应作为最不希望出现的不良反应,赋予权重100%,其余风险指标基于上述指标权衡比较后分别进行赋权,见表1。
表1 3项药物方案治疗CHB肝纤维化的效益、风险指标的权重、最优值和最差值变化范围的设定
Table 1 Weights and change range of optimal value and worst value for benefits and risk index of three drug regimens in treatment of CHB liver fibrosis
一级指标权重/%二级指标权重/%最优值最差值 效益50AST 60 −97 −4 ALT 60 −78 −4 HA100−135 −8 LN 70 −92 −1 PC-III 80−119 −8 IV-C 80 −80−11 HBV-DNA转阴率 40 3 0 风险50胃肠道反应100 0 4 头痛眩晕 40 0 1 疲劳乏力 40 0 1
1.5 效益风险值的计算
将权重和偏好值输入Hiview 3软件中,该软件会依预设公式计算各决策方案的效益值、风险值以及效益风险总值()。
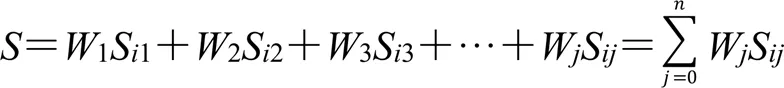
S代表决策方案在指标上的偏好分数,代表指标的权重
1.6 敏感性分析
摆动权重法中的主观因素可能对实验结果产生影响,因此需要考察其稳健性。本研究应用Hiview 3软件观察各级指标的相对权重调整后对各决策方案排序的影响,若结果发生变化时的相对权重变化幅度大于20%,则说明当前赋予权重对模型影响较小,所得结果较为稳定[17]。
1.7 蒙特卡洛模拟
效益风险评估的结果本质为Meta分析中的合并点估计值,往往存在数据的波动性。因此,本研究采用安装了Crystal Ball插件的Excel软件进行蒙特卡洛模拟,对所得结果进行不确定性分析,即以30 000次迭代模拟3种药物方案风险值、效益值和效益风险总值的差异点估计值95% CI及出现组间差异的概率。
2 结果
2.1 纳入文献基本信息
本研究共检索到中英文文献1808篇,剔除重复文献1232篇,并剔除不相关文献328篇。全文阅读剩余文献后,进一步剔除不符合纳入标准的192篇,最终纳入56项RCTs[18-73],均为中文文献,发表年限为2008—2020年,文献筛选流程如图2。其中,恩替卡韦联用FHC的研究20项[18-37],恩替卡韦联用BRT的研究28项[38-65],恩替卡韦联用AHP的研究8项[67-74]。纳入文献基本信息见表2。
在纳入的文献中,共有28项研究报告了随机化方法,8项研究没有采用完全随机分组方法,其余研究仅提到随机分组,但没有明确报告随机方法。在数据完整性方面,1项研究存在数据缺失。所有纳入研究仅有1项明确提到盲法,其余研究则无法判断在试验中是否采用了盲法。此外,在所有纳入研究中均没有选择性报告。质量评价结果见图3,56项研究的质量均处于中等水平。
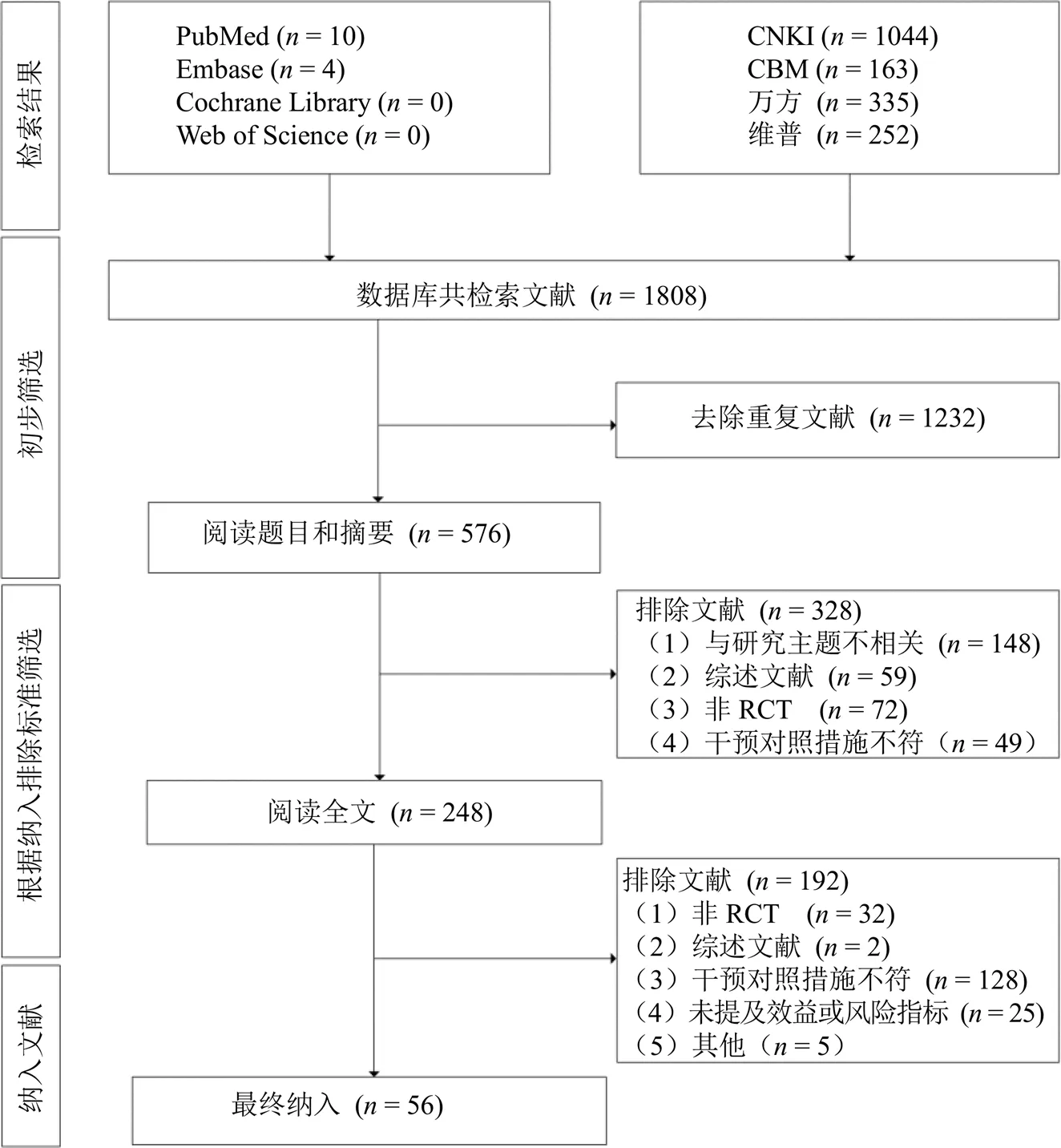
图2 文献筛选流程
表2 纳入文献基本信息
Table 2 Basic information of included literature
纳入文献n/例(男/女)年龄/岁(C/E)干预措施疗程结局指标 ECEC效益风险 夏小芳等[18]70(39/21)70(36/24)43.73±6.58/44.28±6.34扶正化瘀胶囊4.5 g·d−1恩替卡韦5 mg·d−124周①②③④⑤⑥⑧⑨⑩ 黄秀明等[19]30(17/13)30(16/14)52.37±2.68/52.24±2.90扶正化瘀胶囊4.5 g·d−1恩替卡韦0.5 mg·d−124周⑤⑥⑦⑧⑨ 夏小芳等[20]606021~69扶正化瘀胶囊4.5 g·d−1恩替卡韦0.5 mg·d−124周⑤⑥⑦N/A 王彩霞[21]25(15/10)25(17/8)52.23±2.89/52.36±2.67扶正化瘀胶囊4.5 g·d−1恩替卡韦0.5 mg·d−124周①②③④⑦⑧⑨ 陶立富[22]60(35/25)61(34/26)53.5±16.5/53.0±17.0扶正化瘀胶囊15粒·d−1恩替卡韦0.5 mg·d−124周①③④⑤N/A 黄慧琴[23]32(23/9)30(19/11)36.6±6.5/36.0±5.9扶正化瘀胶囊4.5 g·d−1恩替卡韦0.5 mg·d−16个月①②③④⑤⑥⑦⑧

续表2
①HA ②Ⅳ-C ③PC-Ⅲ ④LN ⑤ALT ⑥AST ⑦HBV-DNA转阴率 ⑧胃肠道反应 ⑨头痛眩晕 ⑩疲劳乏力 N/A-未报道
①hyaluronic acid ②collage type Ⅳ ③procollagen type III ④laminin ⑤alanine aminotransferase ⑥aspartate aminotransferase ⑦HBV-DNA conversion rate ⑧gastrointestinal reaction ⑨headache and dizziness ⑩fatigue N/A-none reported

图3 纳入研究的质量评价
2.2 纳入RCT数据合并结果
3项药物方案的效益、风险指标RCT数目、Meta分析点估计值合并结果及值见表3。Meta分析结果显示,与单用恩替卡韦相比,联用3种中药能显著下调患者的HA、PC-Ⅲ、Ⅳ-C和LN等肝纤维化指标,也能显著改善ALT、AST、HBV-DNA转阴率等一般肝功能指标。联用组的胃肠道反应、头痛眩晕、疲劳乏力等不良反应的发生率与单用组间差异没有统计学意义。
2.3 效益值比较
恩替卡韦联用FHC、BRT、AHP的效益值分别是32、27、31,其中FHC对HA、PC-Ⅲ和HBV-DNA转阴率的改善情况最具优势,AHP则是在改善LN、ALT和AST方面强于其余2项药物方案。该结果提示恩替卡韦联用FHC治疗CHB肝纤维化的效益最高,AHP次之,BRT效益值最低,见表4。蒙特卡罗模拟对3项药物方案效益值进行不确定性分析,见表5。
表3 3项药物方案的效益、风险指标合并结果
Table 3 Combined results of benefits and risk indicators of three drug regimens
一级指标二级指标FHC联合恩替卡韦治疗组BRT联合恩替卡韦治疗组AHP联合恩替卡韦治疗组RCT/项合并结果(MD/RR [95% CI])RCT/项合并结果(MD/RR [95% CI])RCT/项合并结果(MD/RR [95% CI]) 效益指标AST13−22.99 [−31.54, −14.44]P<0.000 0117−15.88 [−22.30, −9.46]P<0.000 016−27.29 [−41.32, −13.26]P<0.000 01 ALT15−24.04 [−33.19, −14.90]P<0.000 0117−14.03 [−18.90, −9.16]P<0.000 016−29.13 [−45.93, −12.33]P<0.000 01 HA19−51.47 [−59.78, −43.16]P<0.000 0125−42.11 [−52.04, −32.18]P<0.000 018−53.18 [−73.93, −32.43]P<0.000 01 LN19−29.74 [−35.89, −23.59]P<0.000 0126−31.43 [−39.43, −22.65]P<0.000 018−35.10 [−64.05, −6.15]P<0.000 01 PC-III17−45.19 [−54.96, −35.43]P<0.000 0119−33.80 [−41.39, −26.31]P<0.000 017−37.62 [−49.59, −25.66]P<0.000 01 IV-C16−36.83 [−46.21, −27.45]P<0.000 0122−38.15 [−54.41, −21.89]P<0.000 018−30.73 [−50.22, −11.23]P<0.000 01 HBV-DNA转阴率 32.67 [1.32, 5.40]P=0.006 71.55 [1.03, 2.33]P=0.0440.74 [0.41, 1.36]P=0.34 风险指标胃肠道反应 41.39 [0.56, 3.47]P=0.48 50.57 [0.29, 1.12]P=0.1032.67 [0.73, 9.76]P=0.14 头痛眩晕 30.36 [0.12, 1.11]P=0.08 11.00 [0.06, 16.59]P=1.00 疲劳乏力 10.13 [0.02, 1.08]P=0.06 20.62 [0.07, 5.14] P=0.65
2.4 风险值比较
恩替卡韦联用FHC、BRT和AHP的风险值分别是70、56、63,其中AHP对胃肠道产生的损害最大,而BRT发生头痛眩晕和疲劳乏力的可能最高,综合各指标使用FHC的风险值最高,即用药风险最低,见表6。蒙特卡罗模拟对3项药物方案效益值进行不确定性分析,见表7。
表4 3项药物方案的效益值及各效益指标的相对权重
Table 4 Benefit value of three drug regimens and relative weight of each benefit index
指标权重/%效益值相对权重/%FHCBRTAHP HA10035273510.2 PC-Ⅲ 80332327 8.2 Ⅳ-C 80383929 8.2 LN 70323537 7.1 ALT 60271434 6.1 AST 60201425 6.1 HBV-DNA转阴率 40413732 4.1 总计49032273150.0
表5 3项药物方案间效益值差异、95% CI及差异大于0的概率
Table 5 Benefit value difference, 95% CI and probability of difference greater than 0 among three drug regimens
效益值FHC vs BRT FHC vs AHPBRT vs AHP 差异值51−4 95% CI[1,10][−6,8][−12,3] 差异大于0概率/%98.9258.4211.21
2.5 效益风险总值的比较
恩替卡韦联用FHC、BRT、AHP的效益风险总值分别为51、41和47,表明FHC的效益风险整体表现最优,见图4-A。蒙特卡罗模拟对3项药物方案效益风险总值进行不确定性分析,见图4-B~D和表8。
表6 3项用药方案的风险值及各效益指标的相对权重
Table 6 Risk value of three drug regimens and relative weight of each benefit index
指标权重/%风险值相对权重/%FHCBRTAHP 胃肠道反应1006586 3327.8 头痛眩晕 4065 010011.1 疲劳乏力 40873810011.1 总计1807056 6350.0
表7 3项药物方案间风险值差异、95% CI及差异大于0的概率
Table 7 Risk value difference, 95% CI and probability of difference greater than 0 among three drug regimens
风险值FHC vs BRTFHC vs AHPBRT vs AHP 差异值147−7 95% CI[1,303][−243,272][−418,186] 差异大于0概率/%97.5854.1224.01

图4 3项药物方案的效益风险总值及差异
表8 3项药物方案间效益风险总值差异、95% CI及差异大于0的概率
Table 8 Difference in total value of benefit and risk, 95% CI and probability of difference greater than 0 among three drug regimens
效益风险总值FHC vs BRTFHC vs AHPAHP vs BRT 差异值104−6 95% CI[3,154][−121,137][−211,90] 差异大于0概率/%98.3754.3522.98
2.6 敏感性分析
效益和风险的相对权重各为50%的情况下,恩替卡韦联用FHC的效益风险总值高于联用BRT及AHP,见图5。值得注意的是,无论权重如何变化,FHC方案的风险值始终高于其余2组方案,可推断本研究主观权重设置合理,效益风险评价结果稳定性较好。
3 讨论
CHB引起的肝纤维化是一种以细胞外基质过度增生为特征的可逆性创伤修复反应,细胞外基质不断积累形成瘢痕组织,影响肝脏正常生理功能,最终导致肝硬化甚至肝癌[74-75]。抗病毒治疗是西医干预CHB的主要手段,核苷(酸)类药物通过竞争乙型肝炎病毒复制过程中延长聚合酶链所需的相应核苷,抑制病毒脱氧核糖核酸复制从而改善肝脏炎症和纤维化。另一方面,中医药在治疗CHB方面亦获得普遍认可,不仅能多靶点治疗、减少不良反应,还能一定程度上降低治疗费用,减轻患者压力。本研究基于文献调研结果选择临床研究最多,不良反应报道最全面的3种中药,对其效益与风险进行深入研究。
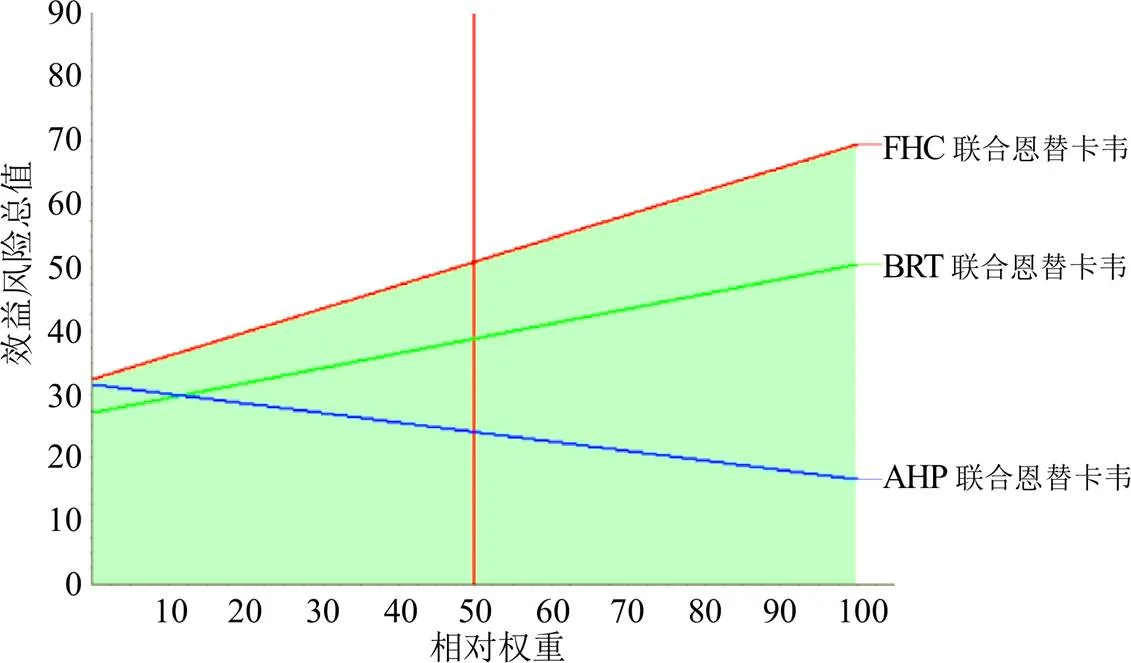
图5 3项药物方案的效益风险敏感性分析
本研究结果表明,与单用恩替卡韦相比,联用FHC、BRT及AHP 3种中成药制剂均能显著改善各效益指标,且不会带来额外的不良反应。MCDA模型评估结果显示,恩替卡韦联用FHC、BRT、AHP的效益值分别为32、27、31,风险值分别为70、56、63,效益风险总值分别为51、41、47。蒙特卡洛模拟分析结果表明,恩替卡韦联用FHC与联用BRT、AHP方案的效益风险总值差异分别为10 [95% CI(3,154)]、4 [95% CI(−121,137)],差异大于0的概率为98.37%和54.35%,说明恩替卡韦联用FHC为最优疗法。采用Hiview 3软件进行敏感性分析,表明本研究权重设置合理,模型稳定。因此,恩替卡韦联用FHC为最值得推荐的用药方案。
恩替卡韦作为新一代的鸟嘌呤核苷类似物,在体内磷酸化后,竞争磷酸脱氧鸟嘌呤核苷,抑制HBV多聚酶启动,从而起到抗病毒作用[76]。FHC主要成分为丹参、冬虫夏草、五味子、绞股蓝、桃仁及松花粉,具有活血祛瘀、益精养肝之功。丹参水提物能抑制肝纤维化过程中谷胱甘肽巯基转移酶(glutathione-transferase,GST-P)和α-平滑肌肌动蛋白(α-smooth muscle actin,α-SMA)的表达,对ALT、AST、HA、c-谷氨酰转移酶、碱性磷酸酶和总胆红素均有显著抑制作用[77]。冬虫夏草活性成分虫草多糖可抑制肝窦星状细胞活化,并减少活化细胞骨架蛋白表达可能是其治疗纤维化的主要机制[78]。五味子活性成分五味子甲素可通过调节转化生长因子- β(transforming growth factor-β,TGF-β)/Smad 3及NOD样受体热蛋白结构域蛋白3/核因子-κB(NOD-like receptor thermal protein domain associated protein 3/Nuclear factor-k-gene binding,NLRP3/NF-κB)通路降低小鼠AST及ALT水平,进而减轻肝纤维化程度[79]。同时,恩替卡韦联用FHC后,恩替卡韦服用疗程及剂量均显著降低,可能是其风险最低的原因。
本研究采用MCDA模型框架,将多个效益风险指标用层次清晰的决策树的方式表达,运用软件转化数据,克服评分主观性,异质性较小,量化恩替卡韦联用3种中药治疗CHB肝纤维化药物决策方案临床应用的效益及风险。本研究严格按照文献检索策略和严格的纳入及排除标准,但是仍然存在一定的局限性,即部分纳入研究未报道具体随机方法及盲法和分配隐藏实施情况;本研究纳入样本量较小,后续仍需纳入大样本RCT以增强证据等级。
综上所述,恩替卡韦联用FHC为CHB肝纤维化推荐治疗方案,在降低血清肝纤维化指标HA及提高HBV-DNA阴转率方面均有显著优势。在安全性方面,仅出现轻微不良反应,不影响治疗进程。但本研究亦存在不足之处,需要更多高质量RCT予以补充验证,为临床提供更多循证参考。
利益冲突 所有作者均声明不存在利益冲突
[1] Graber-Stiehl I. The silent epidemic killing more people than HIV, malaria or TB [J]., 2018, 564(7734): 24-26.
[2] 王贵强, 段钟平, 王福生, 等. 慢性乙型肝炎防治指南(2019年版) [J]. 实用肝脏病杂志, 2020, 23(1): 9-32.
[3] Lozano R, Naghavi M, Foreman K,. Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: A systematic analysis for the Global Burden of Disease Study 2010 [J]., 2012, 380(9859): 2095-2128.
[4] Su T H, Hu T H, Chen C Y,. Four-year entecavir therapy reduces hepatocellular carcinoma, cirrhotic events and mortality in chronic hepatitis B patients [J]., 2016, 36(12): 1755-1764.
[5] Tang L S Y, Covert E, Wilson E,. Chronic hepatitis B infection: A review [J]., 2018, 319(17): 1802-1813.
[6] 赖月贤, 赖晨露. 恩替卡韦联合安络化纤丸治疗慢性乙型肝炎肝纤维化的疗效观察 [J]. 中国医药指南, 2011, 9(34): 371-372.
[7] 宋玉迪. 中成药联合恩替卡韦治疗慢性乙型肝炎相关肝纤维化或肝硬化疗效的网状Meta分析[D]. 广州: 广州中医药大学, 2019.
[8] 刘志雄, 田玥, 朱方, 等. 复方鳖甲软肝片联合恩替卡韦治疗慢性乙型肝炎纤维化的长期疗效探究 [J]. 今日药学, 2019, 29(6): 427-430.
[9] 吕超, 毛德文, 石清兰, 等. 中药及其复方抗肝纤维化作用机制的研究进展 [J]. 中国实验方剂学杂志, 2020, 26(4): 242-250.
[10] Zhang H P. Clinical efficacy of integrated Chinese and western medicine in the treatment of chronic hepatitis B with liver cirrhosis ascites [J]., 2015, 2(11): 109-110.
[11] 中国药典 [S]. 一部. 2020: 1088.
[12] Diaby V, Campbell K, Goeree R. Multi-criteria decision analysis (MCDA) in health care: A bibliometric analysis [J]., 2013, 2(1/2): 20-24.
[13] Phillips L D, Al E. Benefit-risk methodology project:work package 2 report: applicability of current tools and processes for regulatory benefit-risk assessment [J]., 2011, 90(8): 101-106.
[14] Chapple C R, Mironska E, Wagg A,. Multicriteria decision analysis applied to the clinical use of pharmacotherapy for overactive bladder symptom complex [J]., 2020, 6(3): 522-530.
[15] Wang T, Jin W, Huang Q Q,. Clinical efficacy and safety of eight traditional Chinese medicine combined with entecavir in the treatment of chronic hepatitis B liver fibrosis in adults: A network meta-analysis [J]., 2020, 2020: 1-15.
[16] Dodgson J, Spackman M, Pearman A,.[M]. London: Department for Communities and Local Government, 2009.
[17] Mussen F, Salek S, Walker S. A quantitative approach to benefit-risk assessment of medicines-part 1: The development of a new model using multi-criteria decision analysis [J]., 2007, 16 (Suppl 1): S2-S15.
[18] 夏小芳, 吴建, 龚玲, 等. 扶正化瘀胶囊联合恩替卡韦对慢性乙型肝炎患者肝纤维化程度的影响 [J]. 中西医结合肝病杂志, 2019, 29(6): 500-501.
[19] 黄秀明, 利旭辉, 周伟泽, 等. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型病毒性肝炎肝纤维化的效果 [J]. 中国处方药, 2020, 18(6): 126-127.
[20] 夏小芳, 吴建, 施维群, 等. 扶正化瘀胶囊联合恩替卡韦治疗慢性乙型肝炎肝纤维化的疗效及对血液流变学和血清IL-17表达的影响 [J]. 中国临床药学杂志, 2020, 29(5): 334-338.
[21] 王彩霞. 扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化的临床效果 [J]. 医学理论与实践, 2019, 32(21): 3459-3460.
[22] 陶立富. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝脏纤维化及肝硬化的临床研究 [J]. 国际感染病学: 电子版, 2019, 8(2): 133.
[23] 黄慧琴. 扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化32例临床观察 [J]. 湖南中医杂志, 2019, 35(4): 51-52.
[24] 王琳, 校彦勇, 吴慧丽, 等. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化88例疗效观察 [J]. 黔南民族医专学报, 2018, 31(4): 245-246.
[25] 李静, 刘璐璐, 金介旺. 恩替卡韦联合扶正化瘀胶囊对慢性乙型肝炎肝纤维化的应用评价 [J]. 中国实用医药, 2018, 13(35): 11-13.
[26] 闵广艳. 观察恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化的临床疗效 [J]. 中国医药指南, 2018, 16(33): 126.
[27] 沈国辉. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化的疗效观察 [J]. 临床医药文献电子杂志, 2018, 5(41): 52-53.
[28] 张艳鹤. 扶正化瘀胶囊合恩替卡韦对慢性乙肝肝纤维化的临床疗效 [J]. 实用中西医结合临床, 2018, 18(3): 10-12.
[29] 刘雯, 张贤兵, 李福华, 等. 恩替卡韦联合扶正化瘀胶囊治疗肝郁血瘀型慢性乙型肝炎疗效观察 [J]. 安徽中医药大学学报, 2019, 38(4): 40-43.
[30] 张正华, 陆强峰, 徐海东. 恩替卡韦分散片联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化的疗效及对肝功能影响 [J]. 中国保健营养, 2019, 29(23): 29-30.
[31] 范瑞琴, 苏传真, 朱刚剑, 等. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化73例疗效观察 [J]. 胃肠病学和肝病学杂志, 2013, 22(1): 31-33.
[32] 吴龙龙. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化疗效观察 [J]. 现代中西医结合杂志, 2013, 22(35): 3952-3953.
[33] 谢宏晟, 蔡丽敏, 颜鸣鹤. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化的效果观察 [J]. 浙江医学, 2016, 38(8): 555-557.
[34] 宋宇震, 庄婷婷. 扶正化瘀胶囊联合恩替卡韦治疗慢性乙型肝炎肝纤维化的疗效分析 [J]. 福建医药杂志, 2012, 34(6): 89-90.
[35] 庞素秋, 吴双, 王国权, 等. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化50例 [J]. 中国药业, 2013, 22(8): 120-121.
[36] 上官增锋. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化疗效观察 [J]. 中国乡村医药, 2013, 20(1): 39-40.
[37] 龚亚华, 陈建杰, 薛建华, 等. 恩替卡韦联合扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化28例 [J]. 中西医结合肝病杂志, 2010, 20(2): 119-120.
[38] 王立坤, 霍丽亚, 卢瑞杰, 等. 复方鳖甲软肝片联合抗病毒治疗对慢性乙型肝纤维化患者HBV-DNA转阴率及超声参数的影响 [J]. 现代诊断与治疗, 2020, 31(1): 31-33.
[39] 李莎莎, 谭林, 姜宁. 恩替卡韦联合复方鳖甲软肝片治疗慢性乙型肝炎肝纤维化临床研究 [J]. 中西医结合肝病杂志, 2017, 27(1): 28-30.
[40] 王鹏雁, 荆进红. 探讨恩替卡韦联合复方鳖甲软肝片治疗慢性乙型肝炎肝纤维化的疗效 [J]. 国际医药卫生导报, 2019, 25(20): 3443-3447.
[41] 何伟. 复方鳖甲软肝片联合恩替卡韦抗乙肝肝纤维化临床疗效观察 [J]. 基层医学论坛, 2019, 23(29): 4271.
[42] 刘玉柱. 恩替卡韦联合复方鳖甲软肝片治疗慢性乙型病毒性肝炎肝纤维化的临床疗效探讨 [J]. 世界复合医学, 2019, 5(6): 76-78.
[43] 段谅. 恩替卡韦联合复方鳖甲软肝片治疗慢性乙型肝炎肝纤维化的效果分析 [J]. 中国社区医师, 2019, 35(16): 74-75.
[44] 刘志雄, 田玥, 朱方, 等. 复方鳖甲软肝片联合恩替卡韦治疗慢性乙型肝炎纤维化的长期疗效探究 [J]. 今日药学, 2019, 29(6): 427-430.
[45] 黄辉红. 慢性乙型肝炎肝纤维化患者联合治疗的效果及对相关标志物和免疫状态的影响 [J]. 检验医学与临床, 2019, 16(8): 1057-1059.
[46] 金艳杰. 恩替卡韦联合复方鳖甲软肝片治疗慢性乙型病毒性肝炎肝纤维化的临床疗效观察 [J]. 中国药物经济学, 2019, 14(2): 69-73.
[47] 田尚昆. 恩替卡韦联合复方鳖甲软肝片治疗慢性乙型肝炎肝纤维化的临床疗效 [J]. 大医生, 2018, 3(8): 64-65.
[48] 王亚钦, 李旭飞. 复方鳖甲软肝片联合恩替卡韦对慢性乙型肝炎肝纤维化患者肝功能及生活质量的影响 [J]. 河南医学研究, 2017, 26(21): 3903-3904.
[49] 徐志. 复方鳖甲软肝片联合恩替卡韦治疗慢性乙型肝炎肝纤维化的临床研究 [J]. 中国社区医师, 2018, 34(19): 113-114.
[50] 莫金荣, 黄思益. 复方鳖甲软肝片联合恩替卡韦治疗慢性乙型肝炎纤维化的临床效果 [J]. 中外医学研究, 2018, 16(17): 11-13.
[51] 张晓梅. 复方鳖甲软肝片结合恩替卡韦治疗慢性乙型肝炎肝纤维化的疗效及对患者肝功能的影响 [J]. 肝脏, 2018, 23(5): 424-426.
[52] 杨琴, 马臻. 复方鳖甲软肝片联合恩替卡韦治疗对慢性乙肝患者肝纤维化进程及免疫应答状态的影响 [J]. 海南医学院学报, 2018, 24(5): 593-596.
[53] 王娟. 复方鳖甲软肝片联合恩替卡韦治疗CHB肝纤维化的疗效及对相关指标的影响 [J]. 菏泽医学专科学校学报, 2018, 30(2): 56-57.
[54] 芦红. 复方鳖甲软肝片联合恩替卡韦对慢性乙型肝炎纤维化的治疗作用[J]. 中国医药指南, 2020, 18(5): 183-184..
[55] 田翠峰. 恩替卡韦联合复方鳖甲软肝片治疗慢性乙型肝炎所致肝纤维化的效果探讨 [J]. 当代医药论丛, 2020, 18(14): 147-148.
[56] 陈端进. 恩替卡韦与复方鳖甲软肝片联用治疗慢性乙型肝炎肝纤维化的效果观察 [J]. 中国卫生标准管理, 2017, 8(28): 111-113.
[57] 谌翠容, 过建春, 俞秀丽, 等. 恩替卡韦联合复方鳖甲软肝片治疗慢性乙型肝炎肝纤维化疗效观察 [J]. 浙江中医药大学学报, 2010, 34(3): 370-371.
[58] 张瑞凤, 姚云洁, 游忠岚, 等. 复方鳖甲软肝片联合恩替卡韦治疗慢性乙型肝炎肝纤维化的观察 [J]. 第三军医大学学报, 2014, 36(18): 1961-1963.
[59] 张海涛, 张晓艳, 么作义, 等. 复方鳖甲软肝片联合恩替卡韦治疗慢性乙型肝炎肝纤维化的临床观察 [J]. 中国煤炭工业医学杂志, 2015, 18(7): 1120-1122.
[60] 张晓林. 复方鳖甲软肝片联合恩替卡韦治疗慢性乙型肝炎肝纤维化临床疗效分析 [J]. 中国冶金工业医学杂志, 2016, 33(6): 680-681.
[61] 张宗刚. 恩替卡韦+复方鳖甲软肝片联合治疗慢性乙型肝炎肝纤维化的效果观察 [J]. 中国医药指南, 2012, 10(36): 456-458.
[62] 邬振国, 周高东, 陈永永, 等. 复方鳖甲软肝片联合恩替卡韦治疗慢性乙型肝炎肝纤维化的临床研究 [J]. 药物评价研究, 2017, 40(3): 351-355.
[63] 孙燕燕, 朱振霞. 恩替卡韦联合复方鳖甲软肝片治疗慢性乙型肝炎肝纤维化的临床疗效 [J]. 临床合理用药杂志, 2017, 10(33): 67-68.
[64] 肖玲, 杨玉宇, 徐莉. 恩替卡韦联合复方鳖甲软肝片治疗慢性乙型肝炎肝纤维化的临床效果观察 [J]. 中国医药科学, 2013, 3(14): 59-60.
[65] 蒋斌. 恩替卡韦联合复方鳖甲软肝片治疗肝纤维化的疗效分析 [J]. 中国卫生标准管理, 2019, 10(5): 78-80.
[66] 赖月贤, 赖晨露. 恩替卡韦联合安络化纤丸治疗慢性乙型肝炎肝纤维化的疗效观察 [J]. 中国医药指南, 2011, 9(34): 371-372.
[67] 刘瑜, 张静. 安络化纤丸联合恩替卡韦治疗慢性乙型肝炎肝纤维化 [J]. 牡丹江医学院学报, 2019, 40(4): 54-55.
[68] 林万宝, 陈海燕, 殷光辉, 等. 安络化纤丸联合恩替卡韦片治疗慢性乙型病毒性肝炎肝纤维化临床研究 [J]. 新中医, 2020, 52(1): 80-82.
[69] 邝宁子. 恩替卡韦联合安络化纤丸治疗慢性乙型肝炎肝纤维化的临床观察 [J]. 深圳中西医结合杂志, 2009, 19(1): 18-20.
[70] 郭威, 周莹, 鲁有水, 等. 恩替卡韦联合安络化纤丸治疗慢性乙型肝炎肝纤维化43例 [J]. 医药导报, 2010, 29(9): 1157-1159.
[71] 黄志杰, 曾翠萍. 恩替卡韦联合安络化纤丸治疗HBeAg阳性慢性乙型肝炎肝纤维化134例 [J]. 中西医结合肝病杂志, 2016, 26(2): 74-75.
[72] 曾映荷. 恩替卡韦联合安络化纤丸治疗乙型肝炎肝纤维化的临床研究 [J]. 湖北中医杂志, 2013, 35(6): 11-12.
[73] 戚合德, 杨阳, 龚守军. 安络化纤丸联合恩替卡韦治疗慢性乙型肝炎肝纤维化疗效观察 [J]. 中国现代医生, 2008, 46(11): 88-89.
[74] Cai Y J, Dong J J, Wang X D,. A diagnostic algorithm for assessment of liver fibrosis by liver stiffness measurement in patients with chronic hepatitis B [J]., 2017, 24(11): 1005-1015.
[75] Ning Q, Han M F, Sun Y T,. Switching from entecavir to PegIFN Alfa-2a in patients with HBeAg-positive chronic hepatitis B: A randomised open-label trial (OSST trial) [J]., 2014, 61(4): 777-784.
[76] 熊丽兰, 曹国鸣, 吴利华. 丹参联合猪苓多糖治疗慢性乙型肝炎疗效观察[J]. 中国中西医结合杂志, 1993(9): 533-535.
[77] Peng Y, Tao Y Y, Wang Q L,. Ergosterol is the active compound of cultured myceliumsinensis on antiliver fibrosis [J]., 2014, 2014: 537234.
[78] 崔兵兵, 李季, 刘可春, 等. 冬虫夏草多糖抑制肝纤维化作用机制的研究进展 [J]. 中国实验方剂学杂志, 2019, 25(15): 228-234.
[79] 王肖辉, 周霖, 杜秋争, 等. 五味子甲素对四氯化碳诱导小鼠肝纤维化的保护作用及其机制研究 [J]. 中国药房, 2020, 31(22): 2725-2730.
Benefit-risk assessment of entecavir combined with three traditional Chinese medicines in treatment of chronic hepatitis B liver fibrosis
YUAN Chu-qiao, DENG Jun-zhu, HUANG Qian-qian, WANG Tao, LI Wei, JIANG Miao, ZOU Wen-jun
College of Pharmacy, Chengdu University of Traditional Chinese Medicine, Chengdu 611137, China
To evaluate the benefits and risks of entecavir combined with Fuzheng Huayu Capsules (FHC, 扶正化瘀胶囊), Fufang Biejia Ruangan Tablets (BRT, 复方鳖甲软肝片) and Anluo Huaxian Pills (AHP, 安络化纤丸) in the treatment of chronic hepatitis B (CHB) liver fibrosis, in order to provide reference for clinical rational drug use.The multi-criteria decision analysis model was applied to determine benefit and risk indicators and establish the value tree. The randomized controlled trials (RCTs) and quasi-randomized controlled trials (qRCTs) were searched and screened. The combined value were generated through Meta-analysis, and each index was weighted according to the swing weight method. The Hiview 3 software was used to calculate the benefit value, risk value and total benefit risk value of entecavir combined with traditional Chinese medicine, and Monte Carlo simulation was used to optimize the research results. Sensitivity analysis was used to test the stability of the results.The benefits of entecavir combined with FHC, BRT, and AHP were 32, 27, 31. The risk values were 70, 56, 63, and the total benefits and risks were 51, 41, 47. The difference between entecavir combined with FHC as the optimal drug regimen and BRT, AHP combined regimens were 10 [95% CI (3, 154)], 4 [95% CI (−121, 137)], and the probability that the difference was greater than 0 was 98.37% and 54.35%.Entecavir combined with three traditional Chinese medicines has significant efficacy and safety in the treatment of CHB liver fibrosis. Among them, the combination of FHC has the highest priority for clinical application. Therefore, entecavir combined with FHC program is worthy of further promotion.
Chinese patent medicine; Fuzheng Huayu Capsules;Fufang Biejia Ruangan Tablets;Anluo Huaxian Pills; chronic hepatitis B; liver fibrosis; multi-criteria decision analysis; benefit risk evaluation
R285.64
A
0253 - 2670(2022)08 - 2449 - 11
10.7501/j.issn.0253-2670.2022.08.022
2021-12-11
成都中医药大学杏林学者学科人才科研提升计划(CXTD2018005)
袁楚桥(1998—),男,硕士研究生,从事中药理论与应用研究。Tel: 15070957727 E-mail: 532789390@qq.com
邹文俊,女,教授,博士生导师,医学博士,从事中药基础理论及应用研究。Tel/Fax: (028)61800237 E-mail: zouwenjun@163.com
蒋 淼,女,在读博士,讲师,从事中药基础理论及应用研究。Tel: (028)61800231 E-mail: jiangmiaocc@163.com
[责任编辑 潘明佳]
