北柴胡及醋北柴胡标准汤剂质量差异性分析
2022-04-19邹佳莉谭娟娟贡济宇
宋 驰,葛 威,邹佳莉,王 悦,谭娟娟,贡济宇
北柴胡及醋北柴胡标准汤剂质量差异性分析
宋 驰,葛 威,邹佳莉,王 悦,谭娟娟,贡济宇*
长春中医药大学 药学院,吉林 长春 130117
建立北柴胡及醋北柴胡标准汤剂质量评价方法,比较二者质量的差异性。制备北柴胡及醋北柴胡标准汤剂各20批,对醋制前后标准汤剂的pH值及出膏率进行考察;建立北柴胡醋制前后标准汤剂HPLC指纹图谱方法和多指标成分含量测定方法,并结合化学计量学和统计学方法对二者差异进行分析。北柴胡醋制后标准汤剂pH值降低,出膏率降低;建立了北柴胡及其醋制品标准汤剂指纹图谱,分别确定了16个共有峰,指认了其中5个共有峰;北柴胡标准汤剂相似度为0.976~0.995,醋北柴胡标准汤剂相似度为0.946~0.996。主成分分析将北柴胡及其醋制品标准汤剂归为2类,正交偏最小二乘法-判别分析找出二者共7个差异色谱峰,分别为峰1、4(柴胡皂苷c)、6、7(柴胡皂苷a)、9(柴胡皂苷b2)、10(柴胡皂苷b1)及13(柴胡皂苷d),为北柴胡及醋北柴胡标准汤剂差异化合物。多指标成分含量测定结果表明北柴胡醋制前后指标成分含量具有显著差异(<0.05),北柴胡醋制后标准汤剂中柴胡皂苷a、柴胡皂苷c及柴胡皂苷d含量较低,柴胡皂苷b1及柴胡皂苷b2含量较高。建立了科学和实用的北柴胡及醋北柴胡标准汤剂质量评价方法,也为北柴胡与其醋制品相关制剂的鉴别和质量控制提供参考。
北柴胡;醋制;标准汤剂;指纹图谱;正交偏最小二乘法-判别分析;柴胡皂苷;质量控制
中药标准汤剂是以中医理论为指导、临床应用为基础的单味中药饮片水煎剂,用于标准化不同的临床用药形式是否与传统汤剂一致,亦可作为配方颗粒、经典名方等产品的物质基准[1]。建立规范、高效的标准汤剂制备工艺,并依照可量化的标准对其进行质量评价,将为中药应用的标准化、科学化提供重要的技术支持与参考。
北柴胡为伞形科柴胡属多年生草本植物柴胡DC.的干燥根[2],又名韭叶柴胡、津柴胡,为大宗药材。具有疏散退热、疏肝解郁、升举阳气的功效,主要化学成分为皂苷类、多糖类、黄酮类、挥发油、有机酸及植物甾醇等[3-5]。
现代药理研究表明,柴胡对于散热、消炎、抗肿瘤、抗抑郁、保肝及免疫调节等具有良好的治疗效果[6-10]。北柴胡有熬制法、酒炒制、蜜制、醋炒、鳖血制、炒制法等炮制方法,其中以醋制最常用,且被《中国药典》2020年版收载。
明代李梃《医学入门》认为:醋可引药入肝,醋柴胡重在养肝柔肝,起到缓和升散、解表退热之功效,可用于治疗腹痛、月经不调等症[11],在现有研究中,柴胡入药煎煮时,原生柴胡皂苷a、柴胡皂苷d会转化为次生柴胡皂苷b1、柴胡皂苷b2,柴胡皂苷b2可抗炎、增强免疫、抑制脂肪分解、刺激PGE2合成[12]。
目前,对北柴胡的研究多集中在不同产地、不同加工方法与药材质量的相关性,以及对炮制前后北柴胡饮片的药效及质量评价研究,而北柴胡临床制剂多为汤剂、散剂及颗粒剂,已失去原饮片所具有的显微与性状鉴别特征,即无法从传统鉴别方法进行检查与鉴别,不利于临床用药质量的控制。因此,对北柴胡及醋北柴胡的标准汤剂进行全面的质量控制与评价具有重要意义。
本研究收集具有代表性的20批北柴胡饮片,制备北柴胡与醋北柴胡标准汤剂各20批,对醋制前后标准汤剂的pH值及出膏率进行考察;建立北柴胡醋制前后标准汤剂HPLC指纹图谱方法和多指标成分含量测定方法,并结合化学计量学和统计学方法对二者差异进行分析,以期建立科学和实用的北柴胡及醋北柴胡标准汤剂质量评价方法,为北柴胡与其醋制品相关制剂的鉴别和质量控制提供参考。
1 仪器与试药
1.1 仪器
LC-2030高效液相色谱仪,包括DGC-20A型在线脱气系统,SIL-20A型自动进样系统,UV检测器,日本岛津公司;AB135-S型1/10万电子分析天平、AL204型1/1万分之一电子天平,瑞士梅特勒-托利多公司;KQ-500E型超声波清洗器,昆山市超声仪器有限公司;KES-W22CS208H型电陶炉,深圳市康佳智能电器科技有限公司;SCIENTZ-12N型冷冻干燥机,宁波新芝生物科技股份有限公司。
1.2 试药
对照品柴胡皂苷a(批号P03M9F50593,质量分数≥98%)、柴胡皂苷c(批号P17A8F41958,质量分数≥98%)、柴胡皂苷d(批号Z08A8L33357,质量分数≥98%)、柴胡皂苷b1(批号58558-08-0,质量分数≥97%)及柴胡皂苷b2(批号58316-41-9,质量分数≥95%),均购自上海源叶生物科技有限公司;乙腈、甲醇、磷酸,色谱级,赛默飞世尔科技有限公司;氨水,25%~28%,西陇科学股份有限公司;屈臣氏蒸馏水,广州屈臣氏食品饮料有限公司。20批北柴胡饮片来源于河南省南阳市(S1~S5)、吉林省伊通县(S6~S10)、山西省运城市(S11~S15)及陕西省(S16~S20)共4个产地,经长春中医药大学中药鉴定教研室蔡广知副教授鉴定,均来源于伞形科柴胡属植物柴胡DC.的干燥根,信息见表1。
2 方法与结果
2.1 醋北柴胡饮片的制备
参照《中国药典》2020年版四部[13]醋炙法(通则0213),取20批北柴胡饮片,加醋(每100 kg柴胡,加20 kg醋)拌匀,闷透3.5 h置炒药机内炒至表面呈淡棕黄色,微有醋香气,经检测北柴胡和醋北柴胡饮片质量均符合《中国药典》2020年版一部要求。
2.2 北柴胡及醋北柴胡饮片指标性成分含量测定
参照文献方法[14-15]测定20批北柴胡及醋北柴胡饮片指标性成分含量,结果见表2。20批北柴胡饮片中柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2质量分数分别为9.02~38.02、0.89~4.95、9.24~35.37、0.11~6.49、2.36~3.39 mg/g,均值分别为28.50、2.66、26.36、3.64、3.01 mg/g。20批醋北柴胡饮片中柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2质量分数范围分别为5.70~33.09、1.91~3.57、5.90~29.97、1.76~8.04、4.43~6.61 mg/g,均值分别为24.93、2.83、22.69、4.38、5.86 mg/g。
表1 北柴胡饮片样品信息
Table 1 Information of prepared slices of B. chinense
样品批号产地样品批号产地样品批号产地 S1Chj1-20170811河南省南阳市S8Chd3-20171013吉林省伊通县S15Chj1-20170915山西省运城市 S2Chj1-20170812河南省南阳市S9Chd3-20171014吉林省伊通县S1619010041陕西省 S3Chj1-20170813河南省南阳市S10Chd3-20171015吉林省伊通县S1719010042陕西省 S4Chj1-20170814河南省南阳市S11Chj1-20170911山西省运城市S1819010043陕西省 S5Chj1-20170815河南省南阳市S12Chj1-20170912山西省运城市S1919010044陕西省 S6Chd3-20171011吉林省伊通县S13Chj1-20170913山西省运城市S2019010045陕西省 S7Chd3-20171012吉林省伊通县S14Chj1-20170914山西省运城市
表2 北柴胡饮片及醋北柴胡饮片中指标成分含量
Table 2 Content of index components in prepared slices of B. chinense and vinegar-processed B. chinense
样品柴胡皂苷a/(mg∙g−1)柴胡皂苷c/(mg∙g−1)柴胡皂苷d/(mg∙g−1)柴胡皂苷b1/(mg∙g−1)柴胡皂苷b2/(mg∙g−1) 北柴胡醋北柴胡北柴胡醋北柴胡北柴胡醋北柴胡北柴胡醋北柴胡北柴胡醋北柴胡 S131.2631.433.512.7028.1829.570.121.833.355.20 S232.9731.042.942.8229.6328.491.591.973.074.90 S332.9533.094.952.8328.9729.971.221.762.944.43 S431.8031.122.842.7528.7529.390.111.883.344.92 S531.0931.192.752.7027.5229.201.101.883.354.94 S637.7031.112.483.1334.5525.885.635.152.886.25 S738.0230.802.853.2035.3725.542.074.993.186.23 S837.6731.522.723.5732.3226.233.085.062.766.33 S937.5130.702.593.0132.0125.971.557.973.396.36 S1037.6330.732.643.5031.6725.992.868.042.366.46 S1135.0830.563.643.4334.0328.344.435.353.386.16 S1235.2630.462.903.3234.2628.834.607.203.356.47 S1335.1630.993.053.3134.6428.723.165.193.356.25 S1434.7131.193.373.3533.7129.364.727.133.356.61 S1535.1030.852.823.3233.8228.945.265.152.816.05 S169.075.700.901.919.365.905.933.592.536.20 S179.566.220.961.939.996.526.123.672.585.54 S189.435.740.891.939.845.906.493.592.815.15 S199.027.002.241.919.247.516.353.072.716.17 S209.067.082.191.929.307.596.453.162.786.54
2.3 北柴胡及醋北柴胡标准汤剂的制备
参照相关指导原则[16-17]中标准汤剂的制备方法,分别取20批北柴胡饮片100 g,浸泡30 min,武火转文火煎煮2次,第1次加7倍量水煎煮30 min,第2次加6倍量水,煎煮20 min。经300目绢布趁热滤过,合并2次滤液,进行分装,−20 ℃预冷冻后,置于冷冻干燥机中冷冻干燥,即得北柴胡标准汤剂冻干粉,编号为CHD1~CHD20。同法制备醋北柴胡标准汤剂冻干粉,编号为VCHD1~VCHD20。
2.4 物性参数测定
2.4.1 pH值测定 分别测定各批次北柴胡及醋北柴胡标准汤剂pH值,结果见表3。20批北柴胡标准汤剂pH值范围在7.95~8.27,均值为8.06,北柴胡标准汤剂显碱性;20批醋北柴胡标准汤剂pH值范围在6.70~7.87,均值为7.56,北柴胡醋制后标准汤剂pH值降低。
2.4.2 出膏率测定 出膏率以标准汤剂冻干粉量计,按公式出膏率=标准汤剂冻干粉质量/饮片投料量。北柴胡标准汤剂和醋北柴胡标准汤剂出膏率计算结果见表3。结果表明,20批北柴胡标准汤剂出膏率范围在12.02%~21.54%,均值为18.14%。20批醋北柴胡出膏率范围在10.15%~20.45%,均值为17.11%,北柴胡醋制后标准汤剂出膏率降低。
表3 北柴胡及醋北柴胡标准汤剂pH值和出膏率
Table 3 pH value and ointment rate of CHD and VCHD
样品pH值出膏率/%样品pH值出膏率/%样品pH值出膏率/% CHDVCHDCHDVCHDCHDVCHDCHDVCHDCHDVCHDCHDVCHD S18.277.84 20.2120.09 S87.976.70 20.5319.46 S157.977.87 18.7818.45 S28.237.83 20.0020.15 S97.966.70 21.1418.86 S168.117.84 12.48 10.88 S38.167.84 19.9220.45 S107.976.70 20.3519.78 S178.107.85 12.46 10.15 S48.237.84 19.5219.68 S117.957.86 19.2618.07 S188.087.85 12.02 11.04 S58.197.86 20.0219.89 S127.967.85 18.5518.45 S198.097.84 13.25 10.53 S67.976.72 21.5419.38 S137.977.82 19.0517.68 S208.077.83 13.45 10.23 S77.966.71 21.0520.03 S147.967.86 19.1518.86
CHD-北柴胡标准汤剂 VCHD-醋北柴胡标准汤剂,图2~4及表4、5同
CHD-standard decoction ofVCHD-vinegar-processed, same as figures 2—4 and tables 4, 5
2.5 北柴胡及醋北柴胡标准汤剂指纹图谱研究
2.5.1 色谱条件 Thermo Hypersil Gold色谱柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.01%磷酸水溶液,梯度洗脱:0~10 min,26%乙腈;10~65 min,26%~46%乙腈;65~90 min,46%~70%乙腈;检测波长210 nm;体积流量1 mL/min;柱温30 ℃;进样量10 µL。色谱图见图1。
2.5.2 对照品溶液的制备 精密称取柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2对照品适量,加甲醇溶解,制成含柴胡皂苷a 0.431 mg/mL、柴胡皂苷c 0.211 mg/mL、柴胡皂苷d 0.512 mg/mL、柴胡皂苷b10.266 mg/mL及柴胡皂苷b20.212 mg/mL的混合对照品储备液,备用。
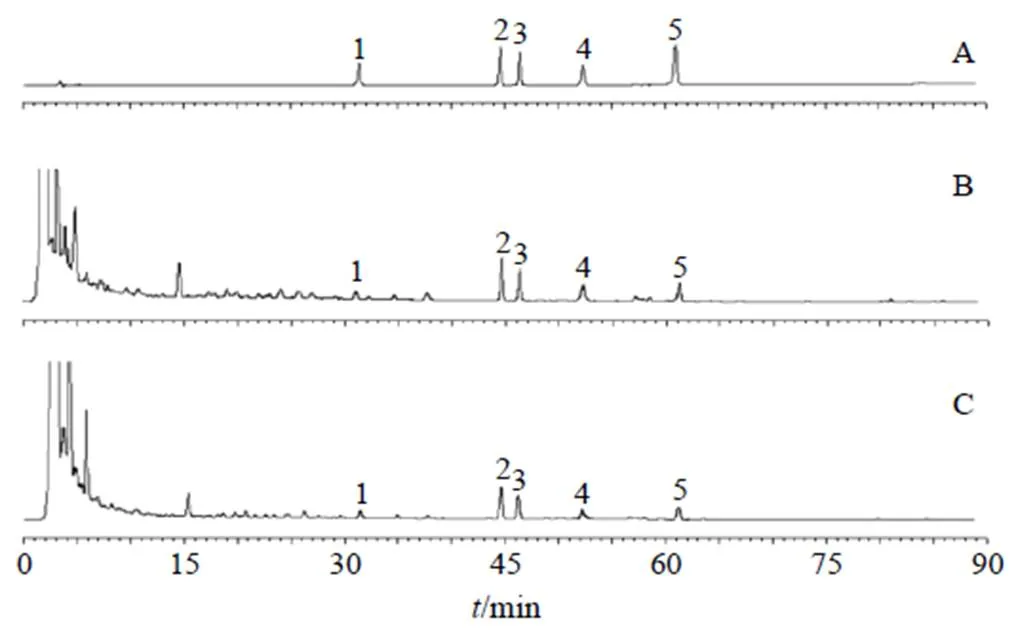
1-柴胡皂苷c 2-柴胡皂苷a 3-柴胡皂苷b2 4-柴胡皂苷b1 5-柴胡皂苷d
2.5.3 供试品溶液的制备 精密称取各北柴胡及醋北柴胡标准汤剂冻干粉1 g,于具塞锥形瓶中,加入含5%浓氨试液的甲醇溶液25 mL,超声30 min,滤过,用甲醇20 mL分2次洗涤容器及药渣,洗液与滤液合并,回收溶剂至干。残渣加60%乙腈水溶液溶解,转移至10 mL量瓶中,加60%乙腈水溶液至刻度,摇匀,0.22 µm微孔滤膜,滤过,即得。
2.5.4 精密度考察 取CHD1样品溶液,按“2.5.1”项下色谱方法重复进样6次,记录色谱图,以7号峰(柴胡皂苷a)为参照峰,计算各共有峰与参照峰的相对保留时间的RSD值均小于0.21%,相对峰面积RSD值均小于4.48%,表明仪器的精密度良好。
2.5.5 重复性考察 取同一批北柴胡标准汤剂冻干粉,按“2.4.3”项下方法平行制备6份供试品溶液,按“2.5.1”项下色谱条件进样,计算各共有峰与参照峰的相对保留时间的RSD值均小于0.74%,相对峰面积的RSD值均小于4.04%,表明该方法的重复性良好。
2.5.6 稳定性考察 取CHD1样品溶液,分别于供试品溶液制备后0、4、8、12、24 h,按“2.5.1”项下色谱条件测定,记录色谱图,计算各共有峰与参照峰相对保留时间的RSD值均小于0.88%,相对峰面积的RSD值均小于3.79%,表明供试品溶液在室温下24 h内稳定性良好。
2.5.7 指纹图谱的建立 分别取北柴胡和醋北柴胡标准汤剂冻干粉,按“2.5.3”项下方法制备供试品溶液,按“2.5.1”项下色谱条件分别依次进样测定,记录色谱图信息。采用中药色谱指纹图谱相似度评价系统软件(2012版)进行评价,设置CHD1号样品色谱图为参照图谱,采用平均数法,进行多点校正和色谱峰匹配,经全谱峰匹配后得到北柴胡标准汤剂指纹图谱(图2-A);同法设置VCHD1号样品色谱图为参照图谱,建立醋北柴胡标准汤剂指纹图谱(图2-B)。建立的北柴胡标准汤剂和醋北柴胡标准汤剂的指纹图谱,分别匹配了16个共有峰,通过对照品比对(图1),指认了其中5个共有峰,峰4(柴胡皂苷c)、7(柴胡皂苷a)、9(柴胡皂苷b2)、10(柴胡皂苷b1)及13(柴胡皂苷d)。
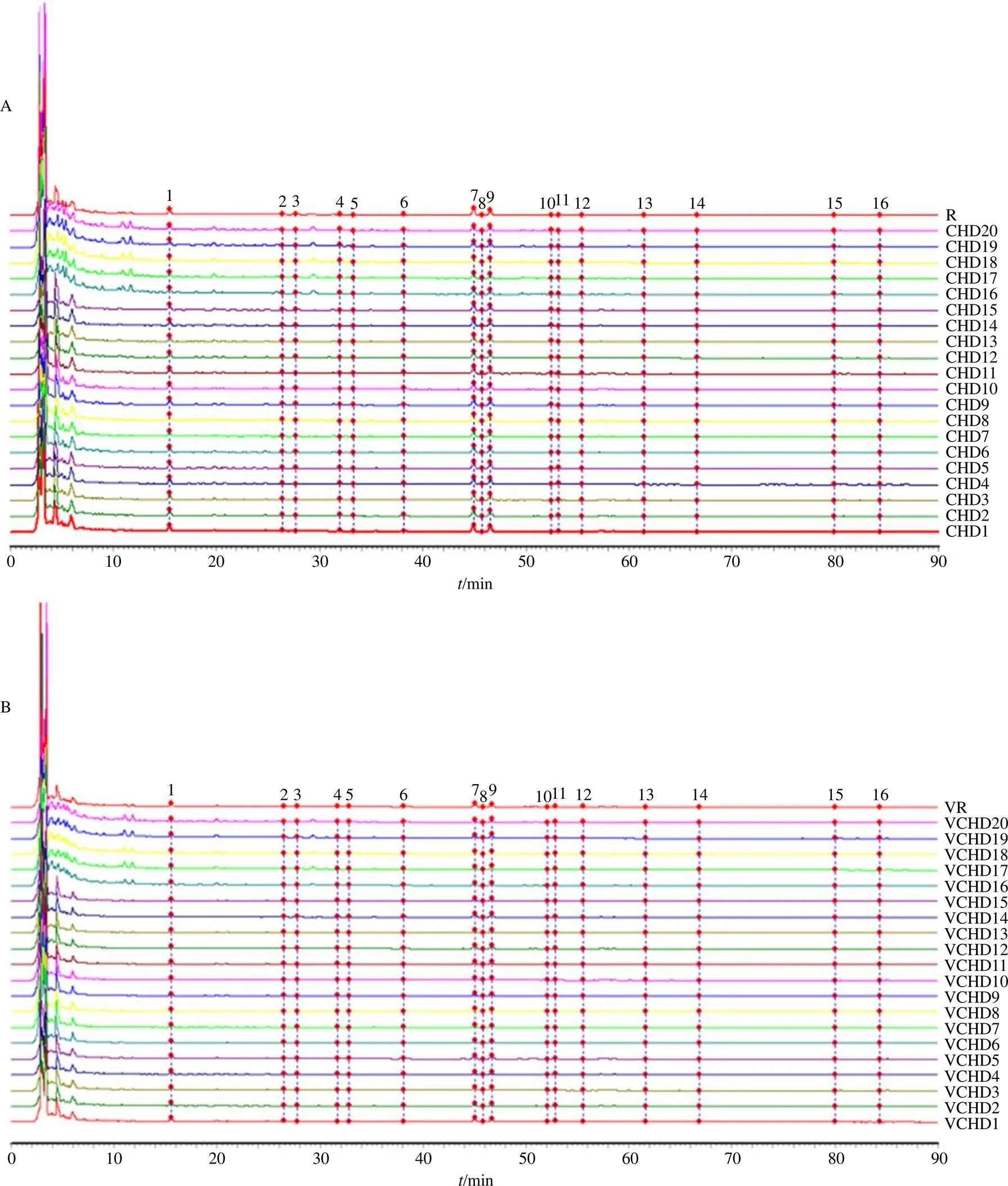
图2 北柴胡标准汤剂(A) 和醋北柴胡标准汤剂(B) 指纹图谱
2.5.8 相似度评价 20批北柴胡标准汤剂(CHD1~CHD20)相似度计算结果为0.990、0.989、0.991、0.994、0.989、0.992、0.993、0.995、0.995、0.991、0.989、0.979、0.983、0.984、0.987、0.979、0.976、0.978、0.979、0.978;20批醋北柴胡标准汤剂(VCHD1~VCHD20)相似度计算结果为0.996、0.996、0.992、0.994、0.995、0.973、0.957、0.958、0.976、0.956、0.987、0.988、0.992、0.985、0.946、0.973、0.973、0.966、0.971、0.967,结果均大于0.90,表明北柴胡和醋北柴胡标准汤剂整体相似性均较好,所建立的指纹图谱可用于北柴胡和醋北柴胡标准汤剂质量评价研究。
2.6 基于指纹图谱的北柴胡与醋北柴胡标准汤剂差异性分析
2.6.1 主成分分析(principal component analysis,PCA) PCA是在尽可能保持原有数据信息的前提下,通过降维处理达到简化指标的目的,目前已被广泛用于中药质量标准研究的数据统计分析中。以北柴胡和醋北柴胡标准汤剂指纹图谱中的16个共有峰峰面积为变量,借助SIMICA 14.0软件,采用无监督模式法PCA进行分析,北柴胡和醋北柴胡标准汤剂被分为2组,见图3,表明北柴胡醋制前后标准汤剂质量存在一定差异。
2.6.2 正交偏最小二乘法-判别分析(orthogonal partial least square method-discriminant analysis,OPLS-DA) 为进一步找出影响北柴胡与醋北柴胡标准汤剂差异的主要变量,在PCA聚类结果基础上,建立有监督模式识别分析法OPLS-DA模型,样本得分矩阵见图4-A,模型对自变量拟合指数2=0.961,对因变量拟合指数2=0.962,模型预测指数2=0.945,说明该模型有较好的解释能力和预测能力,可用于区分北柴胡和醋北柴胡标准汤剂。图4-B为OPLS-DA模型的变量重要性投影值(variable importance in projection,VIP),VIP值的大小代表了各指标成分对模型贡献率的大小,值越大贡献越大,表明该色谱峰对于北柴胡和醋北柴胡标准汤剂的分类贡献越大,同时也是导致北柴胡和醋北柴胡标准汤剂相区分的差异成分。以VIP>1为界限进行筛选,结合北柴胡和醋北柴胡标准汤剂指纹图谱中的16个共有峰峰面积检验分析,结果共确定7个差异性色谱峰,分别为峰1、4(柴胡皂苷c)、6、7(柴胡皂苷a)、9(柴胡皂苷b2)、10(柴胡皂苷b1)及13(柴胡皂苷d)。
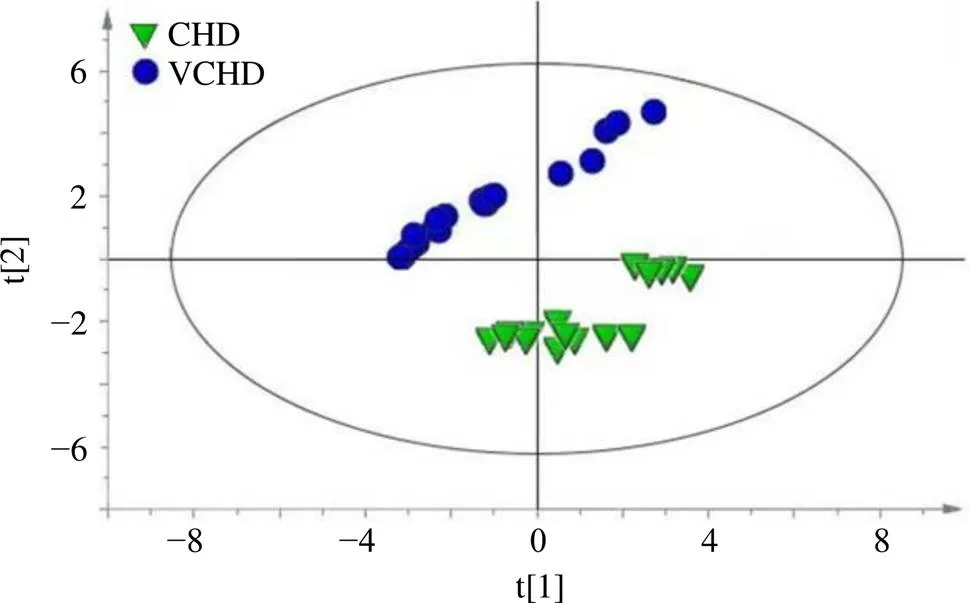
图3 PCA得分图
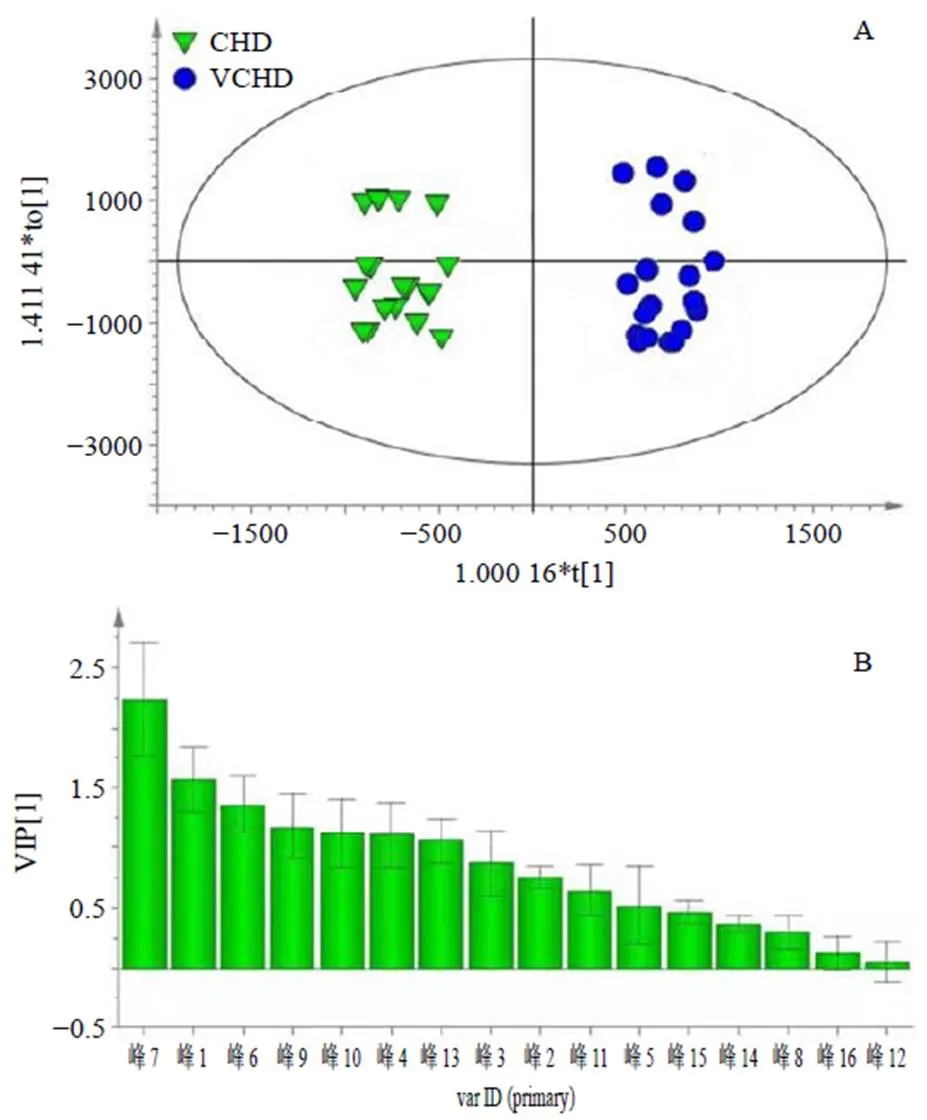
图4 OPLS-DA得分图(A) 和VIP值(B)
2.7 北柴胡及醋北柴胡标准汤剂含量测定研究
2.7.1 线性关系考察 精密移取“2.5.2”项下各对照品溶液适量,稀释成一系列不同质量浓度的对照品溶液,按照“2.5.1”项下色谱条件进行测定,以对照品质量浓度为横坐标(),以对照品峰面积为纵坐标()绘制标准曲线,进行线性回归,得到5种成分的回归方程,结果分别为柴胡皂苷a=3 153.1-22 544,2=0.999 6,线性范围204.67~1228.00 μg/mL;柴胡皂苷c=2 428.8-1 056.3,2=0.999 4,线性范围30.83~185.00 μg/mL;柴胡皂苷d=3 431.6-4 363.2,2=0.999 5,线性范围150.83~905.00 μg/mL;柴胡皂苷b1=2 576.0-435.47,2=0.999 5,线性范围6.65~133.00 μg/mL;柴胡皂苷b2=2 620.1+146.96,2=0.999 3,线性范围5.30~106.00 μg/mL。
2.7.2 精密度考察 取CHD1样品溶液,按“2.5.1”项下色谱方法重复进样6次,计算柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2峰面积RSD值分别为0.68%、2.00%、1.98%、2.00%、0.97%,表明仪器的精密度良好。
2.7.3 重复性考察 取同一批北柴胡标准汤剂冻干粉,按“2.5.3”项下方法平行制备6份供试品溶液,按“2.5.1”项下色谱条件进样,计算柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2含量RSD值分别为0.38%、3.07%、0.49%、1.78%、1.12%,表明该方法的重复性良好。
2.7.4 稳定性考察 取CHD1样品溶液,室温放置 0、2、4、8、12、24 h。按“2.5.1”项下色谱条件进样,计算柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2峰面积RSD值分别为1.13%、0.95%、2.81%、1.01%、1.16%,表明供试品溶液在室温下24 h内稳定性良好。
2.7.5 加样回收率 取已知含量北柴胡标准汤剂冻干粉约0.5 g,精密称定,共6份,按1∶1加入对照品,按“2.5.3”项下方法制备供试品溶液,按“2.5.1”项下色谱条件进行测定,计算柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2的平均回收率分别为97.63%、96.12%、97.00%、96.17%、96.71%,符合相关规定,表明方法准确度良好。
2.7.6 北柴胡及醋北柴胡标准汤剂指标成分的含量测定 分别取北柴胡和醋北柴胡标准汤剂冻干粉,按“2.5.3”项下方法制备供试品溶液,按“2.5.1”项下色谱条件测定并计算柴胡皂苷a,柴胡皂苷c,柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2的含量,结果见表4,20批北柴胡标准汤剂的柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2质量分数分别为4.90~6.22、0.83~3.80、0.19~0.65、3.34~10.40、20.76~34.99 mg/g,均值分别为5.56、2.16、0.38、7.24、28.09 mg/g。20批醋北柴胡标准汤剂的柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2质量分数范围分别在3.21~6.09、0.58~3.38、0.08~0.54、5.31~10.79、21.07~49.67 mg/g,均值分别为4.30、1.67、0.17、8.10、31.81 mg/g。
表4 北柴胡及醋北柴胡标准汤剂中指标成分含量
Table 4 Multi-index components content of CHD and VCHD
批号柴胡皂苷a/(mg∙g−1)柴胡皂苷c/(mg∙g−1)柴胡皂苷d/(mg∙g−1)柴胡皂苷b1/(mg∙g−1)柴胡皂苷b2/(mg∙g−1) CHDVCHDCHDVCHDCHDVCHDCHDVCHDCHDVCHD S15.754.281.731.240.200.133.356.3220.8328.27 S25.633.611.651.160.190.124.266.6620.7621.07 S35.785.631.751.710.200.203.345.3120.8629.74 S46.205.902.242.140.210.204.136.6922.9122.15 S55.645.321.661.570.200.195.276.3120.8028.92 S65.733.591.550.720.470.166.248.1730.8124.13 S75.703.281.990.580.490.147.448.1631.5422.33 S86.223.482.200.620.560.167.776.1734.9923.45 S96.196.092.142.100.550.547.757.1934.8922.62 S105.543.212.000.580.430.146.729.1429.4121.89 S115.973.571.500.980.340.1010.409.2823.0629.76 S125.034.070.831.210.230.107.458.1525.5834.69 S135.513.451.221.170.290.088.378.2729.2428.63 S145.534.181.231.060.290.108.278.1629.4034.99 S155.054.191.350.780.260.107.569.1625.6835.24 S165.283.883.802.830.650.169.8110.7932.8338.86 S174.904.633.513.240.300.208.149.6830.0148.63 S185.193.943.602.910.560.159.459.6832.7839.76 S195.234.893.643.380.580.349.538.9032.7451.37 S205.164.753.603.370.560.159.509.7832.6549.67
2.7.7 北柴胡及醋北柴胡标准汤剂指标成分含量差异性分析 运用GraphPad Prism 8.0.1软件,采用方差分析分别对北柴胡及醋北柴胡标准汤剂中5种指标成分含量进行统计学分析,<0.05表示差异显著,结果见表5。结果显示,北柴胡醋制前后指标成分柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2含量均有统计学意义。北柴胡醋制后标准汤剂中柴胡皂苷a、柴胡皂苷c、柴胡皂苷d含量较低,柴胡皂苷b1、柴胡皂苷b2含量较高(<0.05)。
表5 北柴胡及醋北柴胡标准汤剂指标成分含量差异性分析(, n = 20)
Table5 Analysis of differences of index components in CHD and VCHD (, n = 20)
样品质量分数/(mg∙g−1) 柴胡皂苷a柴胡皂苷c柴胡皂苷d柴胡皂苷b1柴胡皂苷b2 CHD5.562±0.3992.160±0.9390.378±0.1607.238±2.17328.089±5.050 VCHD4.297±0.881*1.668±0.987*0.173±0.103*8.099±1.489*31.809±9.672*
与CHD比较:*<0.05
*< 0.05CHD
3 讨论
3.1 饮片的收集
北柴胡主产区和道地产区为陕西省,河北、河南、山西及吉林等地,本实验收集的20批北柴胡来源于道地产区、主产区及集散地共4个产地,实验取材在一定程度上能够涵盖药材市场实际情况,使本实验的标准汤剂具有较好的代表性,可用于后续质量评价研究。
3.2 指纹图谱差异性分析
本研究分别建立北柴胡及醋北柴胡标准汤剂HPLC指纹图谱,分别确认了16个共有峰,对指纹图谱进行相似度评价,各批次相似度结果均良好。为进一步分析北柴胡与醋北柴胡标准汤剂,寻找二者差异性成分,本实验引入化学计量学方法,通过PCA和OPLS-DA分析确定指纹图谱中7个具有显著差异的色谱峰,通过对照品指认峰4为柴胡皂苷c,峰7为柴胡皂苷a,峰9是柴胡皂苷b2,峰10为柴胡皂苷b1,峰13为柴胡皂苷d,峰1及峰6尚未知,后续将会进一步采用液质联用手段对其进行鉴定,以便更好地对北柴胡及醋北柴胡标准汤剂进行质量控制。
3.3 含量测定差异性分析
北柴胡中皂苷类化合物是其主要化学成分,也是其发挥药理药效最重要的成分[18]。《中国药典》、《香港中药材标准》及各部分地方标准评价柴胡药材多以柴胡皂苷a、柴胡皂苷d为质量检测指标。中药饮片是中药制剂的原料药,本研究对北柴胡饮片及醋柴胡饮片进行含量测定分析,北柴胡饮片中柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2质量分数均值分别为28.50、2.66、26.36、3.64、3.01 mg/g。醋北柴胡饮片中柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2质量分数均值分别为24.93、2.83、22.69、4.38、5.86 mg/g。结果表明北柴胡饮片醋制后柴胡皂苷a、柴胡皂苷d含量下降,柴胡皂苷c含量无显著变化、柴胡皂苷b1及柴胡皂苷b2含量升高。
结合HPLC指纹图谱差异分析,北柴胡及醋北柴胡标准汤剂中共7个差异性成分,为进一步验证差异性结果,建立其中5个化学成分含量测定方法,对醋制前后标准汤剂含量结果对比分析研究。结果表明北柴胡醋制后标准汤剂中柴胡皂苷a、柴胡皂苷c、柴胡皂苷d含量下降,柴胡皂苷b1、柴胡皂苷b2含量升高。
综上研究表明,柴胡皂苷a、柴胡皂苷c、柴胡皂苷d、柴胡皂苷b1及柴胡皂苷b2含量在各工艺环节(饮片-醋制饮片-标准汤剂)均有变化,分析原因可能是醋制对各成分的含量存在影响,在质量传递过程中醋制北柴胡饮片可能会增强其有效成分的溶出,研究表明[19-20]柴胡皂苷a、柴胡皂苷c、柴胡皂苷d的苷元为环氧醚型,结构中含有13,28-环氧键,属I型柴胡皂苷,在酸性环境中控制温度等条件可使柴胡皂苷c转化为柴胡皂苷h(II型柴胡皂苷)。同时有研究表明在水煎液中,柴胡皂苷a及柴胡皂苷d结构中13和28号位的氧醚环结构易断裂,柴胡皂苷a、柴胡皂苷d会转化为柴胡皂苷b1(II型柴胡皂苷)、柴胡皂苷b2(II型柴胡皂苷),柴胡皂苷d结构不稳定,会转化为大量的柴胡皂苷b2,柴胡皂苷a相对于柴胡皂苷d较稳定,但柴胡皂苷a在中性环境中转化产物主要是羟基柴胡皂苷a,且羟基柴胡皂苷a会转化为柴胡皂苷b1,这与现有研究结果相一致[21-22]。
北柴胡醋制后对二甲苯所致大鼠耳肿胀有拮抗作用[23-24],同时能减轻CCl4造成的小鼠肝损伤,降低小鼠体内的谷草转氨酶转氨酶和谷丙转氨酶。文献报道[25],柴胡皂苷b2具有同样药理活性,此外还具有抗凋亡[26]、抗肿瘤[27]、抗病毒[28]等药理作用。由本研究结果推测,II型柴胡皂苷可能是发挥药理作用的重要成分,I型柴胡皂苷向II型柴胡皂苷的转化可能是引起北柴胡标准汤剂和醋北柴胡标准汤剂差异的主要原因之一,建议对二者质量控制时应考虑对I、II型柴胡皂苷的测定。
3.4 小结
中药饮片标准汤剂作为临床制剂的标准参照物,为衡量中药配方颗粒是否与临床汤剂基本一致的物质基准,用来标准化不同的临床用药形式,保障用药的准确性和剂量的一致性,具有重大的现实意义。
北柴胡与醋柴胡的标准汤剂作为相关成型制剂与传统汤剂的中间桥梁,在配方颗粒、中成药、经典名方等制剂生产过程有着十分重要的地位。本研究从北柴胡及醋北柴胡标准汤剂的pH值、出膏率、HPLC指纹图谱和多指标成分含量测定方法入手,全面对二者质量进行分析,建立了科学和实用的北柴胡及醋北柴胡标准汤剂质量评价方法,为二者相关制剂的鉴别和质量控制提供参考。
利益冲突 所有作者均声明不存在利益冲突
[1] 陈士林. 标准汤剂——提升中药配方颗粒质量的重要桥梁[N]. 中国医药报, 2021-03-09(003).
[2] 中国药典[S]. 一部. 2020: 280.
[3] 夏召弟, 刘霞. 北柴胡化学成分及质量控制方法研究进展 [J]. 中国现代中药, 2021, 23(5): 940-949.
[4] 黄海强. 柴胡属植物化学成分和质量控制研究及天目藜芦化学成分研究 [D]. 上海: 第二军医大学, 2010.
[5] 陈朝, 伍小燕. 柴胡有效成分提取分离方法的研究进展 [J].实用临床医药杂志, 2011, 15(19): 190-192.
[6] Yu M, Chen H, Liu S H,. Differential expression of genes involved in saikosaponin biosynthesis betweenDC. andWilld [J]., 2020,doi: 10.3389/fgene.2020. 583245.
[7] 李书启. 柴胡疏肝散抗氧化活性及其活性成分柚皮苷药代动力学的研究 [D]. 北京: 北京化工大学, 2010.
[8] 孙婷婷. 北柴胡饮片化学成分及质量标准研究 [D]. 长春: 吉林农业大学, 2020.
[9] 赵香妍, 刘长利. 中药柴胡的研究概况与发展趋势 [J]. 时珍国医国药, 2015, 26(4): 963-966.
[10] Zhang W H, Sun X L, Sui W W,. Quality control of Xiebai San Standard Decoction assisted by network pharmacology strategy [J]., 2020, 83(9): 873-884.
[11] 张伟, 陈萍, 朱蕾. 醋制柴胡炮制经验探讨 [J]. 基层医学论坛, 2019, 23(17): 114-115.
[12] 李军, 姜华, 张延萍, 等. 柴胡水煎液中柴胡皂苷a和d的溶出与转化差异 [J]. 中国药学杂志, 2014, 49(19): 1692-1696.
[13] 中国药典[S]. 四部. 2020: 251.
[14] 高文义, 王康宇, 贡济宇, 等. 基于化学模式识别分析的醋北柴胡HPLC指纹图谱研究 [J]. 中药材, 2020(9): 2200-2203.
[15] 马守芳, 孙江伟, 高晓洁, 等. HPLC-ELSD同时测定北柴胡中柴胡皂苷A、C、D、B1、B2及山奈苷含量 [J]. 沈阳药科大学学报, 2021, 38(8): 821-826.
[16] 陈士林, 刘安. 《中药饮片标准汤剂》(第二卷) [J]. 北京: 科学出版社, 2019: 8.
[17] 窦志华, 许波, 居宇峰, 等. 栀子标准汤剂量值传递规律研究 [J]. 中草药, 2021, 52(23): 7162-7175.
[18] 许磊, 田稷馨, 宋瑞, 等. 柴胡醋制前后柴胡皂苷a、b2、c、d的LC-MS/MS法测定及比较 [J]. 中国药科大学学报, 2012, 43(4): 334-340.
[19] Shimizu K, Amagaya S, Ogihara Y. New derivatives of saikosaponins [J]., 1985, 33(8): 3349-3355.
[20] 闵宇航, 王京辉, 范妙璇, 等. 柴胡饮片皂苷类成分变化及质量控制研究 [J]. 药物分析杂志, 2014, 34(5): 836-843.
[21] 刘树强, 王术玲, 高晓玲, 等. 柴胡水煎过程中皂苷成分的变化规律 [J]. 中药新药与临床药理, 2013, 24(6): 602-606.
[22] 王丽娜, 汪巍, 徐驰, 等. 柴胡醋制前后抗炎作用比较研究 [J]. 中成药, 2013, 35(5): 1079-1081.
[23] Li Z Y, Sun H M, Xing J,. Chemical and biological comparison of raw and vinegar-baked[J]., 2015, 165: 20-28.
[24] Shin J S, Im H T, Lee K T. Saikosaponin B2suppresses inflammatory responses through IKK/IκBα/NF-κB signaling inactivation in LPS-induced RAW 264.7 macrophages [J]., 2018, 42: 342-353.
[25] 高子涵, 王红伟, 吕行直, 等. 柴胡皂苷b2通过抑制线粒体凋亡通路减轻过氧化氢诱导的L-02细胞损伤 [J]. 中国药理学与毒理学杂志, 2018, 32(7): 543-549.
[26] Zhao Y, Feng L M, Liu L J,. Saikosaponin b2enhances the hepatotargeting effect of anticancer drugs through inhibition of multidrug resistance-associated drug transporters [J]., 231: 116557-116557.
[27] Lin L T, Chung C Y, Hsu W C,. Saikosaponin b2is a naturally occurring terpenoid that efficiently inhibits hepatitis C virus entry [J]., 2014, 62(3): 541-548.
[28] Lee W P, Lan K L, Liao S X,. Antiviral effect of saikosaponin B2in combination with daclatasvir on NS5A resistance-associated substitutions of hepatitis C virus [J]., 2019, 82(5): 368-374.

Quality difference analysis of standard decoction ofand vinegar-processed
SONG Chi, GE Wei, ZOU Jia-li, WANG Yue, TAN Juan-juan,GONG Ji-yu
College of Pharmacy, Changchun University of Chinese Medicine, Changchun 130117, China
To establish the quality evaluation method and investigate the quality differences of standard decoction of Chaihu () (CHD) and vinegar-processed(VCHD).Twenty batches of CHD and VCHD samples were prepared, the extract rates and pH were determined, respectively. Chromatographic fingerprints and multi-index content determination method of CHD and VCHD were generated from thehigh performance liquid chromatography (HPLC) and the quality differences were analyzed using the method of chemometrics and statistics.The extract rates and pH value of VCHD standard decoction was decreased. The fingerprints of the CHD and VCHD were established, a total of 16 common peaks were determined respectively, and five peaks were identified; The similarity of CHD and VCHD were 0.976—0.995 and 0.946—0.996, respectively. A clear classification among CHD and VCHD sample was observed in the score plot of the principal component analysis (PCA), then seven marker compounds were selected and identified by orthogonal partial least square discriminant analysis (OPLS-DA), including peaks 1, 4 (saikosaponin c), peaks 6, 7 (saikosaponin a), peak 9 (saikosaponin b2), peak 10 (saikosaponin b1), and peak 13 (saikosaponin d). Multiple-index content determination results showed that there was significant difference in the content of index components before and after vinegar processing of CHD (< 0.05). The contents of saikosaponin a, saikosaponin c and saikosaponin d were lower. Besides, saikosaponin b1and saikosaponin b2was higher in the standard decoction of VCHD.A scientific and practical quality evaluation method of CHD and VCHD was established, which also provided a reference for the identification and quality control of related preparations ofand its vinegar-processed products.
DC.; vinegar-processing; standard decoction; chromatographic fingerprints; orthogonal partial least squares-discriminant analysis;saikosaponin;quality control
R283.6
A
0253 - 2670(2022)08 - 2331 - 10
10.7501/j.issn.0253-2670.2022.08.009
2021-11-06
国家中药标准化项目(ZYBZH-Y-JL-25);吉林省科技发展计划项目(20210204078YY)
宋 驰(1998—),女,硕士研究生,研究方向为中药分析学。E-mail: 2697733699@qq.com
贡济宇,教授,博士生导师,主要从事中药分析学研究。E-mail: gjy0431@126.com
[责任编辑 郑礼胜]
