CuO⁃SiO 2⁃CeO 2催化剂的设计、制备及性能研究
2022-04-15张财顺刘道胜高志贤
卢 畅,张财顺,刘道胜,张 磊,高志贤
(辽宁石油化工大学石油化工学院,辽宁 抚顺 113001)
近年来,CuO⁃CeO2催化剂作为典型非贵金属CeO2复合催化剂材料在甲醇/水蒸气重整制氢领域备受关注[1]。在CuO⁃CeO2催化剂体系中,虽然CeO2具有良好的储/放氧能力以及独特的氧化还原性能[2],但CeO2在高温下热稳定性较差,比表面积、储/放氧能力、氧化还原性能均受到影响[3];Cu的引入在一定程度上提高了催化剂体系的热稳定性,且CuO在CeO2中高度分散并产生较强的相互作用,然而CuO⁃CeO2催化剂的比表面积相对较小[4],特别是在高温条件下因烧结和积碳导致的催化剂比表面积降低的问题仍然没有得到很好的解决[5]。因此,制备具有良好储/放氧能力、热稳定性,并且具有较大比表面积的CuO/CeO2催化剂对于甲醇/水蒸气重整制氢领域的发展至关重要。
目前,众多科研学者主要围绕催化剂形貌以及催化剂掺杂组分两个方面对CuO⁃CeO2催化剂进行研究。形貌研究方面,S.C.Yang等[6]报道了模版法制备可用于甲醇水蒸气重整制氢的纳米棒状CeO2催化材料,纳米棒状CeO2材料具有更多的氧空穴,因此催化活性更高。X.L.Guo等[7]对CeO2催化材料形貌与催化性能之间的关系进行研究,结果表明,具有纳米棒和纳米多面体形状的CeO2催化材料的催化性能较好。组分掺杂方面,J.Li等[8]将Cr作为助剂添加到Cu⁃Ce催化剂体系中,催化剂表面氧空穴数量因助剂Cr的添加而增多;N.A.S.Amin等[9]发现,Cr的引入可以降低Cu⁃Ce催化剂中CuO的结晶度,进而降低CuO的晶粒大小;李吉刚等[10]发现,Cr的引入可使催化剂具有良好的低温活性。以上研究虽然在一定程度上提高了催化剂性能,但所报道的催化剂比表面积相对较小,催化剂的活性仍然可以提高。SiO2具有较强的键结合能、良好的热稳定性和较大的比表面积[11⁃13]。将SiO2作为第三组分引入到CuO⁃CeO2催化剂中,可以有效增大催化剂的比表面积,提高催化剂的活性。
基于以上分析,本文利用水热合成法制备了CuO⁃SiO2⁃CeO2催化剂并对其进行表征及测试,最后将其应用于甲醇水蒸气重整制氢实验,研究了SiO2摩尔分数对催化剂比表面积和催化性能的影响。
1 实验部分
1.1 实验原料
Ce(NO3)3⋅6H2O、正 硅 酸 乙 酯TEOS(上 海 麦 克林生化科 技 有 限 公 司,AR);Cu(NO3)2⋅3H2O、尿 素(国药集团化学试剂有限公司,AR);蒸馏水,自制。
1.2 催化剂的制备
分别称取5份12.612 g的Ce(NO3)3⋅6H2O固体和适量尿素溶解于142 mL水中,分别称取0.155、0.336、0.491、1.070 g正硅酸乙酯(TEOS)并配制成SiO2摩尔分数为0、2.5%、5.0%、7.5%、15.0%的混合液体,具体原料用量见表1。
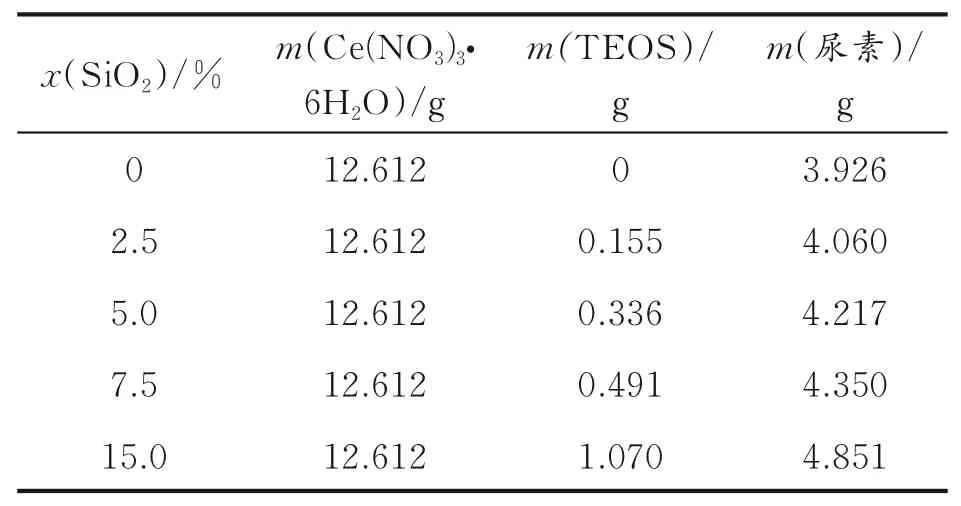
表1 载体制备所用原料Table 1 The raw material of supports
将制备的混合液装入200 mL反应釜,在均相反应器中反应12 h(180℃),反应结束后,抽滤,得到沉淀,将所得沉淀干燥12 h后待用。分别取5份沉淀,在空气气氛下400℃焙烧3 h,得到不同SiO2摩 尔 分 数 载 体CeO2、SiO22.5%⁃CeO2、SiO25.0%⁃CeO2、SiO27.5%⁃CeO2、SiO215.0%⁃CeO2,对所得沉淀分别进行饱和吸水量测试。称取5份1.900 g Cu(NO3)2⋅3H2O固体并溶于对应硅摩尔分数的饱和吸水量去离子水中,加入9.374 g载体混合均匀,搅拌3 h陈化2 h,烘箱干燥12 h,400℃空气气氛下焙烧3 h,制得5种催化剂,分别命名为CuO25.0%⁃CeO2、CuO25.0%⁃SiO2x⁃CeO2(x=2.5%、5.0%、7.5%、15.0%)。
1.3 催化剂的表征
通过德国Bruker D8 Advance型X射线粉末衍射仪对样品进行检测并对其图谱进行分析。利用贝士德BSD⁃PS(M)物理吸附仪对载体和催化剂进行N2吸附⁃脱附表征。使用泛泰FINESORB⁃3010C全自动程序升温化学吸附仪进行H2⁃TPR测试,具体过程见参考文献[14]。
1.4 催化剂的评价
取2 mL催化剂,使其在含有体积分数5.0%H2的H2⁃N2混合气体中,在280℃条件下预还原3 h,然后切换成N2降至室温后,关闭N2。用微量泵将水和甲醇的混合液输入至反应器(n(H2O)/n(CH3OH)=1.2∶1.0),调节至反应温度。反应结束后,生成气经冷凝器和干燥管脱除未反应的H2O和CH3OH后,通入上海诜兴科学仪器1690型气相色谱在线分析站,并使用流量计测得生成气的流量。
利用甲醇转化率和产氢速率评价催化剂的催化性能[15⁃16]。具体公式如下:
甲醇转化率:
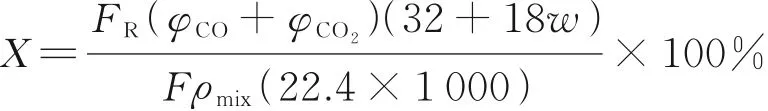
产氢速率:
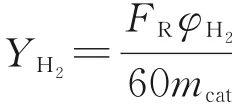
式中,FR为重整气在标况下的流量,mL/min;φCO、φCO2、φH2分别为重整气尾气中的CO、CO2、H2的体积分数,%;F为泵的进料量,mL/min;w为水与醇的物质的量比;ρmix为甲醇水溶液的混合密度,g/mL;mcat为评价时催化剂的质量,kg。
2 结果与讨论
2.1 XRD分析
图1为载体的XRD谱图,表2为不同SiO2摩尔分数载体晶胞参数和晶粒大小数据。由图1和表2可 见,5种 载 体 在28.55°、33.08°、47.48°、56.34°、59.09°、69.42°附近出现了CeO2结构的(111)、(200)、(220)、(311)、(222)、(400)晶面的特征衍射峰;经水热合成法处理的CeO2载体对比发现,制备的SiO2⁃CeO2载体的平均晶粒均小于CeO2载体的平均晶粒,当x=7.5%时,SiO2⁃CeO2载体的平均晶粒仅为11.73 nm。
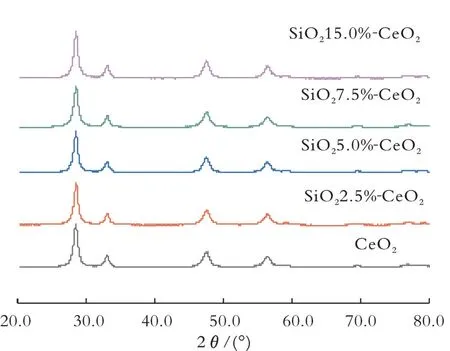
图1 不同SiO 2摩尔分数载体的XRD谱图Fig.1 XRD of carriers with different mole fractions of SiO2
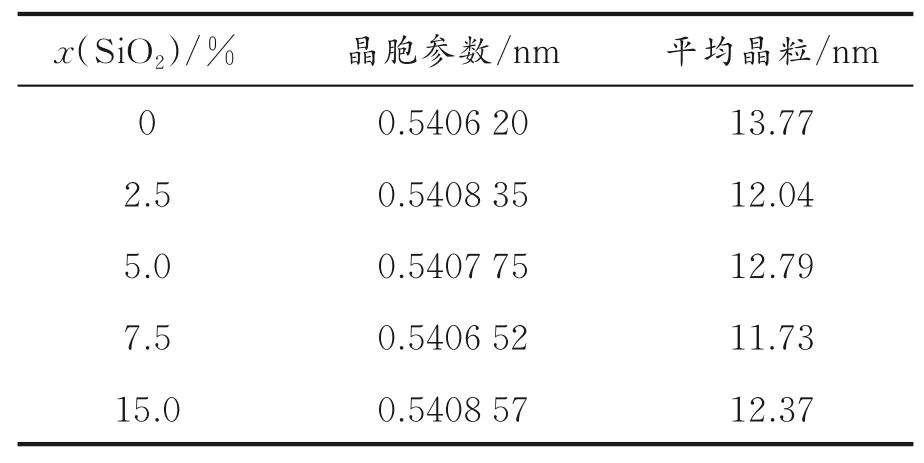
表2 不同SiO 2摩尔分数载体的晶胞参数与平均晶粒大小Table 2 Cell parameters and average grain size of different SiO 2 mole fraction carriers
另外,与CeO2的XRD数据相比,4组SiO2⁃CeO2载体中CeO2的特征衍射峰强度降低,此现象与5种载体平均晶粒大小变化规律保持一致。此外,通过水热合成法制备的SiO2多为无定型结构,因此未能在XRD图谱中观察到标准的SiO2特征峰[17]。
图2为5种CuO5.0%⁃SiO2x⁃CeO2(x=0、2.5%、5.0%、7.5%、15.0%)催化剂的XRD谱图。由图2可见,5种催化剂X射线衍射特征峰的角度与5种对应载体SiO2x⁃CeO2相比无明显变化。另外,无法观察到CuO的特征衍射峰,这可能是因为5种催化剂的Cu负载量较低,并且在催化剂体系中Cu的分散度较好所致[18]。

图2 不同SiO 2摩尔分数催化剂的XRD谱图Fig.2 XRD patterns of catalysts with different mole fractions of SiO2
2.2 BET分析
对所制备的载体及催化剂分别进行了物理吸附⁃脱附实验,并对比表面积、孔体积及孔径等参数进行测试和计算,结果见表3。

表3 不同SiO 2摩尔分数载体的比表面积、孔体积和孔径Table 3 Specific surface area,pore volume and pore diameter of different mole fractions of SiO 2
由表3可见,CeO2的比表面积为120.5 m2/g,载体SiO22.5%⁃CeO2的比表面积为145.9 m2/g,与CeO2相比,其比表面积增大25.4 m2/g。但是随着载体中SiO2摩尔分数增加,载体比表面积呈下降趋势。分析其原因可能是因为SiO2具有比CeO2更大的比表面积,向CeO2添加适量的SiO2形成新的载体体系,其比表面积由CeO2和SiO2共同组成,因此适量添加SiO2可有效增大SiO2⁃CeO2载体的比表面积。但是,随着SiO2摩尔分数的逐渐增加,在其形成过程中反应生成的SiO2占据了SiO2⁃CeO2载体部分孔道以及SiO2自身的团聚作用导致SiO2⁃CeO2载体的比表面积减小,SiO2摩尔分数越大,SiO2⁃CeO2载体的比表面积减小程度越明显,载体SiO215.0%⁃CeO2的比表面积仅为112.5 m2/g,与CeO2相比,比表面积减小8.0 m2/g。CeO2的孔体积为0.093 7 mL/g,添加SiO2后,4种SiO2⁃CeO2载体的孔体积略有增加(0.108 3~0.124 5 mL/g)。5种载体的孔径位于3.054 7~3.698 3 nm,鉴于载体制备过程中SiO2在CeO2表面生成过程较为复杂,因此载体孔径变化无明显规律。
图3为载体和催化剂的比表面积变化曲线。由图3可见,与对应载体的比表面积相比,负载5.0%的CuO后,5种催化剂的比表面积均大幅度减小。以载体CeO2和载体SiO22.5%⁃CeO2为例(如图3、表3-4所示),当负载5.0%的CuO后,催化剂CuO5.0%⁃CeO2和催化剂CuO5.0%⁃SiO22.5%⁃CeO2的比表面积分别为79.3、112.8 m2/g,与对应载体相比,比表面积分别降低41.2、33.1 m2/g。分析其原因如下:当CuO负载在载体上,部分CuO占据了载体的孔道,因此导致催化剂比表面积减小。

图3 载体和催化剂的比表面积变化曲线Fig.3 Diagram of specific surface area of support and catalyst
此外,5.0%CuO的负载量未能改变催化剂比表面积的变化规律,表4为不同SiO2摩尔分数催化剂的比表面积、孔体积和孔径。由表4可见,催化剂CuO5.0%⁃SiO2x⁃CeO2(x=2.5%、5.0%、7.5%、15.0%)的比表面积分别为112.8、102.3、100.8、97.7 m2/g,其下降趋势明显。
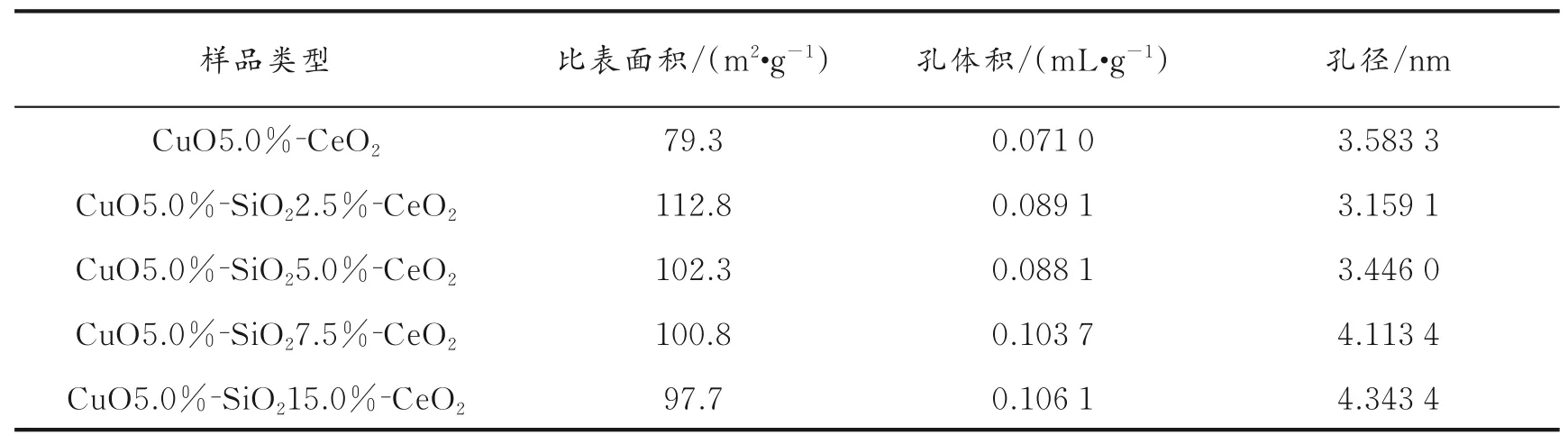
表4 不同SiO 2摩尔分数催化剂的比表面积、孔体积和孔径Table 4 Specific surface area,pore volume and pore size of catalysts with different mole fractions of SiO 2
经数据分析发现,载体SiO22.5%⁃CeO2的比表面积和催化剂CuO5.0%⁃SiO22.5%⁃CeO2的比表面积均为同体系最大比表面积,因此此类催化剂体系较佳SiO2摩尔分数为2.5%。
2.3 H 2⁃TPR分析
图4为5种催化剂的H2⁃TPR谱图。由图4可见,催化剂的表相铜与体相铜的还原温度位于130.0~190.0℃,远低于氧化铜的还原温度范围(300.0~480.0℃)。5种催化剂的表相铜特征峰分别位于155.3、147.4、158.8、144.0、149.7℃,体相铜特 征 峰 分 别 位 于173.3、171.3、178.9、168.6、177.8℃。当CuO加入后,Cu-Ce之间产生较强的相互作用的同时也促进了Cu-Cu之间的相互作用,因此5种催化剂表相铜与体相铜的H2⁃TPR还原特征峰的出峰温度均降低[18]。

图4 不同SiO 2摩尔分数催化剂的H 2⁃TPR谱图Fig.4 Catalysts with different mole fractions of SiO 2
3 催化性能评价
为进一步研究催化剂的甲醇水蒸气重整制氢性能,本文将所制备的5种催化剂用于该实验测试,结果见图5。由图5可见,5种催化剂转化率随着温度升高而升高,这是因为随着温度的升高化学反应速率加快。在260~320℃,体积空速为800 h-1时,催化剂CuO5.0%⁃SiO22.5%⁃CeO2和CuO5.0%⁃CeO2的综合催化性能较好,甲醇的转化率均超过70.0%。整个催化反应过程中的甲醇转化率均高于CuO5.0%⁃CeO2催化剂的甲醇转化率。
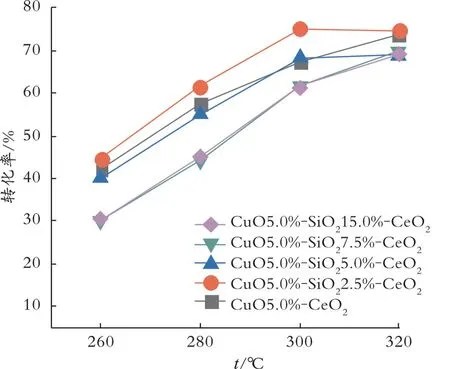
图5 催化活性与重整温度的关系Fig.5 Relationship between catalytic activity and reforming temperature。
基于前文催化剂比表面积比较可知,催化剂CuO5.0%⁃CeO2的比表面积仅为79.3 m2/g,远小于催化剂CuO5.0%⁃SiO22.5%⁃CeO2的比表面积112.8 m2/g(如表3所示)。因此催化剂CuO5.0%⁃CeO2的甲醇转化率在各个温度均低于催化剂CuO5.0%⁃SiO22.5%⁃CeO2的甲醇转化率。当SiO2摩尔分数超过5.0%后,由于过量SiO2产生的团聚现象,导致催化剂比表面积大幅度下降,因此其在实验过程中的甲醇转化率低于70.0%。当反应温度为300、320℃时,催化剂CuO5.0%⁃SiO22.5%⁃CeO2的甲醇转化率分别为75.1%和74.6%,随着温度的升高,甲醇转化率下降了0.5%。该现象产生的原因可能是在高温条件下催化剂表面出现精细结构烧结,孔道塌陷,从而使催化剂比表面积减小,进而降低了催化剂的催化活性。
4 结 论
通过水热合成法和浸渍法制备了系列CuO5.0%⁃SiO2x⁃CeO2(x=0、2.5%、5.0%、7.5%、15.0%)催化剂,探究SiO2的摩尔分数对催化剂比表面积及甲醇水蒸气重整制氢反应活性的影响。结果表明,少量添加SiO2可以增大Cu-Ce催化剂的比表面积,提高甲醇的转化率。其中CuO⁃5.0%SiO2⁃2.5%CeO2催化效果最好,该催化剂比表面积为112.8 m2/g,较CuO5.0%⁃CeO2催化剂的比表面积增加了23.5 m2/g;甲醇水蒸气重整制氢实验中,该催化剂的甲醇转化率为75.1%
