NaYF4:Yb,Tm@TiO2复合催化剂光催化降解盐酸四环素*
2022-04-11马永梅李思悦
饶 涵,马永梅,李思悦
(1. 中国科学院重庆绿色智能技术研究院,中国科学院水库水环境重点实验室,重庆 400714;2. 中国科学院大学,北京 100049;3. 武汉工程大学 环境生态与生物工程学院, 武汉430205)
0 引 言
盐酸四环素具有抑制或杀灭各种病原体或有害微生物的效用,是防治感染性疾病的重要药物,被广泛应用在医疗、畜牧业、水产养殖以及农业生产等领域[1]。但是大部分的抗生素不能被人体和动物完全消化吸收,其中80%以上的抗生素会以原形式随着粪便和尿液排出体外,造成土壤地下水和地表水等污染,进而威胁到人类的生命健康[2]。因此,高效去除水体中的盐酸四环素具有重要意义。
目前报道的比较常规处理该类废水的方法主要包括物理[3]、生物[4]和化学方法[5- 6]等。在这些处理方法中,光催化氧化技术作为一种无毒低成本的新型废水处理技术[7],在处理难降解废水污染物方面具有良好应用前景[8-10]。在光催化氧化技术中,纳米TiO2光催化材料因结构稳定,催化反应迅速以及反应产物无二次污染等优点得到广泛应用[11-14]。Li等人通过旋涂法合成TiO2薄膜光催化剂,并探究了该催化剂降解水中残留抗生素的活性与机理,取得了良好降解效果[15]。但是,由于TiO2吸收阈值为387 nm只能吸收紫外光,具有光谱响应范围窄的特点。而太阳光中,紫外光仅占5%,可见光占46%,红外光占49%。紫外光在太阳光中极低占有率严重限制了纯二氧化钛光催化剂在环境治理中的应用[16]。因此,设计并构筑一种既能扩展二氧化钛在可见光和近红外光的吸收,同时又可以保证二氧化钛光催化降解效率的复合材料具有重要的意义[17-19]。
上转换材料是有着特殊发光机制的一种材料,它可以将长波辐射转换为短波辐射,通过非线性的光学过程,实现了低能量的激发,而发射出高能量光谱[20]。上转换发光材料通常是由掺杂离子和基质材料组成的,掺杂离子又可分为激活剂和敏化剂[21]。六方晶相的稀土元素氟化物被认为是最理想的上转换发光材料的基质[22]。最常用的敏化剂是Yb3+[23],不同的激活剂离子可以发射出不同波长的激光。稀土铥掺杂的上转换材料可以将近红外光转换为紫外光,有望被二氧化钛吸收用于驱动光催化降解反应的发生,近红外光和紫外光的同时利用将会大大提高对太阳光的利用率[24-25]。
本文利用水热法合成NaYF4:Yb,Tm@TiO2复合催化剂,用X射线衍射仪(XRD)和扫描电子显微镜(SEM)等手段对合成的上转换材料以及复合催化剂的形貌结构进行表征。采用紫外-可见分光光度计监测的方法,研究氙灯模拟太阳光下,催化剂用量、TC浓度以及pH对TC降解的影响,优化复合催化剂NaYF4:Yb,Tm@TiO2光催化降解TC的操作条件,揭示复合催化剂降解TC的机理。
1 实 验
1.1 试剂与仪器
试剂:盐酸四环素(tetracycline, TC)、柠檬酸钠(C6H5Na3O7·2H2O)、钛酸四丁酯(C16H36O4Ti)、氟化钠(NaF)、无水乙醇购于上海国药试剂公司,氯化钇(YCl3)、氯化镱(YbCl3)、氯化铥(TmCl3)购于sigma试剂公司,所有试剂未做进一步处理。本实验用水均为二次水。
仪器:干燥箱(上海一恒,PH-050A);数控超声波清洗器(舒美,KQ5200DB);磁力搅拌器(上海梅颖浦,85-2);离心机(湖南湘仪,H1650-W);光化学反应仪(上海比朗,BL-GHX-V);冷却水循环装置(上海比朗,BILON-T-1000);紫外可见分光光度计(上海元析,UV-5500PC);pH计(德国WTW,D-82326);X射线衍射仪(荷兰帕纳科,X‘Pert3 Powder);扫描电子显微镜(SEM)(Hitachi日立,Hitachi TM3000);实验室超纯水机(重庆安特生,ATS19-1223-034);分析天平(上海梅特勒,ME54)。
1.2 催化剂制备
(1)上转换材料NaYF4:Yb,Tm的制备:用电子天平称取5.8 g柠檬酸钠置于干净的烧杯中,后加入25 mL的二次水,超声溶解。后称取0.38 g YCl3、0.19 g YbCl3、0.0076 g TmCl3加入上述溶液中,超声溶解,并磁力搅拌30 min。再称取1.26 g氟化钠溶于25 mL的二次水中,后将氟化钠的水溶液逐滴加入到上述混合溶液中,继续磁力搅拌10 min,后将混合溶液转入到60 mL的反应釜中,再将反应釜放到180 ℃的烘箱里加热12 h。后将产物离心分离,并用二次水洗涤3次,再放入60 ℃真空干燥箱内进行干燥。
(2)复合催化剂NaYF4:Yb,Tm@TiO2的制备:NaYF4:Yb,Tm@TiO2的制备是根据一种经典的方法进行的。称取0.05 g的NaYF4:Yb,Tm置于盛有10 mL乙醇的小烧杯中,超声分散,后向烧杯内加入100 μL钛酸四丁酯,搅拌分散,再将烧杯放入盛有5 mL二次水的反应釜内胆里,装入反应釜中,将反应釜置于180 ℃的烘箱中反应20 h。反应结束后用离心机将产物离心收集并用二次水洗涤,后将产物放在60 ℃真空干燥箱内干燥。
1.3 光催化降解实验
根据徐婷等人对磁性NiO复合材料光催化处理盐酸四环素废水的研究[26],先选择10-5mol/L的盐酸四环素确定催化剂的最佳浓度,即:5支试管分别加入60 mL浓度10-5mol/L的盐酸四环素,再分别加入0.33、0.5、0.67、0.83、1 g/L的催化剂,黑暗处静置2 h,让催化剂与盐酸四环素溶液充分作用达到吸附-脱附平衡。催化实验开始前,先取静置后的溶液3 mL作为0时刻的样品,后将试管置于氙灯下,每隔一定时间后取样3 mL离心分离,将离心后的上清液进行紫外表征。确定了催化剂的浓度后,再降解不同浓度的盐酸四环素,确定最佳的盐酸四环素浓度,如上操作。确定催化剂浓度和盐酸四环素浓度后,调节不同的pH值后,如上操作确定最佳的pH值。
1.4 活性物质捕获实验
为了确定促进TC降解的主要活性物种,光催化过程中,在TC水溶液中加入异丙醇(IPA, 1 mmol/L)、对苯醌(BQ, 1 mmol/L)和草酸铵(AO, 1 mmol/L)作为捕获剂分别捕获·OH、·O2-和空穴。
2 实验结果与讨论
2.1 上转换材料和复合催化剂的理化性质表征
图1(a)是制备得到的上转换材料扫描电镜图,通过图片观察到上转换材料形状为六棱柱形状,棱边长度约为300 nm,并且颗粒分散性非常好。图1(a)的插图是上转换材料荧光发光图,在980 nm光的激发光下,上转换材料NaYF4:Yb,Tm可转换发出349和362 nm左右的紫外光。这些转换后的紫外光将协同作用于TiO2的光催化降解行为。图1(b、c)是复合催化剂NaYF4:Yb,Tm@TiO2扫描电镜图,通过图片观察到整个复合催化剂形状仍然是六棱柱形,覆盖在上转换材料表面有着薄薄的二氧化钛壳层。根据之前的工作基础,选择100 μL钛酸四丁酯作为钛源合成TiO2壳层,得到的壳层厚度约为50~100 nm,且呈现疏松蜂窝状,可以保证内核吸光性能的同时又兼顾TiO2的光催化活性[27]。图1(d-f)是复合催化剂NaYF4:Yb,Tm@TiO2单个粒子的元素映射图,证明了Yb、Tm、Ti元素分散在整个粒子中。
图2是上转换材料NaYF4:Yb,Tm、复合催化剂NaYF4:Yb,Tm@TiO2的XRD谱图,图片下端部分红蓝指示线分别为六方晶相NaYF4和锐钛矿型TiO2标准峰。通过将上转换材料XRD光谱图与XRD标准峰JCPDS NO. 28-1192对比发现,合成的上转换材料对应于六方相结构的NaYF4:Yb,Tm晶面,六方相结构的上转换材料转换效率非常高[28]。分析复合催化剂XRD峰时发现,在合成的上转换材料NaYF4:Yb,Tm呈现出来衍射峰之余,有新衍射峰出现。通过将这些新出现衍射峰与XRD标准峰JCPDS NO. 21-1272对比得到,这些峰对应于锐钛矿型二氧化钛。利用XRD对合成的上转换材料和复合催化剂进行分析,证明复合催化剂NaYF4:Yb,Tm@TiO2成功合成。
2.2 盐酸四环素的光催化降解
2.2.1 复合光催化剂的光催化性能
为了检验上转换材料在光催化过程中的作用,设计了一系列科学合理的平行实验。复合催化剂的光催化性能分别通过氙灯滤去紫外波段(<420 nm)光照下(图3a,b)和氙灯下(图3c,d)对TC的光催化降解来评价。图3(a)是TC溶液的降解率Ct/C0随时间t变化的关系图,其中Ct表示对应的取样时间下测得的TC溶液浓度,这个浓度值可以由TC溶液在384 nm处的特征峰值对比TC标准液得到,而C0表示的是将TC溶液与催化剂达到吸附平衡后,在光催化降解前取样作为0时刻的TC溶液浓度。由图3(a)可知,在氙灯滤去紫外波段光照下,光照60 min后,无催化剂、TiO2、NaYF4:Yb,Tm@TiO2对TC溶液的光催化降解率分别为1%、20%、80%。

图1 合成的(a)上转换材料NaYF4:Yb,Tm (内插图是NaYF4:Yb,Tm的荧光发光图);(b-c)复合催化剂NaYF4:Yb,Tm@TiO2的SEM图 ;(d-f) 元素映射NaYF4:Yb,Tm@TiO2单粒子,包括Yb Mα, Tm Mα和Ti Kα1Fig 1 SEM images of the synthesized (a) up-conversion material NaYF4:Yb,Tm (inset in A: the corresponding emission spectrum of NaYF4:Yb,Tm); (b、c) composite catalyst NaYF4:Yb,Tm@TiO2; (d-f) element mapping of a single particle of NaYF4:Yb,Tm@TiO2 , including Yb Mα, Tm Mα and Ti Kα1

图2 NaYF4:Yb,Tm和NaYF4:Yb,Tm@TiO2的XRD图以及NaYF4 (JCPDS 28-1192)和锐钛矿相TiO2 (21 - 1272)的XRD标准峰Fig 2 XRD patterns of NaYF4:Yb, Tm and NaYF4:Yb, Tm@TiO2 and standard XRD patterns of NaYF4 (JCPDS 28-1192) and anatase phase TiO2 (21-1272)
图3(b)是将TC溶液降解率Ct/C0取对数后与时间t进行线性拟合,拟合的结果显示其降解动力学过程符合准一级动力学过程,如公式(1)所示[29]。
(1)
降解动力学采用拟一阶模型进行模拟,如公式(2)所示[30]。
(2)
这里At和A0是t和0时刻的吸光度,At/A0=Ct/C0,k为拟一阶速率常数,t为时间。根据公式(1)和公式(2)可以推算出氙灯滤去紫外光照射下无催化剂、TiO2、NaYF4:Yb,Tm@TiO2对TC溶液光催化降解的反应速率常数k分别为0、0.002、0.024。
图3(a)和(b)结果显示,没有催化剂时,TC的浓度基本无变化,表明了TC溶液光稳定性良好。TiO2和NaYF4:Yb,Tm@TiO2对TC降解结果揭示上转换材料可以将非紫外光转换为紫外光用于激发TiO2光催化降解TC。
图3(c)显示,氙灯光照60 min后,无催化剂、TiO2、NaYF4:Yb,Tm@TiO2对TC溶液的光催化降解率分别为6%、35%、99%。反应速率常数分别为0.001、0.004、0.095(3D).结果证明复合催化剂NaYF4:Yb,Tm@TiO2可协同利用紫外光和近红外光从而提高对TC的光催化降解效率。
2.2.2 催化剂浓度对光催化降解效率的影响
图4是氙灯照射下,不同浓度NaYF4:Yb,Tm@TiO2对TC溶液光催化降解的影响。图4(a)是氙灯照射下NaYF4:Yb,Tm@TiO2降解TC溶液在不同时间下的紫外可见光谱图。由图可知,TC溶液在384 nm处特征峰随着降解时间增长逐步下降,在60 min后几乎降解完。图4(b)是TC溶液的降解率Ct/C0随时间t变化的关系图。由图得,光照45 min后,催化剂浓度为0.33、0.50、0.67、0.83、1.00 g/L时对TC溶液的光催化降解率分别为88%、98%、98%、96%、93%。图4(c)是将TC溶液降解率Ct/C0取对数后与时间t进行线性拟合,拟合的结果显示其降解动力学过程符合准一级动力学过程。根据公式(1)和公式(2)可以推算出氙灯照射下不同浓度的NaYF4:Yb,Tm@TiO2对TC溶液光催化降解的反应速率常数k,在催化剂浓度分别为0.33、0.50、0.67、0.83、1.00 g/L时, TC溶液的降解速率分别为0.062、 0.077、0.106、0.075和0.055,如图4(d)所示。随着光催化剂浓度的增加,降解反应速率加快,在催化剂浓度为0.67 g/L时,降解反应速率达到最佳。之后随着催化剂浓度的持续增加,降解反应速率开始下降。光催化剂浓度增加使得溶液的浊度增加,降低光在溶液中的渗透力,抵消了光催化剂表面积的影响,从而造成光催化降解反应速率下降[31]。

图3 (a、b)各种催化剂在氙灯滤去紫外波段光照下对TC的降解率、反应速率拟合;(c、d)各种催化剂在氙灯下对TC的降解率、反应速率拟合Fig 3 (a、b) The calculated time-dependent ratios of Ct/C0, first-order degradation rates in the absence or presence of different photocatalysts under UV-filtered Xe lamp;(c、d) The calculated time-dependent ratios of Ct/C0, first-order degradation rates in the absence or presence of different photocatalysts under full-spectrum Xe lamp
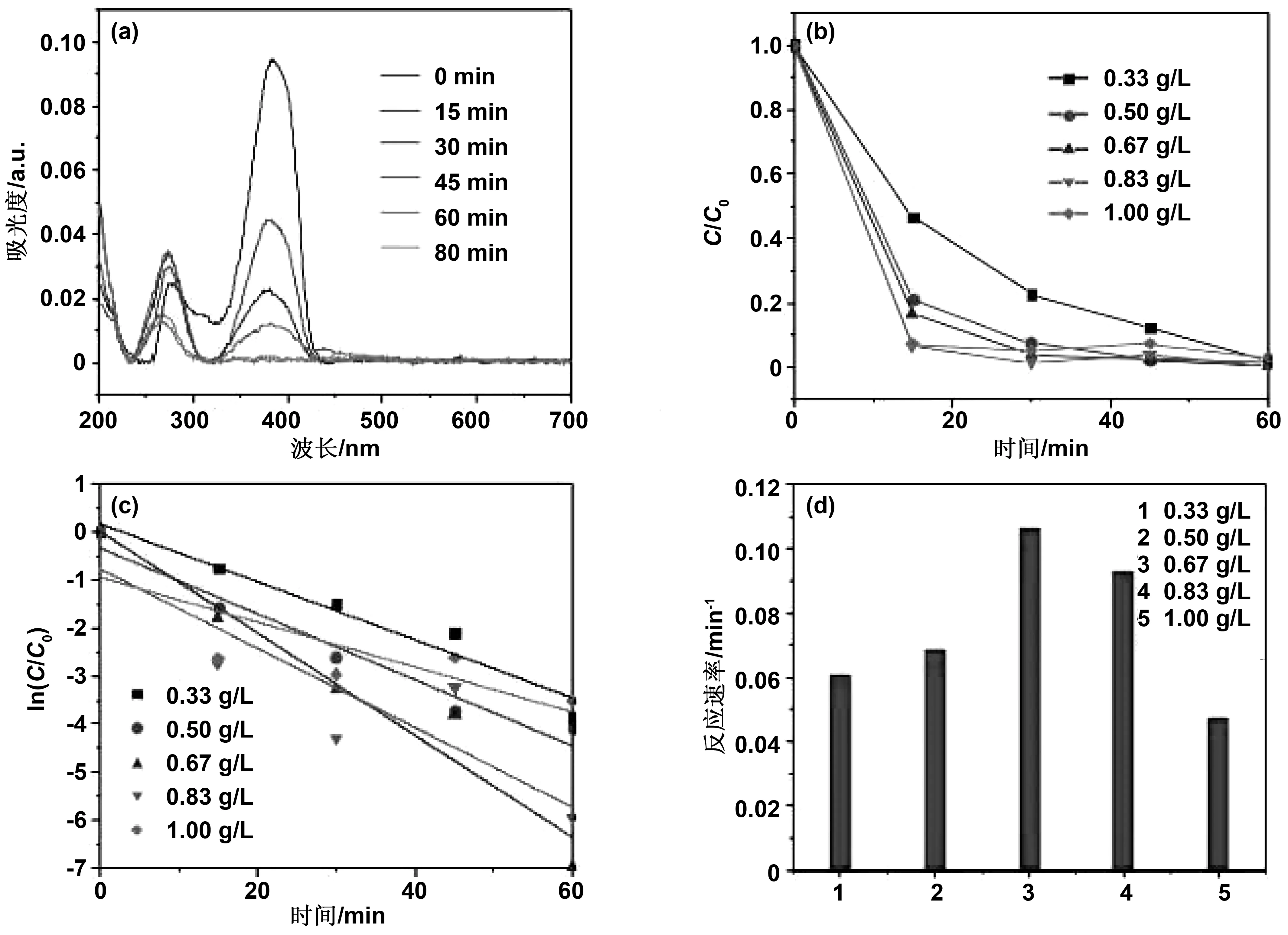
图4 (a)氙灯照射下NaYF4:Yb,Tm@TiO2光催化降解TC溶液时间分辨紫外-可见吸收光谱图;(b-d)氙灯照射下不同浓度的NaYF4:Yb,Tm@TiO2对TC溶液光催化降解率、反应速率拟合和反应速率常数Fig 4 (a) Time-course UV-Vis absorbance spectra of TC photocatalyzed by NaYF4:Yb,Tm@TiO2 under Xe lamp;(b-d) The calculated time-dependent ratios of Ct/C0, first-order degradation rates, and reaction rate constants of TC solution photocatalyzed by different concentrations of NaYF4:Yb,Tm@TiO2 under xenon lamp
2.2.3 盐酸四环素浓度对光催化效率的影响
图5是在氙灯照射下,NaYF4:Yb,Tm@TiO2浓度为0.67 g/L的基础上,进一步考察TC浓度对光催化降解效率的影响。图5(a)是氙灯照射0.67 g/L NaYF4:Yb,Tm@TiO2降解TC溶液在不同时间下的紫外可见光谱图。由图可知,TC溶液在384 nm处特征峰随着降解时间增长逐步下降,在45 min后几乎降解完。图5(b)是TC溶液的降解率Ct/C0随时间t变化的关系图。由图得,在照射时间为60 min时,浓度为5×10-6、10-5、2.5×10-5、5×10-5、10-4mol/L的TC溶液光催化降解率分别为82%、99%、98%、62%、23%。图5(c)是将TC溶液降解率Ct/C0取对数后与时间t进行线性拟合,拟合的结果显示其降解动力学过程符合准一级动力学过程。根据公式(1)和公式(2)可以推算出氙灯照射0.67 g/L的NaYF4:Yb,Tm@TiO2对不同浓度TC溶液光催化降解的反应速率常数k,在TC浓度分别为5×10-6、10-5、2.5×10-5、5×10-5、10-4mol/L时,TC溶液的降解速率分别为0.028、0.106、0.065、0.016和0.005,如图5(d)所示。结果显示,在TC浓度为10-5mol/L时,降解反应速率最快。在一定范围内,随着污染物浓度的降低,反应速率常数会增大。然而,当污染物浓度过低时,较少的量会到达光催化剂表面,使得光催化剂的降解性能不显著[32]。

图5 (a)氙灯照射下0.67 g/L NaYF4:Yb,Tm@TiO2光催化降解TC溶液时间分辨紫外-可见吸收光谱图;(b-d)氙灯照射下0.67 g/L的NaYF4:Yb,Tm@TiO2对不同浓度TC溶液光催化降解率、反应速率拟合和反应速率常数Fig 5 (a) Time-course UV-vis absorbance spectra of TC photocatalyzed by 0.67 g/L NaYF4:Yb,Tm@TiO2 under Xe lamp;(b-d) The calculated time-dependent ratios of Ct/C0, first-order degradation rates, and reaction rate constant for different concentration of TC solution were photocatalyzed by 0.67 g/L NaYF4:Yb,Tm@TiO2 under xenon lamp
2.2.4 溶液的pH对光催化效率的影响
TC在不同pH条件下表面带有不同的基团[33],因此溶液的初始pH值是光催化降解过程中的重要参数,影响着光催化剂对TC的去除效率。图6显示了溶液的pH对NaYF4:Yb,Tm@TiO2光催化降解TC溶液的实际影响。图6(a)是氙灯照射0.67 g/L NaYF4:Yb,Tm@TiO2降解10-5mol/L TC溶液在不同时间下的紫外可见光谱图。由图可知,TC溶液在384 nm处特征峰随着降解时间增长逐步下降,在45 min后几乎降解完。
图6(b)是TC溶液的降解率Ct/C0随时间t变化的关系图。由图得,光照45 min后,溶液起始pH为4、6、8、10时,分别有77%、99%、98%、92%的TC溶液被降解掉。图6(c)是将TC溶液降解率Ct/C0取对数后与时间t进行线性拟合,拟合的结果显示其降解动力学过程符合准一级动力学过程。根据公式(1)和公式(2)可以推算出氙灯光照下复合催化剂在不同pH条件下降解TC溶液的反应速率常数k。当pH分别为4、6、8、10时,TC溶液的降解速率常数分别为0.033、0.105、0.083和0.055,如图6(d)所示。结果显示,pH为6时,降解反应速率最快。当溶液pH < 4时,TC表面因存在TCH3+而带正电;在溶液pH为4~6的范围内,TC表面为中性不带电荷,此时TC很容易到达催化剂的表面,使得光催化降解效率在这一范围内随着pH增加而增加,并在pH为6时达到最佳;碱性条件下,TC表面因为TCH-、TC2-的存在而带有负电荷。因此,pH过低或者碱性条件下存在静电斥力使得TC不能很好地到达催化剂表面,从而影响复合光催化剂NaYF4:Yb,Tm@TiO2对TC的降解效率[33]。

图6 (a)氙灯照射下0.67 g/L NaYF4:Yb,Tm@TiO2光催化降解TC溶液(10-5 mol/L)时间分辨紫外-可见吸收光谱图;(b-d)氙灯照射且不同pH下,0.67 g/L的NaYF4:Yb,Tm@TiO2对TC溶液(10-5 mol/L)光催化降解率、反应速率拟合和反应速率常数Fig 6 (a) Time-course UV-vis absorbance spectra of TC(10-5 mol/L) photocatalyzed by 0.67 g/L NaYF4:Yb,Tm@TiO2 under Xe lamp;(b-d) The calculated time-dependent ratios of Ct/C0, first-order degradation rates and reaction rate constants for TC (10-5 mol/L) photocatalyzed 0.67 g/L NaYF4:Yb,Tm@TiO2 with different pH values under xenon lamp
2.3 NaYF4:Yb,Tm@TiO2降解盐酸四环素的机理
图7是活性物质捕获实验,为了找出NaYF4:Yb,Tm@TiO2复合材料光催化降解TC的主要活性物质。分别选用草酸铵(AO)、对苯醌(BQ)和异丙醇(IPA)作为空穴、·O2-和·OH的捕获剂[34]。如图所示,加入捕获剂后,IPA对光催化效率抑制作用较弱,然而AO和BQ的添加显著降低了降解率。结果表明,制备的NaYF4:Yb,Tm@TiO2样品对TC的光催化降解过程中,·O2-、空穴所起的作用要远远大于·OH。

图7 不同捕获剂对NaYF4:Yb,Tm@TiO2光催化降解TC的影响Fig 7 Effects of different scavengers on the TC photocatalyzed by NaYF4:Yb,Tm@TiO2
基于上述结果和讨论,提出了NaYF4:Yb,Tm@TiO2复合材料在可见光照射下降解TC的可能机理。如图8所示,在氙灯照射下,上转换材料中作为敏化剂的Yb离子会吸收能量,并将能量传递给扮作发光中心的激活剂Tm离子。Tm离子吸收能量后被激活并发生连续的电子跃迁,由激发态向低能级跃迁得到所需要的紫外光[35]。上转换材料转换后的紫外光协同原有的紫外光一起照射在TiO2表面时,其价带电子就会获得能量跃迁至导带上,形成光生电子,价带上相应地生成光生空穴,部分空穴会向NaYF4:Yb,Tm@TiO2复合材料表面移动,直接降解TC。同时,光生电子被水中溶解氧捕获形成·O2-,·O2-能有效降解TC[36]。

图8 NaYF4:Yb,Tm@TiO2在氙灯照射下光催化反应机理图Fig 8 NaYF4:Yb,Tm@TiO2 under Xe lamp irradiation
3 结 论
采用水热法合成NaYF4:Yb,Tm@TiO2复合催化剂,在扫描电镜图中呈现出光转化率较高的六棱柱形的形貌结构,棱边长约为300 nm,该复合催化剂在太阳光照射下对TC有较好的降解效果。太阳光条件下,复合催化剂中的上转换材料将太阳光中的近红外光转换为紫外光,在催化剂浓度为0.67 g/L、TC溶液浓度为10-5mol/L、pH=6时,光催化降解效率最佳,降解速率常数为0.105。复合催化剂可协同利用近红外光和紫外光,实现对抗生素的高效降解。
