高效液相色谱法测定牛奶中3种防腐剂
2022-04-11马晓年陈俊秀农蕊瑜李文廷蒋梦
马晓年,陈俊秀,农蕊瑜,李文廷,蒋梦
(1.昆明市疾病预防控制中心,昆明 650228;2.昆明医科大学,昆明 650500)
0 引言
牛奶能为人体提供多种营养物质[1],在日常生活中不可或缺。食品防腐剂具有良好的杀菌作用[2],能延长食品保质期,被广泛应用于食品加工中。
少量的食品添加剂对人体没有影响,过量则会对人体健康造成损害[3]。国标对于食品防腐剂的添加做出了明确规定[4],苯甲酸、山梨酸、脱氢乙酸不能添加到牛奶中。目前,国内的研究中检测3种防腐剂的方法主要有:气相色谱法[5-7]、液相色谱法[8-10、13-14]、薄层色谱法[11],但能同时快速检测3种防腐剂的方法较少。本文对实验条件进行研究改进,建立了高效液相色谱法同时测定牛奶中3种防腐剂。结果表明,该法快速、准确、简便,适合于日常检验。
1 材料与方法
1.1 仪器与试剂
Thermo U3000高效液相色谱仪(配二极管阵列检测器),美国赛默飞;高速冷冻离心机,湖南 赫西仪器;电子天平(0.01 mg),Sartorius。
牛奶,市购;苯甲酸(坛墨质检-标准物质中心);山梨酸、脱氢乙酸,坛墨质检-标准物质中心;甲醇(色谱纯),美国JT Baker;乙腈(色谱纯)、磷酸二氢钾(分析纯)、乙酸胺(分析纯),国药集团化学试剂有限公司;乙酸(分析纯),北京化工厂。
1.2 方法
1.2.1 标准溶液配制
准确量取苯甲酸、山梨酸和脱氢乙酸标准溶液各1 mL,用纯水定容至10 mL,得到苯甲酸、山梨酸和脱氢乙酸均为100μg/mL的混合标准应用液。混合标准应用液保存于4℃冰箱内备用。
1.2.2 样品前处理
0.2 %乙酸沉淀法:准确称取2 g样品于50 mL离心管中,加入10 mL体积分数为0.2%乙酸水溶液,涡旋2 min,于转速4 000 r/min离心1 min,留取上清液,残渣重复上述操作两次,合并水相,并用体积分数0.2%乙酸溶液定容至30 mL,混匀。取适量上清液过0.22μm滤膜,待液相色谱测定。
1.2.3 色谱条件
色谱柱:Agilent Eclipse C18(250 mm×4.6 mm,5μm);流动相A为浓度0.02 mol/L乙的酸铵溶液,流动相B为乙腈,梯度洗脱;流速为1.0 mL/min;检测波长为230 nm;进样量为10μL;柱温为室温。洗脱条件如表1所示。
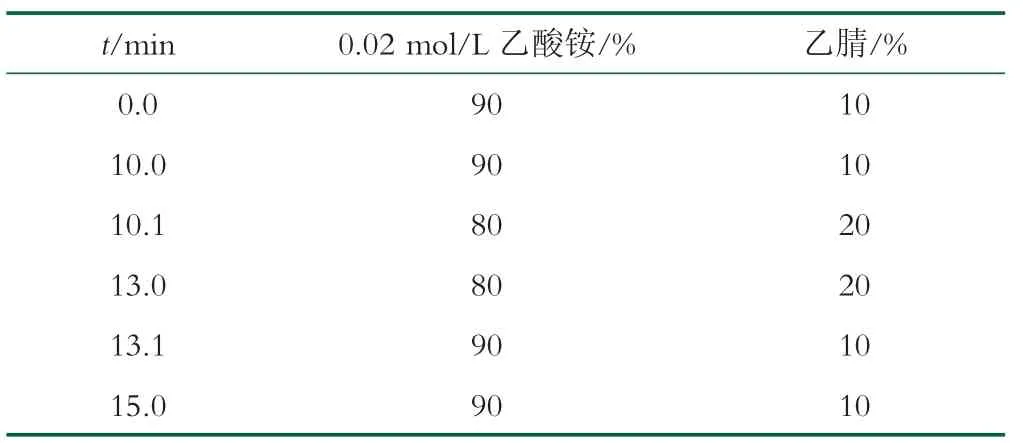
表1 流动相梯度洗脱
2 结果与分析
2.1 色谱条件的优化
2.1.1 检测波长的选择
在200~300 nm范围内对分析物进行紫外波长扫描,结果发现,在流动相中3个组分的最大吸收波长分别是苯甲酸230 nm、山梨酸254 nm、脱氢乙酸230 nm。为兼顾各组分的灵敏度和吸收峰值,在实验中对比254 nm和230 nm波长处取得的混合组分色谱图,根据各组分紫外吸收情况,确定在230 nm波长处检测苯甲酸、山梨酸、脱氢乙酸均取得更高响应如见图1所示,故选用230 nm作为本实验的检测波长。
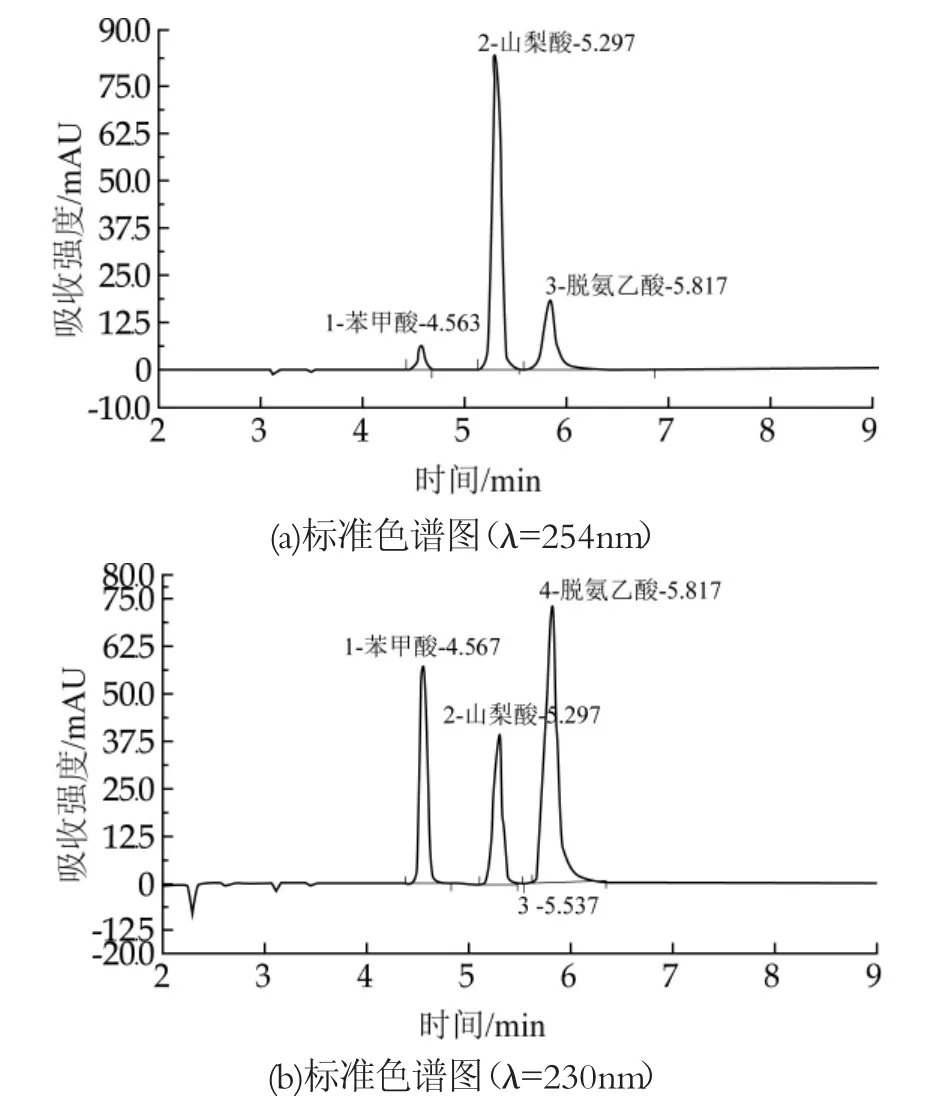
图1 不同检测波长下3种物质的标准色谱
2.1.2 流动相的选择
本文实验了甲醇-乙酸铵、乙腈-乙酸铵、乙腈-磷酸二氢钾,并调整有机相及水相比例以得到最佳的分离效果。实验表明,磷酸二氢钾作为水相时,在不改变pH的情况下,苯甲酸和山梨酸无法实现基线分离,改变流动相比例改善效果也并不显著;乙酸铵作为水相则可较好的分离3种防腐剂,甲醇作为有机相,3种防腐剂均可实现基线分离,分析时间约为15 min;乙腈作为有机相,3种防腐剂均实现基线分离且峰型收窄,响应增大,分析时间在7 min内如见图2所示。综上所述,本文选择乙腈-乙酸铵作为流动相进行后续分析工作。
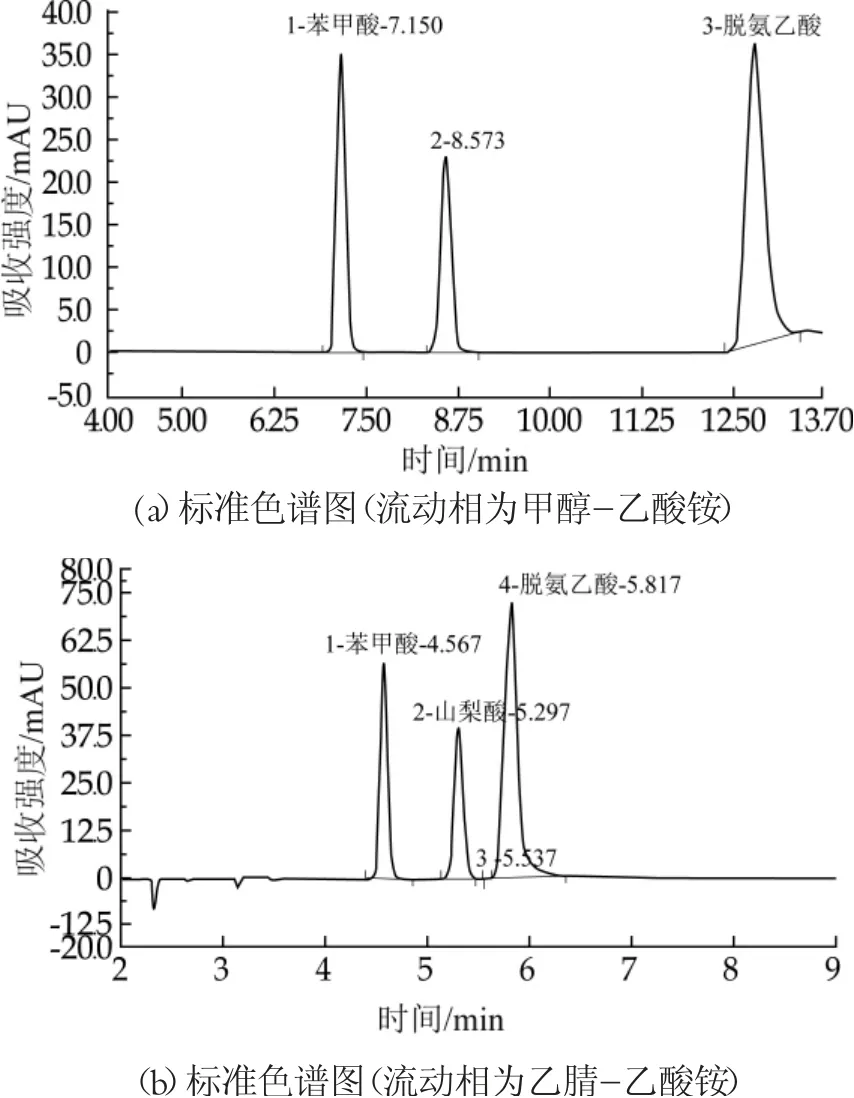
图2 不同流动相下3种物质的标准色谱图
2.2 样品前处理方法的确定
牛奶样品中的蛋白质会干扰测定结果,故需除去蛋白质。目前除蛋白有沉淀法和萃取法两大类[15]。实验主要考察了沉淀法中的GB 5009.28-2016[12]无机试剂乙酸锌-亚铁氰化钾沉淀蛋白及有机试剂沉淀蛋白。
本文对苯甲酸、山梨酸、脱氢乙酸进行加标6次重复平行实验,对比3种方法的加标回收率和相对偏差值,结果如表2所示。实验发现,国标方法过程较为繁琐,苯甲酸的回收率在82.6%~116.2%,虽达到方法验证学的要求,但RSD大于10%,实验重复性不佳;山梨酸的回收率较低,在60.6%~70.0%;脱氢乙酸的回收率则完全达不到方法学要求。
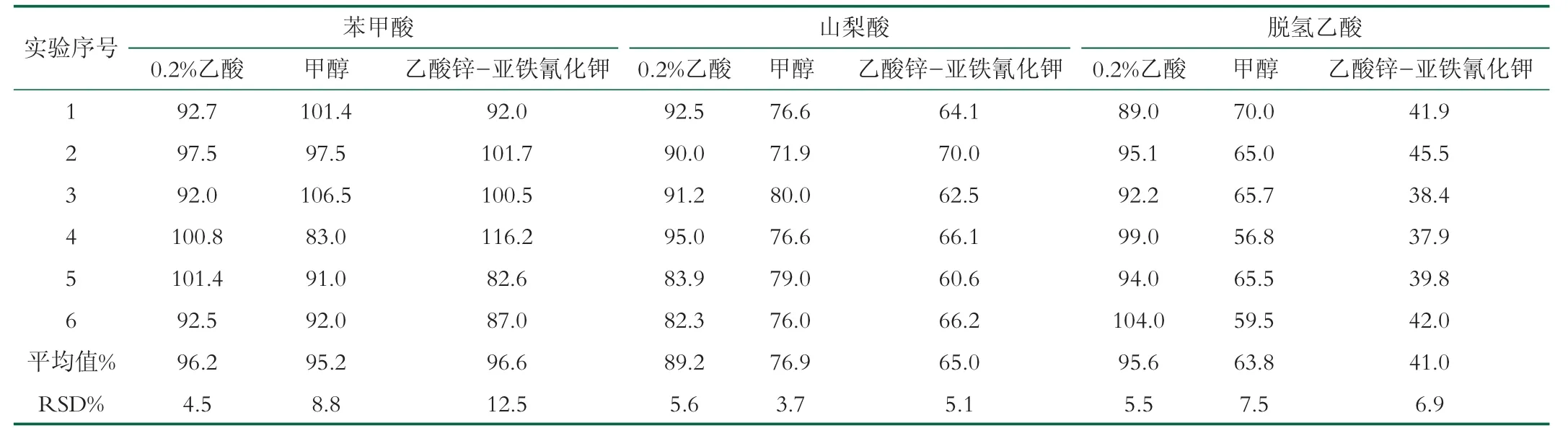
表2 不同前处理方法样品的平均加标回收率
本文试验了甲醇及乙酸两种有机溶剂沉淀蛋白。采用甲醇沉淀蛋白质对苯甲酸、山梨酸的回收率基本达到要求,但实验中存在沉淀不完全的现象,且脱氢乙酸的回收率低至56.8%~70%。乙酸对水的亲和力较大,能破坏蛋白质颗粒的水化膜,在等电点时使蛋白质沉淀,故体积分数为0.2%乙酸沉淀法能克服实验过程繁琐、沉淀不完全两个缺点,取得理想效果,对3种组分的回收率在82.3%~104.0%,RSD在4.5%~5.6%。综合考 虑,因而选择体积分数0.2%乙酸作为蛋白质沉淀剂。
2.3 样品提取次数的选择
试验按样品前处理的步骤,对比了体积分数为0.2%乙酸分别对加标样品进行1次和3次提取,最后用体积分数为0.2%乙酸定容至30 mL,每个加标水平重复4次,得出样品的平均加标回收率和RSD值,实验结果如表3所示。
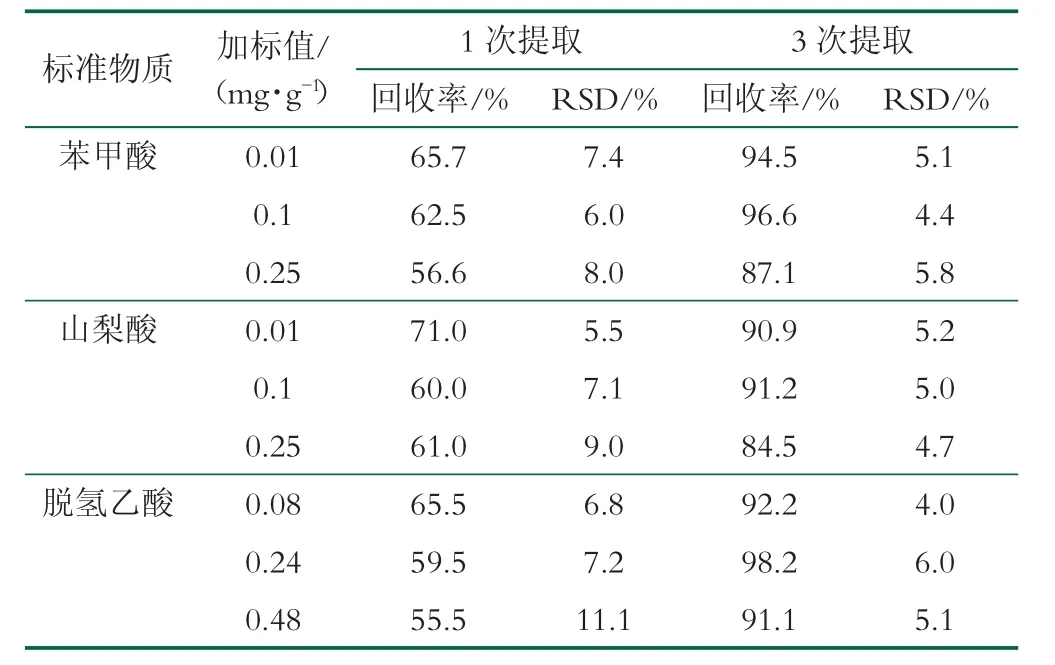
表3 不同提取次数的样品加标回收率
从表中可以看出,采用3次提取各组分的加标回收率均优于1次提取,且3次提取的RSD值小于1次提取,重复性较好。为确保实验准确性,实验再次使用体积分数为0.2%乙酸进行4次提取,发现其平均回收率在88.4%~95.1%,和3次提取结果无显著性差异,因而提取次数选择3次。
2.4 标准曲线及检出限
用纯水将混合标准应用液配制成含苯甲酸质量浓度分别为1.56,12.5,25.0,50.0,100.0μg/mL;含山梨酸质 量 浓 度 分 别 为0.78,6.25,12.5,25.0,50.0μg/mL;含脱氢乙酸质量浓度分别为3.12,6.25,12.5,25.0,50.0μg/mL的标准工作溶液;在确定的分析条件下进行测定,采用外标法以峰面积计算定量,以质量浓度为横坐标,以峰面积为纵坐标绘制标准曲线,得到的线性方程、相关系数、检出限及定量限如表4所示。
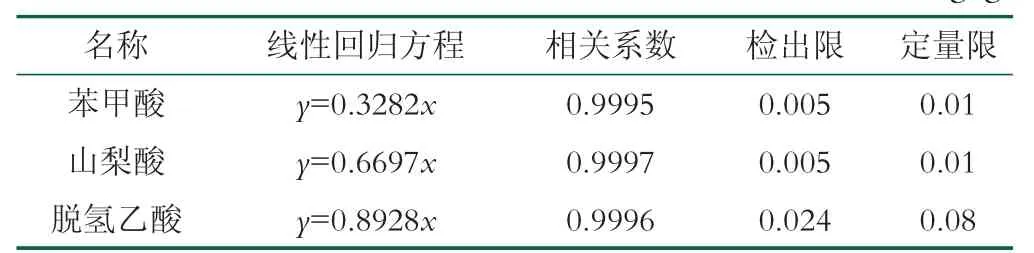
表4 3种组分的线性方程、相关系数、检出限及定量限mg/g
2.5 回收率和精密度实验
取不含苯甲酸、山梨酸、脱氢乙酸的牛奶样品,加入高中低3个浓度梯度的防腐剂混标,加标浓度分别见表5,分别测定6次,计算其平均回收率和精密度。苯甲酸平均回收率在86.7%~101.0%,RSD在3.6%~5.7%;山梨酸平均回收率在83.4%~91.9%,RSD在4.4%~6.0%;脱氢乙酸平均回收率在90.1%~97.2%,RSD在3.9%~5.1%。图3为牛奶样品加入3种混标的色谱图,由图可见,3种组分与杂质峰完全分离,无干扰,可准确定性、定量检测。
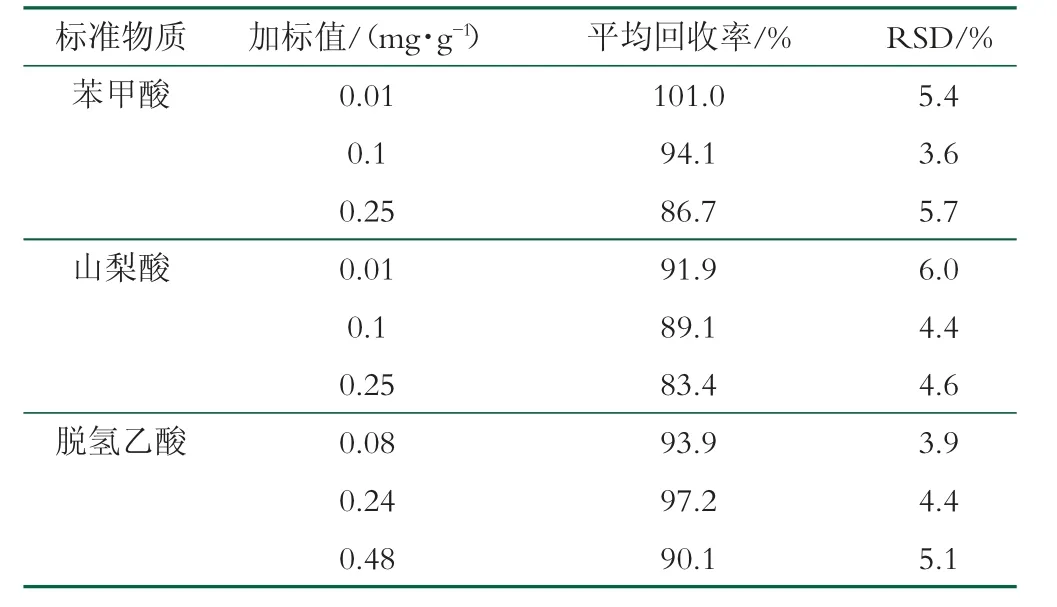
表5 样品加标回收率结果
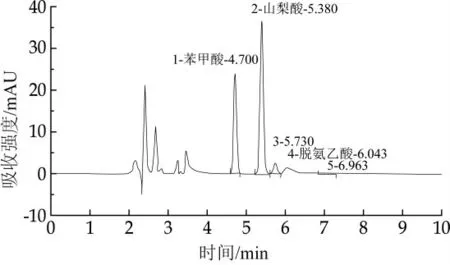
图3 加标样品色谱图
3 结论
在本方法的条件下,3种防腐剂与牛奶中其他干扰杂质峰完全分离,在10 min内可快速检测出,且定量准确。可以节约检测成本并提高检测效率,适合牛奶中苯甲酸、山梨酸、脱氢乙酸的日常监控测定。
