乙二醛-尿素树脂改性花生蛋白胶黏剂的制备
2022-04-06王晨曦安丽平
王晨曦,安丽平,高 敏
(内蒙古农业大学 理学院,呼和浩特 010018)
随着我国经济的快速发展,木材行业取得稳步提升。其中以木质单元与胶黏剂制备的人造板已成为人居环境中家具地板、室内装修装饰的主要原材料,刺激着我国木材胶黏剂需求量日益增大[1]。至2019年底,我国胶黏剂行业产量达到约881.9万t,同比增长5.21%。到2025年胶黏剂产量及需求量均将增长至1 350 t左右。目前,我国人造板用胶黏剂主要为三醛胶(脲醛、酚醛和三聚氰胺甲醛树脂胶),其产量占胶黏剂总产量的40%左右[2]。然而三醛胶类胶黏剂不具有生物可降解性和可再生性,且在制造和使用过程中释放出的游离甲醛和苯酚不仅对环境造成污染,还对人体健康存在威胁[3-4]。
以植物蛋白为主流的生物质胶黏剂,因其可再生性、低生态影响、可降解等独特特性而越来越受到人们的关注[5]。其中最热门的为大豆蛋白,目前对于大豆蛋白胶黏剂的研究已相对成熟,一部分产品已投入实际生产中[6]。为了进一步扩大蛋白质的资源,同时缓解生物质胶黏剂对大豆市场的过分依赖,有必要探索其他植物蛋白的开发利用。我国是花生生产大国,花生主要被用来榨油,而对高蛋白含量的花生粕主要用作饲料[7],缺少深度的开发和利用。与大豆蛋白相比,花生蛋白中约87%为球蛋白,主要为花生14S和7.8S球蛋白组成[8],这与大豆蛋白中产生黏结力的11S球蛋白和7S球蛋白类似[9]。但是花生蛋白胶黏剂与大豆蛋白胶黏剂都存在着耐水性差的问题,人们曾通过使用氢氧化钠[10]、SDS[11]和尿素[12]等打开植物蛋白的部分结构,使得疏水基团得以暴露,有助于其与其他化合物反应,如加入乙二醇二缩水甘油醚,有效提高了胶黏剂的耐水性能[13]。
为了探究更多提高花生蛋白胶黏剂耐水性的方法,本文采用氢氧化钠对花生蛋白进行降解处理,使花生蛋白的活性基团暴露出来,再利用价格低廉的尿素和无毒且挥发性小的乙二醛(半数致死量(大鼠)≥2 960 mg/kg;半数致死量(小鼠)≥1 280 mg/kg)[14]合成树脂作为改性剂对其进行改性。因合成树脂中的羟甲基与花生蛋白的活性基团发生化学反应,形成致密的交联网络,使改性后的胶黏剂性能提高。
1 材料与方法
1.1 实验材料
花生蛋白粉,浙江多味生物科技有限公司;氢氧化钠,天津市风船化学试剂科技有限公司;尿素,福晨(天津)化学试剂有限公司;乙二醛(质量分数40%),天津市大茂化学试剂厂;蒸馏水,实验室自制;实验药品除花生蛋白粉外均为分析纯。
DF-101S集热式恒温加热磁力搅拌器,巩义市予华仪器有限责任公司;JY2001电子天平,上海浦春计量仪器有限公司;STARTER2100 pH计,奥豪斯仪器(上海)有限公司;101A-3B烘箱,北京普析通用仪器有限公司;SCIENTZ-12N冷冻干燥机;Spectrum65傅里叶变换红外光谱仪,铂金埃尔默股份有限公司;S-3400扫描电子显微镜,日立公司;ZCMW-W5KN微机控制电子万能试验机,济南中创工业测试系统有限公司;NDJ-5涂-4涂料黏度计,上海越平科学仪器有限公司;XLB-350*350平板硫化机,青岛光越橡胶机械制造有限公司;DSC-4000 DSC测试仪,美国Perkin Elmer公司。
1.2 实验方法
1.2.1 改性剂的制备
将一定量的乙二醛加入三颈烧瓶中,用2 mol/L的氢氧化钠溶液调节pH至5~6,然后加入尿素总质量的2/3,升温至一定温度,反应2 h后将pH调节至中性,再加入剩余尿素反应一定时间后,冷却至40℃以下[15]得乙二醛-尿素(GU)树脂改性剂,并进行红外光谱、固体含量、储存期及黏度的测试。
1.2.2 改性花生蛋白胶黏剂的制备
室温下,向配有搅拌子的三颈烧瓶中加入200 mL蒸馏水和一定量的花生蛋白粉,搅拌20 min,待其均匀溶解后,用2 mol/L氢氧化钠溶液调节pH为10~11进行碱处理30 min,得碱处理花生蛋白,加入一定量改性剂磁力搅拌一定时间,得改性花生蛋白胶黏剂,以湿态胶合强度为指标,优化制备条件。
1.2.3 胶合板的制备
采用胶黏剂对杨木单板实行双面施胶,施胶量为5~10 g,开放陈化10 min后放入平板硫化机,在热压温度140℃、热压压力1.2~1.5 MPa、热压时间15 min的条件下进行热压。热压后的胶合板在室温环境下放置24 h,然后参照GB/T 17657—2013《人造板及饰面人造板理化性能试验方法》中Ⅱ类胶合板要求锯制试件(100 mm×25 mm)[16]。
1.2.4 胶合强度测试
干态胶合强度:将室温放置24 h后的试件按照GB/T 17657—2013直接进行检测。
湿态胶合强度:将试件放入(63±3)℃的热水中浸泡3 h,取出,室温冷却10 min,在万能试验机上检测胶合强度,拉伸速率为10 mm/min。
取5个平行样测试的算术平均值作为实验结果。
1.2.5 固体含量测试
按照GB/T 2793—1995要求,取样(1.0±0.5)g于干燥清洁铝盒中,在(105±2)℃烘箱中烘干(180±5)min,取出,称重。以加热后试样质量与加热前试样质量的比值表示固体含量。每种样品重复5次,取算术平均值作为实验结果。
1.2.6 黏度测试
按照GB/T 2794—1995要求,将50 mL黏度杯垂直固定在支架上,流出孔距离量筒底面20 cm,并在黏度杯流出孔下面放1只50 mL量筒。用手堵住流出孔,将试样倒满黏度杯,记录手指移开流出孔至接收的量筒中试样达到50 mL时的时间,以流出时间作为试样黏度,每个试样重复两次,取算术平均值作为实验结果。
1.2.7 储存期测试
按照GB/T 7123.2—2002要求,测量样品储存前后黏度的变化,结果以胶黏剂仍能保持其操作性能和规定强度的最长存放时间为储存期。
1.2.8 DSC测试
称取5~10 mg样品于铝坩埚中加盖测试DSC曲线,升温速率为10℃/min,温度范围为30~240℃[17]。
1.2.9 红外光谱测试
称取2 g样品于培养皿中,放入140℃烘箱烘干至恒重,冷却,研磨至粉末状,参照文献[17]进行红外光谱测试。
2 结果与分析
2.1 改性剂合成工艺的单因素实验优化
按1.2.1方法,分别在不同的乙二醛与尿素摩尔比、反应温度和总反应时间下合成乙二醛-尿素(GU)树脂改性剂,测定不同条件下改性剂的固体含量、黏度、储存期,结果见表1。

表1 不同合成条件下改性剂的固体含量、黏度、储存期
由表1可以看出:在反应温度80℃、总反应时间3 h条件下,随着乙二醛与尿素摩尔比的升高,改性剂的固体含量逐渐降低;黏度先增加后减小,在乙二醛与尿素摩尔比1.4∶1时达到最大;而储存期先增加,在乙二醛与尿素摩尔比为1.4∶1后,均超过30 d。当乙二醛与尿素摩尔比较大时,乙二醛与游离的羟基发生了羟醛缩合反应,阻碍了产物的生成,致使黏度下降[18]。综合考虑,选择乙二醛与尿素摩尔比为1.4∶1。
由表1可以看出,在乙二醛与尿素摩尔比1.4∶1、总反应时间3 h条件下,随反应温度的升高,改性剂的黏度和固体含量呈现递增趋势,而储存期在75℃以下小于10 d,75℃以上时大于30 d。考虑到固定时间内,温度低会影响尿素与乙二醛的反应,致使二者反应不彻底,而温度过高,乙二醛挥发快,会出现冻胶现象[19],因此选择最佳反应温度为80℃。
由表1可以看出,在乙二醛与尿素摩尔比1.4∶1、反应温度80℃条件下,随总反应时间的延长,改性剂的固体含量和黏度呈增大趋势,3.5 h后变化不明显,储存期在总反应时间超过2 h后均大于30 d,为了保证反应能够得以完全且保证黏度,选择反应时间为3.5 h。
综合单因素实验的结果,得到改性剂合成优化条件为:乙二醛与尿素摩尔比1.4∶1,反应温度80℃,总反应时间3.5 h。
2.2 改性剂红外光谱图
对优化合成条件下制备的GU树脂改性剂进行红外光谱扫描,结果见图1。

图1 改性剂的红外光谱图

2.3 改性花生蛋白胶黏剂制备的正交实验
在前期单因素实验基础上,以碱处理pH、反应时间、改性剂与碱处理花生蛋白质量比和花生蛋白粉质量为考察因素,湿态胶合强度为考察指标进行正交实验,正交实验因素水平见表2,正交实验设计及结果见表3。
由表3可知,4个因素对胶合板湿态胶合强度的影响大小依次为改性剂与碱处理花生蛋白质量比>碱处理pH >反应时间>花生蛋白粉质量。最佳因素水平组合为A3B4C3D4,即碱处理pH 10.4、反应时间3 h、改性剂与碱处理花生蛋白质量比16∶84、花生蛋白粉质量70 g。
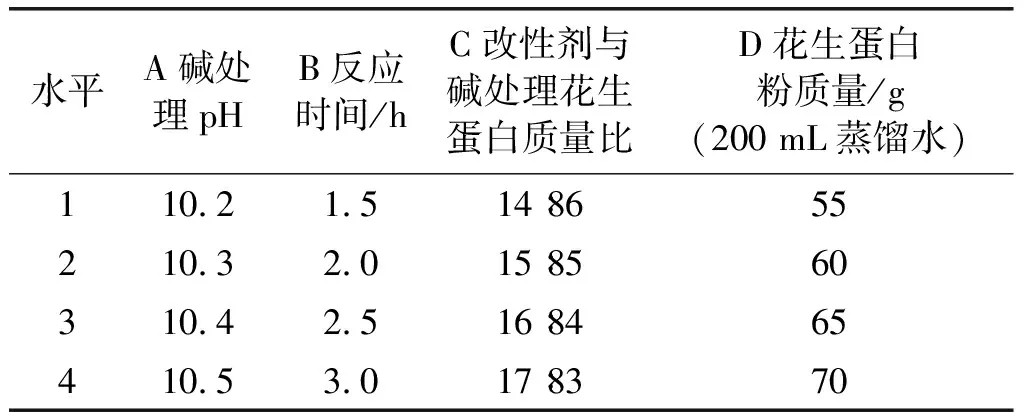
表2 正交实验因素水平

表3 正交实验设计及结果
2.4 胶黏剂性能测试结果
采用上述优化的条件制备改性花生蛋白胶黏剂,同时在相同的碱处理pH和花生蛋白粉质量条件下按1.2.2制备碱处理花生蛋白胶黏剂,对二者的性能指标进行测定。
2.4.1 固体含量及储存期(见表4)

表4 花生蛋白胶黏剂改性前后固体含量及储存期
固体含量高的胶黏剂会导致黏度过大,流动性变低,施胶困难,在热压过程中出现溢胶现象,不利于胶黏剂渗入木材内部,从而影响形成胶钉作用,且导致活性期短,影响胶合强度的改善[21]。由表4可看出,改性花生蛋白胶黏剂与碱处理花生蛋白胶黏剂相比,固体含量较低,且储存期延长。
2.4.2 胶合强度(见表5)

表5 改性前后花生蛋白胶黏剂及改性剂的胶合强度
由表5可看出,改性花生蛋白胶黏剂干、湿态胶合强度明显大于相同制备工艺条件下的碱处理花生蛋白胶黏剂和改性剂本身的,均大于GB/T 9846—2004中对Ⅱ类胶合板的标准要求(≥0.7 MPa)。
2.4.3 红外谱图分析
图2为花生蛋白粉(PM)、碱处理花生蛋白胶黏剂(OH-PM)和改性花生蛋白胶黏剂(GU-OH-PM)的红外光谱图。

图2 不同类型胶黏剂的红外光谱图
由图2可知:在PM中3 334 cm-1附近为自由O—H、N—H伸缩振动;2 874 cm-1附近为—CH2、—CH3基团的振动吸收峰;酰胺I带和II带出现在1 633 cm-1和1 532 cm-1处,酰胺III带(N—H和C—N拉伸)和C—NH2弯曲有关的谱带分别位于1 392、1 239 cm-1和1 045 cm-1。
由图2可知,与PM相比,OH-PM的O—H、N—H和—CH2、—CH3的吸收峰增强,原因是经过碱处理后的蛋白质暴露出疏水基团,耐水性提高,同时—OH、—NH2、—CH2等极性基团的暴露,可以在蛋白质分子间交联形成化学键,增加胶黏剂的内聚力,表现为胶合强度的提升[22]。但在光谱中没有新的峰值,这表明碱降解蛋白只是一个蛋白质变性过程。
由图2可知,GU-OH-PM的—COOH在1 633 cm-1和1 392 cm-1处的峰相较于PM和OH-PM减小,在1 705 cm-1处逐渐出现一个新的峰,为羰基的吸收峰,这是由于GU中的羟甲基与花生蛋白分子羧基发生酯化反应所致,这表明胶黏剂中的亲水性基团的量减少了,耐水性增强[23]。此外,酯的C—O拉伸振动产生的其他吸收峰由C—O—C组成,通常发生在1 000~1 300 cm-1附近[24],其与GU-OH-PM本身的酰胺III带和树脂中C—N弯曲重叠。
2.4.4 DSC分析
图3为花生蛋白粉(PM)、碱处理花生蛋白胶黏剂(OH-PM)和改性花生蛋白胶黏剂(GU-OH-PM)的DSC图。

图3 不同类型胶黏剂的DSC图
由图3可知,GU-OH-PM在60~200℃区间内有2个吸热峰,OH-PM、PM曲线的形貌相似,在相同温度区间内仅有1个吸热峰,三者均在65~85℃之间出现吸热峰,但GU-OH-PM与OH-PM的吸热峰较PM更明显,这可能与花生蛋白中产生黏结力的14S和7.8S球蛋白的碱改性吸热过程有关[25]。GU-OH-PM曲线在150℃出现的吸热峰应该是花生蛋白中的氨基、羧基与GU发生酯化等反应产生,这一现象表明GU与花生蛋白发生了化学反应。
通过分析得出PM、OH-PM和GU-OH-PM的吸热峰起始温度分别为50.23、46.76、57.28℃,峰值温度分别为76.40、76.42、84.97℃。GU-OH-PM 的吸热起始峰温度和峰值温度均比PM与OH-PM的高,应该是GU-OH-PM的一部分的疏水基团和GU完全结合,亲水基团和蛋白质分子紧密结合,阻碍了蛋白质进一步展开,致使峰值温度升高,热稳定性增强[26]。此外,PM、OH-PM和GU-OH-PM的峰值温度均低于100℃,后续实验可以选择降低热压温度,这样不仅可以防止蛋白质变性带来胶合性能变差问题,而且可以节省能耗。
3 结 论
以花生蛋白粉为原料,经氢氧化钠处理后,采用乙二醛-尿素合成树脂改性,制备改性花生蛋白胶黏剂以提高其耐水性。采用单因素实验对改性剂制备工艺进行优化,结果发现,当乙二醛与尿素摩尔比1.4∶1、反应温度80℃、总反应时间3.5 h时,制备的乙二醛-尿素合成树脂黏度较好,储存期较长,且不含游离醛。将其用于改性花生蛋白的制备,发现当改性剂与碱处理花生蛋白质量比16∶84、反应时间3 h、碱处理pH 10.4、花生蛋白粉质量70 g(200 mL蒸馏水)时,制备的胶黏剂干态胶合强度为2.293 MPa,湿态胶合强度为1.305 MPa,远大于GB/T 9846—2004中对Ⅱ类胶合板用胶强度的要求(≥0.7 MPa)。傅里叶变换红外光谱结果表明,氢氧化钠可使花生蛋白变性并暴露出更多的反应基团,使改性剂与碱处理后的花生蛋白形成了酯键,亲水基团减少,耐水性提高;差示扫描量热仪结果表明,改性后的花生蛋白胶黏剂吸热起始峰温度和峰值温度均升高,热稳定性提高,且制备的胶黏剂的峰值温度低于100℃,后续实验可以选择降低热压温度,以节省能耗。本研究在贯彻环境友好型策略的同时又能高效地利用生物质资源,满足了市场对无甲醛释放的绿色环保胶黏剂的需求。
