前列倍喜联合盐酸坦洛新治疗前列腺炎对患者疗效、NIH-CPSI评分及血清炎性因子的影响
2022-04-06王伟
王 伟
(慈利县象市镇卫生院,湖南 慈利 427220)
前列腺炎(Chronic prostatitis, CP)是一种常见的男性生殖系统疾病。在所有泌尿外科门诊疾病中,此病的占比为8% ~25%。此病在中青年男性群体中较为多发,其中以Ⅲ型前列腺炎最为常见,约占90% 以上[1]。调查研究显示,近年来前列腺炎的发病率呈逐渐上升的趋势。有研究指出,前列腺炎可引起精液质量的改变,从而可引发男性不育[2]。前列腺炎具有久治不愈、易复发等特点,目前尚无标准的治疗方案。盐酸坦洛新是一种新型的α1A受体阻滞剂。此药对前列腺中的α1A受体具有高选择性阻断作用[3]。前列倍喜胶囊具有活血化瘀、清热利湿、利尿通淋的功效。现代药理学研究表明,前列倍喜胶囊具有显著的改善微循环状态、改善血液流变学指标、抗炎、提高局部免疫力及调节免疫平衡等作用[4]。在本文中,笔者主要是探讨分析用前列倍喜胶囊联合盐酸坦洛新缓释片治疗前列腺炎对患者疗效、美国国立卫生研究院慢性前列腺炎症状指数(NIHCPSI) 的评分及血清炎性因子表达的影响。
1 资料与方法
1.1 临床资料
选择2019 年4 月至2020 年3 月慈利县象市镇卫生院收治的Ⅲ型前列腺炎患者158 例,按照随机数表法将其分为观察组和对照组,每组各79例患者。两组患者的年龄、病程、NIH-CPSI 评分相比,P>0.05。详见表1。本研究经慈利县象市镇卫生院医学伦理委员会批准。
表1 两组患者临床资料的比较(± s)
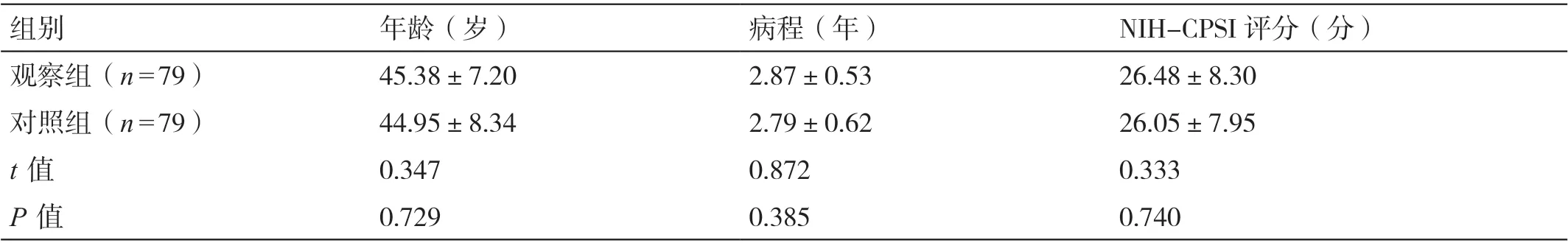
表1 两组患者临床资料的比较(± s)
组别年龄(岁)病程(年)NIH-CPSI 评分(分)观察组(n=79)45.38±7.202.87±0.5326.48±8.30对照组(n=79)44.95±8.342.79±0.6226.05±7.95 t 值0.3470.8720.333 P 值0.7290.3850.740
1.2 研究对象的纳入标准与排除标准
纳入标准:1)病情符合《泌尿外科学》[5]中关于慢性非细菌性前列腺炎(Ⅲ型前列腺炎)的诊断标准;2)年龄为20 ~50 岁;3)病程为1 ~8年;4)近3 个月内未使用过前列腺炎相关药物;5)知情并同意参与本研究。排除标准:1)对本研究中所用的药物过敏;2)合并有前列腺增生、泌尿系统结石、间质性膀胱炎、精索静脉曲张等;3)合并有恶性肿瘤;4)合并有心血管、肝、肾及造血系统的严重原发性疾病。
1.3 方法
为对照组患者采用盐酸坦洛新缓释片(生产厂家:昆明积大制药股份有限公司,批准文号:国药准字H20051461,规格:0.2 mg)进行治疗。盐酸坦洛新缓释片的用法是:口服,0.2/ 次,1 次/d(饭后服用)。在此基础上,为观察组患者采用前列倍喜胶囊(生产厂家:贵州太和制药有限公司,批准文号:国药准字Z20025028,规格:0.4 g)进行治疗。前列倍喜胶囊的用法是:口服,6 粒/次,3 次/d。两组患者均连续治疗2 个月。
1.4 观察指标
1)观察治疗前后两组患者的NIH-CPSI 评分。该评分包括疼痛或不适评分、生活质量评分及排尿症状评分三个维度,总分为43 分。评分越高,表示患者的病情越严重。2)采用酶联免疫吸附法(ELISA)检测两组患者治疗前后血清炎性因子〔包括肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)及白细胞介素-8(IL-8)〕的水平。
1.5 疗效评价标准
临床治愈:治疗后,患者的NIH-CPSI 评分降低>90% ;有效:治疗后,患者的NIH-CPSI评分降低30% ~90% ;无效:治疗后,患者的NIH-CPSI 评分降低<30%。总有效率=(总例数-无效例数)/ 总例数×100%[4]。
1.6 统计学分析
采用统计学软件SPSS 25.0 分析研究数据,计量资料用均数± 标准差(±s)表示,采用t检验,计数资料用百分比(%)表示,采用χ² 检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者临床疗效的比较
观察组患者治疗的总有效率(93.67%)显著高于对照组患者治疗的总有效率(83.54%),P<0.05。详见表2。
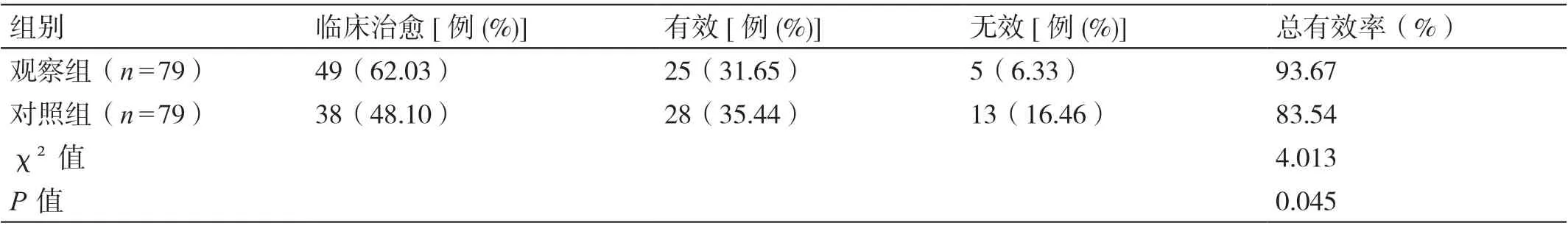
表2 两组患者临床疗效的比较
2.2 两组患者治疗前后NIH-CPSI 评分变化情况的比较
治疗后,两组患者的NIH-CPSI 评分均较治疗前显著降低,P<0.05 ;观察组患者的NIHCPSI 评分显著低于对照组患者,P<0.05。详见表3。
表3 两组患者治疗前后NIH-CPSI 评分变化情况的比较(分,± s)

表3 两组患者治疗前后NIH-CPSI 评分变化情况的比较(分,± s)
组别治疗前治疗后t 值P 值观察组(n=79)26.48±8.3011.84±3.9414.1630.000对照组(n=79)26.05±7.9515.73±4.2010.2020.000 t 值0.3336.004 P 值0.7400.000
2.3 两组患者治疗前后血清炎性因子水平变化情况的比较
治疗后,两组患者血清TNF-α、IL-1β、IL-8的水平均较治疗前显著降低,P<0.05 ;观察组患者血清TNF-α、IL-1β、IL-8 的水平均显著低于对照组患者,P<0.05。详见表4。
表4 两组患者治疗前后血清炎性因子水平变化情况的比较(ng/L,± s)

表4 两组患者治疗前后血清炎性因子水平变化情况的比较(ng/L,± s)
注:* 与对照组比较,P <0.05。
组别时间TNF-αIL-1βIL-8观察组(n=79)治疗前19.72±2.547.28±1.852.84±0.57治疗后10.58±1.09*2.37±0.58*0.79±0.22*t 值29.39222.50929.822 P 值0.0000.0000.000对照组(n=79)治疗前19.42±2.017.41±1.932.91±0.60治疗后13.38±1.544.52±0.791.36±0.37 t 值21.20112.31719.544 P 值0.0000.0000.000
3 讨论
Ⅲ型前列腺炎在所有前列腺炎中所占的比例最高。目前,临床上对Ⅲ型前列腺炎的发病机制尚不明确。此病患者的临床症状无特异性,临床上对其仍无特效性的治疗方式[6]。调查研究显示,Ⅲ型前列腺炎患者大多存在下尿路功能性梗阻,而下尿路功能性梗阻可导致尿道内压力增高,使含有细菌的尿液反流进入前列腺,进而可导致患者出现前列腺炎症反应,使其出现会阴部疼痛酸胀、排尿费力等症状[7]。由于人体存在血- 前列腺屏障,在治疗前列腺炎时感染灶部位通常难以达到理想的血药浓度,从而导致病原微生物不易被彻底清除[8-9]。在前列腺炎患者接受治疗后,即使其临床症状有所改善,其病灶部位的炎症反应及病理改变通常也会持续存在。有研究指出,Ⅲ型前列腺炎主要是由病原微生物感染引发炎症反应后导致盆底神经肌肉及神经内分泌功能出现异常、免疫失调等多种因素共同作用引起的[10]。盐酸坦洛新缓释片对α1A受体具有高选择性阻断作用。α1A受体主要集中于膀胱颈、前列腺、后尿道等部位,盐酸坦洛新可作用于此部位,舒张膀胱及前列腺平滑肌,从而可缓解尿道梗阻,改善排尿功能紊乱,减轻前列腺炎相关症状[11]。前列倍喜胶囊是一种苗药。此药具有活血化瘀、利尿通淋、清热利湿等作用。现代药理学研究表明,此药中的皂角刺可有效抑制血小板聚集,并可通过抑制凝血酶的活性而发挥抗凝血的作用;王不留行具有一定的活血功效,可改善机体微循环,缓解血液高黏状态;蝼蛄的含钾量较高,具有较强的利尿作用[12]。研究显示,前列倍喜胶囊可有效改善微循环,扩张血管,抗菌消炎[13]。本研究的结果显示,观察组患者治疗的总有效率(93.67%)显著高于对照组患者治疗的总有效率(83.54%),P<0.05。治疗后,观察组患者的NIH-CPSI 评分、血清TNF-α、IL-1β、IL-8的水平均显著低于对照组患者,P<0.05。这与相关研究报道的结果相似[14]。
综上所述,用前列倍喜胶囊联合盐酸坦洛新缓释片治疗前列腺炎的临床疗效显著,可有效抑制患者体内的炎症反应,改善其排尿困难症状,减轻其疼痛不适感,提高其生活质量。
