基于自主神经功能模型探讨迷走神经机制与体重变化
2022-04-01艾磊,叶强,李森,刘凌*
艾 磊 ,叶 强 ,李 森 ,刘 凌 *
体重控制是竞技体育领域的普遍现象,如体操、跳水、长跑等项目的运动员认为较低的体重有助于运动表现,常将体脂减到最低并期望将体重长期控制在某一特定水平。另有一些项目因参赛级别的限制,如摔跤等项目的运动员,可能会在赛前采用增大运动量、禁食以及大量脱水等方法在较短时间内降低体重,体重作为重要的考量因素,存在被过分追求的现象。不当的体重控制行为往往让运动员处于某种极限状态,一般表现为脱水过量和营养不良,导致竞技失能和引发健康问题,甚至可能发生猝死。体重下降的实质是体成分变化,其机制十分复杂。急性控体重存在较大风险,因此,在风险识别和捕捉上有着较强的专业化和职业化要求,依靠个人经验和较低的认知水平易带来风险误判,导致风险失控(Carl et al.,2017;Werner et al.,2013)。针对运动员控制体重现状,在以体重为观察变量的生理机制探讨中引入风险指标,以提高体重控制的安全性,是运动医务监督在该领域的关注重点。
心率变异性是目前最为推荐的度量自主神经功能的非侵入性指标,长期以来一直作为心脏猝死和风险的分层因子,用于临床预后的判断。通过自主神经功能对健康风险进行识别和评价是目前国内外研究的共识,是公认的极具价值的风险指标(郭继鸿,2002),体重变化引发的风险也涵盖其中。心率变异性是在常规心电图扫描过程中所获得的一系列技术参数,其中时域法(time-domain)是对逐次R-R间期(瞬时心率)的变化差异由统计学方法计算得出。借助高频心电图机技术的发展,对瞬时心率曲线和QRS波进行傅立叶转换,通过频谱观察心动周期变化被称为心率变异性频域法(frequency-domain),并从心脏做功的角度计算人体代谢水平(张开滋,2002),成为载氧水平和运动能力评估的新方法。在体育领域,心率变异性常作为机能指标,通过无侵害评价急性及中长期运动训练带来的自主神经功能变化,指导运动训练,并预警过度训练(Marocolo et al.,2007)。
本研究采用因子分析方法,观察自主神经各指标的共变性和独立性,依据数据结构获取公共因子并统一量纲,其目的是使迷走神经和交感神经的功能变化更具解释性。以因子分析结果构建研究模型(Billman,2015;Lucini,2014),探讨自主神经调节变化对体重的影响。
1 研究对象与方法
1.1 研究对象
在运动员机能评定技术平台中选取优秀跆拳道小级别运动员14名,样本总数95例。主要由女子49公斤级和男子58公斤级组成,运动年限4年以上。在赛前均完成体重预设目标,男子最大减重量为10 kg,女子为8 kg,并在比赛中取得优异成绩,减控体重期间无就医史,研究对象基本信息见表1。
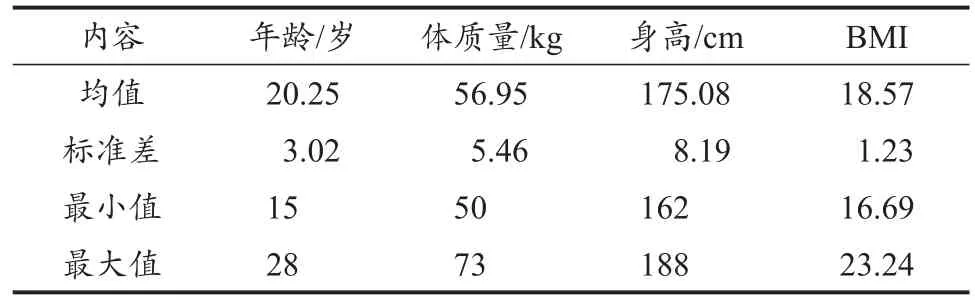
表1 研究对象基本信息Table 1 The Basic Information of Research Subjects n=95
1.2 研究方法
通过对跆拳道小级别优秀运动员10余年的数据进行回顾。在减控体重期间,采用高频心电图机技术对心电信号进行扫描和解析,受试者进行标准5 min的十二导联心电图连续采集。通过对R-R间期的精准描计,对心率变化进行统计学分析,以获得心率变异性时域指标参数。采用Fourier转换法,计量心动周期的频率成分,获得心率变异性的频域指标参数。同时,对V3R、V2、V6导联的QRS波进行高频解析,对心电差异进行频谱分析,计算心脏作功功率,依据能量代谢与功率的固定关系,完成最大摄氧量(V.O2max)和代谢指数的测试,定标方法为doglus实验室法。所有参数的获得由美国Omegawave Technologies LLC公司的Omega Wave系统一次操作完成,主要测试指标包括:时域指标、频域指标、心电差异指标。
时域指标包括:正常窦性R-R间期的标准差(standard deviation of all normal to normal R-R intervals,SDNN),相邻N-N间期差值均方根值(the root mean square of successive differences between adjacent normal cycles,rMSSD),相邻间期差值的标准差(standard deviation of successive differences between adjacent normal cycles,SDSD),NN50占所有N-N间期个数的百分数(percent of NN50in the total number of NN intervals,PNN50)。
频域指标包括:总功率(TP,频段≤0.4 Hz),高频率范围内的功率(HF,频段0.15~0.4 Hz),低频率范围内的功率(LF,频段0.04~0.15 Hz),低频高频比(LF/HF),极低频率范围内的功率(VLF)。
心电差异指标包括:V.O2max,相对最大摄氧量(RV.O2max),有氧代谢指数(aerobic index),酵解代谢指数(anaerobic index),无氧代谢指数(alactic index),交感神经张力指数(sympathtic index)。
1.3 数据统计分析
1.3.1 因子分析
以自主神经功能指标为主要观察对象进行因子分析,依据多个变量间的关联性或依存性进行分析降维,以“特征根≥1”为公因子提取原则,并用方差最大化方法进行因子旋转,获得因子得分,从而完成自主神经机能原始数据的参数化分析。根据提取的公因子建立心脏扰动因子模型,其综合得分的公式为:(权重1×公因子1+权重2×公因子2+……+权重n×公因子n)/(权重1+权重2+……+权重n),公因子得分及心脏扰动模型的总得分将作为后续回归分析的原始变量,达到统一量纲的目的。
1.3.2 回归分析
应用逐步筛选回归分析法建立最优或者最合适的体重回归模型,采用F检验、R2、DW自相关检验和残差观察,验证自主神经机能与体重间相关依赖关系。所有分析使用美国IBM SPSS公司SPSS 22.0统计软件进行处理,统计显著性水平设为0.05。
2 研究结果
2.1 验证因子分析
依据信效度检验,共遴选出指标11项,进入正定矩阵,结果显示KMO统计量为0.852,Bartleltt球形检验χ2=1 554.388,P=0.00<0.001,表明研究所使用的样本适合因子分析。各因子特征根值和累计贡献率详见图1。
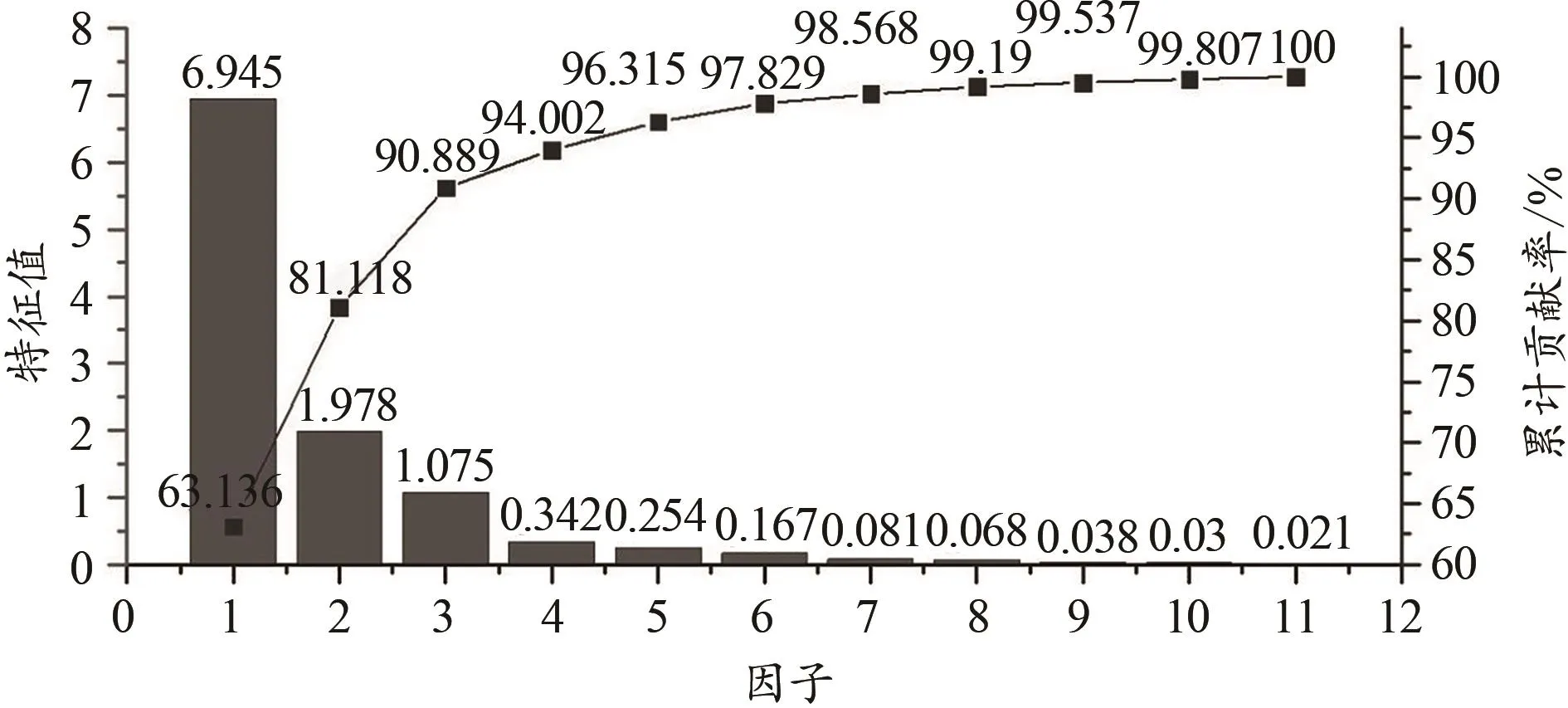
图1 主成分分析帕累托图Figure 1. The Pareto Chart of Principal ComponentAnalysis
根据主成分法分析结果,共提取3个特征根大于1的公因子,公因子1包含SDNN、rMSSD、SDSD以及HF等迷走神经功能的指标(定义为迷走神经因子),公因子2包含酵解代谢指数和无氧代谢指数等与无氧代谢有关的指标(定义为无氧代谢因子),公因子3包含LF/HF和交感神经张力指数等交感神经功能的指标(定义为交感神经因子)。数据经过4次迭代并收敛,表明数据拟合度好具有结构简洁、重复性好的特点。所提取的3个公因子贡献率分别为62%、18%、11%,因此,心脏扰动因子模型的综合得分公式为:(0.62×迷走神经因子+0.18×无氧代谢因子+0.11×交感神经因子)/0.91。图2反映的是通过综合得分反映体重的离散程度,结果表明,相同体重的综合评分存在明显波动。
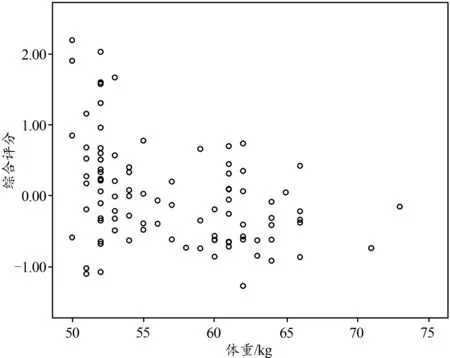
图2 体重与综合评分的散点图Figure 2. The Scatter Plot of Body-Weight and Comprehensive Score
如图3所示,经过θ角旋转,因子分布互为对角线,数据结构明析、因子间相对独立,模型具有解释强的优点。
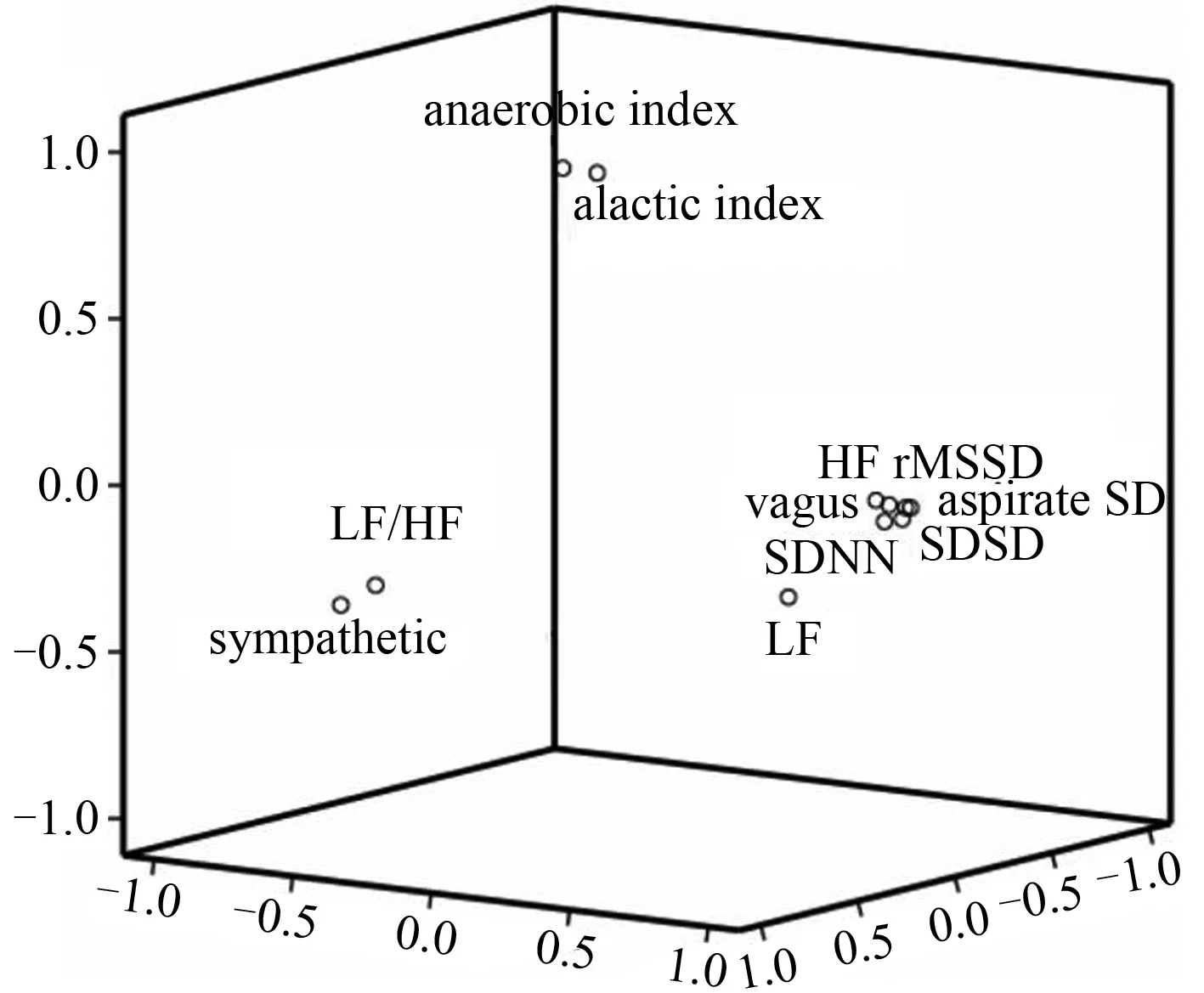
图3 旋转后主成分聚类分析图Figure 3. The Principal Component ClusteringAnalysis Graph After Rotation
2.2 逐步回归分析
通过主成分因子分析得出观察变量的公共变化因素,并完成公共因子的量纲数字化处理,以得分计量获得新的原始数据用于构建体重预测数学模型。用95例实测数据作为观测值,经逐步筛选回归分析法,得出以体重作为因变量其自变量为RV.O2max、迷走神经因子、无氧代谢因子。F检验表明,回归所得出线性模型的可靠性具有显著性意义(F=30.246、P=0.000)。调整后的R2并未明显下降(0.447,P=0.000),DW值达临界值(1.295),自变量间不存在共线性(VIF<10),回归模型基本满足随机调查要求(表2、表3),表明RV.O2max、迷走神经功能和无氧代谢与体重存在因果关系,即体重变化归因为RV.O2max、迷走神经功能和无氧代谢能力,观察三者可解释体重变化的机制。

表2 逐步回归分析后的统计结果Table 2 Statistical ResultsAfter Stepwise RegressionAnalysis
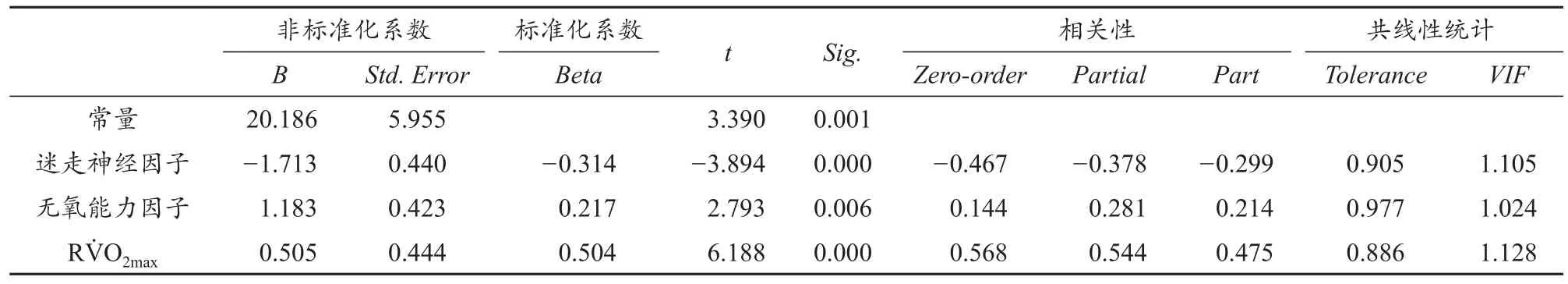
表3 回归方程系数及其检验结果Table 3 Coefficient of Regression Equation and Its Test Results
如图4所示,残差观察显示残差直方图正态分布,P-P图散点均沿对角线近似直线排列,标准化残差散点图无明显规律,表明实际观测值与预测值的差异为实验误差所致。
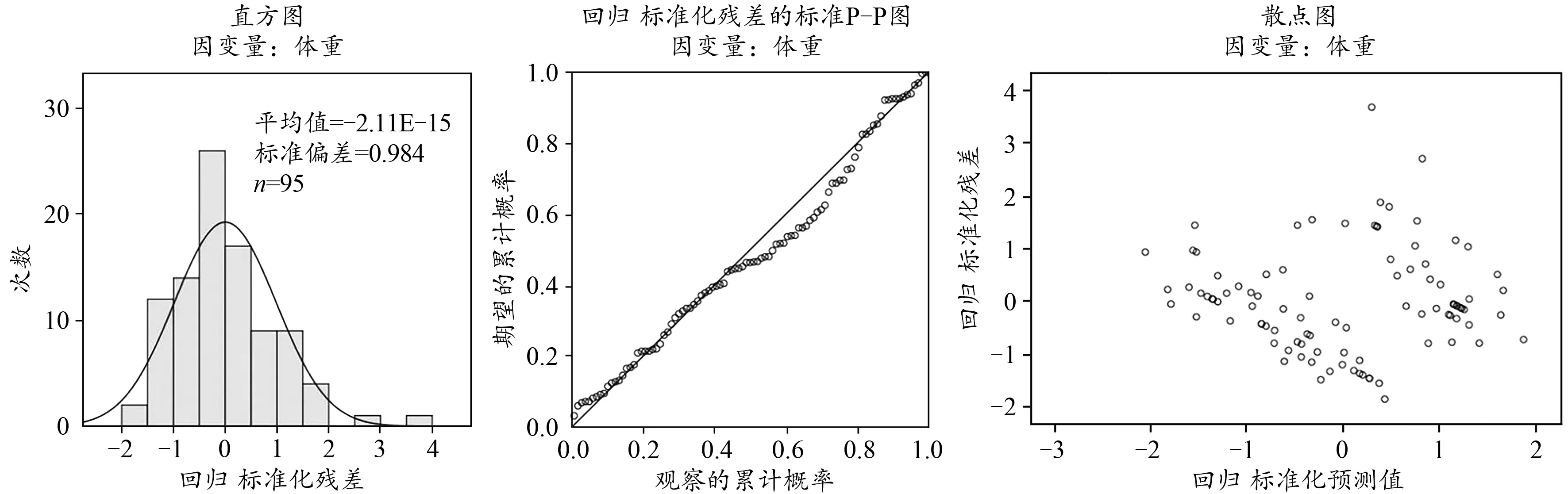
图4 回归方程残差分析Figure 4. The ResidualAnalysis Diagram of Regression Equation
3 分析与讨论
3.1 公共因子与风险评估
在模型矩阵中,各因子得分与原始数据呈正相关变化,即迷走神经功能增强,该因子得分增高。作为权重最大的因子,迷走神经因子得分决定了综合得分的变化趋势。迷走神经功能增强能有效的降低风险,因此,综合得分高者风险发生概率下降。综合得分是风险数字化的处理方式,结合无氧代谢和自主神经功能平衡两个次要因子,可以进一步细化风险评估。通过得分构成系数可以看出,迷走神经因子得分高者,综合评分升高明显。同理,无氧代谢因子上升可在一定程度上提升评分,表明在减控体重过程中应维护或提升无氧能力。交感神经因子也具有提升综合评分的作用,平衡性趋于交感神经功能,有助于运动时交感神经效应的表达,进而有利于竞技表现。由此可以看出,研究模型应用于体重变化的分析,实质上探讨的是减控体重是否失能的问题。反之,公共因子得分的下降将导致综合评分的下降,意味着减控体重的失能甚至可能引发健康问题,对竞技体育具有较强的应用价值。
公共因子是指多变量中潜在的共性因子,多用于造模研究,解释变量间的相互关系。近10年针对运动员、高血糖、高血压及多种临床疾病患者的自主神经模型研究中,公共因子多为2~4个,均以代表迷走神经功能的因子为权重最大的公共因子。本研究建模KMO和Bartleltt球形检验分别为0.852和0.00,迷走神经因子作为主因子,权重占比高于国外类似研究(62%>40%),无氧代谢因子(权重18%)和交感神经因子(权重11%)与主因子权重差异大于国外认可的20%(Lucini et al.,2018),表明该模型对变量的解释更简练,主次关系更明确。研究表明,在无氧运动后或运动适应早期阶段,交感神经功能增强比迷走神经功能增强更易出现,良好的迷走神经功能退让是人体对强度适应的调控方式之一(Pichot et al.,2002)。长期剧烈的肌肉运动对自主神经的平衡能力提出了更高的要求,最终会出现迷走神经张力伴随交感神经张力增高而增高,重新达到平衡性。自主神经调节过程存在强度效应(刘凌等,2007),具有更强迷走神经功能的受试者更能承受极限量运动(Blaber et al.,2003)。训练结束后短期的迷走神经功能降低是普遍现象,这一改变可作为判断应激存在的依据,迷走神经功能的恢复涵盖应激消退的全过程(Langelotz et al.,2008)。良好的迷走神经功能是自主神经功能正常的表现,提示机体可再次承受极限量运动负荷;而长期的迷走神经功能下降表明应激持续存在,多属病理性应激,提示机体再次承受较大量的运动负荷具有高风险性(Dennis et al.,2016)。本研究在模型建立的过程中,确实观察到体重相同而综合评分不同的情况,而评分高者在安全性上应优于评分低者,因为迷走神经因子得分增高是综合评分升高的最主要影响因素。
在信度检验中,迷走神经因子中的HF(P=-0.01)、SDSD(P=-0.01)与BMI显著负相关,迷走神经因子得分增加表明体重的下降以体脂下降为优,而不是脱水,脱水必将带来HF下降,导致迷走神经因子评分下降,迷走神经功能呈现下降趋势,以脱水获得的体重减少存在风险(Early et al.,2018)。有研究表明,体重下降更多的表现为运动员载氧水平的下降,并非一定导致无氧功下降,良好的无氧代谢能力有利于运动表现,在减控体重过程中应维护无氧能力(Yang et al.,2018),通过无氧代谢因子得分的变化可作判断,并以升高为优。交感神经因子得分增高表明自主神经功能平衡趋于交感神经,有利于快速适应运动状态,也具有降低运动中风险发生概率的作用(Lucini et al.,2018)。无氧代谢因子和平衡因子的引入,增加了减控体重与运动失能的观察因素。
3.2 迷走神经功能与体重变化的机制探讨
体重是对人体的称量描述,受到饮食和体成分等诸多混杂因素的影响,人体水分的变化使体重在短期内呈现明显的波动变化,给体重的变化趋势判断带来相当的难度。此次以公共因子对体重进行回归分析,其目的是对混杂因素的收敛,为判断体重的变化趋势提供依据。通过回归分析结果验证,本研究建立的自主神经模型具有较高的可信度和应用价值,该模型对自主神经功能的定标方法在特异性与灵敏上具有一定的价值。回归分析表明,RV.O2max、迷走神经因子和无氧代谢因子可作为体重变化存在因果关系的描述变量,交感神经因子因与RV.O2max显著相关而没有进入回归分析中。意大利一项公共健康研究表明,自主神经功能与心、肺运动耐受能力(CPET)密切相关,其中LF/HF最为敏感,无论是最大负荷还是最大氧耗均存在显著性差异(R2=0.186,P=0.014;R2=0.242,P=0.004),即交感神经越兴奋,氧耗升高越快,并可作为氧耗的自变量(Di Paolo et al.,2018)。LF/HF升高后的恢复来自体重的下降(R2=0.216,P=0.007)。在极限量负荷研究中,人体均会出现一过性LF/HF过度升高,安静时机体处于较高氧耗状态,人体通过增高迷走神经活性,表现为HF输出增加,使LF/HF重新回到平衡,带来氧耗的降低,研究认为体重的丢失是对氧耗降低的适应性反应(Blasco-Lafarga et al.,2017)。研究认为,过强的交感神经张力是体重下降的必要条件(Shiraishi et al.,2018),此次因子分析将LF/HF旋转成为公共因子,也表明交感神经对体重变化具有潜在的贡献。在回归分析中,RV.O2max是反映人体氧耗的主要指标,作为氧耗自变量的交感神经因子应被RV.O2max收敛存在于体重变化机制中,而不再作为机制中的独立要素。
体成分的变化是围绕蛋白质变化的一系列组织和结构的变化,可通过V.O2max观察(Ilic et al.,2015)。跆拳道运动员在减控体重期出现V.O2max下降,但RV.O2max升高,是国外研究中常观察到的现象,提示体重变化的机制是人体对RV.O2max的维护(Jabbour et al.,2013),而本研究回归分析中RV.O2maxBeta系数最大(0.504)也佐证了这一观点。脱水是体重变化的最强因素,一次大运动量活动,急性脱水可引起体重下降,丢失的水来自蛋白质的分解,蛋白的分解导致RV.O2max和无氧代谢水平降低(Villiger et al.,2018)。人体在脱水时,运动中核心体温升高明显,热应激更为强烈,蛋白组织的分解加剧。研究表明,人体体温每升高1℃,安静代谢率会增加13%,从而出现体重的持续下降(Nathaniel et al.,2012)。飞行员慢性脱水的研究显示,平均心率的升高与体脂存在显著负相关(r=-0.617,P=0.03),表明体脂高者对抗慢性脱水优于体脂低者,考虑脂肪代谢内生水是改善水合的主要途径,心率变化缓慢提示迷走神经功能与脂肪动员存在一定联系(Oliveira-Silva et al.,2015)。长期严格的低卡饮食,机体尽量运用脂肪酸和酮体供能,骨骼肌也可释放氨基酸(主要为丙氨酸)异生成糖。自主神经通过增加迷走神经活性使安静时代谢率下降10%左右以减少能耗需求(布郎沃德,2003;陈灏珠,1999),同时使尿氮降低达65%以提升蛋白质利用率、周转率和氨基酸再利用率。迷走神经功能的增强呈现出强烈的护氮效应,体脂分解成为蛋白营养最主要的供能方式。迷走神经功能增强,最终带来蛋白质重吸收和体脂率下降,其净效应表现为体重下降(Cherkas et al.,2015;Hulmi et al.,2015;Taffe et al.,2016),由回归方程得出,迷走神经因子每上升1个标准单位,体重将下降0.3个标准单位。无氧代谢因子也是体重的自变量(Geenway,2015),提示高强度运动导致的无氧代谢能力下降也将促进体重下降,无氧代谢因子每下降1个标准单位将带来0.2个标准单位体重的下降。综上所述,迷走神经功能下降具有风险预警作用,鉴于此,安全的体重下降过程可解读为迷走神经功能的允许效应,观察迷走神经功能变化为设定合理的体重控制范围和个人经验提供了评判依据,但有待进一步达成共识。
4 结论
1)通过探索性因子分析降维处理,运动员减控体重期间应从迷走神经、无氧代谢、功能平衡3个维度进行运动风险评价和策略调整,其中迷走神经功能因素尤为突出。
2)使用逐步回归分析将RV.O2max联合迷走神经功能和无氧代谢能力作为输入因子进行体重预测,有助于体重控制中的风险管控。
