高尿酸通过氧化应激诱导心肌细胞胰岛素抵抗
2022-03-31陈映群张卫星
陈映群,张卫星,李 智
高尿酸已经被证实与心血管疾病密切相关,包括高血压、缺血性心脏病、心力衰竭和心源性猝死等[1-5]。动物实验发现高尿酸可加重缺血/缺氧条件下小鼠心肌细胞凋亡[6]。临床研究[7]表明高尿酸血症是胰岛素抵抗的独立危险因素,基础研究证明高尿酸能诱导肝脏、肌肉和脂肪细胞的胰岛素抵抗。研究[8]证实胰岛素抵抗是影响心衰预后的一个标志物。然而,高尿酸血症是否可以通过诱导心肌细胞胰岛素抵抗影响心功能目前仍不清楚。高尿酸可增加多种靶细胞内氧化应激[9-10],课题组前期研究[5]表明高尿酸处理后肝细胞和胰腺β细胞中活性氧(reactive oxygen species,ROS)产生增加,且与胰岛素抵抗有关。高尿酸在胰岛素抵抗及心脏功能障碍中是否起到关键作用尚未确定。该研究通过体外原代心肌细胞、H9c2心肌细胞株实验以及高尿酸动物模型,探讨高尿酸对细胞内氧化应激、胰岛素信号通路和胰岛素抵抗的影响。
1 材料与方法
1.1 试剂荧光标记葡萄糖2-(N-7-硝基-2,1,3-苯并恶二唑-4-氨基)-2-脱氧-D-葡萄糖(简称:2-NBDG)购自美国Invitrogen公司;氧化应激荧光探针2′,7′-二氯荧光素二乙酸酯(简称:DCFH-DA)、尿酸购自美国Sigma公司;抗氧化剂N-乙酰-L-半胱氨酸(简称:NAC)购自美国ENZO Life Sciences公司;磷酸化Akt(Ser473)和Akt抗体购自美国Bioworld公司;磷酸化IRS1(Ser307)和IRS1(Ser307)抗体购自美国Millipore公司;兔GAPDH抗体购自美国Abcam公司。所有化学试剂具有分析纯级。尿酸储备溶液浓度为15 mg/ml,最终实验浓度为15 mg/dl;NAC储备溶液浓度为500 mmol/L,最终实验浓度为5 mmol/L。
1.2 细胞培养与处理细胞研究使用H9c2大鼠心脏来源的胚胎肌细胞,用含有10%胎牛血清、100 U/ml青霉素的DMEM或低糖DMEM作为培养基进行细胞培养,在37 ℃含5%CO2和95%空气的细胞培养箱中孵育。根据试验目的将细胞实验分为两部分:① 明确高尿酸可使心肌细胞内ROS增加,心肌细胞实验分组为:对照组(Control)、高尿酸作用组(HUA)、抗氧化剂作用组(NAC)、抗氧化剂+高尿酸作用组(NAC+HUA);② 明确高尿酸通过氧化应激抑制心肌细胞对葡萄糖的摄取并诱导心肌细胞胰岛素抵抗,心肌细胞实验分组为:对照组(Control)、高尿酸作用组(HUA)、抗氧化剂作用组(NAC)、抗氧化剂+高尿酸作用组组(NAC+HUA)、胰岛素作用组(Insulin)、胰岛素+高尿酸作用组(Insulin+HUA)、抗氧化剂+胰岛素作用组(NAC+Insulin)、抗氧化剂+胰岛素+高尿酸作用组(NAC+Insulin+HUA)。将细胞以2.0×105个/ml密度接种在6孔板;在含高尿酸处理组,将细胞与含有15 mg/dl尿酸在新鲜细胞培养基中孵育24 h;含抗氧化剂NAC作用组,将细胞与含5 mmol/L NAC新鲜细胞培养基预处理30 min;然后收集细胞用于生物化学或分子测定。所有实验至少重复3次。
1.3 荧光显微镜分析心肌细胞对荧光葡萄糖摄取使用荧光显微镜(CX21倒置荧光显微镜,日本奥林巴斯公司)对心肌细胞对荧光葡萄糖摄取进行定性分析。2-NBDG是一种2-脱氧荧光葡萄糖的类似物,被细胞吸收以后,由于无法代谢而在细胞内积累,因此可作为细胞葡萄糖代谢的示踪剂,荧光强度反映了葡萄糖吸收的情况。本实验通过荧光葡萄糖类似物2-NBDG评估H9c2心肌细胞对的葡萄糖摄取。用含FBS的低糖DMEM培养基处理细胞24 h,然后用含有胰岛素(100 nmol/L)和2-NBDG(100 μmol/L)的KRB缓冲液替换培养基。在37 ℃下作用30 min,用激发和发射波长分别为485 nm和535 nm的荧光测定H9c2心肌细胞对的葡萄糖摄取。
1.4 流式细胞仪分析心肌细胞对荧光葡萄糖摄取使用流式细胞仪(BD Biosciences,San Jose,CA,USA)对心肌细胞对荧光葡萄糖摄取进行定量分析。用含FBS的低糖DMEM培养基处理细胞24 h,然后用含有胰岛素(100 nmol/L)和2-NBDG(100 μmol/L)的KRB缓冲液替换培养基在37 ℃下30 min。处理后从培养基中洗去游离的2-NBDG,分别在激发和发射波长为488 nm和525 nm下通过流式细胞术测量心肌细胞对葡萄糖2-NBDG的摄取。数据分析使用流式细胞仪相关软件。统计分析使用单因素方差分析及Tukey-Kramer多重比较分析。
1.5 细胞内活性氧ROS测定将细胞在6孔板(2.0×105个/孔)中传代培养并使其附着作用于高尿酸24 h,并如上所述在37 ℃用10 mmol/L DCFH-DA染色30 min。通过荧光显微镜对染色的细胞成像,并分别在激发和发射波长为530 nm和480 nm下通过流式细胞术对细胞内ROS分析。
1.6 急性高尿酸模型的构建8周龄C57BL/6J雄性小鼠,体质量(20±2)g,购自北京维通利华实验动物技术有限公司。经汕头大学医学院动物伦理委员会批准。给予标准饮食,实验前经过1周的环境适应时间。取9周龄小鼠12只,随机选择6只作为对照组,另外6只作为实验组。对照组和实验组小鼠禁食过夜,对照组根据体质量给予0.5%羧甲基纤维素钠灌胃和腹腔注射,实验组给予500 mg/kg次黄嘌呤灌胃以及300 mg/kg氧嗪酸钾腹腔注射处理;用磷钨酸法检测不同时间(0、1、2、3、4、6 h)小鼠血清中尿酸水平,建立急性高尿酸模型。
2 结果
2.1 高尿酸抑制胰岛素诱导的H9c2心肌细胞对葡萄糖摄取为了确定高尿酸是否在体外诱导心肌细胞胰岛素抵抗,将H9c2心肌细胞用不同浓度(0、5、10、15、20 mg/dl)的尿酸预处理不同时间(0、0.5、1.0、8.0、16.0、24.0 h),通过流式细胞仪对胰岛素刺激的心肌细胞2-NBDG摄取进行测定,结果发现胰岛素显着增加H9c2心肌细胞中2-NBDG摄取,高尿酸(15 mg/dl)预处理24 h后明显抑制心肌细胞胰岛素诱导的2-NBDG摄取率[(23.13±1.92)%vs(72.85±4.88)%,P<0.05]。因此,高尿酸诱导心肌细胞胰岛素抵抗并抑制胰岛素刺激下心肌细胞葡萄糖的摄取。见图1。

图1 尿酸对H9c2心肌细胞2-NBDG摄取的影响
2.2 高尿酸诱导H9c2心肌细胞的氧化应激与Control组比较,高尿酸预处理24 h后H9c2心肌细胞内的ROS水平明显升高[Control:(4.15±0.89)%vsHUA:(50.03±4.53)%,P<0.05]。用抗氧化剂NAC预处理能够部分逆转心肌细胞内高尿酸产生的ROS[HUA+NAC:(17.55±1.85)%vsHUA:(50.03 ± 4.53)%,P<0.05],表明高尿酸可直接引起H9c2心肌细胞的氧化应激。见图2。

图2 高尿酸对H9c2心肌细胞ROS的影响
2.3 高尿酸通过氧化应激诱导H9c2和原代心肌细胞胰岛素抵抗抗氧化剂NAC预处理逆转了高尿酸抑制的胰岛素诱导H9c2心肌细胞2-NBDG葡萄糖摄取[NAC+Insulin+HUA:(62.20±4.51)%vsInsulin+HUA:(31.98±3.74)%,P<0.05],表明氧化应激在高尿酸诱导的心肌细胞胰岛素抵抗中起到关键作用。见图3。

图3 高尿酸对H9c2心肌细胞2-NBDG葡萄糖摄取的影响
2.4 高尿酸激活心肌细胞胰岛素负调节蛋白IRS1(Ser307)磷酸化,抑制胰岛素信号蛋白Akt磷酸化与激活胰岛素信号传导的其他磷酸化位点的IRS1(Ser307)比较,磷酸化IRS1(Ser307)抑制胰岛素信号传导。在本研究中,高尿酸增加H9c2心肌细胞中的磷酸化IRS1(Ser307)水平(HUAvsControl:P<0.01,F=27.71)。此外,高尿酸部分逆转了胰岛素对H9c2心肌细胞中磷酸化IRS1(Ser307)的抑制(HUA+InsulinvsInsulin:P<0.01,Q=11.70)。为了确定高尿酸诱导的氧化应激是否激活H9c2心肌细胞中的磷酸化IRS1(Ser307),课题组用抗氧化剂NAC预处理细胞观察高尿酸诱导磷酸化IRS1(Ser307)水平的表达。NAC抵消了高尿酸诱导的磷酸化IRS1(Ser307)过表达(NAC+HUAvsHUA:P<0.05,Q=4.79),表明氧化应激在高尿酸诱导心肌细胞胰岛素抵抗中起到关键作用。见图4A。

图4 高尿酸对H9c2心肌细胞磷酸化IRS1(Ser307)及磷酸化Akt的影响
Akt是胰岛素依赖性PI3K通路在信号转导过程中激活的Ser/Thr蛋白激酶。课题组检测了高尿酸在H9c2细胞中是否抑制了胰岛素诱导的Akt磷酸化,结果显示高尿酸显着抑制胰岛素诱导的磷酸化Akt水平(HUA+InsulinvsInsulin:P<0.01,Q=9.45)。见图4B。
另外,课题组进一步讨论了抗氧化剂NAC对高尿酸抑制心肌细胞Akt磷酸化的影响。NAC不影响胰岛素诱导的磷酸化Akt水平,但明显改善高尿酸对胰岛素诱导的磷酸化Akt的抑制(NAC+HUA+InsulinvsHUA+Insulin:P<0.05,Q=5.08)。抗氧化剂逆转高尿酸对磷酸化Akt水平的抑制,证明氧化应激在高尿酸对胰岛素下游信号通路具有重要影响。见图4B。
2.5 高尿酸血症增加磷酸化IRS1(Ser307)水平并抑制小鼠心肌组织中胰岛素诱导的Akt磷酸化高尿酸血症小鼠模型中血清尿酸水平高于诱导前,这与原发性高尿酸血症患者一致。在葡萄糖或胰岛素注射后15和30 min,小鼠模型显示葡萄糖耐量受损(P<0.05,图5A)和胰岛素耐受(P<0.05,图5B)。进而检测急性高尿酸血症对小鼠模型的心脏组织中的胰岛素信号通路蛋白的影响。胰岛素腹膜内注射高尿酸血症小鼠10 min,然后处死获得心肌组织。高尿酸血症增加小鼠心肌组织中IRS1(Ser307)的磷酸化水平(P<0.01,图5C);在急性高尿酸血症小鼠的心肌组织中磷酸化Akt水平明显低于对照组(P<0.05,图5D),表明高尿酸血症在体内明显影响胰岛素下游信号通路的传导。高尿酸通过氧化应激激活磷酸化IRS1(Ser307)水平,进而抑制Akt(Ser 437)磷酸化,从而导致心肌细胞胰岛素抵抗(图5E)。
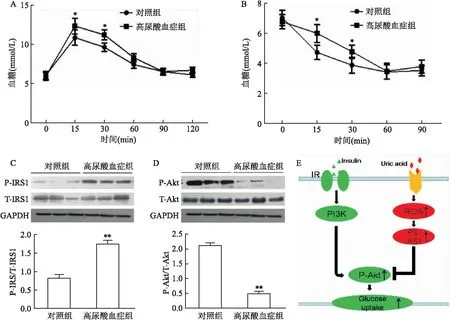
图5 高尿酸血症诱导小鼠心肌组织胰岛素抵抗及示意图
3 讨论
本研究讨论了高尿酸诱导对心肌细胞胰岛素抵抗及葡萄糖摄取的影响。高尿酸血症与许多心血管疾病密切相关[1],如心力衰竭、高血压和冠状动脉疾病,但缺乏解释这种关联的病理机制。体外高尿酸增加胰腺β细胞、脂肪细胞和系膜细胞的氧化应激[7-8],而研究表明氧化应激是许多细胞类型(包括心肌细胞)中胰岛素抵抗的主要介质[10-11]。此外,胰岛素抵抗是心力衰竭患者死亡的危险因素,心肌氧化应激通常伴有胰岛素抵抗[12-13]。高尿酸可以加重胰岛素抵抗,这在课题组前期的研究[5]中得到证实:证明高尿酸可以通过氧化应激直接诱导心肌细胞胰岛素抵抗。本研究结果为高尿酸作为心血管疾病的独立危险因素提供了新的证据,为高尿酸如何抑制心肌细胞葡萄糖代谢及高尿酸相关心血管疾病提供新的解释。
研究[14]表明细胞内胰岛素信号通路通过调节细胞葡萄糖代谢来调节细胞代谢、生长和存活,心脏生长和代谢是通过复杂的细胞外和细胞内信号整合来协调。高尿酸明显抑制了心肌细胞中胰岛素诱导的葡萄糖摄取,导致胰岛素抵抗,但高尿酸是通过何种机制诱导心肌细胞胰岛素抵抗并抑制了心肌细胞对葡萄糖的摄取,仍不得而知。
已有研究[15]表明骨骼肌中H2O2诱导的氧化应激与胰岛素抵抗有关,本研究发现高尿酸直接增加了心肌细胞内活性氧水平,提示高尿酸诱导了心肌细胞氧化应激。此外,课题组检测了抗氧化剂NAC在高尿酸抑制胰岛素刺激下心肌细胞葡萄糖摄取的影响,结果发现在心肌细胞中,抗氧化剂NAC明显逆转了心肌细胞中高尿酸抑制胰岛素刺激的2-NBDG摄取,结果表明高尿酸通过氧化应激诱导的胰岛素抵抗从而抑制了心肌细胞对葡萄糖的摄取,这与新近一项研究[16]相符,该研究显示氧化应激可诱导心肌细胞胰岛素抵抗进而增加H9c2心肌细胞凋亡。
本研究讨论了高尿酸诱导心肌细胞胰岛素抵抗的机制,高尿酸通过降低葡萄糖摄取来改变心肌细胞能量代谢,高尿酸诱导的心肌细胞胰岛素抵抗可能导致心脏功能障碍,为高尿酸血症相关代谢性心血管疾病的提供了新的证据。然而,本研究仅从体外细胞实验证实了高尿酸通过氧化应激诱导的胰岛素抵抗从而抑制了心肌细胞对葡萄糖的摄取,但人高尿酸血症是一种慢性过程,需要进一步在动物模型上研究高尿酸血症和胰岛素抵抗的关系。
