氢化物发生-电感耦合等离子体串联质谱法分析大米中的无机砷
2022-03-30李爱阳黄建华
李爱阳,黄建华
(1.湖南工学院材料科学与工程学院,湖南 衡阳 421002;2.湖南中医药研究院中医研究所,湖南 长沙 410013)
大米为世界上一半人口的主食,特别是亚洲和非洲发展中国家,所提供能量占日常食物摄入量的70%[1]。大米的基质组成复杂,主要由碳水化合物、蛋白质、脂肪、纤维素以及矿物营养成分组成[2]。然而,大米中还含有毒理性微量元素,其中砷是研究最多的元素[3-5]。砷的毒性取决于其化学形态或物种,而不仅取决于总量,无机砷(inorganic arsenic,iAs)以亚砷酸盐(As(III))、砷酸盐(As(V))和氧化物(As(III、V))的形式存在,主要来源于岩石和土壤改变和侵蚀的自然释放,或来源于采矿、冶金活动、使用杀虫剂和燃烧不同的材料等[6-8]。iAs是已知的致癌物,被认为是毒性最强的砷物种之一,而有机砷(oAs)主要以一甲基胂酸(monomethyl arsonic acid,MMA)和二甲基胂酸(dimethyl arsonic acid,DMA)的形式存在,通常被认为毒性较小[9-11]。水稻很容易从其生长的土壤和水中吸收砷积累到谷粒中,从而导致大米中iAs浓度相对较高[12]。我国作为大米摄入量高的国家,对大米中iAs含量制定严格的国家标准(GB 2762—2017《食品中污染物限量》),规定大米中iAs不大于0.2 mg/kg[13]。因此,建立简单、快速、灵敏、可靠检测大米中iAs含量的分析方法具有重要意义。
大米中砷含量通常很低,在测定前需从样品中提取和分离出不同形态的砷,固相萃取、浊点萃取、分散液液微萃取、氢化物发生(hydride generation,HG)等技术通常被用于提取不同形态的砷[14-17],而离子色谱、高效液相色谱(high performance liquid chromatography,HPLC)以及毛细管电泳是分离不同形态砷最常用方法[18-20]。其中,HG技术使用硼氢化钠在酸性介质中将水溶液中的物质转化为挥发性氢化物。由于不同形态砷与硼氢化钠反应的原理不同,并不是所有形态砷均可形成氢化物,但可以通过控制转化条件选择性地形成单个形态砷或具有相同性质多个形态砷的氢化物,从而无需使用色谱分离技术即可进行提取和分离出不同形态的砷。
目前,测定大米样品中不同形态的砷含量已有大量文献报道,通常采用原子光谱检测技术,主要包括原子荧光光谱法[21]、原子吸收光谱法[22]、电感耦合等离子发射光谱法[23]和电感耦合等离子体质谱(inductively coupled plasma-mass spectrometry,ICP-MS)法[24]。与其他检测技术相比,ICP-MS具有检出限低、灵敏度高、选择性好等优点[25],但来自ICP工作气与样品基质所形成的质谱干扰仍然影响痕量砷元素的准确测定,尤其是基于四极杆ICP-MS缺少消除质谱干扰的通用方法。电感耦合等离子体串联质谱(inductively coupled plasmatandem mass spectrometry,ICP-MS/MS)利用双重四极杆精准控制碰撞反应池(collision reaction cell,CRC)内的反应过程和反应产物,通过选择合适的反应气,几乎可以消除所有质谱干扰[26]。本实验利用多模式进样系统(multimode sample introduction system,MSIS)在HG模式下,通过控制HG条件将大米中iAs选择性生成气态氢化物(AsH3),导入ICP-MS/MS进行测定,在MS/MS模式采用O2为反应气消除质谱干扰,旨在无需使用色谱分离准确测定大米中iAs的含量。
1 材料与方法
1.1 材料与试剂
大米样品湖南籼米(产地湖南)、湖南粳米(产地湖南)、湖南糯米(产地湖南)、江西籼米(产地江西)、重庆籼米(产地重庆)、重庆粳米(产地重庆)、东北粳米(产地黑龙江)、泰国茉莉香米(产地泰国)、日本米(产地日本)、柬埔寨茉莉香米(产地柬埔寨),购于大型超市。
砷单元素标准溶液(1 000 mg/L)、铑单元素标准溶液(1 000 mg/L)、氢氧化钠(分析纯)、硼氢化钠(分析纯)、磷酸二氢铵(分析纯)、氨水(分析纯)国药集团化学试剂有限公司;质量分数65%硝酸、质量分数37%盐酸、质量分数30%双氧水 德国Merck公司;MMA标准物质(GBW08668)、DMA标准物质(GBW08669)、砷酸标准物质(GBW08667)、亚砷酸标准物质(GBW08666) 中国计量科学研究院;国家标准参考物质大米粉成分分析标准物质(GBW(E)100348a,GBW(E)100349a) 钢研纳克检测技术股份有限公司;标准参考物质大米粉(NIST SRM1568b) 美国国家标准与技术研究院。
1.2 仪器与设备
8800 ICP-MS/MS仪(配备MSIS附件、玻璃同心雾化器、石英双通道Scott雾化室)、1260 HPLC仪(配备手动进样器、单元泵) 美国Agilent公司;PRP-X100阴离子交换分析和、保护柱 瑞士Hamilton公司;Sorvall ST16R台式高速离心机 美国Thermo Scientific公司;MARS微波消解仪 美国CEM公司;FZ102微型植物粉碎机 天津泰斯特仪器有限公司;HWS28电热恒温水浴锅 上海一恒科学仪器有限公司;Milli-Q超纯水仪美国Millipore公司。
1.3 方法
1.3.1 工作条件
ICP-MS/MS条件:射频功率1.55 kW;等离子气流速18.0 L/min;辅助气流速1.8 L/min;载气流速1.09 L/min;采样深度8.0 mm;反应气O2流速0.30 mL/min;积分时间3 s;第一质量过滤器(Q1)m/z75;第二质量过滤器(Q2)m/z91。
HPLC条件:流动相20 mmol/L磷酸二氢铵;流动相流速1 mL/min;进样量50 μL;柱温室温;pH 8.0;采集时间650 s。
MSIS条件:样品提取溶液流速0.5 mL/min;盐酸流速2.0 mL/min;硼氢化钠流速0.5 mL/min;内标溶液流速0.8 L/min;Ar流速0.5 L/min。
1.3.2 样品中砷的提取
酸提取法:准确称取0.5 g经粉碎机粉碎后的大米样品于离心管中,依次加入0.15 mol/L硝酸9.0 mL,30%的双氧水1.0 mL,混合均匀静置过夜后放入恒温水浴锅内50 ℃提取5 min,75 ℃提取5 min,95 ℃提取10 min。冷却至室温,经8 000 r/min离心10 min,取上清液经0.45 μm滤膜过滤后,用超纯水定容至100 mL,用于不同形态砷的测定。
微波消解法:准确称取0.5 g经粉碎机粉碎后的大米样品于微波消解罐内,依次加入65%硝酸4.0 mL,30%双氧水6.0 mL,经微波消解后用超纯水定容至100 mL,用于总砷的测定。
1.3.3 样品中iAs的分离
在MSIS的HG模式下(图1)。将大米样品的酸提取溶液与预还原剂5 mol/L盐酸进入MSIS前经三通毛细管线圈混合均匀,与还原剂2 g/100 mL硼氢化钠溶液在MSIS中发生反应,在Ar的推动下,利用测定非氢化物元素的样品引入通道加入25 μg/L铑内标溶液,将生成的氢化物气体和内标雾化溶液导入ICP-MS/MS,测定大米中的iAs。
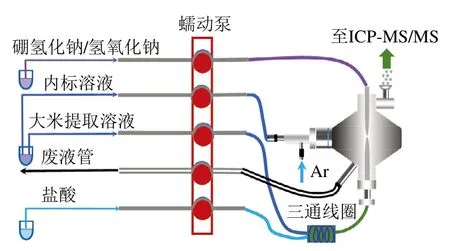
图1 ICP-MS/MS的MSIS原理图Fig. 1 Schematic diagram of the MSIS for ICP-MS/MS
1.3.4 HG-ICP-MS/MS分析
配制质量浓度分别为0.0、0.5、1.0、2.0、5.0、10 μg/L的系列砷标准溶液,在选定的MSIS和ICP-MS/MS条件下进行测定,同时对样品酸提取溶液和空白溶液(酸提取法)进行测定,根据砷信号强度与内标元素铑信号强度的比值所对应的砷标准溶液的浓度建立校准曲线,并进行线性回归,计算样品提取溶液中总砷和iAs的含量。
1.4 数据处理
ICP-MS/MS实验数据采用MassHunter软件进行评估和统计,实验图标采用Origin 9.0绘制。
2 结果与分析
2.1 不同形态砷发生氢化物反应条件
高价砷不易发生氢化物反应,需还原为低价砷,盐酸既能将As(V)还原为As(III),又能对样品进行酸化,是HG最常用载流介质。分别配制1 μg/L的As(III)、MMA、DMA标准溶液,固定硼氢化钠质量浓度为2 g/100 mL,考察盐酸浓度变化对不同形态砷信号强度的影响。As(III)、MMA、DMA的氢化物反应方程式如下:

从图2a可以看出,随着盐酸浓度的增大,As(V)在盐酸介质中还原为As(III),经反应(1)As(III)的信号强度,当盐酸的浓度达到1 mol/L时,As(III)的信号强度达到最大值,随后处于平稳状态,表明在As(III)通过氢化物反应已完全形成AsH3,当盐酸浓度增大至4 mol/L后,As(III)的信号强度开始小幅度下降;MMA经氢化物反应(2)可生成挥发性甲基胂(CH3AsH2),但随着盐酸浓度的增大,MMA的信号强度逐渐减小,表明高浓度盐酸介质抑制MMA生成甲基胂的氢化物反应,虽然MMA的信号强度一直持续下降,但由于大米中MMA的含量极低[18],所形成的氢化物甲基胂不影响iAs的测定;DMA经氢化物反应(3)可生成弱挥发性二甲胂((CH3)2AsH,沸点35 ℃),相比As(III)和MMA,其信号强度较低,随着盐酸浓度的增大,DMA的信号强度逐渐减小,当盐酸达到4 mol/L,DMA的信号强度保持在最低水平,表明DMA氢化物反应在高浓度盐酸介质中被抑制。因此,本实验选择5 mol/L盐酸作为HG的载流介质,确保了iAs处于高信号强度而DMA处于低信号强度。
固定盐酸浓度为5 mol/L,考察硼氢化钠质量浓度变化对不同形态砷信号强度的影响。从图2b可以看出,As(III)和MMA的信号强度均随硼氢化钠溶液质量浓度的增大而增大,而DMA的信号强度很低且基本无变化,表明增大硼氢化钠溶液质量浓度有利于As(III)和MMA的氢化物反应,但对DMA的氢化物反应无影响。当硼氢化钠溶液质量浓度达到2 g/100 mL后,As(III)的信号强度不再增大,DMA的信号强度仍然保持低水平,MMA的信号强度仍然继续增大。由于大米中MMA的含量极低,仅需关注As(III)和DMA信号强度的变化。本实验选择硼氢化钠溶液质量浓度为2 g/100 mL,确保As(III)保持高信号强度而DMA的信号强度处于极低水平。

图2 盐酸浓度(a)和硼氢化钠质量浓度(b)对不同形态砷信号的影响Fig. 2 Effect of HCl concentration (a) and NaBH4 concentration (b) on the signal intensity of different arsenic species
2.2 质谱干扰及消除
在盐酸介质中,砷的唯一同位素75As会受到40Ar35Cl和40Ca35Cl的严重干扰[27],当样品中稀土元素Sm和Nd含量较高时,还会受到Sm和Nd所形成的双电荷离子(150Sm++和150Nd++)干扰[28]。He碰撞模式是基于四极杆ICP-MS最通用的消除质谱干扰方式,能消除大量多原子离子所形成的干扰,不能消除双电荷离子干扰,当样品中Sm和Nd含量较低,所形成的双电荷离子150Sm++和150Nd++对75As+的干扰可以忽略不计时,采用He碰撞模式可以消除40Ar35Cl和40Ca35Cl的干扰,但在碰撞过程中75As+不可避免地发生能量损失,影响75As的分析灵敏度,尤其是分析样品中超痕量As会影响结果的准确性。在ICP-MS/MS的MS/MS模式,设置Q1的m/z为75,仅允许m/z为75的离子(75As+、40Ar35Cl+、40Ca35Cl+、150Sm++、150Nd++)进入CRC,将来自ICP的其他大量离子阻止在CRC外,向CRC内通入O2为反应气,75As+与O2发生质量转移反应(75As++O2→75As16O++O,反应焓(ΔHr)=-0.63 eV),而40Ar35Cl+、40Ca35Cl+、150Sm++、150Nd++均不与O2反应,设置Q2的m/z为91,将75As+通过质量转移为75As16O+进行测定[29]。本实验在MS/MS模式下,选择O2为反应气,利用75As+与O2发生质量转移反应消除干扰,考察了不同O2流速下75As16O+背景等效浓度(background equivalent concentration,BEC)的变化情况,当O2流速达到0.30 mL/min时,75As16O+的BEC最小,本实验选择O2反应气的最佳流速为0.30 mL/min。
2.3 方法的线性与检出限
采用ICP-MS/MS对系列砷标准溶液进行测定,以砷信号强度与内标元素铑信号强度的比值(y,相对信号强度)与对应的砷标准溶液质量浓度(x,μg/L)进行线性回归,得到砷的校准曲线为y=1.1×10-3x+9.3×10-5,线性相关系数R=0.999 9,表明方法的线性良好;分别以空白溶液(酸提取法)连续测定10 次的3 倍和10 倍标准差所对应质量浓度为仪器的检出限(limit of detection,LOD)和定量限(limit of quantification,LOQ),砷的LOD为0.004 μg/L,LOQ为0.013 μg/L,将LOD乘以200(稀释因子)换算得到方法的检出限为0.8 μg/kg。
2.4 HG-ICP-MS/MS与HPLC-ICP-MS/MS的对比分析
采用HG-ICP-MS/MS对标准参考物质GBW(E)100348a(大米粉)、GBW(E)100349a(大米粉)、NIST SRM1568b(米粉)中的iAs进行测定,并采用ICP-MS/MS和HPLC-ICP-MS/MS分别对标准参考物质中的总砷和不同形态的砷进行测定,每个标准参考物质平行测定6 次,结果见表1。通过HPLC-ICP-MS/MS的测定结果可以看出,大米中砷的主要存在形态为iAs和DMA,而MMA的含量极低,与文献[18]报道结果一致。采用HG-ICP-MS/MS测定标准参考物质中iAs的含量与HPLC-ICP-MS/MS的测定结果基本一致,并与标准参考物质的认定值吻合,表明通过控制HG条件(5 mol/L盐酸和2 g/100 mL硼氢化钠溶液)能选择性将iAs完全转化为AsH3,抑制DMA形成二甲胂,虽然大米中低含量的MMA能发生氢化物反应,但由于所形成的甲基胂含量太低不影响AsH3的测定,从而实现了大米中iAs含量的准确测定。HG-ICP-MS/MS在4 min内可重复测定样品溶液5 次,而HPLC-ICP-MS/MS在10 min内仅能重复测定样品溶液1 次,由于HPLC-ICP-MS/MS数据处理更为复杂,因此,HG-ICP-MS/MS特别适合大批量样品的高通量分析。

表1 标准参考物质中砷的分析结果(n=6)Table 1 Analytical results of arsenic in standard reference materials (n = 6) μg/kg
2.5 样品分析
采用HG-ICP-MS/MS分别测定10 种大米(湖南籼米、湖南粳米、湖南糯米、江西籼米、重庆籼米、重庆粳米、东北粳米、泰国茉莉香米、日本米、柬埔寨茉莉香米)中iAs含量,同时采用国标法(GB 5009.11—2014《食品中总砷及无机砷的测定》)进行对比分析[30],每个样品重复测定6 次。从表2可以看出,10 种大米中iAs含量在58.7~122 μg/kg之间,相对标准偏差(relative standard deviation,RSD)在1.9%~4.5%之间,其中湖南粳米iAs含量最高,重庆籼米iAs含量最低。采用HG-ICPMS/MS分析结果与国标法基本一致,表明无需使用色谱技术对大米中砷进行形态分离,仅利用HG技术即可选择性分离大米中的iAs,从而实现大米中iAs的准确测定。参照GB 2762—2017规定大米中iAs含量限量200 μg/kg的指标,10 种大米中iAs含量均低于国家标准限量值。
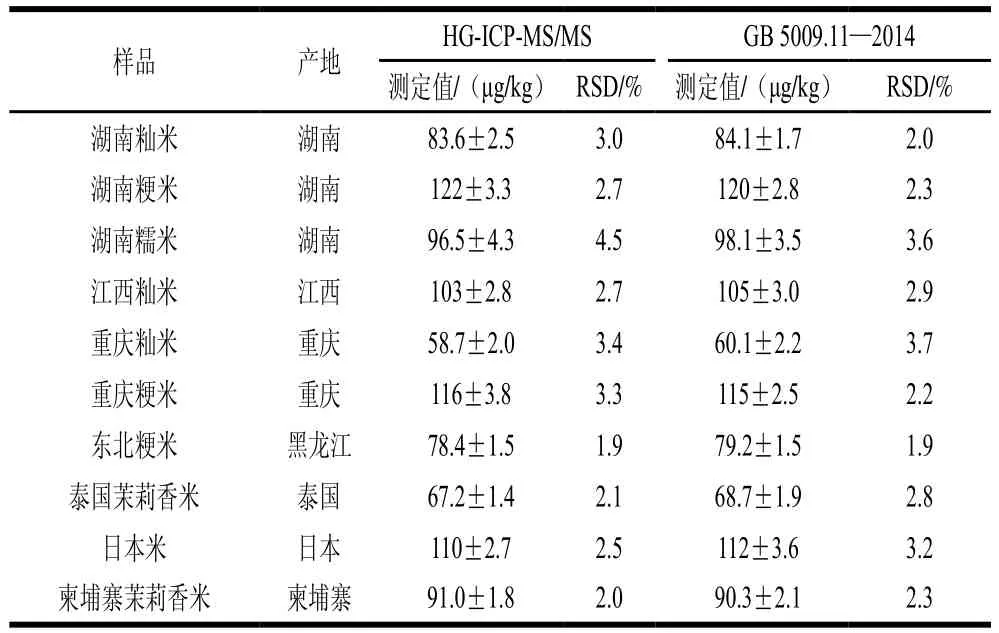
表2 10 种大米样品中iAs的分析结果(n=6)Table 2 Analytical results of inorganic arsenic contents in rice samples (n = 6)
3 结 论
基于大米中砷的主要存在形态为iAs和DMA,通过优化HG条件,选择性地将iAs转化为AsH3, 而DMA未发生氢化物反应或发生反应形成了挥发性较弱的二甲胂,从而实现大米中iAs与oAs的分离;利用ICP-MS/MS的O2反应模式,使砷发生质谱转移消除干扰。通过与HPLCICP-MS/MS分析结果和标准参考物质的认定值进行比较,发现该方法具有操作简单、分析速度快、灵敏度高、准确性好、精密度高的特点,其最大的优势是无需使用色谱技术进行砷的形态分离也能单独测定大米中iAs的含量。对10 种大米样品中的分析结果表明,所有样品中iAs含量均没超标,该方法分析能力可满足大米中iAs的限定标准要求。
