佛甲草的质量标准研究
2022-03-30黄玮李翔宇赵彩云
黄玮 李翔宇 赵彩云




【摘 要】 目的:制定佛甲草饮片质量标准。方法:采用显微鉴别、薄层色谱法对佛甲草饮片进行鉴别,按2015年版《中国药典》(四部)通则进行水分、总灰分、酸不溶性灰分和浸出物的测定,采用高效液相色谱法测定其槲皮素、山柰素和异鼠李素的含量。结果:样品的显微特征明显,薄层色谱鉴别斑点清晰,专属性强;7批样品水分含量为8.04%~9.73%,总灰分含量为15.07%~20.53%,酸不溶性灰分5.12%~8.99%,水溶性浸出物含量为25.42%~40.12%;槲皮素、山奈素和异鼠李素3个成分的线性关系良好,精密度、稳定性和重复性的RSD均低于2.0%,加样回收率分别为98.33%、98.92%和97.96%,RSD均小于2.0%(n=6);3种成分的线性关系均良好(r≥0.9990) 结论:方法准确稳定,可用于佛甲草的质量控制。初步拟定佛甲草水分不得过11.0%,酸不溶性灰分不得过9.0%,浸出物不得少于24.0%,槲皮素含量不得少于0.025%。
【关键词】 佛甲草;质量标准;显微鉴别;薄层色谱法;含量测定
【中图分类号】R282 【文献标志码】 A 【文章编号】1007-8517(2022)03-0046-05
Study on the Quality Standard of Sedilinearis Herba
HUANG Wei1 LIN Xiangyu2 ZHAO Caiyun1
1.Xuzhou food and Drug Administration and inspection center, Xuzhou 221006,China;
2. Xuzhou Medical Univercity, Xuzhou 221006,China
Abstract:Objective To establish the quality standard of Sedilinearis Herba. Methods Microscopic identification,thin layer chromatography(TLC) were carried out, According to the corresponding methods in 2015 edition of Chinese Pharmacopoeia(Part Ⅳ), the contents of moisture, total ash and doluble extractive from 7 batches of Sedilinearis Herba were determined. The contents of quercetin, kaempferol and isorhamnetin were determined by high performance liquid chromatography(HPLC).Results The microseopic characteristics of Sedilinearis Herba were described in detail. TLC spots were clear and the specificity was strong.The contents of moisture, total ash, acid insoluble ash,and soluble extract from samples were 8.04%~9.73%,15.07%~20.53%, 5.12%~8.99%,25.42%~40.12%, respectively.The linear relationships of quercitrin, kaempferol and isorhamnetin were all good., and the RSDs were all less than 2.0%. The recovery rates of the 3 components were 98.33%,98.92% and 97.96%, and the RSDs were all less than 2.0%(n=6); the linear ralationships of the 3 components were all good(r≥0.9990).Conclusions This method is accurate and stable, which can be used for the quality control of Sedilinearis Herba. It is preliminarily proposed that moisture and acid insoluble ash content should not exceed 11.0% and 9.0%, and extract and quercetin content should not be less than 24.0% and 0.025% respectively.
Key words:Sedilinearis Herba;Quality Standard;Microscopic Identification;Thin Layer Chromatography;Content Determination
佛甲草為景天科植物佛甲草Sedum lineae Thunb.的干燥全草 。主要分布于中南及江苏、浙江、安徽、福建、江西、四川、贵州、云南、陕西、甘肃、台湾等地[1]。有清热解毒、消肿止血等功效。用于咽喉肿痛、目赤、痢疾、丹毒、带状疱疹、痈肿、烫、火伤和外伤出血[2] 。现收载于《江苏省中药饮片炮制规范》2002年版,原标准只有性状鉴别,目前尚无有关佛甲草质量控制方面的文献报道,为了更好地控制该饮片的质量和安全性,结合参考文献[3-5],本研究通过增加显微鉴别、薄层鉴别、常规检查、浸出物测定及以槲皮素、山奈素和异鼠李素作为指标成分进行含量测定,以期建立完善的质量标准,以便控制佛甲草饮片的质量。
1 仪器与试药
1.1 仪器 FW177高速万能粉碎机(北京市永光明医疗仪器有限公司);LEICA DM 2500透射光显微成像系统(德国莱卡公司);XSR205电子天平(瑞士Metter公司,精度十万分之一);101A-1E型电热鼓风干燥箱(上海实验仪器厂有限公司);SX2-5-12型箱式电阻炉(天津市华北实验仪器有限公司);HH-6数显恒温水浴锅(常州国华电器有限公司);Waters e2695高效液相色谱仪(包括Empower3工作站,四元梯度泵,2998PDA检测器,自动进样器和柱温箱),均购自于美国Waters公司。
1.2 样品与试药 槲皮素对照品(批号:100081-200907,纯度为97.4%),山奈素对照品(批号:110861-201611,纯度为95.5%),异鼠李素对照品(批号:110860-201611,纯度为99.8%),均购于中国食品药品检定研究院;佛甲草对照药材(自制);甲醇为色谱纯(Fish公司),水为超纯水,其他试剂均为分析纯(国药集团化学试剂有限公司)。7批佛甲草饮片由企业提供,经徐州市食品药品监督检验中心赵彩云主任中药师鉴定为佛甲草Sedum lineae Thunb.的干燥全草。详细信息见表1。
2 方法与结果
2.1 显微鉴别 本品粉末棕色。取本品粉末加水合氯醛试液加热透化装片,置显微镜下观察:叶上表皮细胞壁较平直,下表皮细胞壁常波状弯曲,气孔不定式。非腺毛单细胞,直径约20 μm。花粉粒近球形,表面可见颗粒状纹饰。纤维狭长而笔直,大多成束。草酸钙簇晶30~75 μm。导管多为螺纹导管 。如图1所示。
2.2 薄层鉴别 取供试品粉末1 g,加甲醇20 mL,超声处理20 min,滤过,滤液蒸干,残渣加甲醇2 mL溶解,作为供试品溶液。另取佛甲草对照药材1 g,同法制成对照药材溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)[6]57试验,吸取上述两种溶液各2 μL,分别点于同一硅胶G薄层板上,以甲苯-三氯甲烷(1∶1)为展开剂,展开,取出,晾干,喷以5%磷钼酸乙醇溶液,在105 ℃加热至斑点显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。如图2所示。
2.3 水分、总灰分、酸不溶性灰分测定 取佛甲草饮片粉末(过二号筛)2 g,精密称定,分别照《中国药典》2015年版四部通则0832项下水分测定法(第二法 烘干法)、通则2302项下总灰分和酸不溶性灰分测定法测定水分[6]103、总灰分和酸不溶性灰分[6]204。各批次饮片均平行操作3次,取平均值。结果显示,7批佛甲草的水分含量为8.04%~9.73%,平均值为9.07%,以平均值的120%设限,为10.88%,故暂定本品水分不得过11.0%。总灰分含量为15.07%~20.53%,平均值为17.87%,以平均值的120%设限,为21.44%,数值较高故暂定不收入正文。酸不溶性灰分含量为5.12%~8.99%,平均值为7.14%,以平均值的120%设限,为8.56%,故暂定本品酸不溶性灰分不得过9.0%。详见表2。
2.4 浸出物测定 取佛甲草饮片粉末(过二号筛)2 g,精密称定,照《中国药典》2015年版四部通则2201水溶性浸出物测定法项下的热浸法测定浸出物含量[6]202。 以干燥品计算供试品中水溶性浸出物的含量(%),结果7批佛甲草饮片水溶性浸出物含量为25.42%~40.12%,平均值为30.30%,以平均值的80%设限,为24.24%,故暂定本品水溶性浸出物不得少于24.0%。详见表2。
2.5 含量测定
2.5.1 色谱条件与系统适应性试验 色谱柱:C18(ZORBAX,XDB,250 mm×4.6 mm,5 μm),流动相:甲醇-0.4%磷酸溶液(45∶55),流速:1.0 mL/min,柱温:32 ℃,检测波长:360 nm,进样量10 μL。槲皮素、山柰素和异鼠李素峰与各自相邻峰的分离度均大于2.0,理论板数均大于5000。
2.5.2 对照品溶液 取槲皮素、山柰素和异鼠李素对照品适量,精密称定,分别100 mL量瓶中,加甲醇溶解并定容至刻度,制备各单一对照品母液。分别精密量取一定量的各对照品母液,置同一50 mL量瓶中,用甲醇稀释制成每1毫升含槲皮素40.87 μg、山柰素5.75 μg和异鼠李素5.92 μg的混合对照溶液。
2.5.3 供试品溶液 取本品2.5 g,精密称定,置具塞锥形瓶中,精密加入甲醇-30%盐酸溶液(4∶1)25 mL,称定重量,置水浴中加热回流30 min,迅速冷却至室温,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.5.4 阴性样品溶液 取制备供试品溶液的溶剂,按照供试品溶液制备方法制备阴性样品溶液。
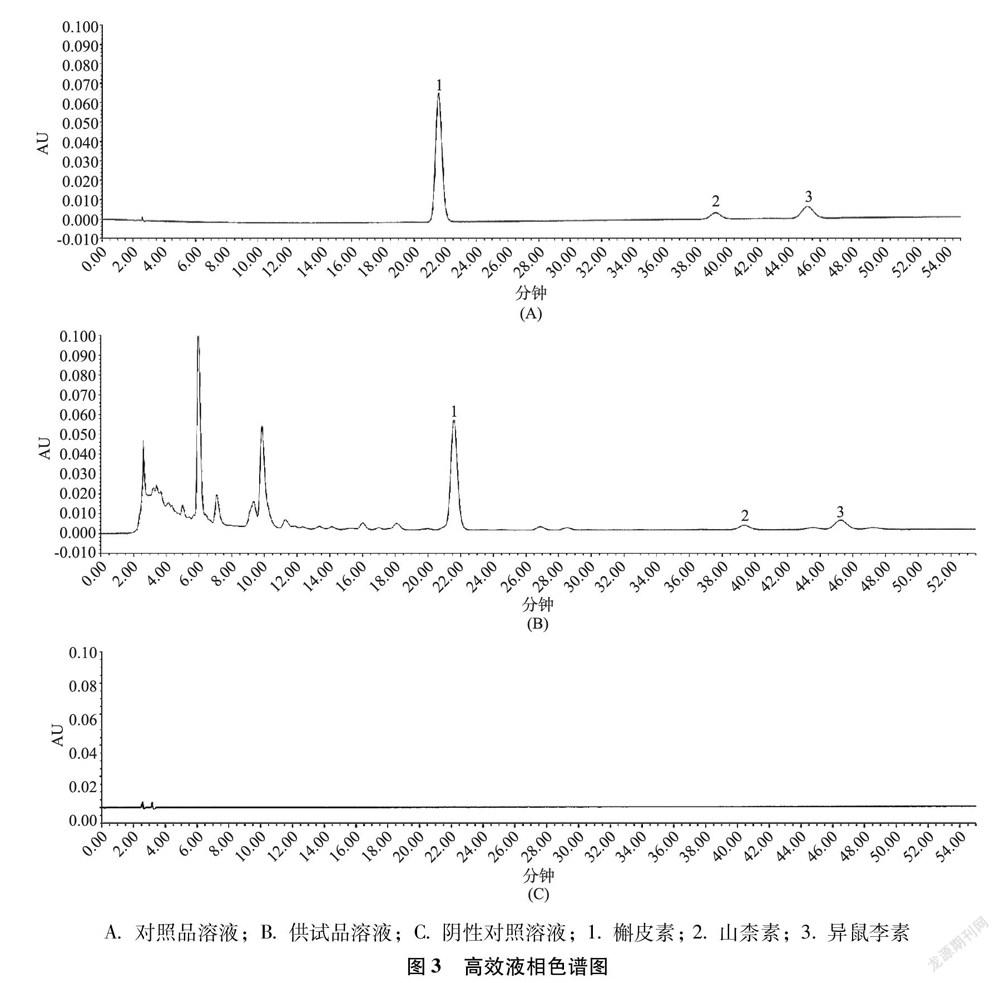
2.5.5 系统适应性试验 分别吸取对照品溶液、供试品溶液和阴性样品溶液各10 μL,按“2.5.1”项下色谱条件进行测定,记录色谱图,结果显示,供试品色谱中槲皮素、山柰素和异鼠李素与各自相邻峰的分离度均大于2.0,理论板数均大于5000,阴性样品无干扰。色谱图如图3所示。
2.5.6 定量限与检测限考察 分别精密量取“2.5.2”项下对照品溶液适量,以甲醇倍比稀释,并按“2.5.1”项下色谱条件进样测定,以信噪比为10∶1和3∶1分别计算3种待测成分的定量限和检测限。结果显示槲皮素、山奈素和异鼠李素的定量限分别为0.0163 μg/mL、0.0230 μg/mL、0.0237 μg/mL,检测限分别为0.006 μg/mL、0.0078 μg/mL、0.0079 μg/mL。
2.5.7 线性关系考察 分别精密量取“2.5.2”项下对照品溶液2、5、10、15、20、25 μL, 按“2.5.1”项下色谱条件进行测定,记录峰面积,以峰面积(Y)为纵坐标,进样量(X, μg)为横坐标进行直线回归,得回归方程: Y(槲皮素)=4.0684×106X-2.1006×103(r=0.9999,n=6); Y(山奈素)=4.6136×106X+7.6703×103 (r=0.9993,n=6);Y(異鼠李素)=4.3187×106X+6.9922×103(r=0.9990,n=6),槲皮素进样量在0.08173~1.2260 μg,山柰素进样量在0.01151~0.1726 μg,异鼠李素进样量在0.01184~0.1776 μg的范围内线性关系良好。
2.5.8 精密度考察 取“2.5.2”项下对照品溶液,按“2.5.1”项下色谱条连续进样6次,测定面积,结果槲皮素平均峰面积为1655646,RSD为0.28%(n=6),山奈素峰平均峰面积为266269,RSD为1.01%(n=6),异鼠李素平均峰面积为259635,RSD为1.68 %(n=6),表明仪器精密度良好。
2.5.9稳定性试验 取同一批供试品溶液(批号:20151210),按“2.5.1”项下色谱条件进行测定,分别在0,2,4,8,12,24 h进样,测定峰面积,结果槲皮素平均峰面积为1664001,RSD为0.41%(n=6),山柰素平均峰面积为114870,RSD为1.67%(n=6),异鼠李素平均峰面积为261482,RSD为1.61%(n=6),表明供试品溶液在24 h内稳定。
2.5.10 重现性试验 取同一批号(批号:20151210)样品6份,按“2.5.3”项下供试品溶液制备方法制备供试液,再按“2.5.1”项下色谱条件进样测定,结果槲皮素、山柰素和异鼠李素的平均含量分别为0.4057 mg/g、0.0229 mg/g和0.0577 mg/g,RSD分别为1.77%、1.97%和1.86%(n=6),表明方法的重现性良好。
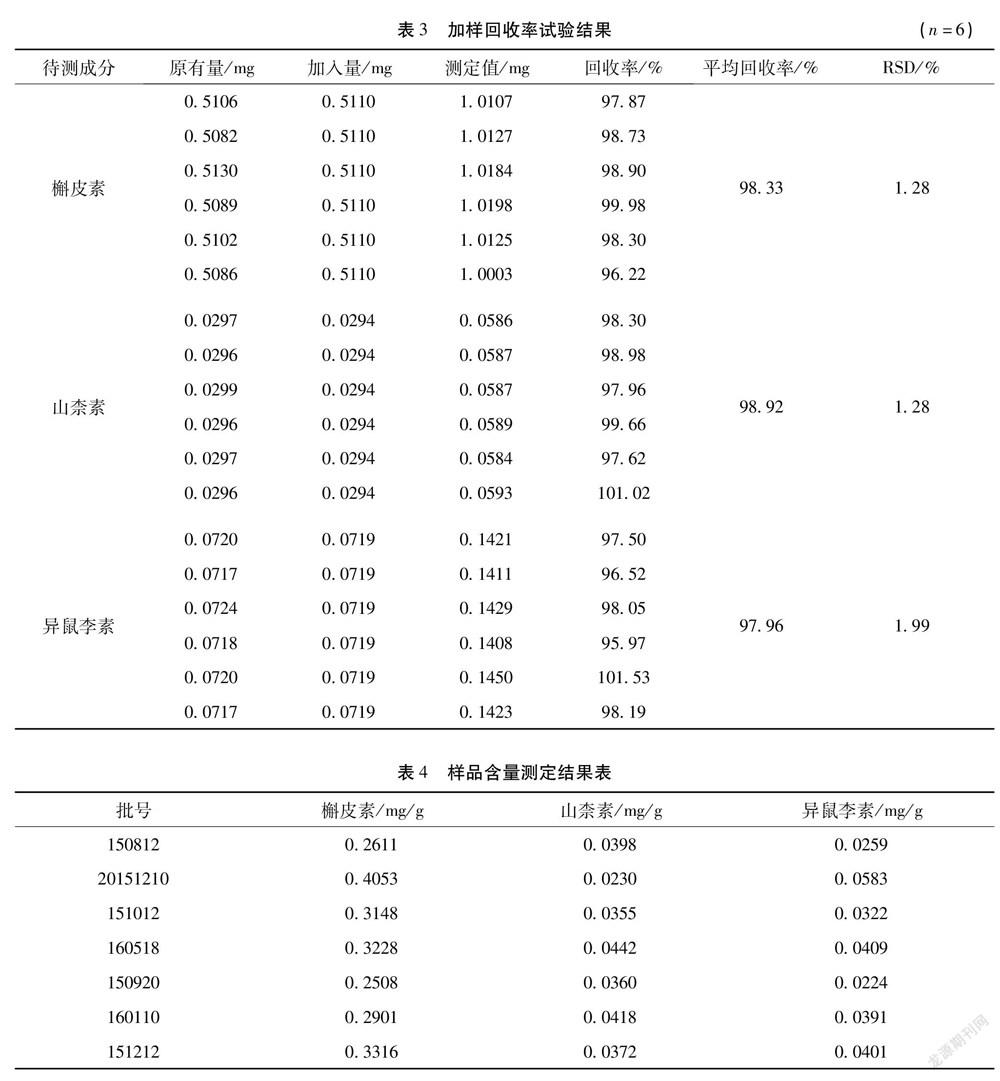
2.5.11 加样回收试验 精密量取已知含量的样品(批号:20151210,槲皮素的平均含量为0.4053 mg/g,山柰素的平均含量为0.0230 mg/g, 异鼠李素的平均含量为0.0583 mg/g)约1.25 g,共6份,精密称定,置具塞锥形瓶中,分别精密加入槲皮素对照品溶液(0.1022 mg/mL)5 mL、山柰素对照品溶液(0.01471 mg/mL)2mL和异鼠李素对照品溶液(0.02396 mg/mL)3 mL,按“2.5.3” 项下供试品溶液制备方法制备供试品溶液,再按“2.5.1”项下色谱条件进行测定,分别测定峰面积并计算加样回收率。结果见表3。
2.5.12 样品测定 分别取各批次饮片细粉适量,按“2.5.3”项下供试品溶液制备方法制备供试液,再按“2.5.1”项下色谱条件进样测定,记录色谱图,并根据标准曲线计算3种成分含量,结果按干燥品计算。见表4。
3 讨论
在薄层色谱鉴别研究中考察了甲苯-三氯甲烷(1∶1)、环己烷-乙酸乙酯(40∶1)为展开剂进行薄层层析,结果甲苯-三氯甲烷(1∶1)为展开剂,层析的结果较好,斑点清晰;不同薄层板(Merck硅胶G板、青岛海洋硅胶G 板、自制硅胶G层板)进行比较,结果不同薄层板,薄层色谱分离效果均好,斑点清晰;不同温、湿度条件(t:5 ℃,RH:30%;t:18 ℃,RH:40%;t:23 ℃,RH:50%))及稳定性(0、2、8、24 h)试验,结果在三种温湿度条件下薄层色谱结果均稳定,斑点清晰,供试品溶液经放置24 h后,层析结果依然稳定,斑点清晰。结果表明该方法可行。
浸出物含量测定中,分别采用不同浸出方法(热浸法、冷浸法),不同溶剂(乙醇、稀乙醇、 70%乙醇、30%乙醇、水)进行了比较,结果表明,采用热浸法,以水为溶剂,测得浸出物量最高。故选择水为溶剂,热浸法进行浸出物测定。
含量测定中,流动相的选择根据有关参考文献[7]报道槲皮素、山柰素与异鼠李素的HPLC测定方法,流动相为甲醇-0.4%磷酸溶液(50∶50)进行试验,发现供试品溶液中异鼠李素峰与前后峰没完全分开,故提高流动相中水相的比例,结果各峰分离度较好,所以最终确定流动相为甲醇-0.4%磷酸溶液(45∶55)。供试品制备方法的选择,对供试品回流温度、时间及加入盐酸浓度等影响因素进行了考察,结果加入甲醇-30%盐酸(4∶1)25 mL沸水浴回流30 min可酸解完全,样品重复性高。本研究建立的含量测定方法能同时测定佛甲草中槲皮素、山柰素和异鼠李素的含量,其中槲皮素含量最高,占测定的3种成分总含量的70%左右。据文献[8]报道,槲皮素具有抗氧化、抗病毒和抗炎的作用,与佛甲草具有清热解毒、消肿止血等功效一致。因此,选择槲皮素作为该饮片含量限定的指标成分,7批样品槲皮素的平均含量为0.031%, 以平均值的80%设限,为0.025%, 故暂定本品含槲皮素不得低于0.025%。
参考文献
[1]国家中医药管理局《中华本草》编委会.中华本草[M].上海:上海科学技术出版社,1999:2416-2417.
[2]江苏省药品监督管理局.江苏省中药饮片炮制规范[S]. 南京:江苏科学技术出版社: 2002:242.
[3]梅青.木芙蓉叶和佛甲草的鉴定与质量评价研究[D].武汉:中南民族大学,2014.
[4]王璐瑶.佛甲草等景天属植物药中黄酮类物质的抗肿瘤活性研究及含量测定[D]. 武汉:中南民族大学,2013.
[5]张莉霞,刘东彦,石晓峰,等. HPLP法同時测定雪松果中槲皮素、山奈素与异鼠李素的含量[J].中华中医药杂志:2018 (4):1540-1542.
[6]国家药典委员会.中华人民共和国药典:四部[M].2015年版.北京:中国医药科技出版社:2015:59,114,232,234.
[7]汪正宇.垂盆草颗粒中槲皮素、山奈素与异鼠李素的HPLC测定方法研究[J].安徽医药,2015,19(8):1474-1476.
[8]马纳,李亚静,范吉平.槲皮素药理作用研究进展[J].辽宁中医药大学学报,2018(8):221-224.
(收稿日期:2021-06-01 编辑:刘 斌)
作者简介:黄玮(1981-),女,汉族,本科,副主任中药师,研究方向为中药材及中成药的检验及质量研究。E-mail:316243060@qq.com
