硅碳复合结构对锂离子电池负极电化学性能的影响
2022-03-29田晓华余晨露郑瀚孙卓张哲娟朴贤卿
田晓华 余晨露 郑瀚 孙卓 张哲娟 朴贤卿

关键词:亚微米硅;硅废料;硅碳负极材料;锂离子电池;联结结构
中图分类号:O649.4 文献标志码:A DOI:10.3969/j.issn.1000-5641.2022.01.007
0引言
近年来,随着储能技术的发展,锂离子电池正在逐渐成为可穿戴设备、电动汽车和太阳能设备的新兴储能媒介[1].目前,大量商业化生产的锂离子电池主要以石墨为负极材料,其最大比容量为372mAh/g[2-3],不能满足当前对于锂离子电池高容量、长寿命的需求[4].硅材料以其高达4200mAh/g[5-6]的理论比容量成为最有应用前景的锂离子电池负极材料.然而,硅在脱嵌锂的过程中高达300%~400%[1,7–9]的体积膨胀,易导致电极破裂和材料间的电接触失效,Si的破裂粉化会造成固态电解质界面(SolidElectrolyte Interphase,SEI)膜不断生成,恶性消耗电池内部的活性锂[7,10],也限制了其作为锂离子电池负极材料在实际应用中的进展.
针对硅负极的膨胀问题,目前研究最多且有效的方案是硅颗粒的纳米化.将硅颗粒尺寸减小至150nm以下时[11-12],硅颗粒在脱嵌锂过程中的龟裂现象就会大幅降低.但是,纳米级硅颗粒在应用中存在弊端.例如:①较大的比表面积使得负极首效偏低;②负极制作过程中纳米硅的表面氧化要比大尺寸的硅更明显,从而难以体现硅基负极的容量优势.因此,更多的研究专注于材料复合对纳米硅负极电化学性能的影响[13–16],硅碳复合材料一度成为锂离子电池硅基负极材料的研究热点.另外,虽然纳米硅颗粒不易皲裂粉化、循环性能优越,但是纳米硅易团聚、制备成本高、工艺复杂,难以实际应用.
前期,课题组余晨露等[17]尝试以废硅泥中尺寸较大的亚微米硅颗粒作为硅原料,采用不同种类的水相碳氢化合物碳源,通过简单的水相混合、低温烧结工艺制备出硅碳复合材料.研究结果证明,壳聚糖热解硬碳与亚微米硅复合策略的有效性,一定程度上提高了硅基负极的稳定性,但是存在碳的包裹量低(两次包裹下才能基本达到WSi:WC=8:2(wt%)的目标)、硅氧化程度高导致负极容量低的问题.本研究改进制备工序,通过单次包裹制备高碳硅比的复合物,以期通过低能耗方式得到高容量的硅碳负极材料,并研究石墨的添加对复合硅基负极的电化学性能及稳定性的影响.
1实验1.1材料制备
晶硅太阳能电池生产过程中的晶硅切削废料(主要成分包括硅颗粒52%、水46%、表面活性剂2%)用无水乙醇离心清洗3次,经60℃干燥后获得硅粉.配置100mL浓度为2%的乙酸溶液,称取2g硅粉加入上述溶液中,经搅拌分散均匀.最后,按照Si∶C元素质量比约为4∶1,在上述悬浊液中加入1.11g的壳聚糖,乙酸使壳聚糖降解形成分子量更小的低聚壳聚糖,从而提高了其水溶性.搅拌24h后,升温至70℃搅拌蒸发水分,获得的基本干燥的产物为硅碳复合前驱体.将Si@CTS前驱体置于管式炉中,在氮气的保护下升温至900℃(5℃/min)并保温2h,待自然冷却后,取出并研磨得到均匀的硅/硬碳复合材料(Si@CTS).将获得的硅/硬碳复合材料Si@CTS与石墨研磨混合均匀后,即得到硅/硬碳/石墨复合材料(Si@CTS/G),其中石墨占50%(wt%).
1.2材料表征
采用带铜靶Ka射线(Panalytica,PRO PW3040/60,电压40kV,电流40mA,波长1.5418?,扫描范围(10°~80°))的X射线衍射仪(X-ray Powder Diffractometer,XRD)分析了材料的物相结构.采用装有Bruker QUANTAX-400能谱系统(Energy Dispersive Spectrometer,EDS)的扫描电子显微镜(Scanning Electron Microscope,SEM,JEOLJSM-7610F)分析样品的形貌和元素分布.采用高分辨透射电镜(High Resolution-Transmission Electron Microscope,HR-TEM,FEI Tecnai G2 F20)分析样品的结构特征.
1.3 电极制备及性能测试
课题组前期研究[17]发现,液相包裹的硅碳复合材料可以与传统的石墨负极材料通过简单的物理混合制备出具有高稳定性和高容量的锂离子电池负极.因此,分别以Si@CTS和Si@CTS混合人造石墨(G)作为锂离子电池负极,研究Si@CTS作为活性物质的性能及应用价值.以去离子水为分散剂,分别将Si@CTS、Si@CTS/G和导电剂(SP)、粘结剂(聚丙烯酸,PAA-1)按照5∶1∶2的比例混合,搅拌24h制成均匀的负极浆料.将得到的浆料通过涂覆机均匀涂布在铜箔上,经精密鼓风干燥箱60℃干燥6h后,再80℃干燥6h.干燥后的极片于辊压机中辊压后,裁成13mm的圆形电极片,电极片的活性物质负载量分别为2.89mg/片和2.99mg/片.在手套箱中,以金屬锂片作为对电极,以Celgard2400聚丙烯多孔膜作为隔膜,1.15mol/LLiPF6的碳酸乙烯酯(EthyleneCarbonate,EC)、碳酸甲基乙基酯(Ethyl Methyl Carbonate,EMC)、碳酸二甲酯(Dimethyl Carbonate,DMC)(体积比VEC∶VEMC∶VDMC=1∶1∶1)+10%氟代碳酸乙烯酯(Fluoroethylene Carbonate,FEC)溶液为电解液,组装成2032型纽扣型半电池.
电池恒流充放电测试通过CT-3001A电池测试系统(武汉蓝河)完成.为了获得稳定的SEI膜[18],在循环性能测试过程中,先在0.01C的倍率下活化10圈.然后,再采用0.1C的倍率进行循环性能测试(对于Si@CTS电极1C=3434.4mAh/g,对于Si@CTS/G电极1C=1903.2mAh/g).采用AutolabPGSTAT302N型电化学工作站进行循环伏安(Cyclic Voltammetry,CV,0.1mV/s)和电化学交流阻抗普(Electrochemical Impedance Spectroscopy,EIS,10–2~105Hz)测试,所有电化学测试均在室温环境下进行.
2结果与讨论
2.1材料结构形貌表征
图1是硅颗粒的表面形貌及XRD谱.图1(a)中Si颗粒的XRD衍射谱在28.4°、47.3°、56.1°、69.1°、76.4°处均有明显的衍射峰,对应于晶体硅的(111)、(220)、(311)、(400)、(331)特征峰[19].另外,在22°左右出现了一个较宽且微弱的峰,结合EDS-mapping图(图2)中的O元素分布可知,该峰为硅的氧化峰,说明原料中Si颗粒表面有弱氧化现象,存在SiO2[19].图1(b)为Si颗粒的SEM图.硅颗粒是晶硅太阳能电池切削所产生的,因此,硅颗粒形貌大多呈不规则片状,片的厚度为20~50nm,片的面尺寸较大且分布较宽,为200~600nm.片状硅颗粒表面粗糙度大,更易产生氧化,与XRD结果一致.
图3为硅(Si)、壳聚糖热解碳(CTS)、石墨(G)、Si@CTS和Si@CTS/G的XRD谱.石墨G的XRD衍射峰主要位于26.5°、42.3°、44.5°、54.6°和77.4°处,分别对应于C的(002)、(100)、(101)、(004)和(110)的特征峰.壳聚糖900℃热解所得产物CTS的XRD谱中,在24°和43°左右出现两个非常宽的馒头峰,说明CTS中石墨结构碳的排列明显是无序的,峰位向小角度偏移,说明CTS中碳层间距比G的大.Si@CTS的XRD谱中保有明显的Si特征峰,且中心峰位和峰宽没有明显变化,说明复合过程中,硅颗粒的晶体结构没有被破坏.Si@CTS的XRD谱与CTS相比,小角度处的馒头峰中心位置略左移,在23°左右,说明该峰是CTS的C(002)峰与SiO2的衍射峰重叠所得[13].
图4(a)是Si@CTS的SEM图,Si颗粒的片状结构不明显,颗粒间互相联结形成堆簇状结构,且堆簇的Si颗粒之间具有一定的孔隙,如图中虚线所示.联结结构是壳聚糖的热解碳产物,在硅片表面形成包覆,并组成硅碳二次颗粒.图4(b)和4(c)是Si@CTS的HRTEM图,图4(b)中红色实线所示区域没有明显的晶面取向,是无定形碳(CTS)复合层,厚度约为8nm.图4(c)为图4(b)方形实线区域的局部放大图,图中可以明显地观察到不同方向的Si的晶格条纹,其晶面间距约为0.311nm,对应晶体Si的(111)晶面.结合XRD和mapping测试结果认为,图4(c)中界面两侧的无明显晶面取向结构的部分,分别对应于CTS和SiO2.硅表面形成氧化层,具有亲水特征,会带有羟基基团,包覆过程中易与壳聚糖中的氨基形成氢键[20],进而有利于壳聚糖分子的粘连,实现互联结构的形成.
图5是Si@CTS与G经研磨后混合物的SEM图,添加的G是尺寸较大的层状结构,一般在5~10μm,较小尺寸的Si@CTS颗粒附着在G的表面和边缘,或填充在G的层状缝隙或断层凹槽处.
为了研究材料的比表面积和孔隙结构对负极性能的影响,对Si、Si@CTS和Si@CTS/G这3种材料进行了氮气等温吸脱附实验测试,得到氮气吸-脱附等温曲线图(图6).由图可知,Si表现为Ⅱ型氮气吸-脱附等温曲线,Si@CTS和Si@CTS/G都表现为Ⅳ型等温曲线,且在0.5P/Po(P为气体的真实压力,Po为气体在测量温度下的饱和蒸汽压)存在明显的回滞环,表明Si@CTS和Si@CTS/G材料中孔隙结构很不规整.采用Brunauer-Emmett-Teller(BET)方法对材料的比表面积进行分析,得到Si、Si@CTS和Si@CTS/G这3种材料的比表面积分别为43.37m2/g、12.03m2/g和9.34m2/g.由此可知,Si@CTS和Si@CTS/G材料由于CTS碳的包裹、黏附,形成新的复合结构,比表面积明显小于原材料Si.
2.2 材料电化学性能测试
为了进一步研究硅碳负极结构对储锂性能的影响,将Si@CTS、Si@CTS/G与课题组前期制备的壳聚糖二次包裹硅碳负极c2@Si(Si80%,C20%)和水热法制备硅碳石墨复合负极SCG0.2(Si45.5%,C9%,G45.5%)作为参比对象[17].不同负极在0.1C倍率下的充放电循环曲线如图7所示,相应的首圈和100圈比容量及库仑效率如表1所列.Si@CTS的首次充电比容量为1429.5mAh/g,放电比容量为1672.8mAh/g,首次库伦效率为85.45%,均远高于c2@Si和SCG0.2.
這主要是因为本工艺中壳聚糖热解形成的联结结构(图4(a))一方面降低了比表面积,有利于硅基负极材料首效的提高.另一方面,构建了导电网络,提升了Li+和电子的传导效率,进而提升了负极材料的比容量.经100圈循环后,Si@CTS的放电比容量为626.4mAh/g,衰减较明显.相比第11圈(0.1C倍率下的首圈)达到47.8%,说明Si@CTS稳定性不佳,主要是因为壳聚糖形成的无定形碳包覆层,在脱嵌锂过程中为Si的体积膨胀提供了一定的缓冲.但是,壳聚糖热解碳通过联结作用形成堆簇状硅碳二次颗粒,随着循环周期延长,锂离子的嵌脱不断增大二次颗粒的内应力,会引起较大尺寸的片状Si颗粒产生粉化等现象[21],从而导致容量的损失.为了提高稳定性,将Si@CTS与G混合,Si@CTS/G的首次充电比容量为962.7mAh/g,首次放电比容量为1138.5mAh/g,首次库伦效率为84.56%.循环100圈后,Si@CTS/G的放电比容量为698.6mAh/g,相比于第11圈(0.1C倍率下的首圈)容量衰减为25.4%,远小于Si@CTS电极的47.8%.Si@CTS分布在石墨颗粒的表面、缝隙和凹陷处(图5),层状石墨为Si@CTS提供了结构支撑,有利于应力释放,且提供了良好的导电性.同时,石墨也有助于构建较为稳定的SEI膜.因此,Si@CTS/G在获得较高容量的同时提升了负极材料的循环稳定性.但是,Si@CTS和Si@CTS/G首效相较于商业化石墨负极较低,主要原因是:①首次充放电时会在电极材料表面形成SEI膜造成锂离子的消耗[22-23];②锂离子不可逆地嵌入无定形碳造成锂离子的消耗[24].Si@CTS和Si@CTS/G的CV曲线如图8所示,测试扫速为0.1mV/s,扫描电压范围为0~1.5V.图8(a)为Si@CTS前5圈的CV曲线,第1圈时0.83V处有一个较宽的还原峰,这是电极表面形成了SEI膜造成的[25],在之后的扫描中该峰消失,表明经首次循环后,SEI膜已趋于稳定.负扫过程中,在0.2V左右出现的峰是Li+嵌入晶体Si形成了无定形的LixSi合金相[13].在正扫的过程中,首圈没有明显的峰,随着圈数增加,分别在0.34V和0.52V逐渐出现两个明显的氧化峰,对应LixSi的去合金化过程[17].图8(b)为Si@CTS/G前5圈的CV曲线,首圈在0.12V、0.2V、0.32V分别出现了还原峰,表明Li+嵌入石墨形成LiC6.在之后的循环中,在0.2V左右出现一个峰是由于Li嵌入晶体Si形成了无定形的LixSi合金相[13].正扫的过程中,首圈在0.22V和0.29V分别出现较明显的峰,对应Li+从LiC6中脱出.在之后几圈中,在0.31V和0.51V出现两个较为明显的峰,对应LixSi的去合金化过程[17].对比Si@CTS的CV曲线(图8(a))可以发现:Si@CTS/G的CV曲线(图8(b))的重合度要更高,说明石墨的协同作用使得Si@CTS/G具有更好的循环稳定性.
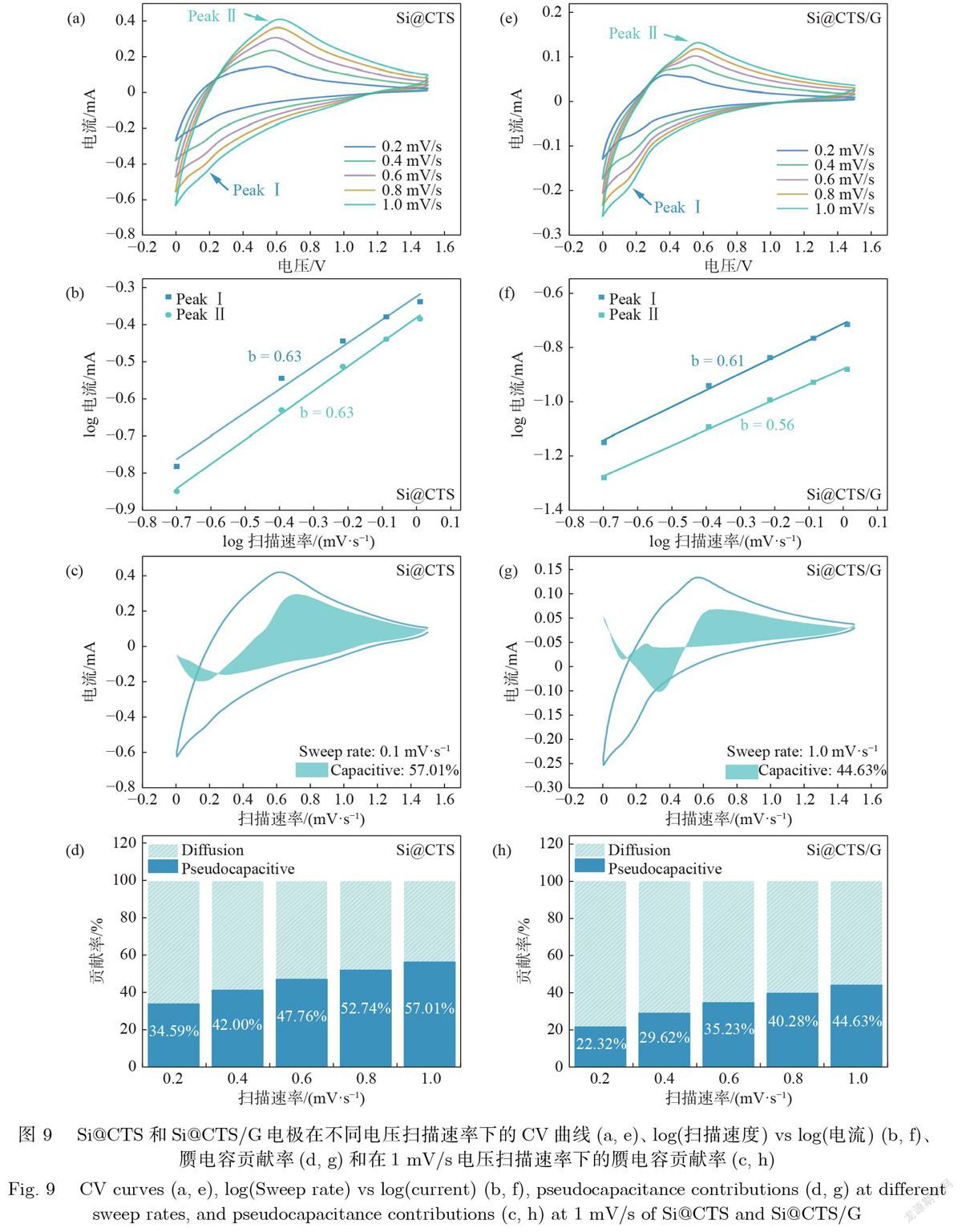
图9(a)和9(e)给出了在不同电压扫描速率下Si@CTS和Si@CTS/G的CV曲线,可以利用式(1)[25]对电极中赝电容行为进行探究.
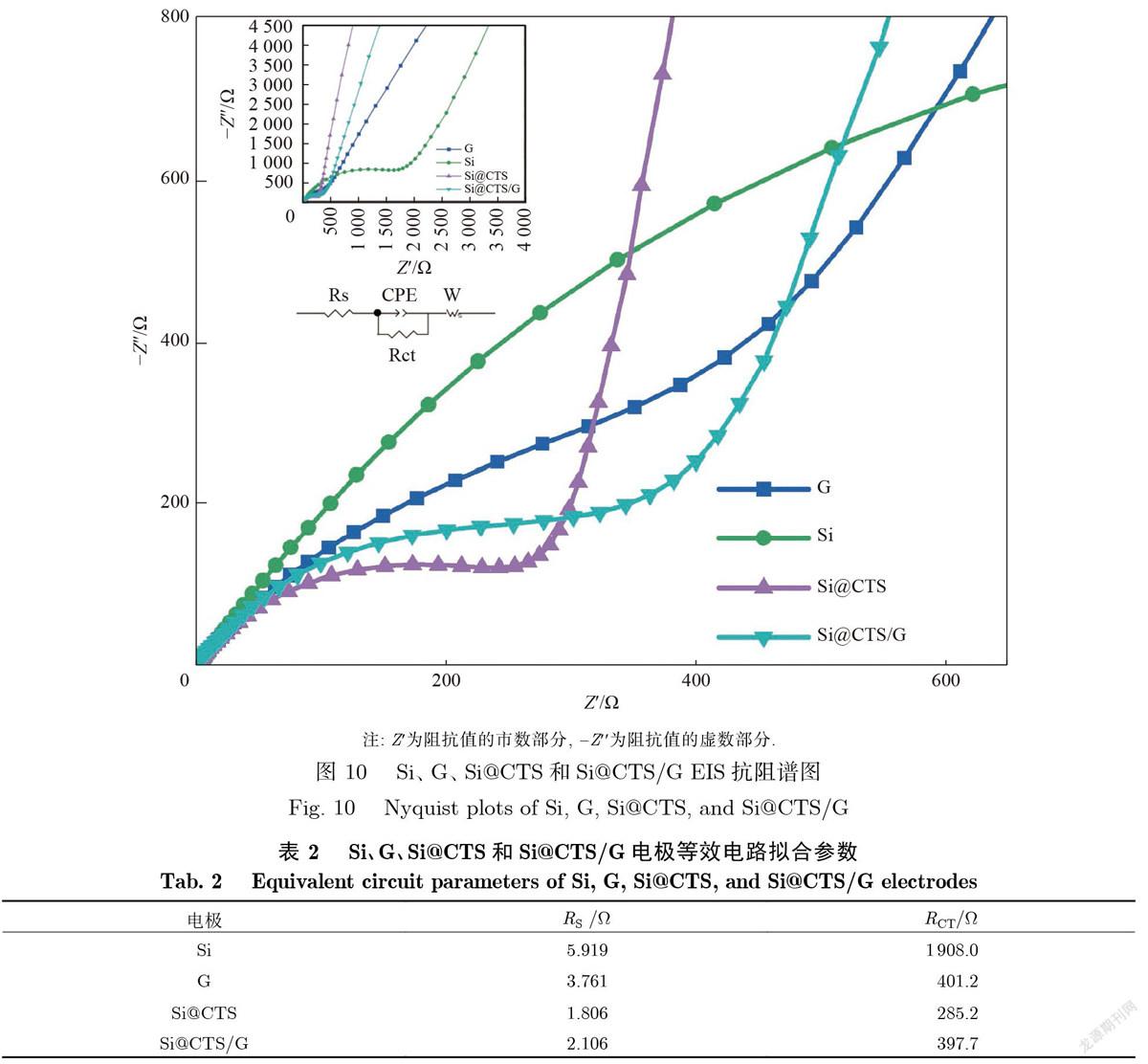
式中:为峰值电流,a,b为可调整参数,v为电压扫描速率,通过b的值可以确定电极中是否存在赝电容属性.当b=0.5时,电极材料表现为电池属性;当0.5 通过origin对logv和logi线性拟合求得斜率.图9(b)给出了Si@CTS电极中两个峰的b值,分别为0.63和0.66;同样,Si@CTS/G电极中两个峰的值分别为0.61和0.56(图9(f)).两个电极的b值都介于0.5和1之间,这说明两个电极都既存在电池属性也存在赝电容属性.特定电压扫描速率下的赝电容的贡献率可以通过式(3)计算得到. 式中:i(V)为赝电容的贡献率,v为特定电压扫描速率,k1;k2為可调参数.k1v和k2v分别代表了赝电容和扩散对电流的贡献.式(3)变形得到式(4): 同样地,利用origin对i(V)/v1/2和v1/2进行线性拟合得到k1,通过计算k1v可得到特定电压扫描速率下赝电容的贡献率.图9(c)和9(d)分别给出了在1.0mV/s的电压扫描速率下Si@CTS和Si@CTS/G电极中的赝电容贡献率,分别为57.01%和44.63%.图9(d)和9(h)分别给出了在其他电压扫描速率下Si@CTS和Si@CTS/G电极中的赝电容贡献率.可以发现,随着电压扫描速率的提高,赝电容的贡献率也在逐步提高. 图10给出了Si、G、Si@CTS和Si@CTS/G在循环前的EIS阻抗谱.高频曲线与横坐标轴的截距表示欧姆阻抗,用RS表示;高频区域为一个半圆,代表电荷在电极与电解液之间的转移阻抗,用RCT表示;低频区域为一段向上的直线,代表锂离子在活性材料中的扩散阻抗,用ZW表示.从图10可以看出,Si、G、Si@CTS和Si@CTS/G在高频区域为一个半圆,通过图中的等效电路分别对4种电极进行拟合,拟合结果如表2所列.其中,Si电极的RCT最大(~1908.0W),这是由于Si是半导体,导电性能不佳,电荷在电极与电解液之间的转移阻抗也就越大.Si@CTS电极RCT最低(~285.2W),说明Si复合CTS之后,电极的导电性有所改善,有利于电荷传输.本实验种采用的G电极RCT(~401.2W)较大,因此,Si@CTS/G电极的RCT(~397.7W)略大于Si@CTS. 综上所述,以低成本太阳能硅电池产线废硅泥为Si原料,通过工艺改良,在一次包裹工艺下制备出了具有孔隙与互联结构的Si@CTS硅碳复合材料.无定形碳层包裹不仅有效缓解Si的体积膨胀,还形成了互联结构,构建导电网络,提升了Si基负极的导电性,减小电荷在电极与电解液之间的转移阻抗.硅碳复合材料与石墨混合,制备的Si@CTS/G负极电极可保持较高的比容量和良好的循环稳定性,提升了硅基负极的实用性. 3结论 本文以太阳能电池产线回收得到的废硅泥为原料,以壳聚糖为碳源,在乙酸水溶液中,硅颗粒经壳聚糖水溶液单次包裹后,制备的硅碳复合材料Si@CTS形成了互联结构,并具有一定的孔隙.研究结果表明,孔隙和互联的Si@CTS负极首次库伦效率为85.45%,循环百圈后的放电比容量为626.4mAh/g,均优于c2@Si(38.5%,225.1mAh/g)[17].壳聚糖热解碳在硅表面包裹并粘结形成特殊的联结结构,为Si充放电过程中的体积膨胀提供支撑和容胀空间,从而在提高负极容量的同时,保证了负极的循环稳定性.将Si@CTS与石墨混合后,Si@CTS/G负极的循环稳定性显著提高,循环100圈后,放电比容量仍为698.6mAh/g,这是因为,较大尺寸的石墨为Si@CTS提供了结构支撑,增强了脱嵌锂过程中颗粒间的接触,有利于负极中生成较稳定的SEI膜.可见,通过改进制备工序、复合石墨,硅碳复合负极的容量和循环稳定性等电化学性能均得到优化,进一步提高了太阳能硅废材料在锂离子电池负极中的应用价值. (责任编辑: 张晶)
