催化强化低温等离子体降解甲苯的研究
2022-03-24王松王星敏
王松,王星敏,2
(1.重庆工商大学 环境与资源学院,重庆 400067;2.催化与环境新材料重庆市重点实验室,重庆 400067)
挥发性有机化合物(VOC)是大气污染的重要污染物之一,是城市光化学烟雾的前身。在以臭氧、细颗粒物和酸雨为特征的区域复合空气污染中也发挥着重要作用,并且是限制社会经济的可持续发展的瓶颈之一[1]。介质阻挡放电(DBD)与金属氧化物催化剂结合处理VOCs,受到愈来愈多研究员的关注。李党生等[2]利用等离子体和催化剂组合治理低浓度的苯,结果表明MnO2的催化效果比TiO2更佳;陆彬等[3]发现DBD与MnO2联用在提高苯的降解率的同时增加了CO2选择性。本文以低温等离子体与Mn催化剂结合,降解甲苯废气,拟达到提升甲苯降解率和减少尾气副产物的目标。
1 实验部分
1.1 材料与仪器
甲苯、乙酸锰、γ-Al2O3颗粒、二硫化碳均为分析纯;去离子水。
反应装置,自组装(DBD反应器为石英管,内外径分别为28,30 mm,长度为400 mm;选用不锈钢丝杆和八角星组成的锯齿尖端电极为高压极,接地极为铁丝网,均匀缠绕在反应器外壁,在反应器内部放电区域放置催化剂);CTP-2000k高压电源;Tektronix TSD 2014C示波器;7820A安捷伦高效气相色谱仪;JA500-M-IR在线高精度复合气体分析仪。
1.2 催化剂的制备及评价指标
采用直径为3~5 mm的γ-Al2O3颗粒作为载体,浸渍法制取催化剂。将γ-Al2O3载体浸入定量前驱体溶液,阴干24 h后放入烘箱中在120 ℃下烘干2 h,以5 ℃/min的升温速率分别升温在400~900 ℃下煅烧1.5~3.5 h,冷却后放入干燥器中备用。
采用气相色谱仪监测反应体系的甲苯质量浓度,根据公式(1)计算甲苯降解率(η,%)。
(1)
式中c1、c2——甲苯气体的进出口浓度,mg/m3。
1.3 均匀设计法优化制备参数

表1 U73因素及水平
2 结果与讨论
2.1 催化剂制备条件对甲苯降解效果的影响
2.1.1 负载含量对甲苯降解效果的影响 在气体流速为2 L/min,放电频率7.5 kHz条件下,对催化剂的负载含量进行讨论,实验结果见图1。
由图1可知,甲苯的降解率随电压的升高而增加,加入催化剂过后甲苯降解率高于空载(83.79%)。随着负载量的增加,甲苯的降解率升高,电压为13 kV 时,在负载量为5%时达到91.29%,随着负载含量进一步提升,甲苯降解效果逐渐下降;负载含量为20%时,甲苯的降解效率下降为85%。该结果的原因可能是,当Mn负载量低时,催化剂的相应活性中心将减少,并且催化性能将变差;然而,Mn的过量负载导致载体表面上的凹凸位置被活性成分过多的占据,这阻塞了内部孔并导致活性降低;当Mn含量为5%时,催化剂的结晶度最佳,晶体尺寸最小,催化活性最佳[4-6]。

图1 负载量对甲苯降解率的影响
2.1.2 煅烧温度对甲苯降解效果的影响 图2中显示出了催化剂煅烧温度对MnOx/γ-Al2O3催化剂对甲苯降解率的影响。
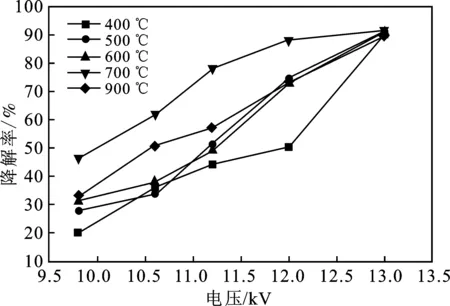
图2 温度对甲苯降解率的影响
由图2可知,随着煅烧温度的提高,甲苯降解率呈现升高后降低趋势,当温度升高为700 ℃时,甲苯的降解率最高达到了91.50%;之后又明显下降,当焙烧的温度为900 ℃时降解率为89.41%。主要原因是,当催化剂的煅烧温度低时,锰盐的活性成分在载体中不能完全分解;当过高的煅烧温度时会出现活性成分的烧结团聚现象[6-8],从而影响了催化效果。
2.1.3 煅烧时间对甲苯降解效果的影响 图3为不同焙烧时间的MnOx/γ-Al2O3催化剂对甲苯降解的影响。
由图3可知,甲苯的降解率随着煅烧时间的延长先增加然后降低。煅烧时间为180 min时,甲苯的降解率可达91.50%;煅烧的时间增加至210 min时,甲苯的降解效果降至88.09%。甲苯降解速率在不同的煅烧时间下为:180 min>150 min>120 min>210 min>90 min。 该结果可能是由于煅烧时间太短,活性成分前体不能完全分解,催化剂的活性成分含量很低;而煅烧的时间太长,催化剂的表面会被烧结,堵塞了部分活性位,使催化活性变低[9-10]。
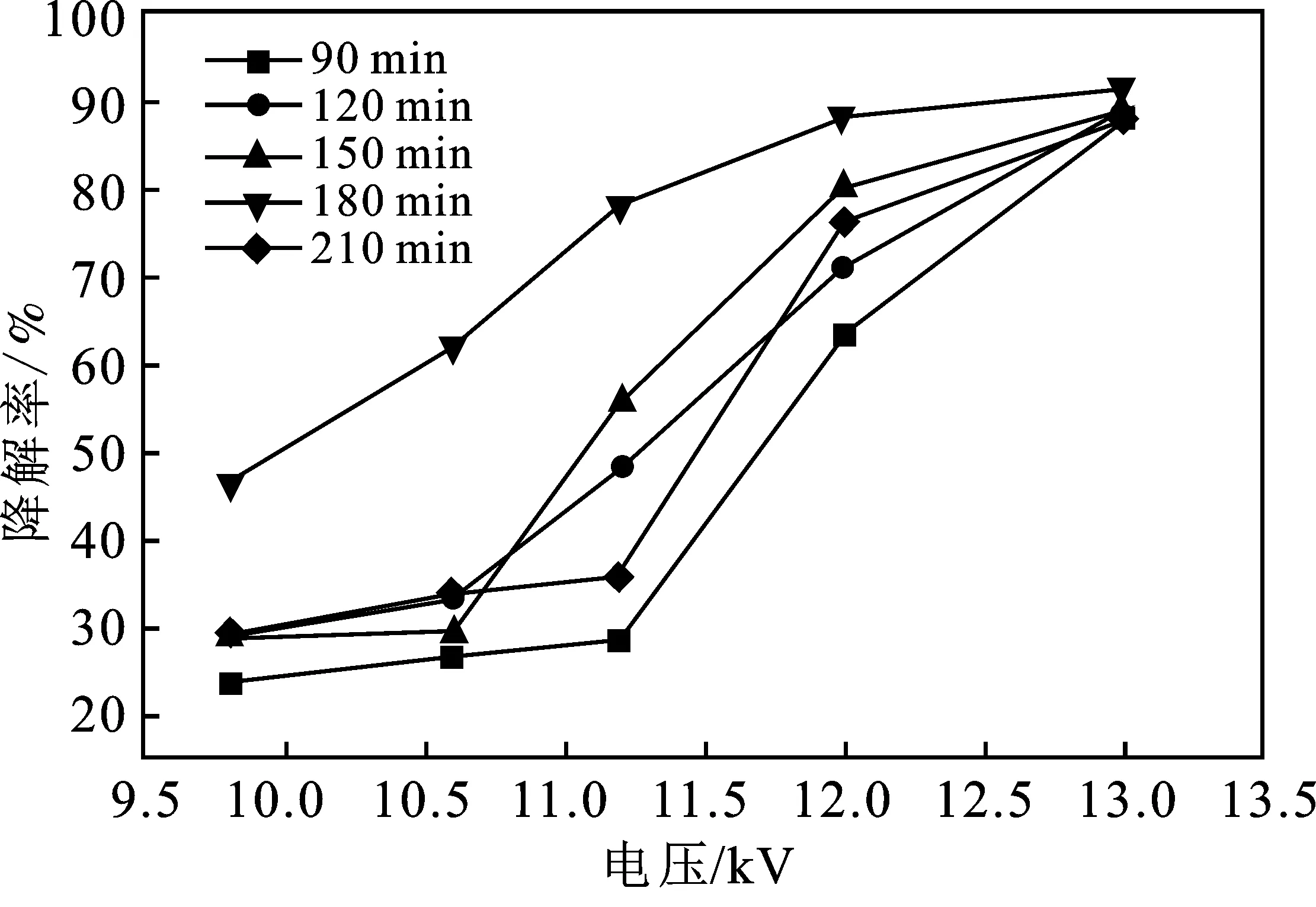
图3 煅烧时间对甲苯降解率的影响
2.2 均匀设计优化催化剂制备工艺条件
为获得催化剂制备的适宜条件,根据均匀设计法进行条件优化,实验结果见表2。选取甲苯降解率为拟合指标,SPSS“逐步、进入”线性回归拟合得甲苯降解方程为:Y=1.044+0.008X1X3+6.743×10-7X2X3-8.44X12+3.679×10-6X32-0.002X3(R=0.999,F=1 935.061,α=0.05)回归方程见 表3。查表得F=1 935.061>F(5,1)=230.2(ɑ=0.05)。

表3 回归分析方程
2.2.1 因素交互作用分析 标准回归系数的绝对值表明因素对实验结果的影响大小。由甲苯降解方程,甲苯降解影响的顺序为:X12(8.44)>X1X3(0.008)>X3(0.002)>X32(3.679×10-6)>X2X3(6.743×10-7),表明甲苯降解与催化剂负载含量、煅烧温度、煅烧时间相关;负载含量对甲苯降解有最大影响,存在着线性关系和平方关系;负载量和煅烧时间之间有明显的交互作用,说明甲苯的降解受到负载含量和煅烧时间交互作用的影响明显;而煅烧温度与煅烧时间之间交互作用较弱。
2.2.2 验证实验 将回归方程引入VF,筛选得出最佳催化剂制备参数,即:5%的催化剂负载量,660 ℃ 的煅烧温度,195 min的煅烧时间。进行 3次甲苯降解实验,取其平均值(表4)。

表4 验证结果
由表4可知,甲苯降解率的平均值为92.48%,大于理论值91.76%,表明最佳条件能满足并用于研究甲苯。
2.3 反应场物质变化趋势
为了获得催化剂对反应场中物质的影响,使用在线高精度复合气体分析仪监测甲苯降解过程中O3、NOx和CO2的变化。
2.3.1 O3生成量的变化 由图4可知,在甲苯废气排放处理的25 min内,O3浓度均呈先增加再稳定的趋势。加入MnOx/Al2O3催化剂后的O3浓度低于未加入催化剂时的O3浓度。不同负载含量的催化反应器臭氧浓度均有不同程度的降低。当放电电压为 13 kV 时,空气流量为 2 L/min,频率为 7.5 kHz,空载反应器中的臭氧浓度为246.76 mg/m3,采用均匀设计方法制备的MnOX催化剂O3浓度降至 90.30 mg/m3。臭氧浓度的减低有以下原因:①一些原子氧会被MnOX催化剂表面吸附,分解甲苯原子氧的量将减少,从而导致臭氧浓度的降低;②臭氧可以被MnOx/Al2O3催化剂分解成活性氧,从而导致臭氧浓度的降低和甲苯降解率的提高。

图4 O3的变化趋势
2.3.2 CO2生成量的变化 对于VOCs的降解,产生的CO2量代表着VOC的氧化降解程度,CO2浓度越高,VOCs降解就越彻底。由图5可知,在放电处理甲苯25 min内,负载了MnOX催化剂的CO2产生量远高于空载,其中均匀设计制备出的催化剂所产生的CO2量最高,达到了2 681.25 mg/m3,这与催化系统对甲苯的降解率相一致。MnOX的引入加快臭氧裂解生成活性氧,氧原子数量增多,提高了对甲苯的降解效率,促使了CO2的产生。

图5 CO2的变化趋势
2.3.3 NOX生成量的变化 NOX主要源于低温等离子体内N2与O2的相互作用,其排放到环境中会对人体和环境造成直接危害。因此,控制NOX的产量也是重要部分。


图6 NOX的变化趋势
2.4 催化剂产物分析及机理探讨
图7为催化剂表面产物的GC-MS图。
由图7可知,产物中有苯甲醛、邻硝基甲苯、3-硝基甲苯、苯甲醇、3-甲基-2-硝基苯酚。黄炯等[10]研究发现催化剂结合等离子体降解甲苯的产物中除了有 CO2和H2O外还有其他未反应完全的有机中间产物:如苯、苯乙醛、苯甲酸、苯乙酸、1,4-二硝基苯等。

图7 催化剂表面产物的GC-MS图
图8是催化剂表面发生的反应,催化剂将甲苯与中间产物和活性物质吸附在其表面,催化剂表面的活性氧将这些物质进一步氧化。放电时产生的臭氧可以被催化剂表面的氧空位(No)转化为活性氧(O*)[11-15]:

图8 等离子体结合催化剂对甲苯的降解机理
O3+No→ O2+O*
(2)
(3)
O*2→ No+O2
(4)
Mn在催化剂表面上的氧转移中起重要作用,促进表面吸附氧转化成活性氧的进程;催化剂产生的活性氧和O3的分解可有效促进甲苯的降解[16-18]。表5显示了甲苯分子的键能分布,在甲苯分解的过程中,甲基上的C—H键的能量最低最容易被破坏,苄基由此形成;生成的苄基被活性氧氧化生成苯甲醛和苯甲醇;接下来,放电空间中的活性粒子(O·,OH·,H·)会进一步与这些环状物发生碰撞并打破苯环,最终生成CO2和H2O[19-21]。

表5 甲苯分子化学键键能
3 结论
(1)考察了DBD反应器中装填MnOx/Al2O3催化剂对甲苯降解率的影响,催化剂的加入使甲苯的降解效率有了显著的提高。
(2)采用均匀设计优化法获得适宜制备催化剂条件为:5%的催化剂负载量、煅烧温度为660 ℃、煅烧时间为195 min,甲苯降解率为92.48%;验证实验中甲苯降解率均高于拟合结果,表明催化剂能有效提高甲苯降解效率。
(3)对甲苯降解过程中的尾气进行在线检测,催化剂能有效降低尾气副产物的生成。
