湿法消解-原子荧光光谱法测定农产品中的硒
2022-03-23罗兰芳周细红胡方凡陈安伟
尚 翠 杨 远 罗兰芳 周细红 胡方凡 陈安伟
(湖南农业大学 资源环境学院,长沙410128)
硒是人体必需的微量元素,具有抗氧化、抑制重金属毒性及其诱导的氧化应激、调节免疫功能、预防甲状腺功能减退等作用[1]。由于硒特有的生物医学作用,越来越多的富硒农产品进入市场,如富硒茶叶、富硒鸡蛋、富硒大米、富硒玉米等。然而,硒是典型的双功能元素,其在人体内的安全范围较窄,适量的硒摄入有利于健康,摄入过量则会导致硒中毒[1]。因此准确测定农产品中硒的含量意义非常重大。
目前,农产品中硒的测定方法主要有原子荧光光谱(AFS)法、荧光分光光度法、电感耦合等离子体质谱(ICP-MS)法、石墨炉原子吸收光谱(GFAAS)法等[2],其中AFS法是测定食品中硒的国家标准第一法,其检出限低,应用最为广泛。AFS法测定食品中的硒时,样品前处理是关系到测定结果准确性的重要环节。样品前处理方法主要有湿法消解和微波消解。现行方法的消解温度、时间等条件需要测试人员根据实验现象和经验判断,尤其是预还原过程,不确定因素较多,影响测定结果的精确度。因此,需要对AFS法样品前处理过程中的各关键步骤及其参数进行探究,以明确该方法的具体操作过程及提高其准确性。微波消解法相对于湿法消解,样品转移操作精度要求高,容易导致误差。因此,本研究拟采用湿法消解-AFS法测定农产品中的硒,优化前处理过程及还原剂浓度,方法可操作性强,结果准确度和精密度高,为批量农产品中硒的检测提供准确、适用性广的方法。
1 实验部分
1.1 仪器设备
AFS-8220原子荧光光度计(北京吉天仪器有限公司),ED54电热消解仪(北京莱伯泰科仪器股份有限公司),ME204电子天平(梅特勒-托利多国际贸易(上海)有限公司)。原子荧光光谱的条件参数如表1所示。

表1 原子荧光光谱仪条件参数
1.2 试剂与材料
农产品标准物质GBW10020(柑橘叶)、GBW10047(胡萝卜)、GBW10046(河南小麦)、GBW10049(大葱)均购自地球物理地球化学勘察研究所。
硒标准溶液(1 000 μg/mL,国家钢铁材料测试中心钢铁研究总院)。
硝酸(GR)、高氯酸(GR)、盐酸(GR)、铁氰化钾(AR)、氢氧化钾(AR)均购自国药集团化学试剂有限公司。硼氢化钾(AR)购自广东光华科技股份有限公司。实验用水为超纯水。
1.3 样品消解
参考GB/T 5009.93—2017方法,采用湿法消解,准确称取样品0.2 g(精确至0.000 1 g)于消解管中,加入10 mL混合酸(硝酸和高氯酸按体积比9∶1配制),盖上弯颈小漏斗,浸泡过夜。次日于消解仪上120 ℃消解2 h,升温至170 ℃继续消解至溶液清亮无残渣,且消解管内无棕色烟,打开弯颈小漏斗赶酸至溶液近干,冷却后加5 mL盐酸(6 mol/L)预还原,冷却后用超纯水定容至25 mL,摇匀待测。按相同的方法制备试剂空白。
1.4 标准曲线配制
将1 000 μg/mL的硒标准溶液用盐酸溶液(5%)逐级稀释至50 μg/L,此为硒标准工作溶液。分别取0、2、4、6、8、10 mL硒标准工作溶液于50 mL容量瓶中,用盐酸溶液(5%)定容至刻度,配得硒标准溶液的浓度依次为0、2、4、6、8、10 μg/L。
2 结果与讨论
2.1 还原剂硼氢化钾浓度选择
分别配制不同浓度的还原剂,氢氧化钾浓度均为5 g/L,硼氢化钾浓度分别设定为8、12、15、18 g/L,载流均为盐酸溶液(5%)。在相同的仪器条件下,测定2 μg/L硒标准溶液的荧光值,重复测定3次,取均值,结果如图1所示。
实验结果表明,随着还原剂硼氢化钾的浓度不断升高,2 μg/L的硒标准溶液荧光值增大,但当硼氢化钾浓度过高时,观察到还原剂进液泵管内有气泡,干扰测定,从而导致测定结果稳定性较差。综合荧光值和稳定性,确定还原剂硼氢化钾浓度为15 g/L。
2.2 铁氰化钾对实验的影响
铁氰化钾在原子荧光法测定硒中的主要作用是屏蔽其他金属离子的干扰,尤其是Cu2+、Bi2+、Hg2+等离子[3]。实验设置了加与不加铁氰化钾两种处理,取标准物质GBW10020和样品1,按实验方法完成消解、赶酸及预还原。一组加入2.5 mL铁氰化钾溶液(100 g/L)后定容至25 mL,另一组不加铁氰化钾,每组每个样品设置两个平行样,同时按相同的方法制备加与不加铁氰化钾两组试剂空白。标准曲线配制两组,一组分别取50 μg/L的硒标准工作溶液0、2、4、6、8、10 mL于50 mL容量瓶中,加入5 mL铁氰化钾溶液,用盐酸溶液(5%)定容至刻度,另一组不加铁氰化钾。在相同的仪器条件下,分别用相应的标准曲线测定两组样品,标准曲线见表2,样品测定结果见表3。

图1 还原剂浓度对荧光值的影响Figure 1 Effect of concentration of reductant on intensity.

表2 硒标准曲线

表3 铁氰化钾对测定结果的影响
实验结果表明,是否加铁氰化钾对硒标准溶液的荧光值没有显著影响。标准物质GBW10020(柑橘叶)在两种处理下的测定结果均在参考值范围内,且两种处理对样品1的测定结果也吻合。
2.3 预还原条件的影响
消解液中硒主要以Se(IV)和Se(VI)两种价态存在,但是只有Se(IV)能够被还原剂还原为氢化物,并通过原子荧光光谱法定量[4]。样品消解完成赶酸至近干后,采用盐酸(6 mol/L)进行预还原,在加热条件下,将Se(VI)还原为Se(IV)。为了确定最佳预还原条件,实验测定了在加盖和开盖两种情况下的加标回收率,结果见图2。不同预还原时间下的加标回收率见图3。

图2 预还原是否加盖对加标回收率的影响Figure 2 The recovery rate of selenium with or without lid during pre-reduction.
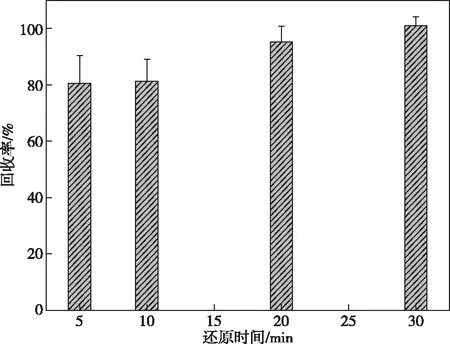
图3 预还原时间对加标回收率的影响Figure 3 Effects of pre-reduction time on the recovery rate.
预还原在开盖情况下进行,加标回收率为78.9%,RSD为8.0%,预还原在加盖情况下进行,加标回收率为99.7%,RSD为3.0%。在加盖情况下,预还原时间分别设置为5、10、20、30 min,其加标回收率依次为80.5%、81.3%、95.3%、101%。根据实验结果,确定预还原过程加盖进行,预还原时间30 min。
2.4 消解液定容体积对测定的影响
将GBW10020(柑橘叶)按以上方法完成样品预处理后分别用水定容至10 mL和25 mL,摇匀,在相同的仪器条件下测定硒含量,结果见表4。

表4 定容体积对测定结果的影响
不同定容体积下,GBW10020均在标准值误差范围内,但定容至10 mL的测定结果明显较25 mL低。且定容至10 mL溶液,由于酸度较高,测定时出峰不规整,稳定性下降。因此测试液定容体积定为25 mL。
2.5 方法检出限与加标回收实验
取10份硒含量为估计方法检出限值3~5倍的样品,按照以上优化的前处理方法制备待测溶液,以盐酸溶液(5%)为载流,还原剂为的KBH4(15 g/L)-KOH(5 g/L)溶液,仪器条件按表1设置,测定硒含量,按公式(1)计算检出限。结果如表5所示,本方法检出限为0.057 μg/L。
MDL=t(n-1,0.99)×S
(1)
式中,MDL—方法检出限,μg/L;n—样品的平行测定次数;t—自由度为n-1,置信度为99%时t分布(单侧);S—n次平行测定的标准偏差,μg/L。
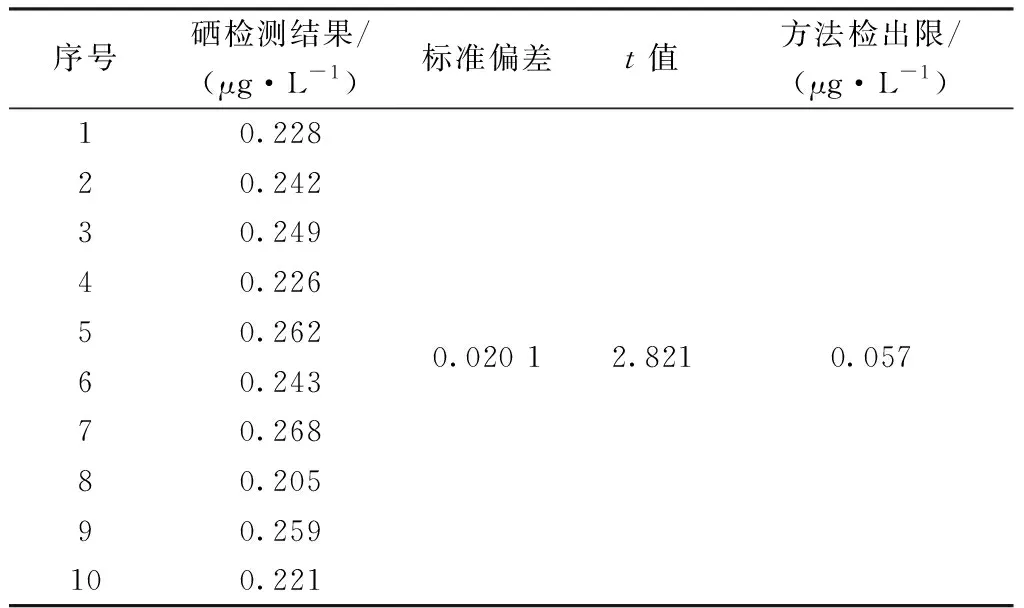
表5 方法检出限
按实验方法对已知本底值的样品进行加标回收实验,计算加标回收率为93.7%~101%(表6)。
2.6 方法准确度和精密度
采用以上优化方法测定国家标准物质GBW10020(柑橘叶)、GBW10047(胡萝卜)、GBW10046(河南小麦)、GBW10049(大葱)中的硒,测定结果见表7。测定结果在标准值误差允许范围内,方法准确度及精密度良好。

表6 加标回收实验结果
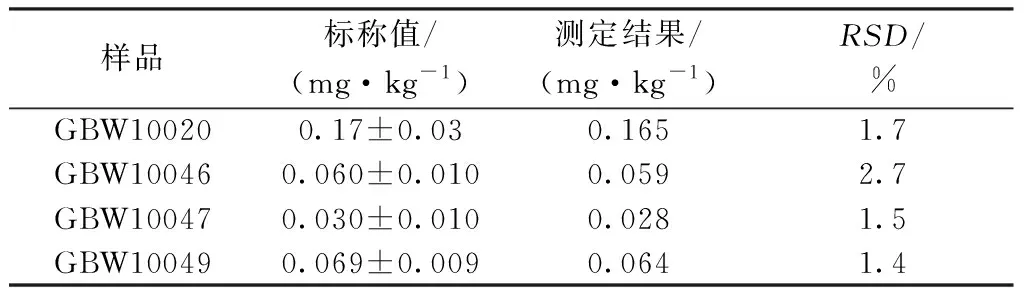
表7 标准物质测定结果
3 结论
在GB/T 5009.93—2017方法的基础上进行优化,明确了样品消解、赶酸及预还原温度为170 ℃,预还原过程需加盖进行,预还原时间为30 min,样品预还原完成冷却后用水定容至25 mL,不加铁氰化钾溶液。载流为盐酸溶液(5%),还原剂为KBH4(15 g/L)-KOH(5 g/L)溶液。方法检出限为0.057 μg/L,相对标准偏差RSD范围为0.89%~2.7%,加标回收率为93.7%~101%。该方法准确度高,稳定性好,适应性广,检出限低,可作为农产品硒含量测定的可靠方法。
