响应面法优化巴旦木壳对废水中Pb、Cu和Cd的吸附及同时测定
2022-03-23加列西马那甫王建华马福东
加列西·马那甫 王建华 万 越 马福东
(新疆农业大学 化学化工学院,乌鲁木齐 830052)
随着工业生产活动的增加,人们生存的环境受到严重破坏。由于重金属在生物体内存在累积效应以及在环境中的难降解性,影响人体神经系统和脑细胞功能,造成难以挽回的伤害,并且会通过母体传递给婴儿[1-4]。
目前重金属的去除方法主要有化学沉淀法、反渗透法、离子交换法和生物吸附法。其中吸附法由于方法简单、易于回收而被广泛使用[5-8]。国外逐渐重视利用廉价的农林废弃物制备吸附剂来清除废水中的重金属。常用的农林废弃物有锯末、橙皮、花生壳、核桃壳等。而我国作为农业大国,农业生产过程中的很多废弃物却没有得到有效的回收利用[9-10]。
巴旦木是新疆特产之一,属于壳类食物,在享用果肉后大量壳成为废料被丢弃,造成资源浪费。本实验以巴旦木壳为原料,探讨其对水中Pb、Cu、Cd的吸附性能,并利用响应面法对巴旦木壳吸附条件进行优化[11-13]。
分光光度法作为常用的测定方法具有操作简便、周期短等优点。但不能对多组分混合体系进行同时测定,当体系内含有多组分互相干扰时,用分光光度法测定之前必须先进行分离,许多组分难以分离,得不到准确测定结果。由于Pb、Cu和Cd的吸收光谱重叠较严重,相互干扰,经典分光光度法无法进行同时测定。本文研究三组分吸光度的加和性,采用正交实验进行校正模型的建立,在确定的波长范围和波长间隔对光谱相互重叠的Pb、Cu和Cd模拟样品进行测定。用PLS对吸附后的模拟废水样品进行计算分析,并间接得出巴旦木壳对Pb、Cu和Cd的去除率和建立Pb、Cu、Cd三组分同时测定的多元校正分析方法[14-15]。实验结果具有一定的实用价值。
1 实验部分
1.1 仪器与试剂
TU-1810型紫外-可见分光光度计(北京普析通用仪器有限责任公司),AL204-IC电子分析天平(梅特勒-托利多仪器有限公司,上海),DHG-9055A电热鼓风干燥箱(上海一恒科学仪器有限公司)。
醋酸铅、硫酸铜、硫酸镉、PAR[4-(2-吡啶偶氮)间苯二酚]、四硼酸钠、盐酸、氢氧化钠、乙醇、甲醛、硫酸、硝酸均为分析纯试剂。
1.2 实验方法
1.2.1 巴旦木壳吸附剂的制备
洗净巴旦木壳,用水浸泡48 h,每12 h更换一次水,于60 ℃烘干,用粉碎机粉碎,待用。
1.2.2 模拟水样的配制
分别移取0.25 mL Pb(10 mg/mL)、0.6 mL Cu(1 mg/mL) 和0.25 mL Cd(1 mg/mL)溶液,混合,用水稀释至50.00 mL,作为模拟混合样品。
1.2.3 吸附实验
称取一定量的巴旦木壳吸附剂,分别置于50 mL含Pb、Cu和Cd或混合试样的模拟废水中,调节pH值,震荡吸附一定时间,离心,取上清液加入缓冲溶液和显色剂,定容,用分光光度法测定,计算浓度及去除率。
去除率=(c0-c)/c0×100%
c0—吸附前重金属浓度,mg/mL;c—吸附后重金属浓度,mg/mL。
1.2.4 巴旦木壳吸附重金属单因素实验
以不同的吸附剂投加量(A)、吸附时间(B)和pH值(C)为单因素进行实验,考察各因素对巴旦木壳吸附重金属的影响。
1.3 标准曲线的绘制
于25.00 mL量瓶中加入2 mL硼砂-硼酸缓冲液、1 mL PAR-乙醇溶液,再分别移取0.80、1.00、1.20、1.40、1.60和1.80 mL Pb(50 μg/mL)、Cu(5 μg/mL)和Cd(5 μg/mL),用水定容,摇匀。反应20 min,用试剂作空白,在522、495和496 nm处测定吸光度。计算得Pb、Cu和Cd的标准曲线回归方程分别为:y=0.12536x-0.08657,R2=0.9949;y=0.50943x-0.0871,R2=0.9993;y=1.63571x-0.07405,R2=0.99767。
2 结果与讨论
2.1 吸附时间对去除率的影响
移取Pb、Cu和Cd废水试样50.00 mL,分别置于150 mL锥形瓶中,加入吸附剂0.2 g,调节pH值为9.0,震荡20、40、60、80、100 min,离心,分取上清液3.0 mL,加入缓冲液和显色剂稀释至25.00 mL,测定其吸光度,考察不同吸附时间对Pb、Cu和Cd去除率的影响,结果见图1。当吸附时间增加到40 min时,Pb2+、Cu2+和Cd2+的去除率分别为76.5%、68.4%和78.4%;之后不再增加,说明吸附时间达到最优值。
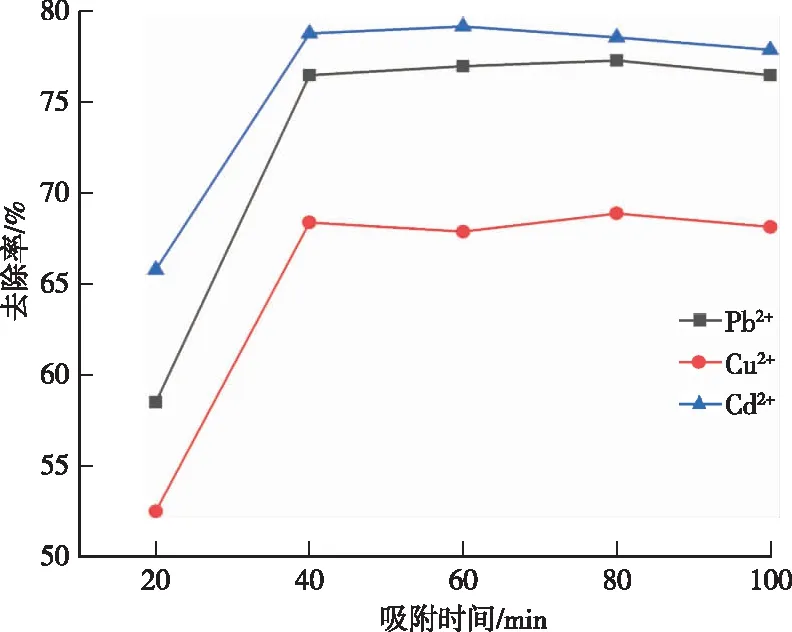
图1 吸附时间对Pb2+、Cu2+和 Cd2+去除率的影响Figure 1 The effect of adsorption time on the removal rate of Pb2+,Cu2+ and Cd2+.
2.2 巴旦木壳投加量对去除率的影响
移取Pb、Cu和Cd废水试样50.00 mL,置于150 mL锥形瓶中,分别加0.1、0.2、0.3、0.4和0.5 g巴旦木壳样品,调节pH值为9.0,震荡40 min,离心,分取上清液3.00 mL,加入缓冲液和显色剂稀释至25.00 mL,测定吸光度,考察不同巴旦木壳投加量对Pb、Cu和Cd去除率的影响,结果见图2。当吸附剂用量增加到0.3 g时,去除率分别在85.1%、71.3%和82.9%,之后上升趋势变得不明显。
2.3 pH值对去除率的影响
移取Pb、Cu和Cd模拟废水试样50.00 mL,置于150 mL锥形瓶中,加入0.3 g吸附剂,调pH值3.0、5.0、7.0、9.0和11.0,震荡40 min,离心,分取上清液3.00 mL,加入缓冲液和显色剂稀释至25.00 mL,测定吸光度,考察不同pH值对Pb2+、Cu2+和Cd2+去除率的影响,结果见图3。当pH值增加到9.0时,Pb2+、Cu2+和Cd2+的去除率分别在85.14%、68.19%和84.70%,之后逐渐减小,pH值为9.0时达到最优值。
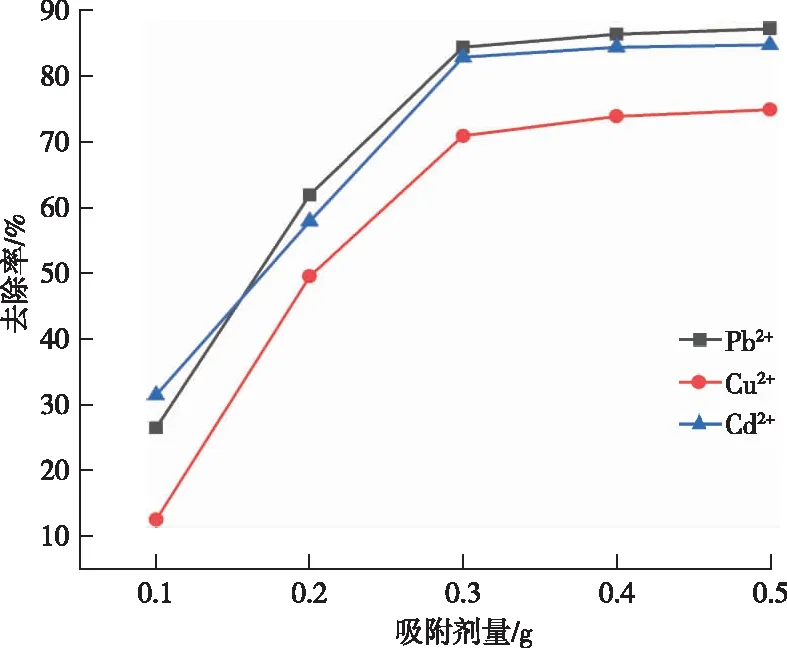
图2 吸附剂用量对Pb2+、Cu2+和 Cd2+去除率的影响Figure 2 The influence of the amount of adsorbent on the removal rate of Pb2+,Cu2+ and Cd2+.

图3 pH值对Pb2+、Cu2+和Cd2+去除率的影响Figure 3 The effect of pH value on the removal rate of Pb2+,Cu2+ and Cd2+.
2.4 吸收光谱分析
分光光度法作为常用的测定方法,具有操作简便、周期短等优点。但不能对多组分混合体系进行同时测定,当体系内含有多组分互相干扰时,要先进行分离。为考察Pb、Cu和Cd的吸收光谱性质,配制各单组分的标准溶液,绘制Pb、Cu和Cd的吸收光谱如图4所示,它们在520、494和497 nm波长处有最大吸收,且吸收光谱重叠较严重,3组分彼此相互干扰,用经典的分光光度法难以进行单一组分的定量。
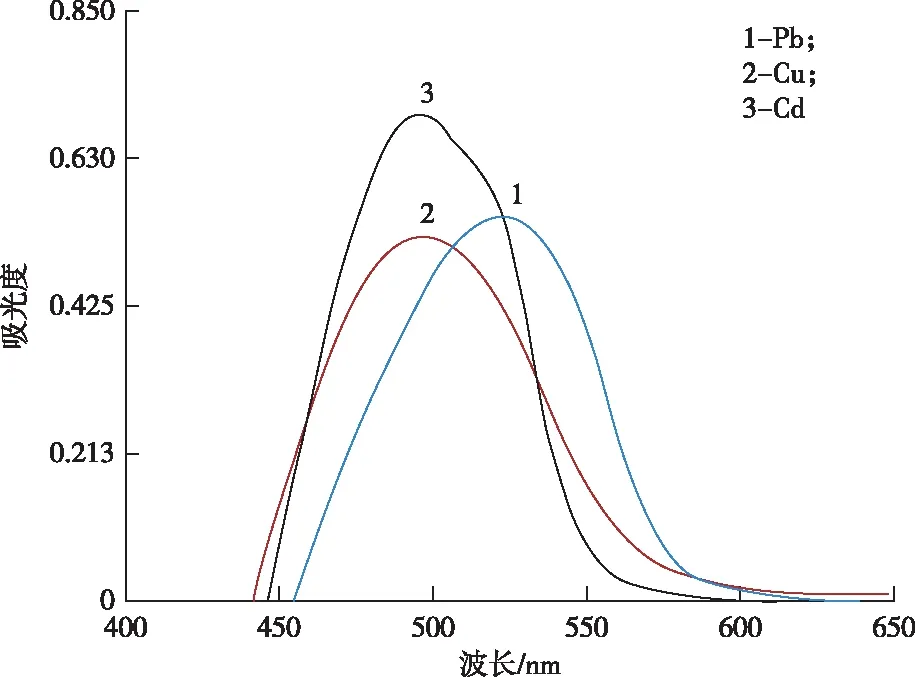
图4 吸收光谱图Figure 4 Absorption spectrum.
2.5 反应条件的优化
实验结果表明,选择PAR(显色剂)的用量为1 mL、硼砂-硼酸缓冲液用量为2 mL、显色时间为20 min时,体系的吸光度值最大且稳定。Pb、Cu和Cd的浓度分别在1.40~8.00、0.24~1.30 和0.10~0.50 μg/mL,遵守朗伯-比耳定律,具有良好的线性关系。
2.6 响应面法优化实验条件
2.6.1 Box-Behnken设计实验

表1 响应面分析因素与水平
2.6.2 模型方程的建立与方差分析
应用Design-Expert 8.0.6软件对表2的实验结果进行数据分析及模型方程建立,得到吸附剂量、吸附时间、pH值与Pb、Cu和Cd的去除率之间的二次多项回归方程:
Y(Pb)=-180.46469+149.7375A+2.21237B+42.38438C-0.63250AB-1.025AC+0.0465BC-144.625A2-0.029162B2-2.40219C2
Y(Cu)=-336.41025+243.22A+1.65760B+72.424C+0.85AB-17.55AC+0.038BC-179.7A2-0.02567B2-3.70175C2
Y(Cd)=-270.57469+97.5625A+1.86287B+64.67063C+0.2725AB+5.9375AC-0.12113BC-225.375A2-0.011737B2-3.30219C2
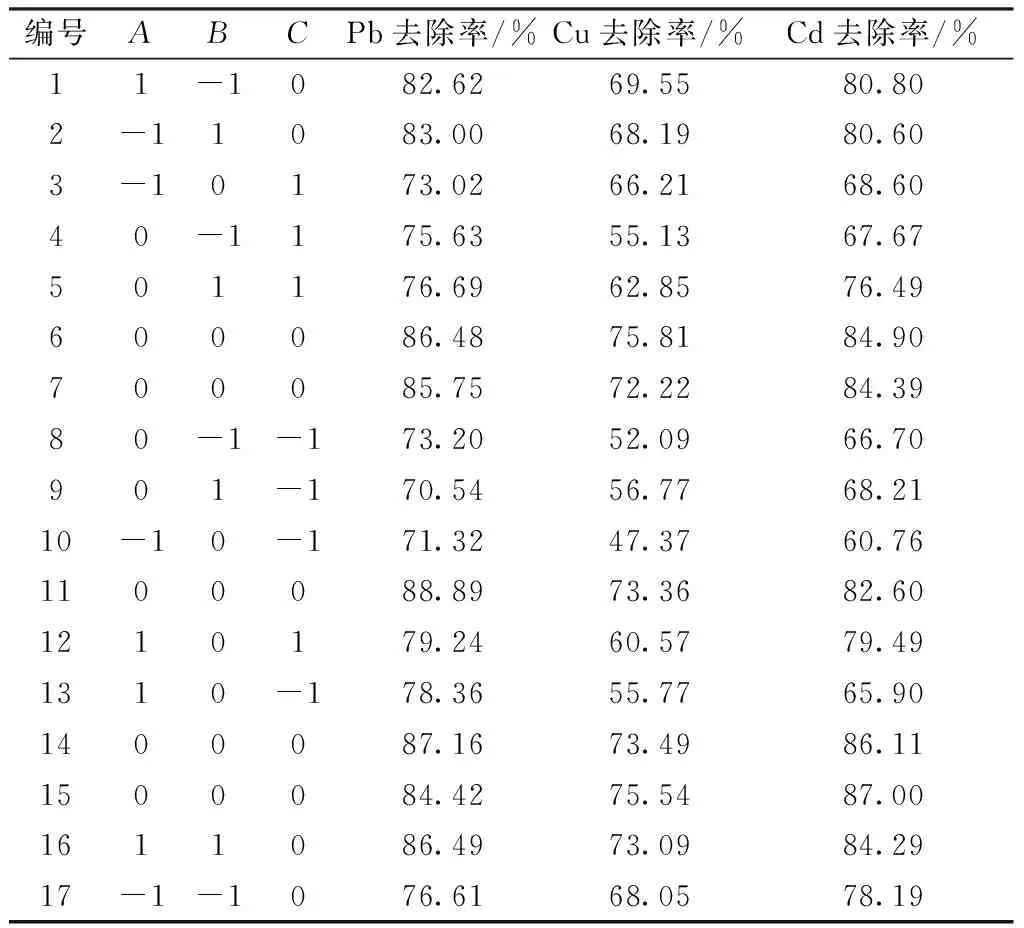
表2 响应面分析方案及实验结果
表3~5为Pb、Cu和Cd的回归模型方差分析结果,其中失拟差分别为0.166 5、0.070 6、0.113 1均大于0.05,不显著;R2分别为0.940 6、0.963 3、0.961 4,说明回归方程与实验相关性较好,不存在异常点。其中Pb的一次项中A为极显著,二次项中C为差异极显著,B为显著,交互项不显著;Cu的一次项中C为极显著,二次项中C为差异极显著,交互项为不显著;Cd的一次项中C为极显著,A为显著,二次项中C为差异极显著,交互项为不显著。说明Pb、Cu和Cd的各因素与实验的影响不是一般的线性关系。
2.7 PLS最佳计算测定条件的确定
2.7.1 吸光度加和性的考察
配制Pb、Cu和Cd的混合溶液和浓度相同的单组分标准溶液,在最大波长处测定单一组分和模拟混合溶液的吸光度,根据公式|I-I0|/I0的大小,分析体系的加和性。当加和性大于0.1表示加和性不好,小于0.1则相反。式中I表示模拟混合体系的吸光度,I0表示3种单组分标准溶液吸光度的加和值。计算可得混合体系的加和性不好。
园林取名为“寓”,本有“寓意则灵”,也蕴涵寄居、寄托之意。《寓山注》总名曰“注”,既隐含山水园林经典化、文本化的概念,诠释寓园的品质;又有“解释”之义,即说明各景点命名的来由、依据,并记录祁彪佳对寓园的认知与实践。在《寓山注》中,《序记》阐发园之沿革、开园总纲、营造原则,其后49记则叙述园林布局、观赏景象等。49个景点多为祁氏亲自命名,其立意高远,独抒性灵,情趣横生。
2.7.2 波长范围及波长间隔的确定
波长范围及波长间隔的选择是进行建模和计算的关键步骤。按正交设计表L9(33) 配制9组不同浓度的Pb、Cu和Cd模拟混合试样(表6),从400~650 nm,每隔1 nm,250个波长点测定各混合组分的吸光度值。根据吸收曲线,在相同波长间隔和不同波长选择范围,对同一模拟混合试样,采用PLS建立校正模型并进行拟合计算,结果为波长范围在400~650 nm较好。保持相同的波长范围,只改变波长间隔,对同一模拟混合试样进行分析,选择2 nm间隔建立的校正模型较为稳定,计算结果为最佳。

表3 Pb的回归模型方差分析

表4 Cu回归模型方差分析

表5 Cd回归模型方差分析

表6 模拟混合样品校正组质量浓度组成
2.7.3 模拟混合试样的测定
按照正交设计表L9(33)配制9组不同浓度的3组分混合模拟样品作为校正组,通过光谱结果建立模型。用确定的波长范围及波长间隔对9组不同浓度的模拟样品预测组进行分析,用PLS计算平均误差和相对预报误差(表7)。
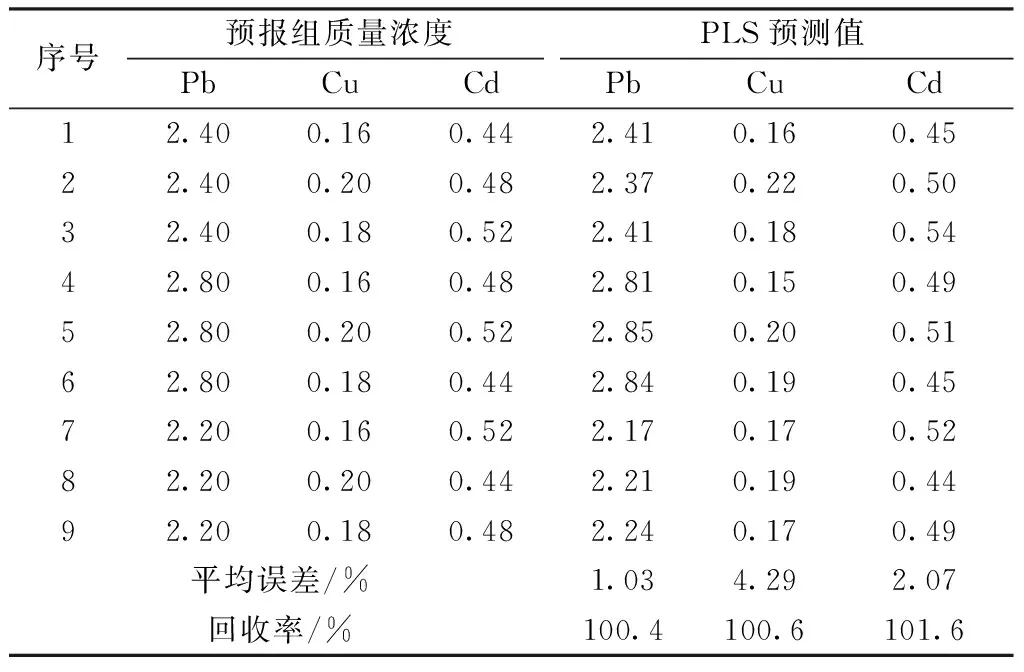
表7 模拟混合样品预报组质量浓度 组成、PLS预测值及误差分析
2.7.4 样品分析
分别移取0.25、0.60、0.25 mL Pb(10 μg/mL)、Cu(1 μg/mL)、Cd(1 μg/mL) 溶液混合。加水稀释至50.00 mL,加入0.3 g吸附剂,调节pH值为9.0,震荡40 min,离心,分取上清液3.00 mL,加入2 mL缓冲溶液、1 mL显色剂,用水稀释至25.00 mL,混匀。在450~570 nm,间隔1 nm,测定其吸光度值。采用PLS计算模拟混合样品吸附后Pb、Cu和Cd的含量,并间接得出巴旦木壳对Pb、Cu和Cd的去除率。结果见表8。

表8 吸附剂对混合试样吸附后PLS测定浓度
3 结论
巴旦木壳对低浓度重金属溶液具有良好的吸附能力。在单因素实验的基础上,采用响应面法对实验条件进行优化,最佳吸附条件为Pb:吸附剂投加量0.4 g、吸附时间49.38 min、pH值为9.96;Cu:吸附剂投加量0.4 g、吸附时间49.91 min、pH值为10.13;Cd:吸附剂投加量0.4 g、吸附时间49.83 min、pH值为10.42。在此条件下,Pb、Cu和Cd的去除率分别为87.42%、73.49%和85.11%。
采用偏最小二乘-分光光度法对Pb、Cu和Cd吸附后的模拟混合试样进行同时测定,解决了因多组分吸收光谱重叠和相互干扰不能进行同时测定的问题。说明采用PLS能够得到较为准确的结果。巴旦木壳作为一种新型吸附剂,具有一定研究意义。
