三维可视化系统联合纤维胆道镜治疗肝胆管结石患者近期疗效研究*
2022-03-21何翼彪王智鹏
何翼彪,王智鹏,白 磊
肝胆管结石特指原发于肝内胆管系统的结石,是胆道外科常见疾病,因其病情复杂,具有术后结石残存率和复发率高、易引起严重的并发症等特点,肝胆管结石已成为我国非恶性胆道疾病患者主要的死亡原因[1]。外科手术是治疗肝胆管结石的主要方法,但当前并无标准的术式选择。研究数据显示,经传统手术治疗的肝胆管结石患者结石残留率可达到30%~90%[2],而随着胆道镜、十二指肠镜等内镜和介入技术在临床应用越来越多,整体上术后肝胆管结石残留率有所改善,但部分患者手术效果仍不尽如意[3]。近些年来,随着数字医学技术的进展,三维可视化技术在肝胆外科疾病诊疗方面的应用越来越多。这类手术可对肝脏各组织结构进行放大、旋转、着色、透明等处理,有利于医师更直观、更精确地观察肝脏结构,从而为诊断和手术方案的制定提供更充分的客观依据[4]。鉴于肝胆管结石解剖结构的复杂性,本研究在手术过程中使用三维可视化系统联合纤维胆道镜治疗肝胆管结石患者,观察了疗效,现报道如下。
1 资料与方法
1.1 一般资料 2015年9月~2020年9月我院肝胆外科收治的肝胆管结石患者117例,男64例,女53例;年龄36~65岁,平均年龄为(49.2±7.5)岁。诊断符合《肝胆管结石病诊断和治疗指南》[5]的标准,且经CT或腹部彩超检查明确诊断,符合胆道镜临床应用适应证[6],其中结石位于左肝管36例,右肝管27例,胆总管15例,左右肝管11例,左肝管合并胆总管19例,右肝管合并胆总管9例;结石直径为3~11 mm,平均为(7.2±2.1)mm。排除标准:合并化脓性胆管炎、胆管癌等其他胆道病变;因严重的感染或免疫系统缺陷性疾病、其他脏器功能不全等原因不宜手术者;有精神病史。将患者分成两组,两组性别、年龄、结石分布和结石直径比较差异均无统计学意义(P>0.05),具有可比性。本研究经我院医学伦理委员会批准,患者及其家属签署知情同意书。
1.2 手术方法 在观察组,在手术过程中使用三维可视化系统和纤维胆道镜,使用256层螺旋CT(荷兰Philips公司)行腹部CT扫描,扫描参数设置:管电压120 kV,管电流300 mA,层厚和层间距均为1 mm,采集平扫期、动脉期、静脉期扫描数据。将数据以DICOM格式存储,并上传至精准手术3D分析规划系统(美国EDDA公司)行三维可视化结构重建,采用不同颜色对比区分重建脏器和肝段,并通过不同程度的转动、放大或缩小、透明化等方式处理重建三维图形,辨析肝内外胆道系统的解剖结构、胆道扩张和血管系统变异、结石分布、结石与胆道和供肝血管的解剖关系。综合结石位置、大小及胆管和肝脏情况等,为患者设计一种或数种手术方案或路径。在行肝叶切除前,拟定肝切除平面和肝切除线,并在三维重建模型的基础上,进行仿真学手术演练,进一步确定个体化的手术方案。经肝叶切除后的肝断面胆管残端或切开的胆总管,置入纤维胆道镜,探查胆道狭窄、胆管结石分布和Oddi括约肌情况,行网篮取石。对较坚硬铸型结石,配合液电碎石术或生理盐水冲洗取石,同时利用活检钳将胆管内的血凝块和絮状物等杂物取出。对胆总管结石,采取胆总管切口取石;对合并胆管重度狭窄和Oddi括约肌异常者,设计修复重建术,进行Roux-en-Y胆管空肠吻合术或胆管狭窄成形术;对局限于肝叶或肝段的区域性毁损病灶、难以处理的肝管囊性扩张或狭窄、难以取尽的多发结石,均采取肝部分切除术。术后,放置“T”型引流管,保持引流通畅,常规予以抗感染、护肝、营养支持等治疗。术后7 d复查CT和超声检查,评价结石清除情况。待无液体流出、无切缘积液时,拔除引流管;在对照组,术前常规行B超或CT检查,制定胆总管切开和肝叶切除等手术方案,并联合纤维胆道镜取石,主要术式、术后处理同观察组。
1.3 检测指标 使用日立7100型全自动生化分析仪检测血生化指标;使用贝克曼DxFLEX型流式细胞仪检测外周血T淋巴细胞亚群(试剂盒购自美国BD公司)。
2 结果
2.1 两组围手术期指标比较 观察组手术时间、术中出血量、术后引流量、首次进食时间和术后住院日显著短于或少于对照组(P<0.05,表1)。
2.2 两组结石清除率比较 术后7 d复查CT或/和超声检查,发现观察组59例(95.7%)肝胆管内未见结石残留,而对照组为48例(85.7%,P<0.05)。
2.3 两组并发症发生率比较 术后,观察组并发症发生率显著低于对照组,差异有统计学意义(P<0.05,表2)。
2.4 两组血生化指标比较 术后7 d,两组血生化指标比较,差异无统计学意义(P>0.05,表3)。
2.5 两组外周血淋巴细胞亚群比较 术后7 d,观察组外周血CD4+细胞百分比和CD4+/CD8+细胞比值显著高于对照组,而CD8+细胞百分比显著低于对照组,差异有统计学意义(P<0.05,表4)。
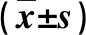
表1 两组围手术期指标比较

表2 两组并发症发生率[n(%)]比较
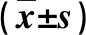
表3 两组血生化指标比较
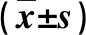
表4 两组外周血淋巴细胞亚群比较
3 讨论
肝胆管结石的发病机制并未完全阐明。一般认为,结石生成主要与胆汁引流不畅和胆管长期反复炎症刺激有关,其发生可受胆道感染、胆道解剖变异、胆汁淤积、不良饮食习惯、营养状态等因素的影响[7]。手术切除在肝胆管结石治疗中占主导地位,其治疗原则在于“清除结石、去除病肝、解决狭窄、消除畸形、顺畅引流、护肝保胆”,但由于肝内胆管解剖结构复杂以及结石分布、大小、数量等不一,其临床诊治难度大,在不少患者难以达到满意的治疗效果,部分患者甚至需接受多次手术[8,9]。因此,如何提高肝胆管结石的治疗效果备受重视。
近年来,胆道镜在肝胆外科诊治方面应用越来越多。纤维胆道镜可于胆道术中直视下进行胆道探查,相比硬质胆道镜具有治疗成角大的优势,其向上可观察到肝内胆道深度的Ⅲ/Ⅳ级胆管,向下可观察到胆总管下部至十二指肠内,能有效评估结石的分布、大小、数量、性质和胆管狭窄,故有利于手术方案的制定及术中取石顺利的进行[10,11]。纤维胆道镜的应用不仅提高了肝胆管结石的诊治效率,而且术后可经“T”管直视胆道情况、取出残余结石,减少了部分患者再次手术的痛苦和手术风险[12]。
既往在肝胆管结石术前检查多应用B超或CT观察结石情况,但影像学检查结果均以二维图像呈现,手术医师需以抽象思维去整合检查结果,再判定肝内胆管组织结构的空间位置关系,并以此设计手术方案,这对术者要求较高,而且存在一定的盲目性和不精确性[13]。随着精准医学理念的推广和外科手术诊治向微创化、细致化、信息化等智能方向转变,数字临床医学外科技术得以发展,其中三维可视化技术在肝胆外科已有一定的应用尝试[14]。在诊治肝胆管结石时,可通过三维可视化系统立体和直观地展现结石在胆管中的分布、大小、数量和与周围组织的解剖关系,更为清晰、真实地显示胆道系统的状况,包括肝内外血管空间结构和组织学改变,可形象逼真地模拟手术,有助于手术医师进行更为精确的评估。手术医师可在三维重建模型上实施可视化仿真学手术演练,预先了解术中可能切除或损伤的组织和血管情况,有助于个体化方案的制定和实施,减少了手术的盲目性,提高了手术的精确性和安全性[15,16]。本文结果显示,观察组手术时间、术中出血量较对照组缩短或减少,可能是因为三维可视化系统应用有助于术者精准定位,减少了手术的盲目性,使手术得以顺利实施,同时精准定位可避免不必要的组织和血管损伤,故能缩短手术时间、减少术中出血。观察组术后引流量、首次进食时间和术后住院日较对照组减少或缩短,提示观察组术后恢复优于对照组,可能主要与术中创伤减轻有关。本研究观察组结石清除率较对照组升高,因为在三维可视化系统下可精准地预判结石的分布和数目,实现精准靶向取石,故能更好地清除结石。观察组术后并发症发生率较对照组下降。有报道显示[17],应用三维重建引导复杂肝胆管结石手术可取得满意的近期疗效,三维可视化技术指导肝段切除能实现术前精确诊断,提高结石清除率[18]。
肝胆管结石引起反复胆道梗阻和感染可损害肝功能[19]。肝胆管结石造成的长期慢性炎症可引起T细胞亚群紊乱,而手术创伤可进一步加重免疫功能紊乱[20]。本文显示,观察组术后外周血CD4+细胞百分比和CD4+/CD8+细胞比值较对照组升高,而CD8+细胞百分比较对照组降低,提示在三维可视化系统指导下可减轻手术创伤,减轻术后炎症反应,术后患者早期进食、恢复快,有助于机体免疫功能的改善。
