术前K线对棘突纵割式椎管扩大成形术治疗颈椎后纵韧带骨化症疗效的影响
2022-03-12李楠赵凯平马赛张宁刘波何达
李楠 赵凯平 马赛 张宁 刘波 何达
颈椎后纵韧带骨化症(cervical ossification of the posterior longitudinal ligament, C-OPLL)会损害脊髓的有效容积,不仅造成患者的脊髓和(或)神经根病变,而且还会增加患者在轻微外伤后出现脊髓损伤的风险[1-2]。目前临床上C-OPLL有多种手术治疗方式,如前路、后路和前后路联合的方式。采用前路减压融合手术尽管能够直接切除骨化灶,固定受累节段,但由于手术过程相对复杂,难度大,风险高,围手术期并发症也显著高于后路椎板成形术,使得更多医生倾向于采用后路手术[3-4]。椎板成形术是常用的治疗C-OPLL的后路手术方式。该术式不但可以扩大椎管面积,还能够保留一定程度的颈椎活动度,疗效肯定[5-6]。但随着手术例数的增加,也有一部分患者术后症状得不到缓解,甚至加重。为了能够在术前对C-OPLL患者做出恰当的预后评估,Fujiyoshi等[7]提出了K线理论,即在颈椎标准侧位X线像上做C2与C7节段椎管中点的连线,若OPLL骨化灶顶点未超过此连线,即为K线(+),反之为K线(-)。该作者认为K线(-)患者由于脊髓后移受限,接受颈后路椎板成形术后通常疗效欠佳。然而,也有研究者报道,即使是对K线(-)的C-OPLL患者,颈后路椎板成形术也可以取得令人满意的疗效[8-9]。因此,目前对K线是否会影响C-OPLL患者接受颈后路椎板成形术后的疗效存在争议。K线的概念是在2008年被提出的,受限于技术条件,当时的椎板成形术方式相对较少。近年来,随着新技术的应用和普及,椎板成形术的术式也在不断优化,疗效也逐步提高。采用颈后路棘突纵割式椎管扩大成形术(改良“双开门”椎板成形术)治疗重度多节段颈椎管狭窄症,可以取得令人满意的疗效[10]。本研究对近年采用颈后路棘突纵割式椎管扩大成形术治疗的C-OPLL患者的临床资料进行回顾性分析,旨在探讨该术式对C-OPLL患者的疗效是否受到K线的影响。
资料与方法
一、资料
1.病例纳入与排除标准:(1)病例纳入标准:①患者年龄<80岁;②CT证实存在OPLL;③伴有脊髓和(或)神经根功能障碍;④随访36个月以上且临床资料完整。(2)病例排除标准:①有颈椎手术史;②术后出现任何可能影响颈脊髓支配功能的疾病如脑出血,脑梗死,颅脑肿瘤以及颈脊髓的创伤、炎症和肿瘤;③术后有感染病史;④未能完成随访。
2.一般临床资料:依据本研究病例纳入与排除标准,对2017年1月至2018年6月北京积水潭医院脊柱外科行棘突纵割式颈椎后路椎管扩大成形术治疗的C-OPLL患者157例的临床资料进行回顾性分析。依据术前K线结果将患者分为K线(+)和K线(-)两组。K线(+)组99例,男56例,女43例,年龄(59.8±8.9)(43~76)岁,随访时间(49.5±4.8)(42~56)个月;K线(-)组58例,男38例,女20例,年龄(59.3±8.2)(44~78)岁,随访时间(50.0±4.2)(43~57)个月。两组患者年龄和随访时间差异均无统计学意义(P=0.720,0.485)。
二、方法
1.手术:(1)切口和入路:采用C2-C7颈部后正中切口。切开皮肤及皮下,用电刀逐层切开颈部颈韧带和软组织,暴露C3-C6棘突及C7棘突上缘。用Cobbs骨膜剥离器将椎旁肌自颈椎棘突上骨膜下推开,暴露C3-C7椎板。(2)棘突劈开和侧沟制备:使用磨钻、小刮匙及2 mm椎板咬骨钳切除C3椎板。如OPLL骨化灶向上超越C3椎体水平,则行C2椎板下半部分的穹窿减压。用椎板咬骨钳和髓核钳咬除C6/7之间的黄韧带,使用磨钻和椎板咬骨钳切除C7椎板上半部分,从C4~C6椎板下方放入空心塑料导管,中间插入T-saw,用T-saw左右对称锯开C4-C6的棘突。用磨钻沿C4-C6两侧小关节内侧磨出两条侧沟,深度直达对侧皮质骨,将劈开的椎板向两侧分开,暴露出下方硬膜。(3)植入人工骨间隔物:将3块珊瑚人工骨(大小约2.6 cm3)用2根10号丝线穿过椎板预制孔道,分别交叉固定于C4-C6棘突间(图1,2)。如果OPLL骨化灶累及C7椎体,需延长手术切口到T1棘突,用T-saw左右对称锯开C4-C7棘突,植入4块珊瑚人工骨并固定。(4)关闭伤口:逐层缝合椎旁肌、颈韧带、皮下和皮肤。伤口内放置负压引流管。缝合切口。
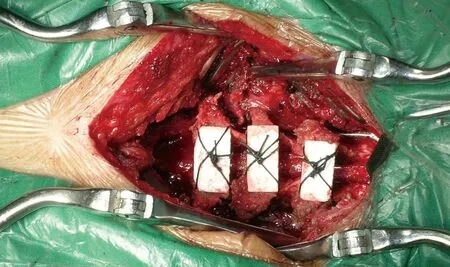
图1 棘突纵割式颈椎后路椎管扩大成形术术中,将C4-C6棘突对称纵割后,植入珊瑚人工骨间隔物,并以10号丝线固定
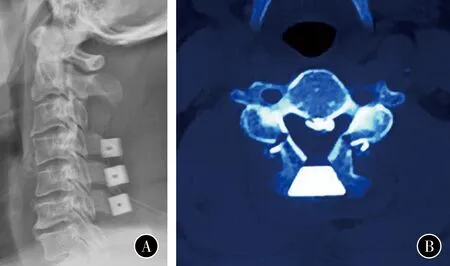
图2 术后7 d影像学检查见C3全椎板和C7上半椎板切除,C4-C6棘突间植入人工骨间隔物,两侧沟槽位于小关节与椎板的移形处,深度直到对侧皮质骨 A 侧位X线像 B CT横截面像
2.术后处理:术后常规应用抗生素48 h。当伤口引流量24 h累计低于50 ml时拔除引流管,而后指导患者进行康复锻炼。颈托佩戴不超过3周,以免影响颈部活动。
3.随访:术后3,6,12个月及每年以电话访问或门诊复查的方式对患者进行随访。
4.疗效评价:采用日本骨科协会(Japanese Orthopaedic Association, JOA)评分和JOA评分改善率[(术后JOA评分-术前JOA评分)/(17-术前JOA评分)]作为临床疗效评价指标。选取术前和术后末次随访(简称“术后”)JOA评分进行组间和组内比较。
5.K线测量:依据Fujiyoshi等[7]提出的K线定义,利用医学影像信息系统(Picture Achiving and Communication Systems,PACS)软件和患者术前颈椎中立位侧位X线像测量K线。
结 果
K线(+)组手术时间和出血量均大于K线(-)组(均P<0.001,=0.004)。见表1。K线(+)与K线(-)两组组内术前与术后JOA评分差异均有统计学意义(均P<0.001);两组间术前JOA评分、术后JOA评分、术后JOA评分改善率差异均无统计学意义(均P>0.05)。见表2。
表1 K线(+)组和K线(-)组患者手术时间与出血量的比较
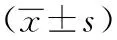
表2 K线(+)组与K线(-)组患者JOA评分及术后JOA评分改善率的比较
讨 论
本研究通过对接受颈后路棘突纵割式椎管扩大成形术治疗的C-OPLL患者的临床资料进行回顾性分析,发现K线(+)C-OPLL患者手术时间和术中出血量多于K线(-)患者。通过影像学对比发现,K线(-)患者OPLL骨化灶位置相对集中,并多累及颈椎头侧节段,而K线(+)患者骨化灶部位相对分散,并更多地向尾侧延伸,累及C7椎体。对后者需延长手术节段,做C7椎体成形、人工骨间隔物植入及T1上半椎板切除。T1椎板皮质骨厚度和松质骨含量均显著高于C7椎板,使得后者术中需要更多时间进行磨削处理,加之手术节段增加,因此较常规手术不仅手术时间延长,出血量也同时增加。但是在术后脊髓功能的改善方面,无论是K线(+)或K线(-)患者,通过接受棘突纵割式颈椎后路椎管扩大成形术,其术后JOA评分均比术前有显著提高,且两组的改善率无显著差异。
相比“单开门”手术,棘突纵割式颈椎后路椎管扩大成形术的优势有以下4点:①在新的术式中,颈椎椎管被左右对称扩大,而非像“单开门”那样变成不规则形,这样可以维持硬膜囊的正常形态,防止发生扭曲。②珊瑚人工骨被置于割开的棘突间,可以诱导形成完整闭合的椎管,防止因内部长入术后增生的瘢痕组织造成潜在的脊髓压迫[11-12]。③珊瑚人工骨通过骨传导作用,能够促进其与割开的棘突发生融合。通过以往的研究发现,珊瑚人工骨与棘突的界面上能够形成连续的骨桥,融合率可达到85%,与自体骨植骨融合的效果相近[13-14]。④珊瑚人工骨与宿主骨之间的融合牢固可靠,故人工骨在术后发生移位的病例罕见报道。其接触发生在面对面,融合面积大,而非像“单开门”仅依赖有限的螺钉或微钢板发生点对点的融合。因此,“单开门”术后螺钉松动移位是常见的并发症,常影响术后脊髓功能的恢复[15]。Liu等[16]报道,在“单开门”手术中,如果使用钉板结构固定,发生螺钉拔出的比例高达16%,即使改为全部使用锚定螺钉,螺钉拔出的比例依然可达到5%。究其原因,作者认为有以下3点:①螺钉固定的方向和角度欠佳,尤其是对于位置比较深的颈椎头侧节段,显露困难造成的手术视野受限,会影响螺钉的固定效果。②由于微钢板的设计因素,螺钉难以充分地锁紧固定。③由于颈椎解剖结构的特性,固定螺钉通常过于细小,难以达到对骨质充分的把持效果。
与传统的“双开门”椎板成形术相比,棘突纵割式颈椎后路椎管扩大成形术主要在以下4个方面存在优势:①将C3的椎板成形改良为椎板切除。Takeuchi等[17]报道由于颈半棘肌在C2棘突上的止点窄于人工骨间隔物的宽度,传统术式后使得颈半棘肌的形态会受到C3被割开的棘突和增大的椎管的干扰,存在诱发术后出现颈椎后凸改变的风险,因为颈半棘肌被看做是维持颈椎前凸和正常生理力线的最重要肌肉结构。将C3椎板切除有利于维持颈半棘肌正常的行程和功能。此外,单纯切除椎板也省去了纵割棘突和双侧沟槽的制备过程,不但节省手术时间,也降低了手术难度。②省去了常规术式中在C3和C7放置人工骨间隔物。颈椎后方过多的人工骨植入会影响颈部的活动度,特别是过伸运动,会显著增加术后轴性症状的发生率[12]。同时体内过多的内置物不但会加重患者的经济负担,也会提高术后感染的风险。③更满意的椎管扩大率。Lee等[18]发现在使用人工骨间隔物的“双开门”椎板成形术中,椎管矢状径增加的幅度为4.2~6.8 mm。尽管Orabi等[19]通过术后CT检查证实使用钉板结构的“双开门”术式也能使椎管矢状径增加6.8 mm,但术后MRI发现在硬膜与钢板之间会长入瘢痕组织,使得实际的椎管矢状径增加小于5 mm。④固定强度更高。Ou等[20]认为钉板结构的“双开门”椎板成形术实际上是做椎板纵劈,而非本研究采用的棘突纵割。由于颈椎椎板的解剖特点,钉板结构偏于小巧,固定强度要逊于人工骨间隔物与棘突间的牢固度,并且存在一定的螺钉松动率。
本研究中K线(+)组和K线(-)组的术后JOA评分及JOA评分改善率的差异均无统计学意义,与Nagashima等[21]的研究结果一致。该学者通过2年随访发现,K线并不能影响C-OPLL患者在椎板成形术后的神经功能恢复情况。K线意义的局限性主要体现在以下3个方面:①相比三维重建CT,仅通过颈椎侧位X线像有时很难判断OPLL骨化灶的形态和(或)C7椎体水平椎管的中心点,特别是对于较矮胖的患者。因此,观察者间的误差难以避免。②K线很容易受拍摄时患者颈部姿势的影响。已有学者对仅凭X线像判断C-OPLL患者的预后提出质疑[22]。有研究结果证实,过伸位K线(+)的C-OPLL患者,即使在中立位K线(-),仍然可以在颈椎后路椎板成形术后获得良好的神经功能恢复,因为这样的患者脊髓还会有一定缓冲和康复的潜力[22-24]。目前,更多学者关注患者屈曲位K线状态,而非中立位。Kimura等[25]报道屈曲位K线阴性的C-OPLL患者,在椎板成形术后神经功能恢复差,有时会残留肢体的严重疼痛。其原因是这部分患者在颈部屈曲时脊髓腹侧的神经细胞受压加重,从而影响神经功能和疼痛的改善。Takeuchi等[26]也报道,屈曲位K线(-)的C-OPLL患者术后运动功能恢复差,JOA评分改善率在这部分患者中仅为23.8%,低于屈曲位K线(+)患者(46.3%),差异有统计学意义(P=0.028)。他将这一结果归咎于患者在颈部屈曲时脊髓反复受到来自腹侧的压迫,造成了脊髓前角运动细胞的功能障碍。③C-OPLL患者在后路椎板成形术后出现颈椎后凸的病例并不少见,因而很难预测患者的K线是否在术后会出现改变,包括那些术前K线(+)患者[27]。椎板成形术后患者颈椎前凸的丢失幅度为0°~12°[28]。Fujimori等[29]发现患者术后颈椎前凸丢失平均为7°,因此提出对于骨化灶占位率超过60%的病例,术前至少颈前凸要达到20°,才能持续维持术后的疗效。因此,K线能否准确预测C-OPLL患者术后的疗效,值得商榷。一些学者已经提出某些动态指标可能会影响椎板成形术后的疗效。Ogawa等[30]指出,如果术后C2-C7的活动度增加,则会导致C-OPLL患者术后出现脊髓功能恶化。Goto和Kita[31]提出通过OPLL骨化灶的相互桥接和前纵韧带的骨化形成,可以诱发颈椎体间自发融合,这也是维持术后神经功能的重要因素。Morio等[32]发现如果脊髓受压节段存在一定的活动度,就会成为椎板成形术后疗效欠佳的危险因素。Fujiyoshi等[33]指出,即使术前存在严重压迫,如果脊髓受压节段的活动度能够被严格限制,则患者在术后的神经功能也不会发生恶化。因此,相比常规K线,动力位的K线改变和局部残留的活动度,更可能是影响C-OPLL患者椎板成形术后疗效的潜在因素。
本研究存在局限性:是回顾性研究,相对证据等级较低;缺乏随访过程中对K线和颈椎局部活动度的动态测量,可能会忽略二者对临床疗效的潜在影响;由于C-OPLL本身发病率低,导致本研究病例数和随访时间均有限。未来将补充更多的病例并延长随访时间来增加研究结果的说服力。
总之,棘突纵割式颈椎后路椎管扩大成形术是治疗C-OPLL的有效方法,其疗效不受患者K线的影响。
