晕可平糖浆中19 种无机元素的形态分析
2022-03-11丁爱华潘富荣陈玲玲支荣荣周会芹
丁爱华,潘富荣,谢 斌,陈玲玲,支荣荣,周会芹*
1 盐城市食品药品监督检验中心,盐城 224055;2 江苏医药职业学院,盐城 224005
微量元素是人体必需的组成部分,也是中药中普遍含有的一类成分。早期元素研究主要集中在总量的测定,自20 世纪50 年代日本水俣病事件发生后,科学家认识到形态分析的重要性。不同形态的元素具有不同的理化性质、毒性或疗效。例如,砷在亚砷酸盐[As(Ⅲ)]和砷酸盐[As(V)]等无机形式中通常都是有毒的,但在砷甜菜碱和砷胆碱等高度甲基化的有机形式中却是无毒的;锌的无机态在生物体内生物利用率较低且有毒副作用,而与多糖或蛋白结合的有机锌更易于吸收,且具有抗氧化、抗高血脂或保护神经元的作用[1-3]。因此,形态分析对了解中药中元素药性和毒性至关重要,也是其有效化学成分研究的补充和发展,这为阐明中药的作用机制提供了有力的证据。
晕可平糖浆由生赭石、夏枯草、法半夏、车前草4 味中药组成,主治肝旺痰阻型的内耳眩晕症、头晕、目眩症。生赭石是方中君药,是氧化物类矿物刚玉族赤铁矿,主含三氧化二铁(Fe2O3),其发挥药效的物质基础值得深入研究。
目前赭石及其他3 味中药中Fe、Mg、Ca、Mn、Ni、Cu、Zn 等元素的检测已有报道[4-6],前期研究对晕可平糖浆中Fe 及重金属元素进行了检测[7,8],而晕可平糖浆中元素的形态分析尚未见报道。因此,以中草药元素形态分析的层次模式[9,10]为基础,结合正辛醇-水分配系数(KOW)评价体系[11,12],采用传统化学分离技术和电感耦合等离子体质谱检测方法(ICP-MS),对晕可平糖浆中19 种元素进行形态分析,计算有关形态分析参数,为阐明以赭石为君药的晕可平糖浆的作用机制提供基础数据。
1 仪器与药品、试剂
1.1 仪器
iCAP RQ 型电感耦合等离子体质谱仪(赛默飞世尔科技公司);Multiwave PRO 微波消解仪(奥地利安东帕(中国)公司);Milli-Q 超纯水处理装置(美国Millipore 公司)。所用器皿均经20%硝酸浸泡24 h 以上,再用超纯水冲洗3 遍,晾干备用。
1.2 药品与试剂
晕可平糖浆(100 mL/瓶,精华制药集团股份有限公司,批号为61200402);多元素标准溶液(100 μg·mL-1,批号为20D8383),锗(Ge)、铟(In)、铋(Bi)的混合内标溶液(10 μg·mL-1,批号为20D3605)国家有色金属及电子材料分析测试中心;钡(Ba)、铋(Bi)、铈(Ce)、钴(Co)、铟(In)、锂(Li)、铀(U)混合标准溶液的调谐溶液(1.0 μg·L-1,赛默飞世尔科技公司);001×7(732)阳离子交换树脂(国药集团化学试剂公司);D401 型螯合树脂(江苏苏青水处理工程集团);三氯甲烷、正辛醇为分析纯;硝酸为UP 级;水为超纯水。
2 方 法
2.1 仪器条件
用质谱调谐液调试仪器至测定要求。射频功率:1550 W;等离子体气体、辅助气体、雾化器、碰撞气体流量分别为14、0.8、1、5 L·min-1,采集深度为5.0 mm,延迟时间为0.03 s,积分时间为7.8 s。数据采集重复次数3 次,扫描次数为10 次,采集模式为KED 模式,定量分析。
2.2 混合对照溶液的制备
精密量取22 种多元素混合标准溶液,用2%硝酸溶液稀释成含各元素为0.2、0.5、1、2.5、5、10、25、50、100、125、200、500、1000 ng·mL-1的系列浓度混合标准工作液。
精密量取Ge、In、Bi 混合内标溶液适量,用2%硝酸溶液稀释成50 ng·mL-1的混合内标溶液(配制时加入Au 单元素标准溶液,最终浓度为100 ng·mL-1)。
2.3 供试品溶液的制备
2.3.1 初级形态分离取晕可平糖浆(供试品溶液A)100 mL,经高速离心后,将离心液用0.45 μm 微孔滤膜过滤,所得滤液为可溶态供试品B;离心及滤膜上的残渣为悬浮态供试品C。
可溶态比重(%)=含量可溶态B/含量供试品A× 100%
2.3.2 次级形态分离树脂的预处理[13]:用75%的乙醇浸泡过夜,用超纯水清洗干净。用1 mol·L-1NaOH 浸泡2 h,用超纯水洗至近中性,改用1 mol·L-1HCl 处理2 h,最后用超纯水洗至近中性,备用。
游离态与非游离态的分离:精密量取可溶态溶液B 5 mL,通过001×7 阳离子交换树脂柱(Φ10 mm×100 mm),流速0.5~1 mL·min-1,用超纯水(60 mL)淋洗树脂柱,收集流出液和水洗液,浓缩转移至5 mL量瓶中,定容至刻度,得非游离态D-Ⅰ。柱截留物用2 mol·L-1硝酸(150 mL)洗脱,收集洗脱液,浓缩转移至5 mL 量瓶中,定容至刻度,得游离态D-Ⅱ。
稳定态与不稳定态的分离:可溶态溶液B 用D401 螯合树脂柱处理,处理方法同001×7 阳离子交换树脂柱,柱截留物为不稳定态E-Ⅰ,穿过物为稳定态E-Ⅱ。
无机态与有机态的分离:精密量取可溶态溶液B 10 mL,用三氯甲烷萃取(20 mL×3 次),每次振荡3 min。水相为无机态F-Ⅰ,差减法计算有机态F-Ⅱ的含量。
非游离态比重(%)=含量非游离态D-Ⅰ/含量可溶态B×100%游离阳离子态比重、稳定态比重、不稳定态比重、无机态比重、有机态比重,计算均同非游离态比重。
2.3.3 正辛醇/水分配体系模拟试验 精密量取可溶态溶液B 各10 mL,用稀硝酸和0.1 mol·L-1氢氧化钠溶液分别调节pH 为1.3(胃液酸度)和7.6(小肠液碱度),置于37 ℃恒温水浴振荡器中保温12 h后,每份加正辛醇10 mL,水浴恒温振荡2 h,萃取2次,合并2 次萃取的水相和有机相,水相浓缩转移至10 mL 量瓶,定容至刻度,分别得到模拟胃液和小肠液条件下各元素的水溶态G-Ⅰ、H-Ⅰ,差减法计算醇溶态的含量G-Ⅱ、H-Ⅱ。KOW值为正辛醇吸收模型中醇溶态含量和水溶态含量的比值。
2.3.4 试样的消解精密量取上述A、B、D-Ⅰ~F-Ⅰ、G-Ⅰ、H-Ⅰ溶液各2 份,每份1 mL,置微波消解罐内,加入硝酸5 mL,密塞,放入微波消解仪。消解完毕后,放冷,将消解液转移至50 mL 量瓶中,用少量超纯水洗涤消解罐3 次,洗液合并于量瓶中,加入Au 单元素标准溶液(1 μg·mL-1)200 μL,用水稀释至刻度,摇匀,即得供试品溶液。精密量取1 mL 置100 mL 量瓶中,用2%硝酸溶液稀释成至刻度,摇匀,作为测定Mg、Si、K、Ca 的供试品溶液。除不加Au单元素标准溶液外,余同法制备试剂的空白溶液。
2.4 标准曲线绘制及各形态样品无机元素含量测定
仪器的内标进样管在仪器分析过程中始终插入内标溶液中,依次将仪器样品管插入各个浓度的标准工作液中进行测定(浓度依次递增),以测量值(3 次的平均值)为纵坐标,浓度为横坐标,绘制标准曲线。重复测定空白溶液11 次,各元素信号响应的3 倍标准偏差(3SD)对应的元素浓度即为仪器检测限。依次将仪器样品管插入各形态供试品溶液及相应的空白溶液中进行测定,从标准曲线上计算得相应的浓度。
3 结果与分析
3.1 分析方法的可靠性
本实验中所采用分析方法的标准曲线和检测限结果见表1。
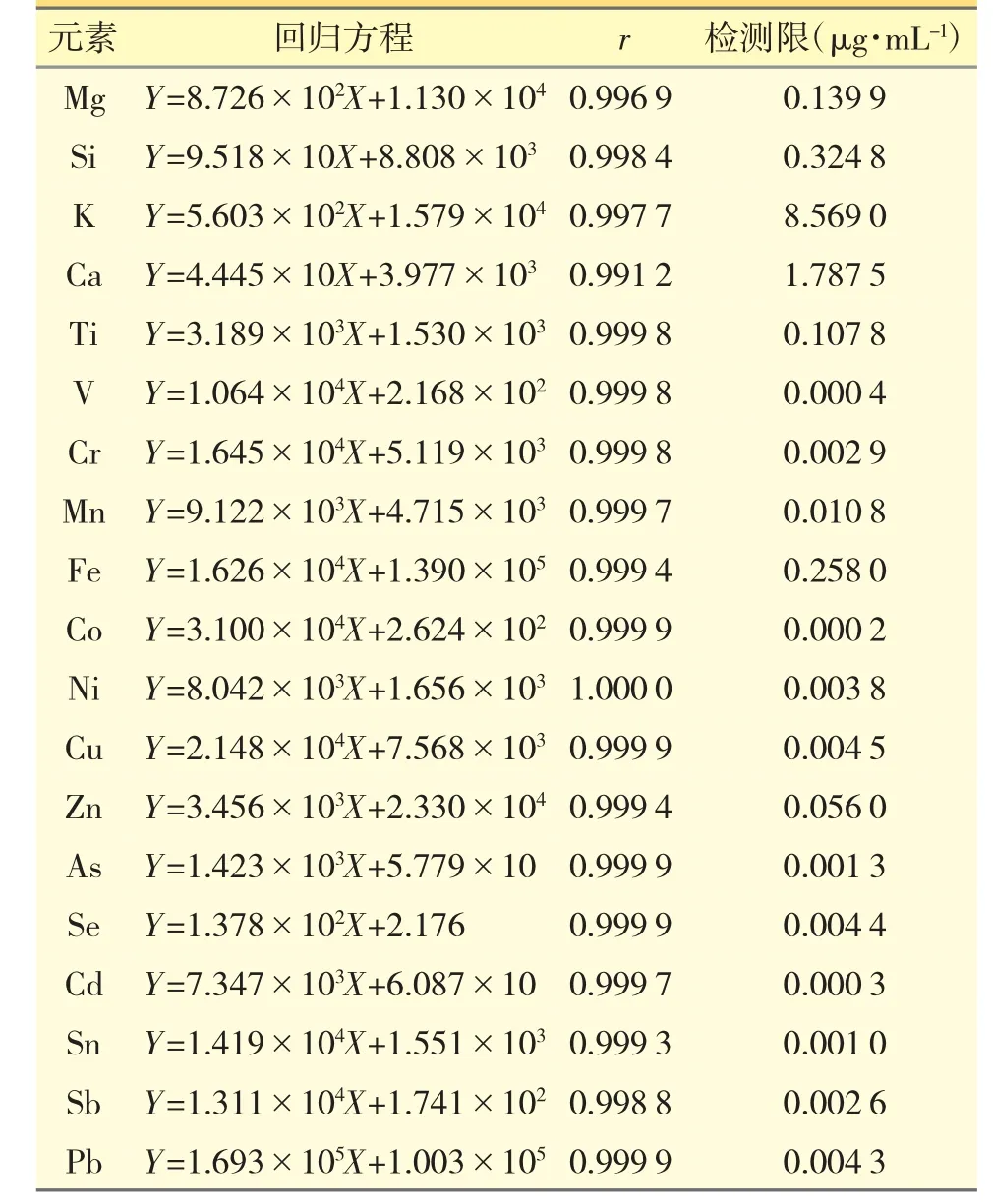
表1 各元素线性关系及检测限
精密量取1 mL 可溶态溶液B,平行6 份,做重复性试验,同时对同一份溶液连续进样6 次,做进样精密度试验。另精密量取1 mL 可溶态溶液B,平行6 份,精密加入多元素标准溶液20 μL,做回收率试验。按可溶态处理方法进行消解测定,各元素的重复性试验结果的RSD 为2.9%~14.1%;精密度试验结果的RSD 为2.0%~9.5%;平均回收率为81.4%~119.0%、RSD 为1.0%~9.5%,均满足方法学考察要求。
3.2 糖浆中微量元素的传统形态分析结果
实验建立了晕可平糖浆中19 种微量元素的形态分析方法(Cr、Se、Sn、Pb 未检出),根据糖浆中各形态分析测定结果,计算形态分析参数,结果见表2和表3。
由表2、表3 可知,在晕可平糖浆中含量较高的有Mg、Si、K、Ca、Ti、Mn、Fe 等元素,其中含量最高的K 浓度达4633.485 μg·mL-1,同时也含有少量对人体有害的Cu、As、Cd、Sb 等重金属。糖浆中Si、V、Mn、Fe、Cu、As 元素的悬浮态比重较高,其中Cu 悬浮态的含量高于可溶态。在可溶态中,Mg、K、Ca、Ti、Mn、Co、Ni、Zn、Cd 大部分以游离态及不稳定态的形态存在;Si、V、Cu、As、Sb 存在比重较高的非游离态及稳定态,其中Si、As、Sb 非游离态及稳定态的比重高达90%以上;Cu、Cd 不稳定络合态比重(非游离态比重与稳定态比重之差)较高,分别为43.3%、35.2%;Fe 的非游离态及稳定态各占50%左右。在可溶态中,Fe 的有机态比重最高,为30.8%,Cu 次之,为14.2%。
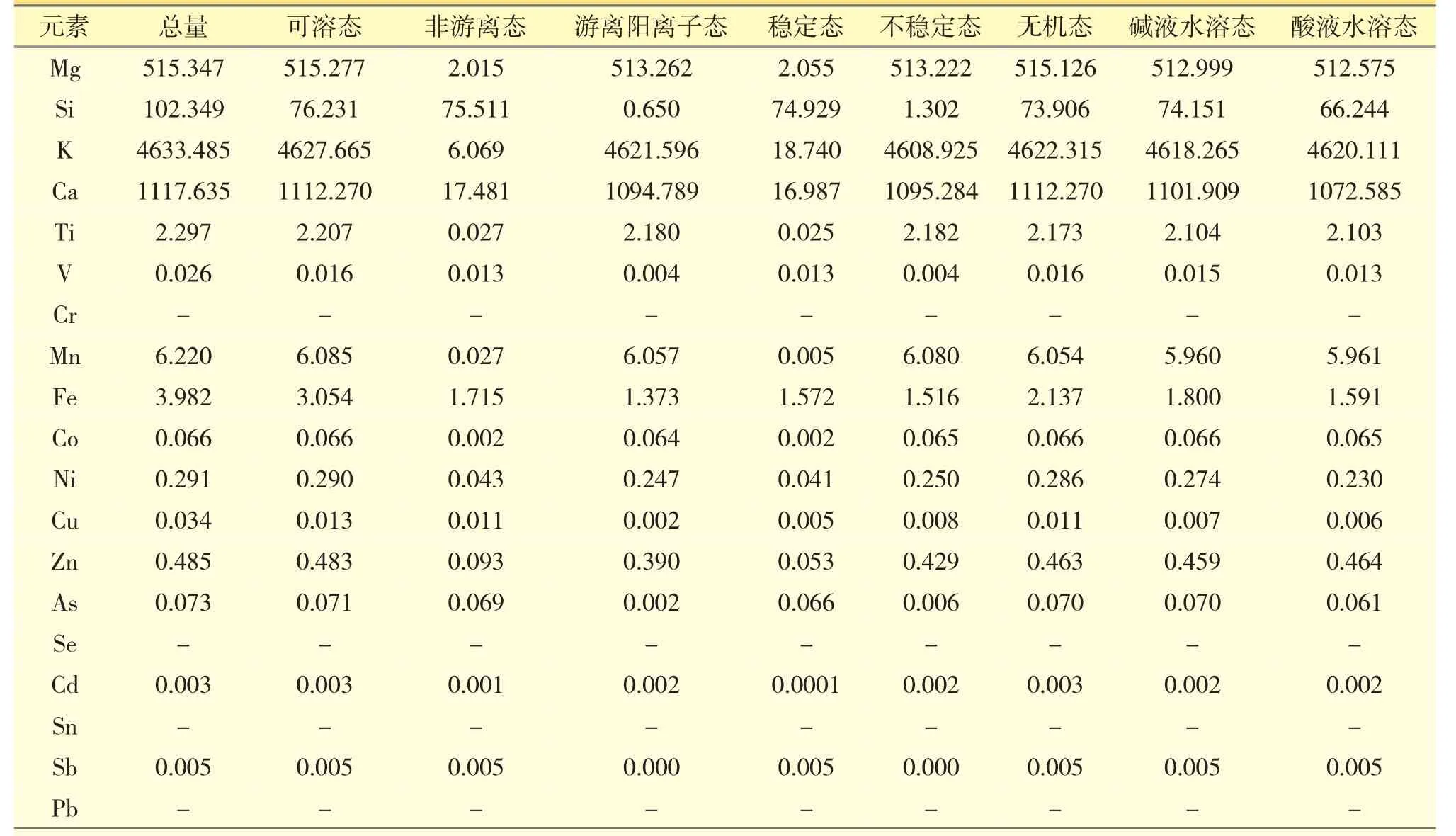
表2 晕可平糖浆中各元素形态分析测定结果(μg·mL-1)
3.3 胃肠酸度变化对糖浆中微量元素形态的影响
正辛醇结构性质与人体碳水化合物和脂肪类似,中药药理学常以正辛醇-水分配系数(KOW)模拟元素在人体胃、肠中的分配情况,评价中药中相关元素的亲脂性和生物活性[14,15]。KOW参数越大,表明正辛醇醇溶态中的微量元素亲脂性及生物活性越强。由表2 和表3 可知,无论在碱性还是酸性条件下,各元素的KOW值均小于1,其中Fe 和Cu 的KOW值接近于1,表明糖浆中各元素的亲脂性和生物活性均较弱,Fe 和Cu 是其中生物活性相对较强的元素。pH 变化对Mg、K、Ti、Sb 等的影响不大,其余微量元素的含量随pH 变化而变化。
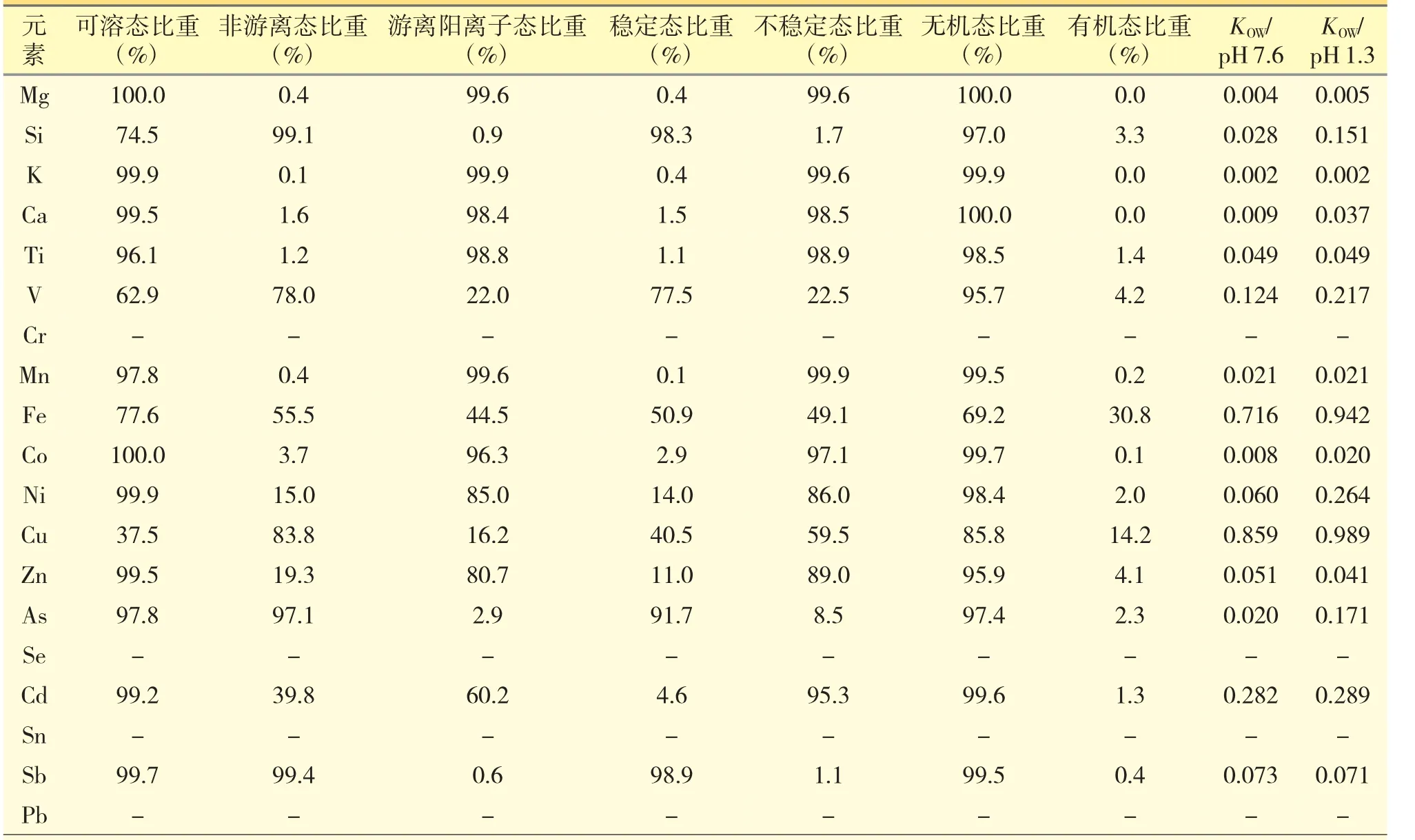
表3 晕可平糖浆中各元素形态分析参数结果
4 讨论
由于中药样品基体复杂且待测组分含量低,形态分析比常规测定元素的总量要困难得多。目前,气相色谱法、高效液相色谱法和毛细管电泳等分离技术联用ICP-MS 可用于多元素形态的检测;但成本偏高,可同时分析的元素种类相对较少。传统化学分离前处理方式联合ICP-MS,具有快速、简便、易推广、不受元素种类限制的优点,是前期挖掘和筛选元素形态信息的便捷技术途径。
本实验对晕可平糖浆中19 种无机元素进行形态分析,结果发现重金属元素As、Sb 主要以稳定态存在,KOW值也远小于1,表明As、Sb 很难被人体吸收、转化成为其他分子形态。Cu、Cd 的不稳定络合态比重较高,易被打破平衡参与新的化学反应;但鉴于其KOW值小于1,所致健康风险在安全范围内[8],因此后期安全性监控主要是检测Cu、Cd 的含量。
本实验还发现,Fe 可能是晕可平糖浆的药效部位之一。糖浆中含量高的元素主要是Mg、Si、K、Ca、Mn、Ti 和Fe,除Fe 以外的其他元素基本以游离态存在,不易与糖浆中的各种配体发生化学反应;此外,Fe 的有机态比重最高,KOW值接近于1,因此推测Fe 是糖浆发挥药效最相关的元素。当生赭石与方中其他药物共煎时,游离态Fe 与有机酸、黄酮等配体成分络合达到动态平衡[16-18];Fe 进入人体后,在不同靶位配合平衡被打破,通过游离态的调整进入新的平衡,出现新的生物活性。相关文献发现,Fe 在线粒体的氧代谢、氧摄取、电子传递、能量代谢、肌肉功能、造血、免疫保护等方面发挥着重要作用[19]。后期将对不同形态Fe 与糖浆中有机成分以及生物体之间的作用进行深入的研究。