基于抗坏血酸的沉淀法除氯
2022-03-09叶志伟段佳男吴思成李登新朱宏艺肖政国
叶志伟,段佳男,吴思成,李登新,朱宏艺,肖政国
(1. 东华大学 环境科学与工程学院,上海 201620;2. 东华大学 国家环境保护纺织工业污染防治工程技术中心,上海 201620)
随着工业化的发展,越来越多的行业涉及含氯废水的排放,产生了大量含氯废水,这些含氯废水不仅影响工业生产,还对生态环境和人体健康产生不利影响。为此,国内许多省市相继出台了关于氯离子排放限值的标准,如上海市最新的氯离子二级排放限值为250 mg/L;河北省氯化物排放标准按照不同的行业以及不同的等级来划分,其中氯离子最高的允许排放限制为600 mg/L。国内外对于含氯废水的处理开展了大量研究,目前主要的除氯方法有反渗透法、离子交换法、化学沉淀法、电渗析法等。其中:离子交换法对水质要求高,且使用价格较贵;电渗析法主要处理低浓度废水,且耗能高;反渗透法的膜组件容易堵塞;而化学沉淀法操作简单,去除氯离子的速度较快。
对已有化学沉淀法去除溶液中氯离子的研究进行分析,发现:由于价格昂贵,银盐沉淀法主要用于检测氯离子;亚硫酸钠法会产生二氧化硫有毒气体,危害环境;而铜粉法和锌粉法的氯离子去除率较低。因此,需要开发一种价格较低、绿色环保且高效的除氯方法。
抗坏血酸(CHO)是一种很强的还原剂,常用于高效还原制备铜纳米粒子。作为一种绿色无毒的还原剂,抗坏血酸也广泛应用于工业生产和环境治理中。
本研究以抗坏血酸为除氯剂,将Cu还原成Cu并与氯离子结合生成氯化亚铜沉淀,从而去除溶液中的氯离子。考察了反应pH、五水硫酸铜(CuSO·5HO)与抗坏血酸的物质的量比、反应时间、反应温度、五水硫酸铜与氯离子的物质的量比、初始氯离子浓度等参数对除氯的影响,并通过XRD和EDS对沉淀产物进行分析,初步探究了反应机理。
1 实验部分
1.1 试剂、材料和仪器
氯化钠、五水硫酸铜、氢氧化钠、硫酸:均为分析纯,购自国药集团。-抗坏血酸(VC):分析纯,购自上海泰坦科技公司。实验用水为去离子水。
模拟废水:用氯化钠和去离子水配制的模拟含氯废水。
实际废水:取自河北省某发电厂脱硫废水,氯离子质量浓度为7 067 mg/L。
PHSJ-3F型pH计、PCl-1-01型氯离子电极和232-1型参比电极:上海雷磁仪器厂。COS-110X5型恒温水浴震荡器:上海比朗仪器有限公司。D/max-2550VB+/PC型18 kW转靶X射线衍射仪:日本理学公司;S-4800型扫描电子显微镜:日本日立公司。
1.2 实验及分析方法
配制200 mL一定浓度的模拟废水,分别投加一定量的五水硫酸铜和抗坏血酸,用氢氧化钠溶液或硫酸溶液调节pH至设定值,在恒温水浴振荡器中以相同的转速(600 r/min)搅拌一定时间。过滤,用离子选择电极法测定滤液中氯离子的质量浓度。根据反应前后溶液中氯离子的质量浓度计算其去除率。
将沉淀产物洗涤、干燥、研磨后进行表征分析。采用XRD分析沉淀产物的物相结构;采用SEM-EDS分析沉淀产物的元素组成,观察沉淀产物的微观形貌。
利用模拟废水考察不同反应条件下抗坏血酸作为除氯剂的除氯效果,优化工艺条件,最后在最佳条件下处理实际废水。
2 结果与讨论
2.1 反应pH的影响
在初始氯离子质量浓度为1 517 mg/L、(Cu)∶(VC)∶(Cl)为3.0∶1∶2、反应温度为20 ℃、反应时间为20 min的条件下,考察在不同反应pH下氯离子的去除效果,结果见图1。

图1 反应pH对除氯的影响
当反应pH小于3.6时,氯离子的去除率随pH的增大逐渐提高,特别是在3.0~3.6的范围内氯离子去除率增长较快;反应pH为3.6时氯离子去除率达到最高;当反应pH高于3.6时,氯离子去除率随pH的升高逐渐降低。原因是抗坏血酸的还原能力随着碱性的提高而增强。在反应pH小于3.6时,抗坏血酸只将铜离子还原成亚铜并与氯离子结合生成氯化亚铜沉淀(见式(1)和式(2),式中HA代表抗坏血酸,A代表去氢抗坏血酸);当反应pH高于3.6时,部分铜离子被直接还原成铜单质(见式(3)),导致去除率降低。因此,反应pH为3.6较适宜。

2.2 五水硫酸铜与抗坏血酸物质的量比的影响
在初始氯离子质量浓度1 517 mg/L、反应pH为3.6、(VC)∶(Cl)为1∶2、反应温度为20 ℃、反应时间为20 min的条件下,考察在不同(Cu)∶(VC)下氯离子的去除效果,结果见图2。

图2 n(Cu)∶n(VC)对除氯的影响
氯离子去除率随着(Cu)∶(VC)的增大而逐渐增大,当(Cu)∶(VC)从1.5∶1增至2.0∶1时,氯离子去除率增长较快,从50%左右增至80%以上。当(Cu)∶(VC)为3.0∶1时,氯离子去除率最高,继续增大(Cu)∶(VC),氯离子去除率的变化较小。因此,(Cu)∶(VC)为3.0∶1较适宜。
2.3 反应时间的影响
在初始氯离子质量浓度为1 517 mg/L、反应pH为3.6、(Cu)∶(VC)∶(Cl)为3.0∶1∶2、反应温度为20 ℃的条件下,考察在不同反应时间下氯离子的去除效果,结果见图3。
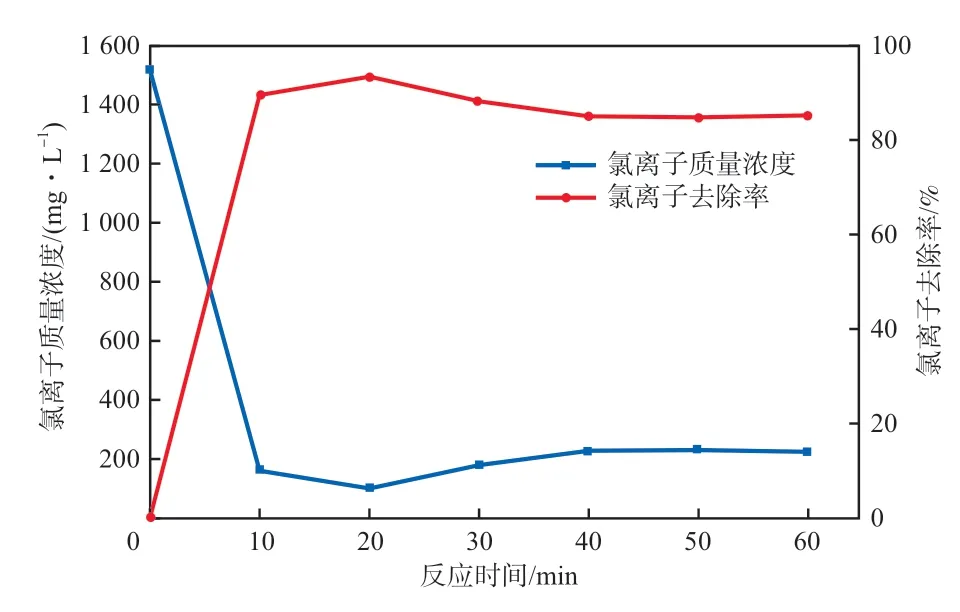
图3 反应时间对除氯的影响
随着反应时间的延长,氯离子去除率快速提高,在20 min左右即达到最大值。继续延长反应时间,氯离子去除率略有降低,并维持在一个水平上。原因是:抗坏血酸在pH为3.6时还原性较强,还原铜离子的速度很快,在反应的初始阶段能够很明显看到溶液中有白色沉淀大量生成,溶液也很快从澄清变为浑浊;当反应时间超过20 min后,因为溶解氧氧化氯化亚铜,氯离子又释放到溶液中,增加了溶液中剩余氯离子的浓度,导致其去除率有所降低。因此,反应时间为20 min较适宜。
2.4 反应温度的影响
在初始氯离子质量浓度为1 517 mg/L、反应pH为3.6、(Cu)∶(VC)∶(Cl)为3.0∶1∶2、反应时间为20 min的条件下,考察在不同反应温度下氯离子的去除效果,结果见图4。
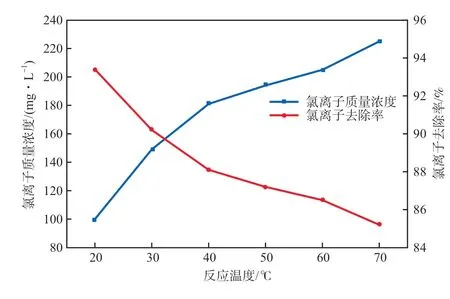
图4 反应温度对除氯的影响
随着反应温度的升高,氯离子的去除率逐渐下降。当反应温度在20 ℃时,氯离子的去除率最高。升高反应温度,反应后溶液中剩余氯离子浓度也逐渐增大。可能是因为温度越高,抗坏血酸的稳定性越差,更易分解,同时温度升高还易引起氯化亚铜复溶,导致了温度越高氯离子的去除率越低。因此,反应温度为20 ℃较适宜。
2.5 五水硫酸铜与氯离子摩尔比的影响
在反应pH为3.6、(Cu)∶(VC)为3.0∶1、反应时间为20 min、反应温度为20 ℃的条件下,考察在不同(Cu)∶(Cl)下氯离子的去除效果,结果见图5。

图5 n(Cu)∶n(Cl)对除氯的影响
(Cu)∶(Cl)在1.0∶1至1.5∶1的范围内,随(Cu)∶(Cl)的增大氯离子去除率逐渐提高,(Cu)∶(Cl)为1.5∶1时,氯离子的去除率最高。继续提高(Cu)∶(Cl),氯离子去除率有所降低。在实验过程中,可观察到(Cu)∶(Cl)在2.0∶1至6.0∶1范围内,均生成了部分铜单质(见图6a橙色部分),其微观形貌各异,大小不一,粒径为1~4 μm(见图6b)。这可能是因为铜离子在溶液中的浓度很高,而抗坏血酸的还原性又很强,直接将部分铜离子还原成铜单质,减少了亚铜的产生,最终导致氯离子的去除率有所降低。因此,(Cu)∶(Cl)为1.5∶1较适宜。

图6 铜单质的照片(a)和SEM照片(b)
2.6 初始氯离子浓度的影响
在反应pH为3.6、(Cu)∶(VC)∶(Cl)为3.0∶1∶2、反应温度为20 ℃、反应时间为20 min的条件下,考察在不同初始氯离子浓度下氯离子的去除效果,结果见图7。

图7 初始氯离子浓度对除氯的影响
总体而言,氯离子去除率随着初始氯离子浓度的增大而提高。在初始氯离子质量浓度为1 000 mg/L时,氯离子去除率为92.8%,且溶液中剩余氯离子质量浓度非常低,仅为71 mg/L,远低于河北省氯离子的排放限值。在初始氯离子质量浓度为4 000 mg/L时,氯离子去除率为96.6%,溶液中剩余的氯离子质量浓度也仅为135 mg/L。上述结果表明,利用抗坏血酸作为除氯剂,对于不同初始氯离子浓度的溶液均有较好的去除效果。
2.7 XRD和EDS分析
最佳条件下沉淀产物的XRD和EDS分析结果如图8所示。将沉淀产物的XRD谱图(图8a)与标准氯化亚铜的谱图JCPDS NO.06-0344对比,可以发现实验的沉淀产物为氯化亚铜。由沉淀产物的EDS谱图(图8b)可知,沉淀产物中的元素只有Cu和Cl,二者的摩尔分数分别为50.3%和49.7%,进一步印证了沉淀产物为氯化亚铜。由于氯化亚铜的特殊性能,使其在工业中得到了广泛应用,可用做催化剂,也可制作电化学电池等。

图8 沉淀产物的XRD(a)和EDS(b)谱图
2.8 实际废水的除氯效果
在上述最佳条件下处理实际废水(初始氯离子质量浓度7 067 mg/L),处理后出水中氯离子质量浓度为87 mg/L,氯离子去除率高达98.7%。
3 结论
a)采用抗坏血酸作为除氯剂脱除氯离子,在反应pH为3.6、(Cu)∶(VC)∶(Cl)为3.0∶1∶2、反应温度为20 ℃、反应时间为20 min的最佳条件下,初始氯离子质量浓度为1 000~4 000 mg/L时均有较高的除氯效率,氯离子去除率最高可达96.6%,且溶液中剩余的氯离子质量浓度均低于250 mg/L。
b)在上述最佳条件下处理实际废水(初始氯离子质量浓度7 067 mg/L),处理后出水中氯离子质量浓度为87 mg/L,氯离子去除率高达98.7%。
c)XRD和EDS的表征结果显示,最佳条件下反应后的沉淀产物为氯化亚铜。氯化亚铜具有一定的商业价值,未来或许可以研究如何在除氯的过程中产生一定的经济效益。
