非对称截面螺旋流道中微粒的惯性聚焦效应
2022-03-07韩帅张鑫杰顾乔刘尧王昕怡
韩帅,张鑫杰*,顾乔,刘尧,王昕怡
非对称截面螺旋流道中微粒的惯性聚焦效应
韩帅1,张鑫杰1*,顾乔2,刘尧1,王昕怡1
(1.河海大学 机电工程学院,江苏 常州 213022;2.苏州大学附属第三医院 妇产科,江苏 常州 213000)
为实现生物微粒/细胞的精确操控,提出了一种非对称截面螺旋流道结构的惯性微流控芯片。基于仿真和实验的方法,对不同尺寸微粒在微流道中的惯性聚焦行为进行了研究。设计了一种“L”形截面的螺旋流道,采用仿真软件COMSOL研究微流道中的二次流场及微粒的运动轨迹。使用UV激光切割与等离子清洗键合的工艺制作芯片样件,采用高速摄像机和荧光显微镜分别拍摄6,10和15 μm粒子在微流道中不同流量时的运动轨迹。最后,对粒子运动图片进行堆叠分析,研究微粒的惯性聚焦迁移机理。结果表明:“L”形截面中产生了两对强度不同的非对称二次流场,使得10 μm和15 μm粒子在微流道外圈实现了强聚焦,而6 μm粒子实现了粗聚焦。该研究表明利用非对称二次流可以调节微粒的聚焦位置,为微粒和细胞的精准操控提供新的思路。
微流控;非对称二次流;惯性聚焦;微粒操控;激光加工
1 引 言
惯性微流控作为一种被动式的微粒/细胞操控技术,利用流体惯性效应诱导微粒在微流道中受惯性力迁移实现精确操控,具有结构简单、操作方便、操控精度高等优势[1],在微尺度流式细胞计[2]、细胞分选[3]、细胞培养[4]和血浆提纯[5]等领域具有良好的应用前景。
惯性微流控的发展历程最早可以追溯到1961年,segre和silberberg首次发现圆管中的悬浮粒子收缩聚焦到离圆心半径0.6倍的环面上,该现象被称为“管状收缩效应”[6]。随后,美国哈佛医学院的Mehmet Toner课题组于2007年首次报道了惯性微流控技术[7]。随着微纳制造技术的发展,国内外一些课题组对惯性微流控理论进行了深入探索,研制了一大批具有特殊结构与功能的惯性微流控芯片,在其生化应用研究中取得了突破性的进展。
目前,已报道的惯性微流控芯片基于流道结构主要分为直线型、扰动型和弯曲型。微粒在直线型流道中主要受到来自流道壁面和流体剪切梯度共同诱导的惯性升力作用,惯性升力促使微粒朝流道壁面方向迁移并最终聚焦在近壁面的对称位置。如圆形截面流道中微粒聚焦在距管道中心约0.6倍半径的同心圆环上,矩形截面流道中微粒聚焦在靠近截面两条长边的中心线上(截面为长方形)或四边的中心线上(截面为正方形)[8]。扰动型流道是在直线型流道基础上拓展而来的一类流道结构,通过在流道中设置微型障碍物诱导流体扰动进而产生二次流效应,使微粒受惯性升力的同时还受到随二次流运动方向的拖曳力,因此可用于不同尺寸微粒的分离操控[9]。在弯曲型流道中,流道曲率使流体由于离心力和径向压力不对称而在垂直于主流动方向上产生二次流漩涡,即迪恩流现象[10]。由于微粒同时受惯性升力与二次流曳力作用聚焦在特定的流层平面内,有效减少了聚焦平衡位置数量,因此有助于微粒的精确操控。
矩形截面流道是最为常见的结构形式,主要原因在于实验室传统的软光刻技术所制备的微流道截面通常为矩形。近年来,国外个别实验室采用精密机加工[11]、3D打印[12]等方式制作了一些复杂截面的惯性微流道,如梯形[13]、菱形[14]、半圆形[15]和组合形[16]等,进一步推动了惯性微流控机理及应用的发展。
虽然惯性微流控技术已有大量研究成果,仍有必要对微粒的惯性聚焦机理进行深入研究,尤其是复杂截面流道中的微粒聚焦效应仍不明确。本文提出了一种新型的“L”形截面螺旋流道结构的惯性微流控芯片,通过仿真和实验的方法,研究了三种不同尺寸粒子在该微流道中的惯性聚焦效应,为实现生物粒子/细胞的精准、多样化操控提供新的思路。
2 材料与方法
2.1 微粒聚焦原理
在特定雷诺数下,微流道中入口处随机分布的粒子会逐渐迁移至流道横截面的特定位置,这种现象被称为惯性聚焦效应。在直流道中,导致粒子产生横向聚焦迁移的力为惯性升力L[17]:

当通道从直流道变为弯流道时,弯流道中心区域与近壁面区域的流体流速不匹配,流体在流道截面上产生两个对称旋转的漩涡,该现象即为Dean流(或二次流)效应。假设流体遵循斯托克斯定律,则迪恩曳力D的计算公式可近似为[18]:

其中:为流体的动态黏度,p为粒子直径,D为Dean流速。
因此,粒子处于弯流道内时会同时受到二次流曳力和惯性升力的作用。由式(1)和式(2)可知,粒子的惯性升力L与粒子直径p的四次方成正比,二次流曳力D与粒子直径p的一次方成正比,因此随着粒子直径的增大,惯性升力L大于二次流曳力D,粒子更容易出现聚焦现象。此外,通过改变Dean流场强度,可以改变粒子的聚焦平衡位置、平衡位置数量和聚焦带宽等。
2.2 芯片结构设计
微流控芯片的流道结构如图1所示,流道截面为内低外高的“L”形,该流道可以看成为上、下两个矩形流道的叠合,上、下矩形流道的截面尺寸分别为250 μm×75 μm和500 μm×75 μm(图1(a))。流道总体空间结构为螺旋形,具有一个入口和一个出口。螺旋流道共8圈,中心起始圈半径为3.25 mm,终止圈半径为21.50 mm,各圈间隔为2.50 mm,流道总长度为563.85 mm(图1(b))。基于上述流道结构设计了惯性微流控芯片。芯片共4层,依次为盖板、1#流道层、2#流道层和底板(图1(c))。每层都有4个定位孔,盖板层具有流体入口和出口,1#流道层和2#流道层分别具有“L”形流道的上、下矩形流道结构。
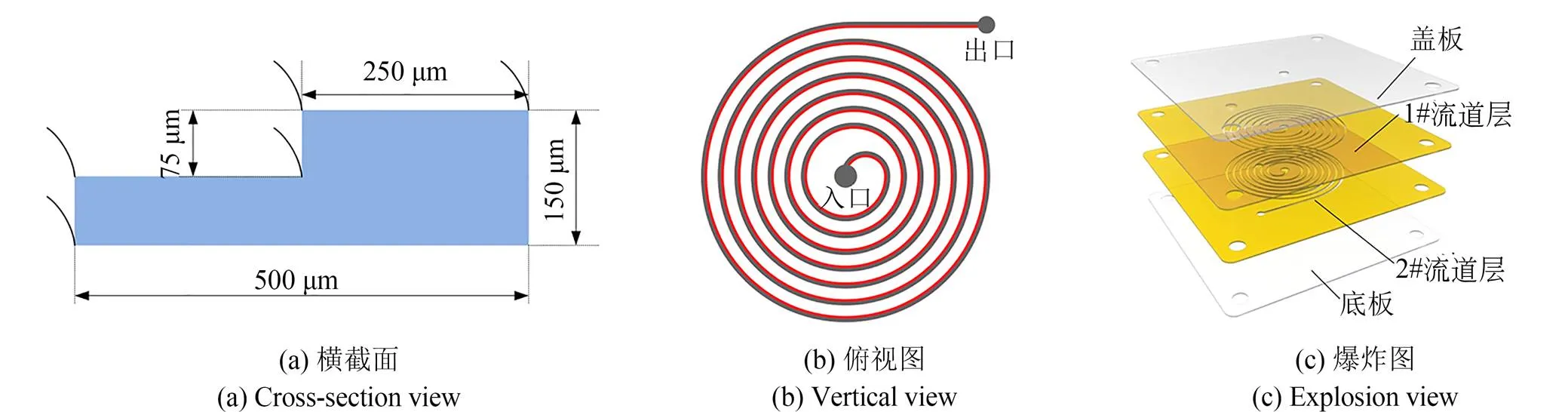
图1 微流控芯片结构示意图
2.3 微粒运动仿真
为初步了解“L”形截面螺旋流道中微粒的惯性聚焦行为,采用多物理场仿真软件COMSOL Multiphysics 5.5®对微流道进行建模,研究流道中的二次流场分布,并利用粒子追踪模块研究粒子的运动轨迹。流道模型层流采用离散化P2+P2(二阶速度+二阶压力),粒子追踪模块中粒子的密度和直径分别为1 064 kg/m3和6,10,15 μm。粒子添加流体曳力和壁诱发升力,每个时间步释放5个粒子。
仿真计算得到流道中二次流场分布及15 μm粒子的运动状况,如图2(a)所示。外壁面处的流体沿着流道上下底面回流,并在流道截面中心线两侧产生内弱、外强两对强度显著不同的非对称二次流旋涡,且两对二次流旋涡中的大部分流体被约束在各自所属的内侧和外侧矩形截面中。此外,在两个漩涡的交界处,左侧漩涡中心有部分流体汇入右侧漩涡中(图2(b))。粒子一开始在流道入口处呈随机分布,随后在流体作用下逐渐向流道外侧运动,最后聚焦于外侧矩形流道的近内壁面处(图2(c)~2(d))。作为对比,常规矩形截面螺旋流道中15 μm粒子聚焦于流道的内壁面处(图2(e))。可以发现,“L”形截面与矩形截面中粒子的聚焦结果并不完全相同。究其原因,可以推断粒子在“L”形截面流道中受外侧强二次流曳力的影响,使得粒子无法在内壁面处达到受力平衡,最终被拽入外侧流道中实现聚焦。6 μm和10 μm粒子在“L”形截面流道中的仿真结果如图2(f)~2(g)所示。其中,绝大多数6 μm粒子被束缚在高侧流道,只有少量粒子在低侧流道中,而10 μm粒子聚焦成带状。
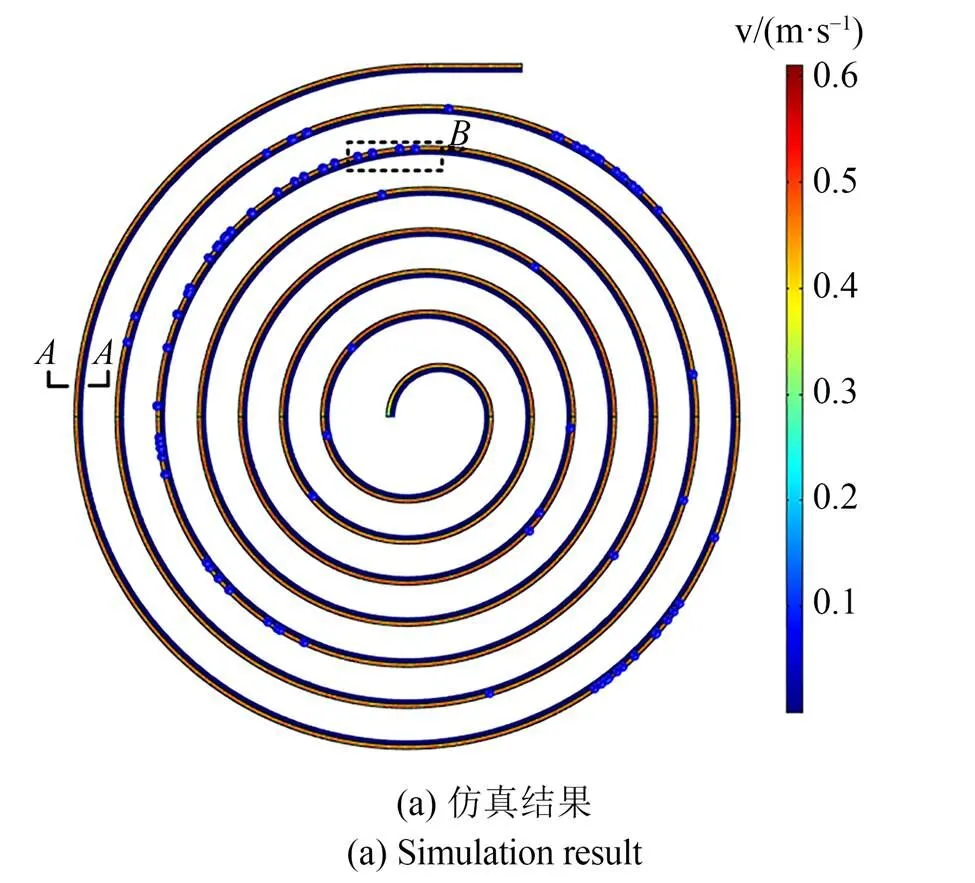
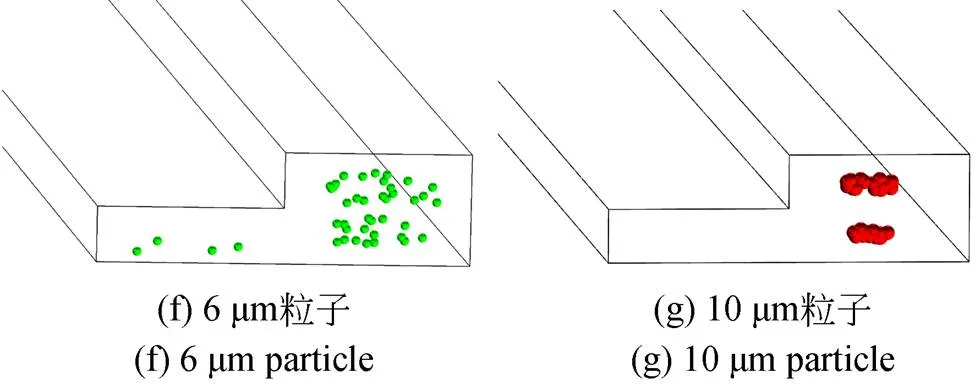
图2 微流道有限元仿真结果
2.4 芯片制作
微流控芯片采用市场上常见的薄膜材料制作而成。其中,盖板和底板材料选择PET薄膜(涂布硅胶),厚度为120 μm。流道层材料为有机硅胶膜,硅胶层厚度为75 μm。芯片制作工艺如图3所示。
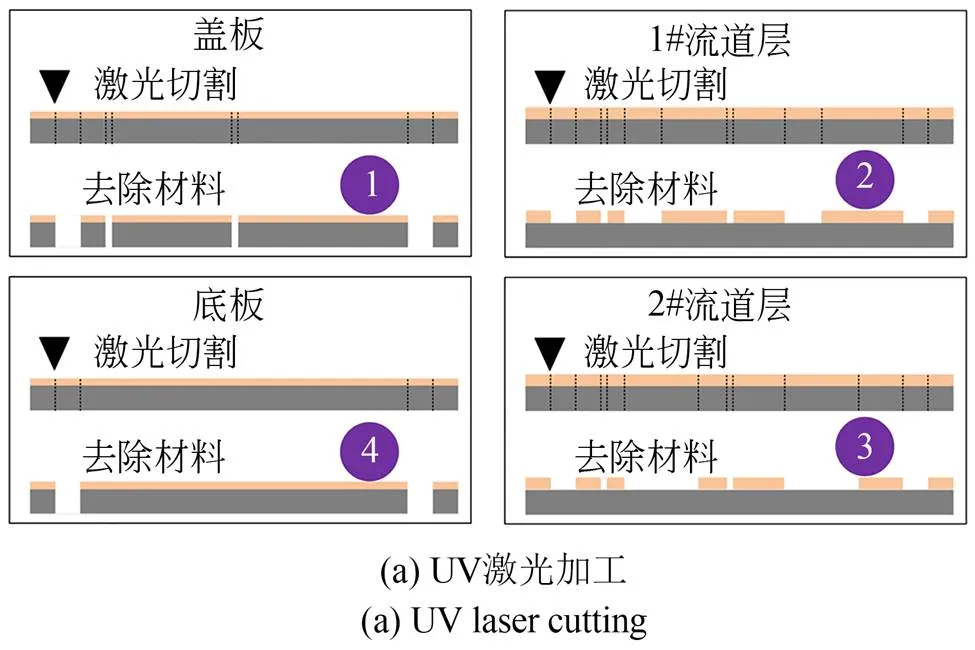
首先,采用UV激光在各层薄膜材料上加工芯片结构(图3(a)),具体步骤如下:
(1)在PET薄膜上用激光直接切透薄膜,加工出定位孔、流道入口和出口,去除掉落的材料,获得盖板和底板(图4(a));
(2)在有机硅胶膜上用激光先加工出定位孔(同第一步),再加工出微流道,为保障流道加工精度,需调节激光参数,使激光仅切透硅胶膜而不切透其下层保护膜,将切透的硅胶膜撕除,获得1#流道层和2#流道层的半成品(图4(a))。
然后,采用等离子清洗工艺对各层薄膜进行键合(图3(b)),具体步骤如下:
(1)将2#流道层半成品固定在定位夹具上,采用等离子清洗机处理1#和2#流道层半成品的上表面后,将两块薄膜利用定位夹具进行键合装配;
(2)撕掉流道层薄膜上的保护膜,在其表面键合并安装盖板;
(3)将半成品上下翻转固定在定位夹具上,撕掉另一侧流道层表面的保护膜,键合并安装底板,完成芯片样件的制作(图4(b))。制备的芯片样件在微流道宽度方向上的误差来源于激光加工和人工装配,误差为±30 μm;高度方向上的误差来源于薄膜厚度,误差为±6 μm。总体而言,芯片流道壁面的光滑性和平整性均较好(图4(c))。
最后,将芯片装入特制夹具中,利用亚克力板和不锈钢夹具夹紧(图3(c)与图4(d)),用于实验测试。对芯片的耐压性和密封性进行测试,发现芯片可以承受8 bar的压力而不泄漏,表明该芯片具有较高的耐压性和良好的密封性。

2.5 样品液配比
实验过程中采用了3种不同尺寸(6,10,15 μm)的聚苯乙烯荧光粒子(密度为1 065 kg/m3, BaseLine Chromtech),分别用于模拟血液中的红细胞(6~9.5 μm)、白细胞(10~12 μm)和癌细胞(如Hela肿瘤细胞:15 μm)。粒子悬浮液配制方法如下:取一只离心管,先加入30 mL去离子水,再加入质量浓度为0.5%的吐温20(Sigma-Aldrich),最后加入6 μm粒子(2.5%/,10 mL)0.3 mL,充分搅拌均匀后得到6 μm粒子悬浮液(约106个粒子/mL)。用同样方法制备10 μm粒子悬浮液(约105个粒子/mL)和15 μm粒子悬浮液(约105个粒子/mL)。
2.6 实验装置
如图5所示,实验装置主要包括计算机、精密注射泵(XFP01-BD,苏州讯飞科学仪器有限公司)、倒置荧光显微镜(XDS-3,上海光学仪器厂)和高速CCD(Stingray F-033B/C, Allied Vision Technologies)。拍摄粒子运动轨迹时,明场拍摄时粒子的运动过程存储为50帧图像,拍摄间隔设为31 μs;暗场拍摄时粒子的运动过程存储为100帧图像,拍摄间隔为10 000 μs。使用imageJ软件(Media Cybernetics, Inc)对明场和暗场拍摄的50帧和100帧图像分别进行堆叠处理。为便于分析粒子在流道中的聚焦位置,将明场和暗场图像中的流道壁用直线对齐标注(黄色实线代表内、外壁面,橙色虚线代表中间壁面),使用Analyze-Plot Profile功能绘制出聚焦粒子束在流道宽度方向上的荧光强度分布灰度值,将该值导入Excel进行归一化处理之后即可得出粒子的荧光强度分布。

图5 微粒聚焦效应实验装置
3 结果与讨论
惯性微流控作为被动式的粒子操控技术,利用特殊的流道结构和特定的流量可以实现粒子的精确操控。为研究“L”形截面螺旋流道中粒子的惯性聚焦效应及聚焦迁移机理,分析流量对粒子聚焦迁移的影响,本文对不同流量下(0.1~1.5 mL/min)3种尺寸粒子在微流道中的运动行为展开实验测试。为定义粒子的聚焦状态,将绝大多数粒子汇聚成较宽带状的现象定义为粗聚焦;粒子聚焦在一条中心线上下两侧的现象定义为良好聚焦;粒子几乎聚焦成单列的现象定义为强聚焦。
3.1 6 μm粒子的惯性聚焦效应
图6(a)显示了明场和暗场下6 μm粒子在微流道出口处的运动轨迹。当流道入口处粒子悬浮液流量低于0.2 mL/min时,内侧和外侧矩形流道中的粒子均处于离散状态。当流量高于0.3 mL/min时,外侧流道内的粒子从离散态逐渐趋于粗聚焦态,且随着流量的增大,粒子束的宽度先变窄后变宽。对聚焦粒子束的荧光强度进行测量,发现流量为0.8 mL/min时,粒子实现了最佳聚焦效果,绝大多数粒子聚焦在距外壁面300~450 μm内,最终出口处粒子束宽度约为150 μm(图6(b))。相应地,内侧流道中的粒子虽然在一定流量范围内(0.5~0.9 mL/min)也表现出粗聚焦行为,但最终随着流量的增大,再也无法维持稳定的聚焦。通过对比明场和暗场图片可以发现,内侧流道中的粒子数量随着流量的增大显著减少。当流量达到1.5 mL/min时,内侧流道的粒子数量与外侧流道相比可以忽略不计。
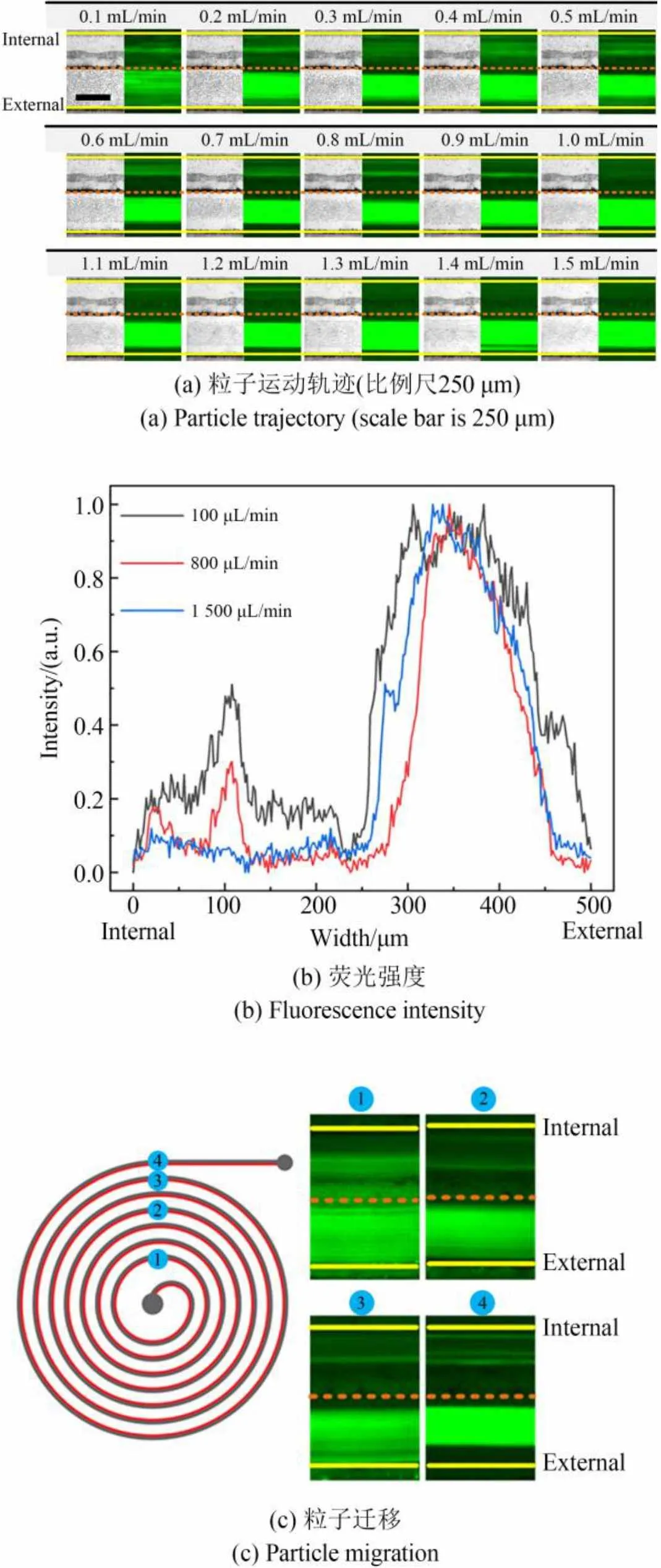
图6 6 μm粒子惯性聚焦
为进一步了解粒子实现最佳粗聚焦时在整个流道内的运动状况,分别对芯片上4个不同位置处的粒子运动轨迹进行观测(图6(c),流量为0.8 mL/min)。观测点①,由于该位置接近流道入口,因此粒子均匀地分散在流道中;观测点②,外侧流道内的粒子初步呈粗聚焦态势,而内侧流道中的粒子大致聚焦为两列;观测点③,外侧流道内的粒子聚焦带变窄并向外壁面迁移,内侧流道内的两列粒子向内壁面迁移;观测点④,外侧流道内的粒子实现了最佳粗聚焦效果,而内侧流道内的粒子从两列聚焦变为三列,且再次向外壁面靠拢。
上述实验结果表明,由于6 μm粒子尺寸较小且外侧流道存在强二次流漩涡,因此绝大多数粒子进入流道时受强二次流曳力影响被约束于外侧流道中,表现为明场图片中外侧流道中较大的粒子密度和暗场图片中较高的粒子荧光强度。当流量增大时,粒子受到逐渐增强的惯性升力和二次流曳力影响,表现出粗聚焦行为。然而随着流量的进一步增大,内侧流道中的粒子被显著增强的二次流曳力拖入外侧流道中,最终导致内侧流道中的粒子逐渐变少。
3.2 10 μm和15 μm粒子的惯性聚焦效应
图7(a)显示了10 μm粒子在微流道出口处的运动轨迹。对比明场和暗场下的粒子运动轨迹,发现从初始流量0.1 mL/min起,外侧矩形流道中的粒子已实现了粗聚焦。当流量高于0.8 mL/min时,外侧流道中的粒子能够良好聚焦,几乎所有粒子都聚焦在同一平衡位置处,最终出口处形成了一条宽约50 μm的荧光带(图7(b))。当流量增大至1.1 mL/min时,粒子聚焦在两列不同焦距上的平衡位置,呈两束荧光带分布。但随着流量的进一步增大,两束粒子带又会聚成一束,且粒子表现出更强的惯性聚焦行为。此外,随着流量的不断增加,粒子聚焦平衡位置也逐渐向外侧壁面缓慢迁移。最终当流量达到1.5 mL/min时,粒子荧光带宽度约为40 μm。相应地,内侧流道中的粒子由于数量极少,因此在低流量时(0.1~0.6 mL/min),始终无法实现稳定聚焦;而当流量高于0.7 mL/min时,内侧流道中的粒子基本都已消失。
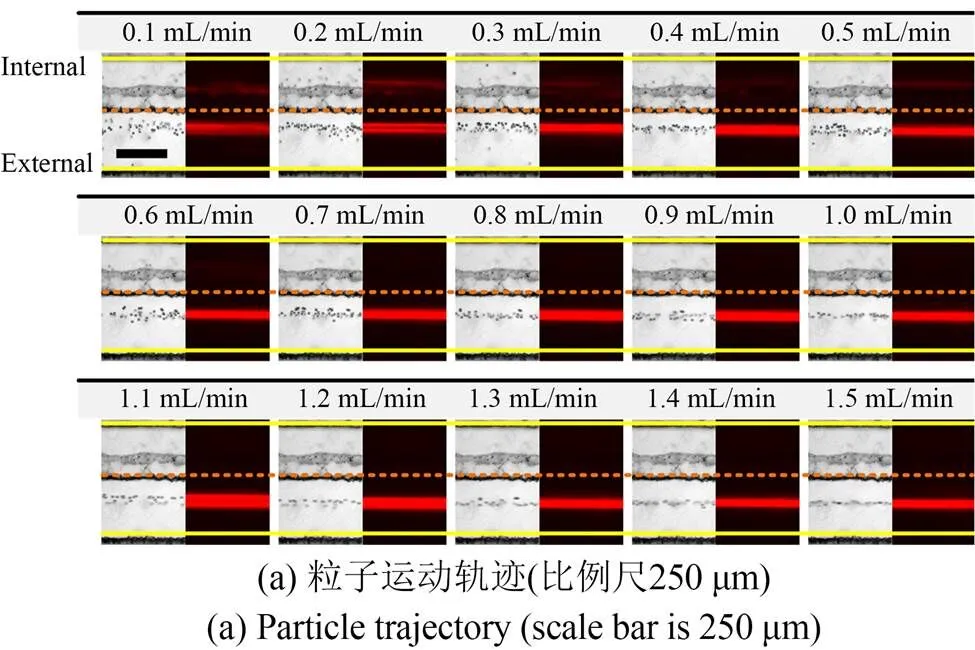
粒子在整个流道内的惯性聚焦迁移过程如图7(c)所示(流量为0.8 mL/min)。在观测点①(接近入口处),粒子呈离散态分布;在观测点②处,外侧流道中粒子实现了粗聚焦,而内侧流道中粒子数量明显减少;观测点③,外侧流道粒子实现了良好聚焦,聚焦带逐步变窄,内侧流道中粒子进一步减少;最后在观测点④,外侧流道中的粒子实现了强聚焦且往流道中心迁移,内侧流道中的粒子基本消失。
15 μm粒子在微流道出口处的运动轨迹如图8(a)所示。与6 μm和10 μm粒子相比,由于15 μm粒子尺寸较大,其惯性升力显著增强,因此外侧矩形流道中的粒子在最低流量时(0.1 mL/min)实现了良好聚焦。随着流量的增大,粒子的聚焦效果进一步增强,粒子在流道中基本呈单列排布,表现出强聚焦态势,且平衡位置也逐渐向流道外壁面缓慢迁移。当流量为1.5 mL/min时,出口处粒子聚焦荧光带的宽度仅为25 μm(图8(b))。由于内侧流道中的粒子数量极少(粒子已无法产生肉眼可见荧光),因此随着流量的增大,内侧流道中的粒子迅速消失殆尽。
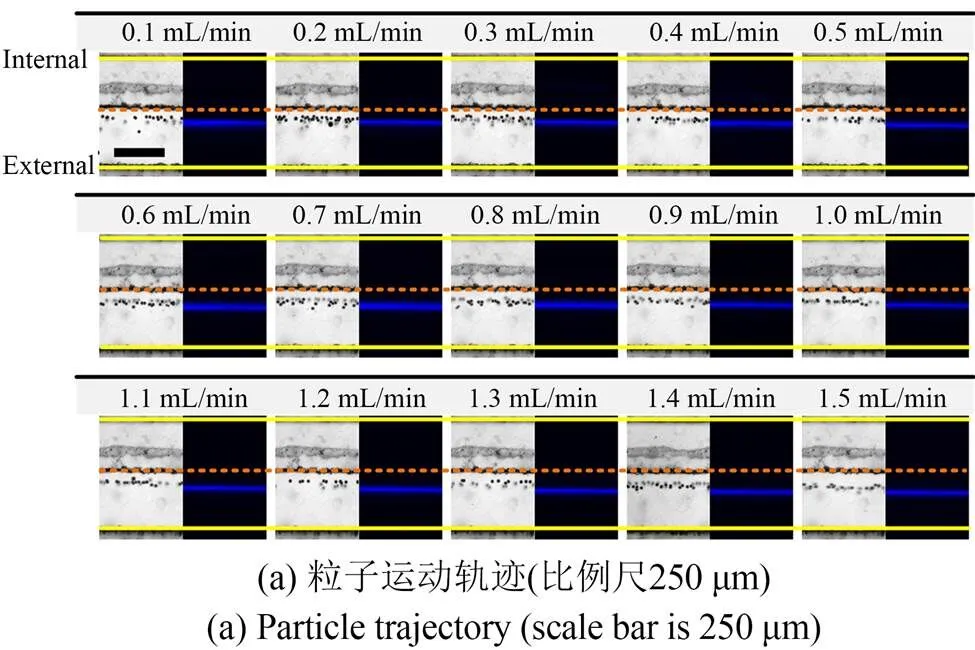
对粒子在整个流道内的惯性聚焦迁移行为进行研究(图8(c),流量为0.8 mL/min),发现在观测点①(接近入口处),粒子呈离散态分布,但外侧流道中已有部分粒子向流道中心聚集;从观测点②起,发现外侧流道中的粒子已呈现出强聚焦行为,且粒子聚焦带紧靠流道中心。随后粒子在流道中一直保持强聚焦状态,直至经过观测点④从流道出口流出。
综合分析10 μm和15 μm粒子的惯性聚焦效应,可以推断当粒子尺寸较大时,粒子受显著增强的惯性升力及外侧流道中的强二次流影响,几乎所有的粒子均被约束于外侧流道中,且粒子聚焦于单一平衡位置上,呈现强惯性聚焦行为。
综合分析3种不同尺寸的粒子在“L”形截面螺旋流道中的惯性聚焦现象,并对比已报道的矩形截面螺旋流道粒子惯性聚焦现象,可以发现粒子在“L”形截面高侧流道中更容易实现惯性聚焦。其原因在于矩形截面流道中只存在一对二次流漩涡,粒子受二次流曳力作用在整个截面流道内旋转回流,粒子运动范围较大;而“L”形截面流道具有两对非对称二次流漩涡,高侧流道的二次流强度显著高于低侧流道,导致整个流道中的粒子几乎都被禁锢于高侧流道中,难以从强二次流旋涡中脱离出来,显著缩小了粒子的运动范围。最终,当粒子同时受到较强的惯性升力影响时,更容易实现聚焦平衡。由此可见,采用非对称二次流可以进一步调控粒子的聚焦行为,有助于实现生物粒子和细胞的精准操控。
4 结 论
本文提出了一种“L”形截面螺旋流道结构的惯性微流控芯片,分别通过软件仿真和实验测试的方法研究了粒子在微流道中的惯性聚焦效应,旨在研究“L”形截面流道中粒子的惯性聚焦机理。仿真结果发现,“L”形截面流道中心两侧形成了内弱(低侧流道)、外强(高侧流道)的两对非对称二次流漩涡,且低侧流道有部分流体汇入高侧流道的二次流漩涡中。为深入研究该流道中粒子的惯性聚焦机理,采用UV激光切割与等离子清洗键合工艺制作了微流控芯片样件,并对不同流量(0.1~1.5 mL/min)下6,10和15 μm粒子在微流道中的运动轨迹展开实验研究。实验发现,6 μm粒子在外侧流道中实现了粗聚焦,而10 μm和15 μm粒子实现了强聚焦。仿真与实验结果表明,“L”形截面螺旋流道可以利用非对称二次流改变粒子的聚焦平衡位置,增加粒子操控的多样性,为实现粒子和细胞的精准操控提供新的思路。
[1] 陈立国,王兆龙,卞雄恒. 扇形电极微液滴分离的数字微流控芯片[J]. 光学精密工程, 2019, 27(9): 1919-1925.
CHEN L G, WANG ZH L, BIAN X H. Micro-droplet split digital microfluidic device with fan-shaped electrode[J]., 2019, 27(9): 1919-1925. (in Chinese)
[2] RAOUFI M A, MASHHADIAN A, NIAZMAND H,. Experimental and numerical study of elasto-inertial focusing in straight channels[J]., 2019, 13(3): 034103.
[3] ZHANG X J, ZHU Z X, XIANG N,. Automated microfluidic instrument for label-free and high-throughput cell separation[J]., 2018, 90(6): 4212-4220.
[4] 江洋,刘冲,魏娟,等. 微流控芯片细胞动态培养装置的设计与制作[J]. 光学精密工程, 2019, 27(9): 2020-2027.
JIANG Y, LIU CH, WEI J,. Design and fabrication of device for cell dynamic culture in microfluidic chip[J]., 2019, 27(9): 2020-2027. (in Chinese)
[5] CHOI K, RYU H, SIDDLE K J,. Negative selection by spiral inertial microfluidics improves viral recovery and sequencing from blood[J]., 2018, 90(7): 4657-4662.
[6] SEGRE G, SILBERBERG A. Behavior of macroscopic rigid spheres in Poiseuille flow[J]., 1961, 14: 115-135.
[7] DI CARLO D, IRIMIA D, TOMPKINS R G,. Continuous inertial focusing, ordering, and separation of particles in microchannels[J]., 2007, 104(48): 18892-18897.
[8] AMINI H, LEE W, DI CARLO D. Inertial microfluidic physics[J]., 2014, 14(15): 2739-2761.
[9] AHMADI V E, BUTUN I, ALTAY R,. The effects of baffle configuration and number on inertial mixing in a curved serpentine micromixer: experimental and numerical study[J]., 2021, 168: 490-498.
[10] RZHEVSKIY A S, RAZAVI BAZAZ S, DING L,. Rapid and label-free isolation of tumour cells from the urine of patients with localised prostate cancer using inertial microfluidics[J]., 2019, 12(1): 81.
[11] 谢晋,郭奥钿,卢阔,等. 微流道精密磨削技术及自驱动检测芯片实验研究[J]. 光学精密工程, 2020, 28(8): 1743-1750.
XIE J, GUO A D, LU K,. Experimental study on grinding technology of microchannel for self-driven detection chip[J]., 2020, 28(8): 1743-1750. (in Chinese)
[12] RAZAVI BAZAZ S, ROUHI O, RAOUFI M A,. 3D printing of inertial microfluidic devices[J]., 2020, 10(1): 5929.
[13] RAFEIE M, HOSSEINZADEH S, TAYLOR R A,. New insights into the physics of inertial microfluidics in curved microchannels. I. Relaxing the fixed inflection point assumption[J]., 2019, 13(3): 034117.
[14] KWON J Y, KIM T, KIM J,. Particle focusing under Newtonian and viscoelastic flow in a straight rhombic microchannel[J]., 2020, 11(11): 998.
[15] MASHHADIAN A, SHAMLOO A. Inertial microfluidics: a method for fast prediction of focusing pattern of particles in the cross section of the channel[J]., 2019, 1083: 137-149.
[16] RAFEIE M, HOSSEINZADEH S, TAYLOR R A,. New insights into the physics of inertial microfluidics in curved microchannels. I. Relaxing the fixed inflection point assumption[J]., 2019, 13(3): 034117.
[17] ASMOLOV E S. The inertial lift on a spherical particle in a plane Poiseuille flow at large channel Reynolds number[J]., 1999, 381: 63-87.
[18] MARTEL J M, TONER M. Inertial focusing in microfluidics[J]., 2014, 16: 371-396.
Inertial focusing effect of particles in spiral microchannel with asymmetric cross-section
HAN Shuai1,ZHANG Xinjie1*,GU Qiao2,LIU Yao1,WANG Xinyi1
(1,,213022,;2,,213000,),:
An inertial microfluidic chip with a spiral microchannel of asymmetric cross-section was proposed to achieve a precise control of biological microparticles/cells. The inertial focusing behavior of particles of different sizes in the microchannel was studied through simulation and experiment. A spiral channel with L shaped cross-section was designed, and the secondary flow field distribution and particle trajectory in the channel were analyzed using COMSOL simulation software. The prototype chip was fabricated by UV laser cutting and plasma cleaning bonding. The trajectories of particles of sizes 6, 10, and 15 μm at different flow rates in the channel were captured by a high speed camera and fluorescent microscope. Finally, the images of particle trajectories were stacked and analyzed and the inertial focusing and migration mechanism of the particles were investigated. The results show that two asymmetric secondary flow vortexes of different strengths are produced in the L shaped cross-section. Furthermore, the particles of 10 and 15 μm sizes focus tightly in the outer ring of the microchannel, whereas those of 6 μm size focus in it roughly. The particle focusing position can be adjusted using asymmetric secondary flow, thus providing new insights into precise particle and cell manipulation.
microfluidics; asymmetric flow; inertial focusing; particle manipulation; UV laser cutting
O352
A
10.37188/OPE.20223003.0310
1004-924X(2022)03-0310-10
2021-09-02;
2021-09-28.
国家自然科学基金资助项目(No.51905150);江苏省自然科学基金资助项目(BK20190167);中央高校基本科研业务费资助项目(No. B200202230);江苏省博士后科研资助计划项目(No.2019K033)
韩帅(1997),男,山东枣庄人,硕士研究生,2019年于河海大学获得学士学位,主要从事惯性微流控方面的研究。E-mail:178092684@qq.com

张鑫杰(1984),男,江苏常州人,副教授,硕士生导师,2006年于合肥工业大学获得学士学位,2009年、2017年于东南大学分别获得硕士和博士学位,现为河海大学机电工程学院智能制造研究所副所长,主要从事微纳制造、软体机器等方面的研究。E-mail:xj.zhang@hhu.edu.cn
