氨基酸对丙酮醛和甲醛的消除效果及其机理分析
2022-03-05胡嘉漫黄才欢欧仕益李瑞阳欧隽滢
胡嘉漫,黄才欢,2,郑 洁,2,欧仕益,2,李瑞阳,欧隽滢
(1.暨南大学理工学院,广东 广州 510632;2.焙烤食品安全粤港联合创新平台,广东 广州 510632;3.暨南大学食品安全与营养研究院,广东 广州 510632)
丙酮醛(methylglyoxal,MGO)又名甲基乙二醛,是具有高反应活性的α-二羰基化合物[1]。在食品加工过程中,MGO主要源于美拉德反应中的Schiff碱和Amadori化合物[2]。MGO广泛存在于面包、饼干、咖啡、奶酪、蜂蜜[3-4]和饮料(碳酸软饮料)[5]以及香烟烟雾[6]中,食品在热加工过程(油炸、焙烤)[7-9]甚至贮藏过程中[10]均会产生MGO。在生物体内(包括人体中),MGO主要由糖酵解途径产生,可通过3-磷酸甘油醛和磷酸二羟丙酮自发形成,在白醋、酒等发酵食品中也含有MGO[2,11]。MGO的口服半致死剂量为1 165 mg/kg,具有细胞毒性[12]。 其化学性质非常活泼,可与食品组分形成有害衍生物,包括晚期糖基化终末产物(advanced glycation end products,AGEs)、丙烯酰胺和4(5)-甲基咪唑[13]。MGO被人体摄入后,不仅会诱发体内活性氧产生,而且容易通过血液循环运输到全身组织,损伤生物大分子,如蛋白质、DNA、RNA、膜脂(含氨基的磷脂)等[14]。研究表明,MGO是高血糖和糖尿病并发症的主要致病因素之一[15],而且MGO、AGEs的形成和积累与衰老相关疾病密切相关,包括癌症、神经退行性疾病、糖尿病和动脉粥样硬化[16]。由此可见,降低MGO水平可能是抑制AGEs形成、预防和治疗相关疾病的有效方法。
甲醛是最活泼的脂肪醛[17],它既可以由食品内源性产生,也可通过外源添加或环境污染存在于食品中[18]。甲醛是细胞的代谢产物,广泛存在于人体内和各种动植物组织中。食品在加工或贮存过程中会通过美拉德反应和热降解反应生成甲醛,尤其是酒、面包等发酵性食品[19]。 甲醛已被国际癌症研究机构列为第一类致癌物,是影响人类健康最危险的化学物质之一[20]。甲醛不仅可与视紫红质蛋白质中赖氨酸的胺官能团发生反应,而且还会与其他蛋白质(包括许多酶)中的氨基发生反应,这些生物催化剂功能的丧失会导致死亡[18]。
科学家们一直致力于研究降低或清除食品中MGO的方法。目前研究最多的MGO清除剂主要为多酚,包括茶多酚、槲皮素、白藜芦醇和姜黄素等[21]。槲皮素可以在生理条件下[22]和小鼠体内[23]通过捕获MGO形成单或双MGO-槲皮素加合物而清除MGO。卢永翎等[24]证明,槲皮素和MGO形成单和双MGO-槲皮素加合物后仍对MGO具有清除作用。当槲皮素的A环位置被MGO占据时,槲皮素的B环可再捕获1个MGO形成三MGO-槲皮素加合物。但在有些模拟体系中,多酚会促进其他有害物质,如1-/3-脱氧奥苏糖、HMF的形成,从而产生二次毒害[25-26]。 Jiang Kaiyu等[27]通过模拟唾液、胃液和肠液等消化体系,对猪肉、鸡肉、奶粉和大豆分离蛋白进行体外模拟胃肠消化实验,发现蛋白质水解产物对MGO具有清除作用,从而减轻了MGO对结肠癌Caco-2细胞的毒性。并在后续实验中构建了模拟生理反应体系[27]以及热加工模拟体系[28],两种体系中MGO和氨基酸的浓度比为1∶10,模拟生理反应体系的pH值为2.0或7.0、反应温度为37 ℃,模拟热加工反应体系的pH值为7.0、反应温度为160 ℃,实验结果证明对MGO具有消除作用的成分是蛋白质的水解产物氨基酸,但氨基酸对MGO的清除机理尚待研究。
γ-氨基丁酸(γ-aminobutyric acid,GABA)是一种非蛋白质氨基酸,属于新资源食品。它广泛存在于哺乳动物、植物和微生物中,尤其在谷物、茶叶、蔬菜等食品中含量较高。例如,在马铃薯中含量高达660 mg/kg[29],仅次于天冬酰胺;在糙米中含量为236.6 mg/kg[30]。GABA参与多种代谢活动,具有很高的生理活性。在神经系统调节方面也具有重要作用,如可以促进神经元生长,以及预防失眠、焦虑和抑郁等[31]。另外,GABA对高胰岛素血症还可能具有缓解作用[32]。
本实验采用模拟体系,研究14种氨基酸对MGO的消除效果,以对MGO消除效果好、食品中含量较高的GABA为对象研究其消除机理,并在此基础上,表征产物结构,研究可能的反应机理。
1 材料与方法
1.1 材料与试剂
MGO(质量分数40%) 上海麦克林生化科技有限公司;甲醛(质量分数40%)、氢氧化钠、盐酸 天津大茂化学试剂厂;L-甘氨酸(Gly,99%)、GABA(99%)、L-丝氨酸(Ser,99%)、L-脯氨酸(Pro,99%)、L-丙氨酸(Ala,99%)、L-组氨酸(His,99%)、L-赖氨酸(Lys,98%)、L-甲硫氨酸(Met,99%)、L-缬氨酸(Val,99%)、L-异亮氨酸(Ile,99%)、L-精氨酸(Arg,99%)、L-天冬酰胺(Asn,99%)、L-半胱氨酸(Cys,99%)、L-色氨酸(Trp,99%)、2,4-二硝基苯肼(2,4-dinitrophenylhydrazine,DNPH) 北京百灵威科技有限公司;甲醇、乙腈(色谱纯)、邻苯二胺 德国默克试剂有限公司;氘代甲醇 美国Cambridge Isotope Laboratories公司;A-HG型十八烷基硅烷(octadecylsilane,ODS)键合相吸附剂 日本东京YMC公司;分离用有机溶剂均为国产分析纯。
1.2 仪器与设备
LC-20AT高效液相色谱(high performance liquid chromatography,HPLC)仪、8045三重四极杆液相色谱-串联质谱(high performance liquid chromatographytandem mass spectrometry,HPLC-MS/MS)仪(配有电喷雾离子源) 日本岛津仪器公司;N-1300型旋转蒸发仪 东京理化器械株式会社;SHA-BA恒温振荡器 江苏金坛医疗仪器厂;X500R QTOF型高分辨质谱仪 美国SCIEX公司;HR-200分析天平 日本A&D公司; 600 MHz Avance III型核磁共振(nuclear magnetic resonance,NMR)仪 瑞士布鲁克公司;Scientz-10N型真空冷冻干燥机 宁波新芝生物科技有限公司。
1.3 方法
1.3.1 氨基酸对MGO的清除作用
用蒸馏水配制氨基酸(Pro、Ala、His、Lys、Met、Val、Ile、Ser、Arg、Gly、GABA、Asn、Cys、Trp)和MGO溶液,浓度均为50 mmol/L,将每种氨基酸溶液分别与MGO溶液按体积比1∶1混合,取4 mL混合溶液置于10 mL具塞比色皿中,于80 ℃水浴反应4 h后,冷却。参考吴泰钢等[33]报道的检测方法,利用邻苯二胺对MGO进行衍生反应后,过0.22 μm有机微孔滤膜,采用HPLC仪检测未被消除的MGO。检测条件:ZORBAX SB-Aq色谱柱(4.6 mm×250 mm,5 μm);流动相为体积分数0.1%乙酸溶液和甲醇(30∶70,V/V),进样体积10 μL,流速1 mL/min,柱温40 ℃;检测波长314 nm。
1.3.2 GABA对MGO和甲醛的同时消除作用
向10 mL钢管中分别加入一定体积的GABA、MGO溶液和甲醛,使其终浓度分别为40、4 mmol/L和4 mmol/L, 用0.1 mol/L的NaOH溶液或盐酸将体系pH值调为7.0,反应液(总体积6 mL)充分混匀后于160 ℃下分别反应5、15、30、45、60 min。采用同样的反应体系,于10 mL具塞比色管中加入GABA、MGO溶液和甲醛各2 mL,其终浓度分别为40、4 mmol/L和4 mmol/L,用0.1 mol/L的NaOH溶液或盐酸调节体系pH值为2.0或7.0,溶液混匀后在37 ℃下水浴反应2 h。
反应结束后,参考Jiang Kaiyu等[27]的检测方法,以DNPH衍生法测定体系中MGO和甲醛的剩余量。具体方法如下:蒸馏水调节至相应pH值,用其将待测溶液稀释10 倍后取200 μL于5 mL试管中,再加入1.8 mL乙腈和1 mL 12.5 mmol/L DNPH溶液(以体积比9∶1的乙腈-浓盐酸为溶剂配制),混匀后于60 ℃水浴衍生2 h。衍生反应后样品过0.22 μm有机微孔滤膜待HPLC仪(配有SPD-M20A光电二极管阵列检测器)检测。检测条件:ZORBAX SB-Aq色谱柱(4.6 mm×250 mm,5 μm);流动相为超纯水-乙腈(30∶70,V/V),进样体积10 μL,流速1.2 mL/min,柱温40 ℃;检测波长352 nm(甲醛衍生物)和425 nm(MGO衍生物)。甲醛和MGO均以标准物质衍生后进样,每个标准样品进行3 次平行实验后,绘制标准曲线,以标准曲线计算得出样品中甲醛和MGO的剩余量。
1.3.3 反应产物的初步鉴定
利用HPLC仪以及HPLC-MS/MS仪对反应产物进行检测。选择ZORBAX SB-Aq色谱柱(4.6 mm×250 mm,5 μm)。HPLC分析程序设置如下:流动相为体积分数0.1%乙酸溶液和甲醇(95∶5,V/V),进样体积1 μL,流速0.6 mL/min,柱温40 ℃,检测波长220 nm。HPLC-MS/MS 分析程序设置如下:流动相为体积分数0.1%乙酸溶液和甲醇(95∶5,V/V),进样体积0.1 μL,流速 0.4 mL/min,柱温40 ℃;离子源为电喷雾离子源,扫描范围m/z50~800,离子源温度300 ℃,去溶剂化温度250 ℃,毛细管电压4 000 V,扫描速率1 000 Da/s,碰撞能量30 eV。
1.3.4 加合物的制备及分离纯化
分别取GABA、MGO溶液和甲醛于装有30 mL去离子水的100 mL三角瓶中,终浓度分别为0.2、0.1 mol/L和0.1 mol/L,于37 ℃水浴反应12 h。反应后通过旋转蒸发仪将反应液浓缩得到1 mL样品,样品经0.22 μm有机微孔滤膜过滤后用胶头滴管滴加到反相硅胶层析柱(ODS填料)上端,通过柱层析法分离纯化反应产物。参照邹照佳等[34]的方法装柱和平衡层析柱。玻璃层析柱规格为30 mm×600 mm,反相硅胶填料体积350 mL,体积分数5%甲醇溶液作为洗脱液,等度洗脱,流速3 s/滴,各馏分体积为5 mL。采用碘熏法监测馏分的成分,具体操作如下:利用毛细管吸取少量馏分点于定性滤纸上,将定性滤纸置于装有硅胶和少量单质碘的磨口广口瓶中进行显色反应。取显深棕色的馏分过0.45 μm微孔滤膜后于HPLC和HPLC-MS/MS测定加合物的纯度,最后合并高纯度的馏分,通过旋转蒸发去除溶剂,用去离子水复溶后进行冷冻干燥收集固体样品。
1.3.5 加合物的结构鉴定
将纯度大于95%的馏分,采用HPLC-MS/MS对加合物进行初步鉴定,获得一级、二级质谱,分析条件同1.3.3节。另外,采用高分辨质谱仪(离子源为电喷雾离子源,扫描范围m/z50~1 500)分析目标加合物样品,获得精确相对分子质量。取25 mg固体样品溶于600 μL氘代甲醇中,采用NMR仪(600 MHz)获得目标加合物的1H NMR、13C NMR和Dept-135谱图。
1.4 数据处理与分析
实验数据采用Microsoft Excel软件处理,以±s表示。应用SPSS 25.0软件对实验数据进行差异显著性分析(P<0.05,差异显著)。
2 结果与分析
2.1 氨基酸对MGO的清除作用
如图1所示,所有氨基酸对MGO均具有一定消除能力,半胱氨酸对MGO的消除率最高(90%);其次为赖氨酸、GABA和甘氨酸,消除率分别为78%、77%和70%。消除率超过50%的氨基酸还有丝氨酸(59%)、丙氨酸(51%)、甲硫氨酸(54%)、色氨酸(63%)、精氨酸(61%)和组氨酸(62%)。半胱氨酸消除效果最好的可能原因是其不仅含有氨基,可以与MGO的醛基反应形成Schiff碱,而且还含有更加活泼的巯基,能与MGO反应生成半缩硫醛或缩硫醛。
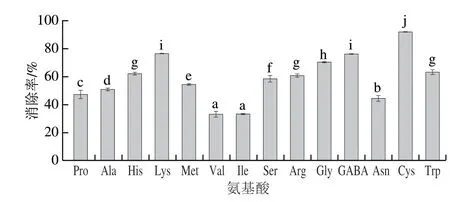
图1 氨基酸对MGO的清除作用Fig. 1 Elimination capacity of methylglyoxal by amino acids
2.2 GABA同时消除MGO和甲醛的能力
利用邻苯二胺作为衍生剂检测MGO的剩余量,评价在甲醛存在下GABA对MGO的消除作用。在37 ℃、pH 2.0或7.0条件下,GABA对MGO的消除能力如表1所示。结果表明,GABA在pH 7.0的中性反应体系中对MGO的清除能力比在pH 2.0的酸性体系中强;在含甲醛的反应体系中,GABA对MGO的清除效果较不含甲醛的反应体系更好。在pH 7.0、不加甲醛时,GABA对MGO的消除率只有59.6%,加入甲醛后,GABA对MGO的消除率增至81.2%。这说明甲醛的存在可以促进GABA对MGO的消减。

表1 37 ℃下GABA对MGO的消除率Table 1 Elimination rate of methylglyoxal by GABA at 37 ℃
利用DNPH同时对甲醛和MGO进行衍生,测定160 ℃反应体系中甲醛和MGO的剩余量,以此评价热加工模拟体系中GABA对甲醛和MGO的同时消除效果。如表2所示,随着加热时间的延长,甲醛和MGO持续减少,直到30 min后,两种羰基化合物剩余量基本稳定。模拟体系加热5~15 min,GABA对甲醛的消除率不到40%,对MGO的消除率只有45%左右,而加热30 min,GABA对甲醛和MGO的消除率分别达到了91.3%和78.8%。在高温加热模拟体系中,GABA对MGO和甲醛均具有良好的消减效果。这一发现说明,当食品体系中MGO和甲醛同时存在时,GABA不仅可以更好地消除MGO,而且还可能显著降低甲醛含量。
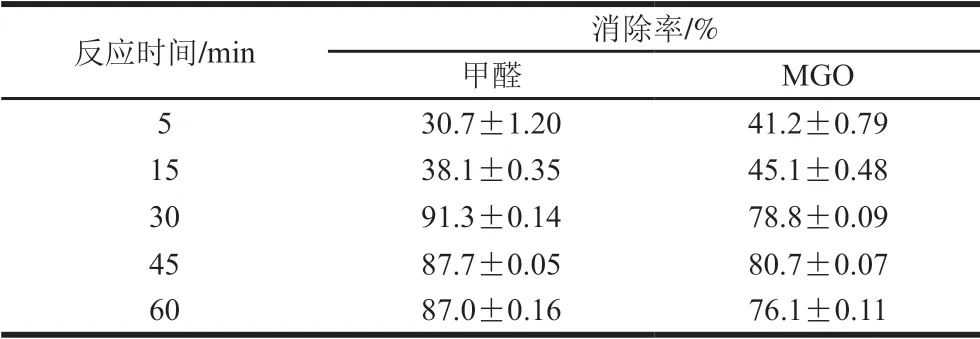
表2 160 ℃下GABA对MGO和甲醛的消除率Table 2 Elimination rates of methylglyoxal and formaldehyde by GABA at 160 ℃
2.3 反应产物的分离纯化
37 ℃水浴2 h,GABA-甲醛-MGO反应产物的HPLC图如图2A所示。除GABA(4.020 min)外,产物中还有一个较高的峰(10.157 min,目标产物),经紫外全波长扫描,得知产物的最大吸收波长为220 nm(图2B)。
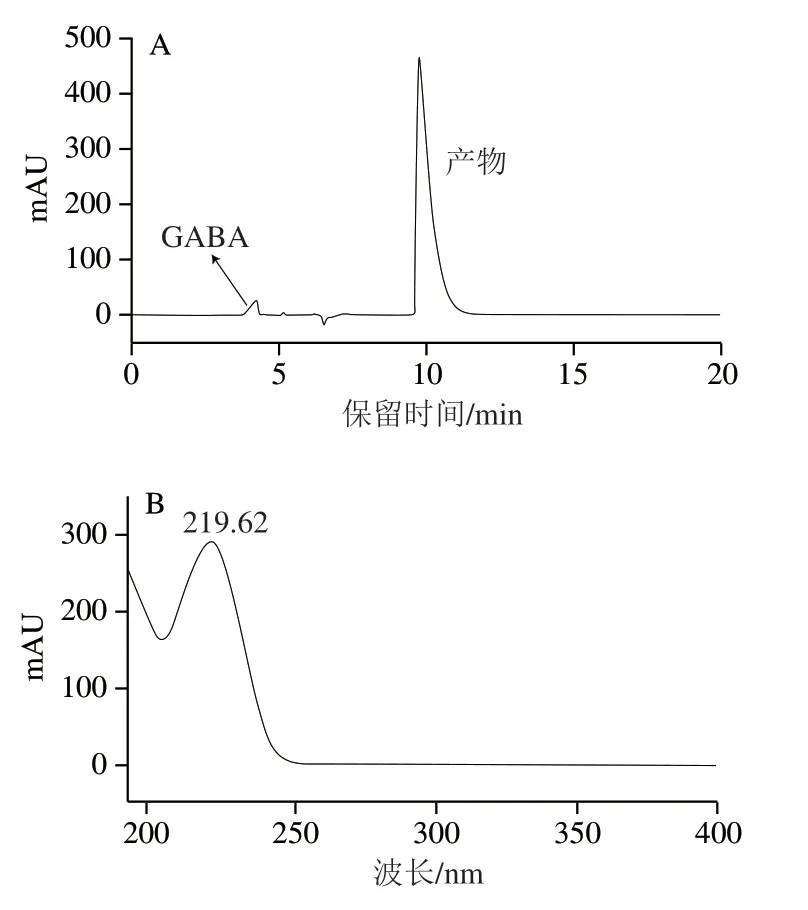
图2 GABA与甲醛和MGO共同反应后产物的HPLC图谱(A)及 目标产物的紫外全波长扫描图(B)Fig. 2 HPLC chromatogram (A) and ultraviolet spectrum (B) of the reaction products of GABA, formaldehyde and methylglyoxal
GABA和产物的保留时间明显不同,说明两者的极性相差较大,因此,本研究采用反相硅胶层析柱(ODS填料)分离纯化目标产物。如图3所示,采用反相硅胶纯化后,只有一个单一峰,说明纯化效果良好。DNPH被用作醛类和酮类的显色剂,而纯化后的目标产物不能使DNPH显色,说明产物中没有醛基或酮基。碘熏法是一种利用有机物遇碘蒸气能显黄色或黄棕色的显色方法。利用碘熏法监测馏分,馏分中含有纯化产物时,碘蒸气吸附于产物上而显棕色。含有氮原子和不饱和键,尤其是含有环内双键的化合物会使碘显色更明显。可以看出,滤纸上的产物为深棕色,说明目标产物保留了GABA的氮原子,且可能含有碳碳双键或环。

图3 纯化后目标产物的HPLC图以及碘熏法显色情况Fig. 3 HPLC chromatogram of purified product and color development using iodine fuming
2.4 加合物的结构鉴定
纯化产物的HPLC-MS/MS一级、二级质谱和高分辨质谱图分别如图4A~C所示。一级质谱图中的2个峰分别为[M+H]+m/z255和[M+Na]+m/z277,可以确定目标产物的相对分子质量为254。由高分辨质谱仪分析得到加合物的准确相对分子质量为254.133 9,分子式为C12H18N2O4。不饱和度(缺氢指数)常用来衡量有机化合物的不饱和程度,泛指结构中不饱和键(如双键)和环数的总和[35]。高分辨质谱结果显示,该产物的不饱和度为5,推测其可能结合了两分子GABA,除了2个羧基以外,还有可能是MGO和甲醛的醛基分别和两分子GABA的氨基形成两分子Schiff碱(含有2个双键),此外,还有可能含有一个不饱和度为1的环状化合物。由二级质谱图可知,目标产物脱去2个羧基和1个亚甲基得到m/z151的碎片峰,再分别脱去2个亚甲基和3个亚甲基得到m/z123和m/z109的碎片峰,综上所述,可以由目标产物得到的最小碎片峰以及醛基和氨基的反应机理推断,可能形成了1个咪唑环。
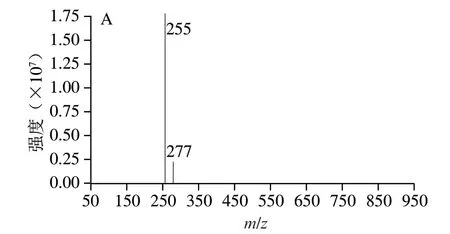

图4 纯化产物的MS1(A)、MS2(B)和高分辨质谱图(C)Fig. 4 MS1 (A), MS2 (B) and high resolution mass spectrum (C) of the purified product
经纯化后的目标产物的13C、1H NMR谱和Dept-135谱图如图5所示。由Dept-135谱图可知目标加合物含有6个亚甲基,与加合物结合的两分子GABA上的亚甲基数目对应。13C NMR谱中共包含12个碳信号,其归属如下:δ176.51(—COOH)、31.64(—CH2COOH)、25.27(—CH2CH2COOH)、46.16(—CH2CH2CH2COOH)、176.44(—COO-)、31.71(—CH2COO-)、25.74(—CH2CH2COO-)、48.81(—CH2CH2CH2COO-)、135.56(环内—NCH=N+)、119.38(环内—NCH=C)、131.86(环内—CH=C—N+)、7.59(—CH3)。由1H NMR谱可知加合物包含9种氢类型,分别为:δ2.36(—CH3,3H)、2.29(—CH2COOH,2H)、2.11 (—CH2CH2COOH,2H)、4.19(—CH2CH2CH2COOH,2H)、2.34(—CH2COO-,2H)、2.13 (—CH2CH2COO-,2H)、4.20(—CH2CH2CH2COO-,2H)、7.38(环内—NCH=C,1H)、8.92(环内 —NCH=N+,1H)、3.31(CH3OD)、4.89(D2O)。氢谱中化学位移为δ7.38和δ8.92的两组峰分别与咪唑环上的两种氢原子对应。NMR结果表明该化合物为3-(3-羧丙基)-1-(3-羧丙基)-4-甲基-1H-咪唑。

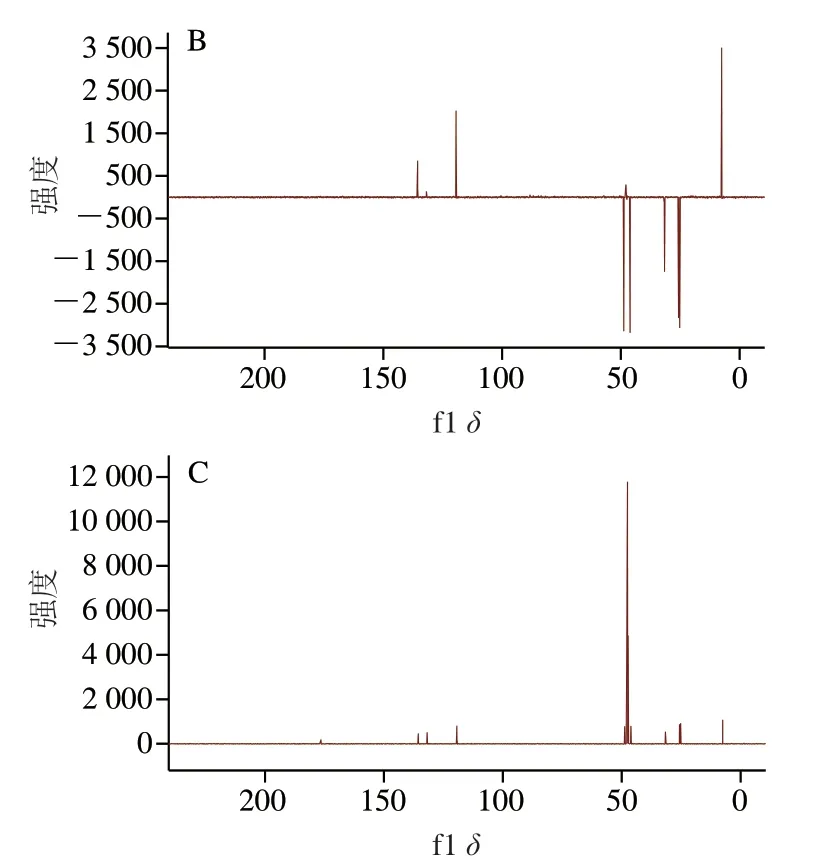
图5 目标加合物的1H NMR谱(A)、Dept-135谱(B)、13C NMR谱(C)Fig. 5 1H NMR spectrum (A), Dept-135 spectrum (B) and 13C NMR spectrum (C) of the adduct
结合HPLC-MS/MS的图谱数据,碎片离子m/z169表示[—CH2CH2COO-]和[—CH]的损失,而m/z109是带有1个甲基的咪唑环。因此,推测其反应机理为:两分子GABA捕获一分子MGO和一分子甲醛,GABA的氨基与甲醛反应生成中间产物Mannich碱,该反应在常温下就可发生。由于N原子的吸电子效应,导致α-C上正电荷堆积,另一分子GABA与之发生亲核加成反应形成另一个含2个亚氨基的中间产物;2个亚氨基同时进攻MGO的2个羰基碳,形成一个五元环化合物,然后分子内脱去两分子H2O,形成咪唑盐(图6)。由于活泼中间产物Mannich碱的形成、以及加成和脱水反应都在分子内发生,使得反应非常容易进行,因此,MGO的消除效率大大提高。GABA在马铃薯中的含量很高,仅次于天冬酰胺,在喷雾干燥的马铃薯片中含量为660 mg/kg[29]。因此,GABA可能与油炸或烘焙等热加工过程中产生的MGO和甲醛形成该产物。
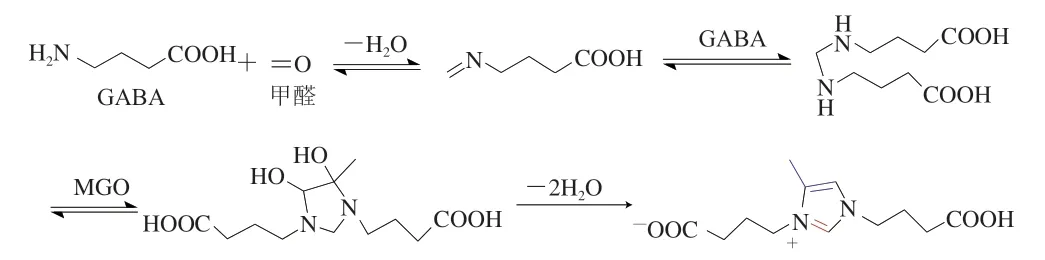
图6 GABA与MGO和甲醛同时反应的可能机制Fig. 6 Possible mechanism for the simultaneous reaction of GABA with methylglyoxal and formaldehyde
3 结 论
在37(生理条件)、80 ℃和160 ℃下,GABA均能有效消减MGO(消除率在77%以上),甲醛的加入促进了 GABA对MGO的消减。经产物分离纯化和结构表征,GABA同时与MGO和甲醛反应,产生一个相对分子质量为254(最大吸收波长220 nm)的含氮五元环化合物,其形成机理是:2 分子GABA与1 分子甲醛和1 分子MGO通过亲核加成反应脱去3 分子水后形成咪唑盐。本研究结果表明,在消化和热加工过程中,补充GABA能有效清除MGO和甲醛,避免其危害人体健康;但产物(咪唑盐)的安全性还有待进一步研究。
