氟苯尼考纳米晶在鸡体内的药动学
2022-03-04陈胡羚辛怡霖侯佳琪王虹雅李青云李引乾西北农林科技大学动物医学院陕西杨凌7200四川省北川羌族自治县动物疫病预防控制中心四川北川622750
陈胡羚,辛怡霖,侯佳琪,王虹雅,唐 熙,李青云,张 欣,李引乾* (.西北农林科技大学 动物医学院,陕西 杨凌 7200;2.四川省北川羌族自治县动物疫病预防控制中心,四川 北川 622750)
氟苯尼考(florfenicol,FFC)是一种动物专用的酰胺醇类高效广谱抗菌药物,于20世纪80年代后期成功研制,在治疗畜禽细菌性疾病中发挥着重要作用[1-4]。但FFC水溶性极低,在动物体内的吸收不良,生物利用度低,临床上通常以混饲方式给药。当畜禽发病时,通常食欲废绝,导致给药困难,造成药浪费,使用药成本提高,且易对环境造成污染[5]。药物纳米晶体是指将药物颗粒自身纳米化制备得粒径在1~1 000 nm范围内的纳米药物[6-8]。将药物制成纳米晶体,除了可以改善难溶性药物的溶解性[9-10],增加药物的生物利用度外[11-13],还具有提高药物疗效,减少使用剂量,降低不良反应等优势[14],在医药领域纳米晶技术已被广泛应用以提升药物的理化性能。氟苯尼考纳米晶(florfenicol nanocrystal,FFC-NC)相较其原粉有更优的溶解度和其他物理性能,本试验旨在对研制的FFC-NC在鸡体内的药动学进行研究,考察纳米晶对药物生物利用度的影响,以期为FFC-NC的临床应用提供试验依据。
1 材料与方法
1.1 药品与试剂FFC(FB2002051)购自江苏恒盛药业有限公司;FFC标准品(H1715060)购自上海阿拉丁生化科技股份有限公司; FFC-NC,本实验室自制;羧甲基纤维素纳(20190712)、肝素钠(20191022)和乙腈(20200309)购自天津市科密欧化学试剂有限公司;醋酸铵(20200508)和甲醇(20200102)购自天津市天力化学试剂有限公司;无水乙醇(200607)购自四川西陇科学有限公司;乙酸乙酯(20200321)购自天津市富宇精细化工有限公司;蛋鸡料购自新希望集团广汉国雄饲料有限公司。
1.2 实验动物600~650日龄健康罗曼粉蛋鸡6只,体质量为(2.3±0.2) kg。饲喂不含任何抗生素及药物的国雄蛋鸡料。饲养环境经过严格消毒,其通风性好,采光好,温度为20~25℃,相对湿度为55%~65%。给药前12 h开始至给药后6 h禁食,自由饮水。
1.3 动物分组及给药方法给药前每只鸡测体质量,并做好标记,抽取0.5 mL血液,置于含肝素钠抗凝剂的离心管中,6 000 r/min离心5 min取上层血浆保存。将FFC原粉和FFC-NC分别用0.2%羧甲基纤维素纳水溶液溶解,配制成FFC质量浓度为10 g/L 混悬液,按20 mg/kg剂量灌胃给药。
试验分为FFC原粉组和FFC-NC组。为了减少干扰变量的影响,两组试验使用同一批健康母鸡6只。适应性饲养2周后,采用交叉试验评价生物利用度。首先以FFC-NC灌胃给药,采血测定其血药浓度。试验母鸡经历3周洗脱后,再以相同剂量灌胃给药FFC原粉。
1.4 血浆样品采集用药后0.083,0.25,0.50,0.75,1,1.5,2,3,4,6,8,12,24 h分别翅下静脉采血0.5 mL,置于含有肝素钠的离心管中,5 000 r/min离心5 min,取上层血浆,置于-20℃冰箱保存,血浆样品在2周内测完。
1.5 样品处理将血浆样品自然解冻后,混匀,取200 μL血浆,加入400 μL乙酸乙酯以提取FFC。将其涡旋振荡2 min,充分混匀后,8 000 r/min离心2 min,吸取上层乙酸乙酯提取液。按上述步骤,下层液中加入乙酸乙酯重复提取1次,合并2次提取液。45℃氮气吹干,加入200 μL流动相,涡旋振荡3 min后,10 000 r/min离心10 min,吸取上清液用0.22 μm微孔滤膜过滤,即得供试品。
1.6 药动学方法学的建立
1.6.1高效液相色谱法(high performance liquid chromatography,HPLC)条件 色谱柱采用Shim-pack GIST C18柱(250 mm×4.6 mm,5 μm),流动相为0.05 mol/L醋酸铵溶液∶乙腈=78∶22(V∶V),流速:1.0 mL/min,柱温:20℃,紫外检测波长:224 nm,进样量:20 μL。
1.6.2方法专属性 取鸡空白血浆200 μL,按1.5方法处理后,按HPLC法进样20 μL得鸡空白血浆HPLC图谱。取鸡空白血浆200 μL,加入5 mg/L FFC标准液200 μL,按1.5方法处理后,进样20 μL得鸡空白血浆中添加FFC HPLC图谱。将FFC组和FFC-NC组血浆样品HPLC图谱与上述两图谱进行比较分析。
1.6.3标准曲线绘制 于空白血浆中加入FFC标准溶液,配制质量浓度为32 mg/L FFC母液,采用梯度稀释法,将其稀释为16.0,8.0,4.0,2.0,1.0,0.1 mg/L,将上述所得不同质量浓度FFC标准血浆样品按1.5项处理后,进行HPLC检测分析。重复测定3次,取平均值。以FFC质量浓度(x)为横坐标,以峰面积(y)为纵坐标,绘制鸡空白血浆中FFC标准曲线,得回归方程。分别按信噪比S/N=3和S/N=10确定检测限(LOD)和定量限(LOQ)。
1.6.4回收率试验 于空白血浆中加入FFC标准液,配制成0.1,4.0,16.0 mg/L低、中、高质量浓度FFC血浆样品,按1.5项方式处理后,进行HPLC检测分析。重复测定3次,计算该质量浓度样品的分析方法回收率和变异系数,计算公式如下:
回收率(%)=A1/A×100%;

1.6.5精密度试验 精密配制0.1,4.0,16.0 mg/L的低、中、高质量浓度的FFC血浆样品,按1.5项方式处理后,进行HPLC检测分析。分别于同日内对每个质量浓度样品测定3次,不同日内连续测定3 d,将测得的色谱峰面积利用标准曲线计算样品质量浓度,将其与加入量比较,计算日内变异系数和日间变异系数。
1.6.6重复性试验 精密配制6份4 mg/L FFC血浆样品,按1.5项方式处理后,进行HPLC检测分析,计算变异系数。
1.7 血药浓度测定对1.5项处理血样所得的供试品,以 HPLC法测定。
1.8 数据处理采用DAS 2.0软件进行数据处理,计算包括药时曲线下面积(AUC)、消除半衰期(t1/2)、平均驻留时间(MRT)、峰浓度(Cmax)和峰时(tmax)在内的药代动力学参数。最佳房室模型的确定是依据赤池信息准则(akaike information criterion,AIC)值最小原则。利用GraphPad Prism 8.0作图软件绘制药时曲线,利用IBM SPSS Statistics 25.0统计分析软件进行相关药动学参数的差异性分析。此研究采用单因素方差分析法来检验显著性,P<0.05为差异显著,具有统计学意义。
2 结果
2.1 方法专属性该试验采用方法操作便捷,样品处理简单。方法专属性试验结果见图1~4。

图1 鸡空白血浆HPLC图

图2 鸡空白血浆添加FFC HPLC图

图3 FFC原粉组血浆样品HPLC图

图4 FFC-NC组血浆样品HPLC图
对比图1,2可知,色谱图基线平稳,血浆峰与FFC峰分离完全,这说明血浆内源性杂质不会干扰FFC的测定,FFC的保留时间在24 min左右,空白血浆在此处无峰出现。图3为FFC原粉组血浆样品的HPLC图,FFC的保留时间为24.301 min;图4为FFC-NC组血浆样品HPLC图,FFC的保留时间为24.459 min;进一步说明此方法的专属性好,适合用于鸡血浆中FFC检测。
2.2 标准曲线和线性范围以FFC质量浓度(x)为横坐标,以峰面积(y)为纵坐标,绘制鸡空白血浆中FFC标准曲线(图5)。
由图5可得回归方程:y=21 693x+4 720.6,(R2=0.999 2,n=3)。FFC在质量浓度为0.1~32.0 mg/L 具有良好线性关系。按信噪比S/N=3求得鸡血浆中FFC的LOD为0.03 mg/L。按信噪比S/N=10得LOQ为0.1 mg/L。
2.3 回收率利用 HPLC分别对0.1,4.0,16.0 mg/L 低、中、高质量浓度FFC血浆样品进行测定,利用鸡空白血浆中FFC标准曲线回归方程计算回收率,结果见表1。
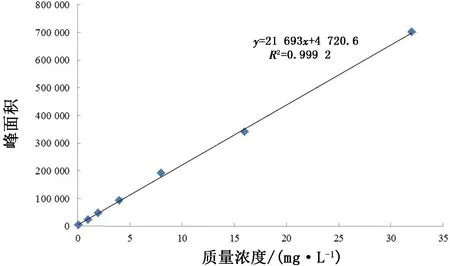
图5 鸡空白血浆中FFC标准曲线

表1 回收率结果(n=3)
由表1结果可知,各组回收率均高于97%,符合测定要求,说明可采用 HPLC测定鸡血浆样品中FFC考质量浓度。
2.4 精密度利用 HPLC法分别对0.1,4.0,16.0 mg/L 低、中、高质量浓度FFC血浆样品进行日内精密度和日间精密度测定,试验结果见表2。
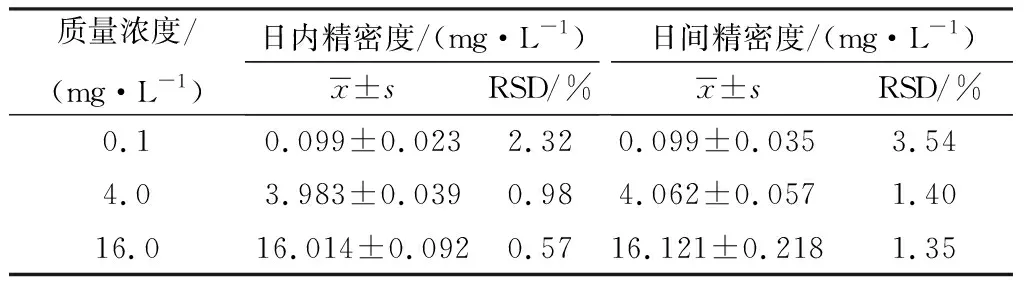
表2 精密度测定结果(n=3)
表2结果表明,低、中、高3个不同质量浓度FFC血浆样品的日内及日间精密度均小于3.54%,符合测定要求,说明此试验建立的HPLC法可用于测定鸡血浆样品中FFC质量浓度。
2.5 重复性试验对6份4 mg/L的FFC血浆样品进行HPLC检测,结果显示其峰面积为(91 976.83±2 890.475),平均质量浓度为(4.022±0.132) mg/L,RSD值为3.28%,表明此试验建立的HPLC法的重复性好,检测结果具有可靠性。
2.6 血药浓度测定分别给鸡灌胃FFC原粉和FFC-NC后,两组鸡的不同时间点血药浓度见表3。

表3 FFC 和FFC-NC 组不同时间点血药质量浓度 mg/L
由表3可知,在给药后0.25~6.00 h,FFC-NC组血药质量浓度均高于FFC原粉组,且从6只鸡的最大血药质量浓度可以看出,FFC-NC组要高于FFC原粉组。
2.7 药时曲线及药动学参数
2.7.1药时曲线 分别给母鸡灌胃FFC原粉和FFC-NC后,两组药物在母鸡体内的血药质量浓度-时间曲线如图6。

图6 FFC和FFC-NC组药时曲线图
由图6可以看出,在试验时间范围内,FFC-NC在鸡体内的血药质量浓度明显高于FFC原粉组。FFC-NC组在(0.875±0.137) h时达到最大值,为(8.249±0.713) mg/L,而FFC原粉组在(1.167±0.258) h时达到最大值,为(2.381±0.796) mg/L。
2.7.2药动学参数 采用DAS 2.0药代动力学分析软件和IBM SPSS Statistics 25.0统计学软件对生物利用度试验获得的数据进行处理。根据AIC值最小原则,选择了最佳模型为一室模型(AIC=7.61),而非二室模型(AIC=16.52)。两组试验所得药动学参数结果见表4。
表4 FFC和FFC-NC组药动学参数
根据表4可得,与FFC原粉组相比,FFC-NC组的达峰时间tmax为(0.875±0.137) h,峰时缩短,药时曲线下面积AUC(0-∞)和峰浓度Cmax分别为(23.957±2.338) mg/(L·h)和(8.249±0.713) mg/L,FFC-NC组的相对生物利用度是FFC组的3.6倍。结果表明,FFC-NC的药动学特征较FFC均有明显改善。
3 讨论
FFC在生物药剂学分类系统(biopharmaceutics classification system,BCS)中属于第Ⅱ类低溶解性、高渗透性药物。FFC极微溶于水,影响其临床使用。将难溶性药物制备成纳米晶,能有效提高其溶解性能,极具发展前景[15]。临床用药可以将药物纳米晶体制成口服制剂、注射制剂、吸入制剂、透皮制剂等多种剂型方便给药[16]。将药物纳米晶体应用于口服制剂,药物的口服药动学特征将得到改善[17]。将纳米晶应用于注射剂,能改善药物的体外溶出率,提高制剂的安全性[18-19]。将纳米晶应用于透皮制剂,药物的溶解性能得到改善,则药物透皮吸收力增强,从而改善药物的药动学特征和生物利用度[20]。
药动学参数是反映药物在体内动态变化规律性的一些常数,是评价兽药质量的重要指标之一。消除半衰期t1/2指血药浓度下降一半所需时间,反映了药物从体内的消除速度,FFC-NC组与原粉组的t1/2无显著性差异,表明将FFC制成纳米晶不影响其在体内的消除速度。药时曲线下面积AUC(0-∞)是血药浓度曲线对时间轴所包围的面积,是评价药物吸收程度的重要指标,FFC-NC组AUC(0-∞)为(23.957±2.338) mg/(L·h)与原粉组AUC(0-∞)(6.749±1.577) mg/(L·h)相比极显著提高(P<0.01),表明FFC-NC在鸡体内的吸收好。达峰时间tmax反映药物进入体内的速度,达峰时间tmax越短则吸收速度越快,FFC-NC组tmax(0.875±0.137) h与原粉组tmax(1.167±0.258) h相比显著缩短(P<0.05),表明FFC-NC在鸡体内的吸收速度快。药峰浓度Cmax是给药后血药浓度的最高值,是评价药物吸收速率和吸收程度的重要指标,FFC-NC组Cmax(8.249±0.713) mg/L与原粉组Cmax(2.381±0.796) mg/L相比极显著提高(P<0.01),表明将FFC制成纳米晶后,其在鸡体内的吸收好且吸收速度快。生物利用度是指药物以一定剂型从给药部位吸收入血的速率和程度,是评价药物质量的重要标准。生物利用度又分为绝对生物利用度和相对生物利用度,绝对生物利用度是内服或其他非血管给药途径所得的AUC与静脉注射的AUC的比值,相对生物利用度则是采用内服参照标准药物的AUC作比较[1]。此试验通过口服给药,比较FFC原粉和FFC-NC在鸡体内的生物利用度。试验结果显示,FFC-NC组的相对生物利用度是FFC原粉组的3.6倍。
SWITALA等[21]研究FFC在火鸡体内的药代动力学,得出在火鸡体内FFC的口服生物利用度为82%。TIKHOMIROV等[22]报道FFC在骡鸭体内的口服生物利用度为73.86%。此外,FFC在肉鸡和犊牛中的口服生物利用度分别为55.3%和88.0%;给猪口服FFC则几乎完全被吸收[23]。鸡静脉注射FFC的半衰期为5.36 h,50%~65%的药物以原形从尿液中排出[1]。以上研究报道FFC在不同动物体内的生物利用度。本试验选择在临床上使用FFC较多的母鸡作为靶动物,采用交叉试验法进行评价,减少了由于机体不同带来的影响。
FFC在兽医临床的使用上受限,主要是其难溶性和生物利用度低的问题。利用纳米技术将难溶性药物制备成纳米晶,增大比表面积,从而增加其溶解度,改善药动学特征和生物利用度[24-25]。此试验利用 HPLC考察FFC和其纳米晶制剂在鸡体内的药动学特征。试验结果显示,FFC-NC组的药动学特征改善明显。说明FFC-NC制剂相较其原粉,具有更优的药动学特征,本试验为FFC-NC的临床使用提供试验依据。
