补骨脂炮制前后水煎液致雌性ICR小鼠胆汁瘀积性肝损伤作用比较
2022-03-03符映均梅春梅华政颖李伟东
符映均,吴 育, ,梅春梅,华政颖,李伟东*
补骨脂炮制前后水煎液致雌性ICR小鼠胆汁瘀积性肝损伤作用比较
符映均1,吴 育1, 2,梅春梅2,华政颖2,李伟东2*
1.南京中医药大学南通附属医院药剂科,江苏 南通 226000 2.南京中医药大学 江苏省中药炮制重点实验室 国家教育部中药炮制规范化及标准化工程研究中心,江苏 南京 210023
探讨补骨脂炮制前后致雌性ICR小鼠胆汁瘀积性肝损伤的差异。采用高效液相色谱仪检测补骨脂炮制前后化学成分含量变化。雌性ICR小鼠连续30 d ig生、盐补骨脂水煎液,末次给药24 h后,取血清,采用全自动生化仪检测肝损伤相关指标丙氨酸转氨酶(alanine aminotransferase,ALT)、天冬氨酸转氨酶(aspartate aminotransferase,AST)、碱性磷酸酶(alkaline phosphatase,ALP)活性和总胆红素(total bilirubin,TBIL)、直接胆红素(direct bilirubin,DBIL)、总胆汁酸(total bile acid,TBA)水平;取肝脏、脾脏和肾脏,称定质量并计算脏器指数,采用苏木素-伊红(HE)染色法进行肝脏病理组织学检查;采用ELISA法检测血清中雌二醇(estradiol,E2)、促卵泡激素(follicle-stimulating hormone,FSH)和白细胞介素-6(interleukin-6,IL-6)以及肝脏中法尼醇受体(farnesoid X receptor,FXR)、雌激素硫酸转移酶1E1(sulfotransferase 1E1,SULT1E1)和E2含量。补骨脂经盐炙后补骨脂苷、异补骨脂苷、新补骨脂异黄酮含量下降,其余8种成分含量均升高,其中补骨脂素、异补骨脂素、corylifol A升高较为明显。雌性小鼠ig生、盐补骨脂水煎液30 d后出现生殖器损伤,小鼠阴道口红肿,有水样浸润。与对照组比较,生、盐补骨脂组小鼠血清ALT、AST、ALP活性及DBIL、TBIL、TBA水平均显著升高(<0.05、0.01、0.001),盐炙后补骨脂致肝损伤较生品更严重;肝脏FXR、SULT1E1含量显著降低(<0.01、0.001),血清E2、FSH、IL-6和肝脏E2含量均显著升高(<0.05、0.01、0.001)。盐补骨脂与生补骨脂比较,IL-6升高更明显,FXR、SULT1E1下降更明显。补骨脂素、异补骨脂素和Corylifol A可能是补骨脂药效成分同时也可能是其主要毒性成分,盐补骨脂较生补骨脂更易造成肝损伤。
补骨脂;盐炙;胆汁瘀积性肝损伤;雌激素样作用;补骨脂素;异补骨脂素;corylifol A;补骨脂苷;异补骨脂苷;新补骨脂异黄酮
补骨脂为豆科植物补骨脂L.的干燥成熟果实,在我国临床上应用已有上千年的历史。补骨脂作为传统的补阳药,具有补肾壮阳、固精缩尿、温脾止泻的功效,其生品味辛、苦,性温,盐炙后能和其辛窜温燥之性,并引药入肾。《中国药典》2020年版一部记载盐补骨脂的炮制方法,取净补骨脂,照盐炙法(通则0213)炒至微鼓起。古代补骨脂主要用于治疗肾虚腰痛、小便频数、小儿遗尿、肾漏,现代多用于抗肿瘤、抗菌、治疗骨质疏松等。古代文献中仅有关于其燥性的描述,《雷公炮炙论》云:“性本大燥,毒。”补骨脂经盐炙入药,古云“盐制入肾”,经炮制后补骨脂的疗效增强。目前以补骨脂为主药生产的制剂有仙灵骨葆胶囊、白蚀丸、复方补骨脂颗粒、青娥丸等,常作为植物雌激素治疗更年期综合征。但随着临床的推广使用,补骨脂的肝毒性逐渐被人发现,并伴随着相关的临床和实验研究[1-4],其肝毒性愈发受人重视。
刘亚蕾等[5]收集了2012—2016年含补骨脂的制剂的药物性肝损伤共110个病例,有91例是由补骨脂引起的肝损伤(占肝损总病例数82.72%);89.01%患者年龄在41岁以上,且女性居多,占参与调查的肝损所有患者的60.9%,具有明显的性别差异。Nam等[6]回顾分析40例补骨脂所致肝损病例发现,约85.0%患者为女性,年龄集中在54~70岁,丙氨酸转氨酶(alanine aminotransferase,ALT)、天冬氨酸转氨酶(aspartate aminotransferase,AST)、总胆红素(total bilirubin,TBIL)和直接胆红素(direct bilirubin,DBIL)含量均显著升高,补骨脂造成的肝损伤多表现为肝细胞损伤,停药后6个月内痊愈,没有出现终末期肝病或死亡。
蔡涛涛等[7]按25 mL/kg给予小鼠补骨脂全粉,发现盐炙后Na+改变肠道渗透压,增大了小鼠肠道对补骨脂全组分的吸收,毒性作用增强,且补骨脂毒性强度与不同炮制品种含补骨脂素与异补骨脂素含量成正相关。夏亚楠等[8]以肾阳虚、脾虚大鼠为研究模型,连续7 d按7 g/kg ig补骨脂生品、水炙品、盐炙品补骨脂提取液,得出相反结论,提示盐炙后可以降低肝毒性。陶益等[9]研究表明,酒炙和盐炙后补骨脂酚含量较生品下降,而补骨脂素和异补骨脂素含量显著升高。且有报道雌性小鼠更易造成肝损伤[10]。为了进一步探究盐制补骨脂的肝毒性,本研究首先检测补骨脂炮制前后化学成分差异,再将生补骨脂、盐补骨脂水煎液分别ig给药30 d,探究其对雌性ICR小鼠的肝毒性。
1 材料
1.1 动物
SPF级雌性ICR小鼠,14~16周龄,体质量32~36 g,购自北京维通利华实验动物技术有限公司,许可证号SCXK(LU)2016-0001,置于动物实验室设施中,标准光照/黑暗周期为12 h。所有接受人道关怀和治疗的动物均符合《中国实验动物管理立法规定和一般建议》,并由南京中医药大学动物护理和使用委员会批准(伦理证号202004A037)。
1.2 药品与试剂
补骨脂(批号191101,云南大理)购自北京同仁堂,由南京中医药大学陈建伟教授鉴定为豆科植物补骨脂L.的干燥成熟果实,标本编号(1804058)保存于南京中医药大学植物标本馆;对照品4′--甲基补骨脂查耳酮(批号120415)、补骨脂甲素(批号101026)、Corylifol A(批号110117)、补骨脂二氢黄酮甲醚(批号110502)、补骨脂宁(批号120612)、新补骨脂异黄酮(批号110409)、补骨脂宁(批号120216)、补骨脂苷(批号120612)、异补骨脂苷(批号120603)、补骨脂素(批号120307)、异补骨脂素(批号120308)购自南京世洲生物科技有限公司,质量分数均为98%;小鼠法尼醇受体(farnesoid X receptor,FXR)试剂盒(批号ANG-E22041M)、小鼠白细胞介素-6(interleukin-6,IL-6)试剂盒(批号ANG-E22036M)、小鼠雌二醇(estradiol,E2)试剂盒(批号ANG-E21444M)、小鼠促卵泡激素(follicle-stimulating hormone,FSH)试剂盒(批号ANG-E22036M)购自南京建成生物工程研究所;小鼠雌激素硫酸转移酶1E1(sulfotransferase 1E1,SULT1E1)试剂盒(批号832X724744)购自南京奥青生物技术有限公司。
1.3 仪器
e2695型高效液相色谱仪(HPLC,美国Allince公司);Microfuge 22R型离心机、AU680型全自动生化仪(美国Beckman Coulter公司);680型酶标分光光度读板仪(美国Bio-Rad公司);DM1L型倒置荧光显微镜(德国Leica公司)。
2 方法
2.1 盐炙补骨脂
盐补骨脂按照《中国药典》2020年版盐炙法(通则0213)标准炮制加工。取净补骨脂,喷淋适量盐水,拌匀,闷润3~6 h,至盐水被吸尽,置已加热炒制容器内,用文火炒至表面未鼓起,并有香气溢出时,取出,晾凉,即得。
2.2 补骨脂生品及盐制品11种化学成分的含量测定[11]
2.2.1 色谱条件 Kromasil C18色谱柱(250 mm×4.6 mm,5 µm),流动相为乙腈(A)-0.1%甲酸水溶液(B),梯度洗脱:0~3 min,5% A;3~15 min,5%~15% A;15~25 min,15%~18% A;25~35 min,18%~35% A;35~50 min,35%~40% A;50~55 min,40%~50% A;55~70 min,50%~100% A;70~88 min,100%~5% A;88~90 min,5% A;体积流量为1 mL/min;柱温为30 ℃;检测波长为254 nm;进样量为10 µL。
2.2.2 对照品溶液的制备 精密称取对照品(表1),1、3、4~7号置于10 mL量瓶,2、8~11号置于5 mL量瓶,精密加入甲醇定容,超声5 min,经微孔滤膜(0.45 µm)滤过,放入液相小瓶,进样测定。

表1 对照品配制信息
2.2.3 供试品溶液的制备 称取补骨脂生品及盐制品各50 g,打粉,过4号筛,精密称取10 g(3份),至砂锅中,量取超纯水150 mL,煎煮30 min,煎煮2次,合并滤液,浓缩至100 mL;精密量取1 mL,加入1 mL无水乙醇,12 000 r/min离心10 min,取上清液,经微孔滤膜(0.45 µm)滤过,放入液相小瓶,进样测定。
2.3 补骨脂生品及盐制品肝毒性研究
2.3.1 生、盐补骨脂水煎液的制备 分别取140 g生补骨脂、盐补骨脂,按传统煎煮方法煎煮,第1次加8倍量水煎煮,第2次加6倍量水煎煮,煎煮液浓缩至200 mL,冷冻干燥处理,制成冻干粉,用于后续毒性试验,临床等效剂量按5倍剂量等比稀释,即得。
2.3.2 动物分组及给药 在确定补骨脂各组分含量符合《中国药典》2020年版规定后,按传统方法煎煮补骨脂进行后续毒性试验。将雌性ICR小鼠随机分为对照组及生补骨脂低、高剂量(5、20 g/kg)组和盐补骨脂低、高剂量(5、20 g/kg)组,每组6只,各给药组ig相应药物,对照组ig等体积0.9%氯化钠溶液,1次/d,连续30 d。
2.3.3 血清生化检测 末次给药24 h后,小鼠经眼后静脉取血,4 ℃、1000×离心10 min,分离得到上清液,于−80 ℃保存。采用全自动生化仪检测血清中ALT、AST、碱性磷酸酶(alkaline phosphatase,ALP)活性和DBIL、TBIL、总胆汁酸(total bile acid,TBA)水平。
2.3.4 组织病理学检查 各组小鼠脱颈椎处死,于9: 00~10: 00时取肝脏,以减少药物代谢酶基因表达的变化。称定肝脏、肾脏、脾脏质量,计算脏器指数。
脏器指数=器官质量×1000/体质量
将10%多聚甲醛固定肝组织,洗涤、脱水,进行石蜡包埋,切片干燥后用二甲苯脱腊,再用梯度酒精脱苯,蒸馏水复水,最后用苏木素-伊红(HE)染色,于光镜下观察。
2.3.5 ELISA法检测血清中E2、FSH、IL-6和肝脏中FXR、SULT1E1、E2含量 取于−80 ℃保存的血清及肝脏,将肝脏用PBS溶液匀浆,按试剂盒说明书检测血清中E2、FSH、IL-6及肝脏中FXR、SULT1E1、E2含量。
2.4 统计学处理
3 结果
3.1 生、盐补骨脂的化学成分含量比较
如图1和表2所示,盐补骨脂相较于生补骨脂,除补骨脂苷、异补骨脂苷和新补骨脂异黄酮含量降低外,4′--甲基补骨脂查耳酮、补骨脂甲素、corylifol A、补骨脂二氢黄酮甲醚、补骨脂宁、补骨脂定、补骨脂素和异补骨脂素含量均有上升。
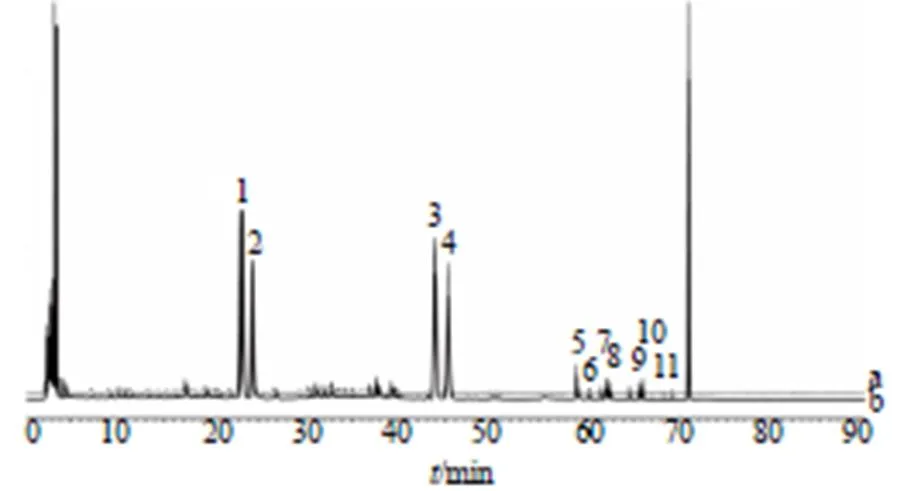
1-补骨脂苷 2-异补骨脂苷 3-补骨脂素 4-异补骨脂素 5-新补骨脂异黄酮 6-补骨脂甲素 7-补骨脂宁 8-补骨脂定 9-补骨脂二氢黄酮甲醚 10-corylifol A 11-4′-O-甲基补骨脂查耳酮
表2 生、盐补骨脂各成分含量(, n = 6)
Table 2 Contents of components in raw and salt processed Psoraleae Fructus (, n = 6)
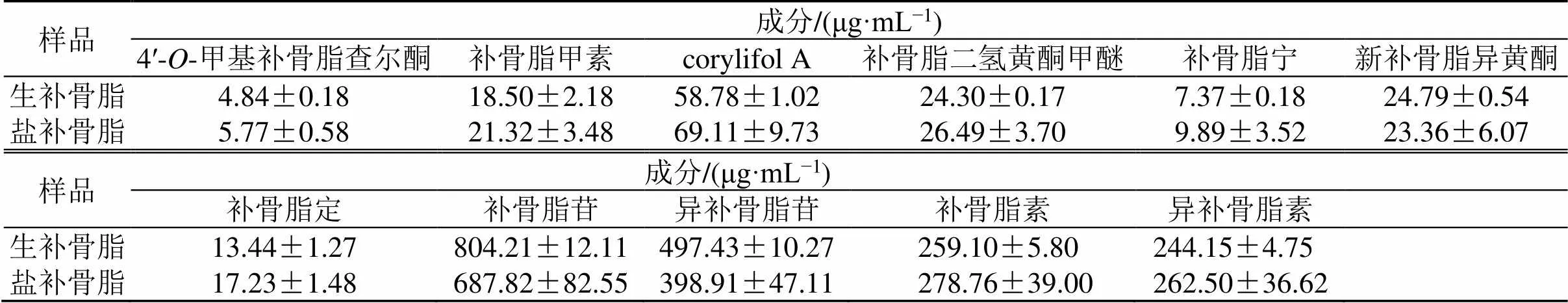
表2 生、盐补骨脂各成分含量(, n = 6)
样品成分/(μg·mL−1) 4′-O-甲基补骨脂查尔酮补骨脂甲素corylifol A补骨脂二氢黄酮甲醚补骨脂宁新补骨脂异黄酮 生补骨脂4.84±0.1818.50±2.1858.78±1.0224.30±0.177.37±0.1824.79±0.54 盐补骨脂5.77±0.5821.32±3.4869.11±9.7326.49±3.709.89±3.5223.36±6.07 样品成分/(μg·mL−1) 补骨脂定补骨脂苷异补骨脂苷补骨脂素异补骨脂素 生补骨脂13.44±1.27804.21±12.11497.43±10.27259.10±5.80244.15±4.75 盐补骨脂17.23±1.48687.82±82.55398.91±47.11278.76±39.00262.50±36.62
3.2 生、盐补骨脂对ICR小鼠表观的影响
如图2所示,雌性小鼠ig生、盐补骨脂30 d后,均出现生殖器损伤,雌性小鼠阴道口红肿,有水样浸润,且盐补骨脂组较生补骨脂组更为严重。
3.3 生、盐补骨脂对ICR小鼠血清中ALT、AST、ALP活性和DBIL、TBIL、TBA水平的影响
如图3所示,与对照组比较,生、盐补骨脂各剂量组血清中ALT、AST、ALP活性和TBIL、TBA水平均显著升高(<0.05、0.01、0.001),生补骨脂高剂量组及盐补骨脂各剂量组血清中DBIL水平显著升高(<0.01、0.001),且呈剂量相关性。比较生补骨脂和盐补骨脂高剂量组,血清中ALT、ALP活性和TBIL、TBA水平有显著性差异(<0.05、0.01、0.001);比较生补骨脂和盐补骨脂低剂量组,血清DBIL、TBIL水平有显著性差异(<0.01);表明盐补骨脂较生补骨脂造成ICR小鼠肝损伤更为严重。
3.4 生、盐补骨脂对ICR小鼠脏器指数的影响
如表3所示,雌性小鼠ig生、盐补骨脂30 d后,与对照组比较,肝脏指数较脾脏、肾脏指数改变更为明显,盐补骨脂高剂量组肝脏、脾脏、肾脏指数较生补骨脂高剂量组有显著性差异(<0.05、0.01)。

图2 生、盐补骨脂对ICR小鼠表观的影响
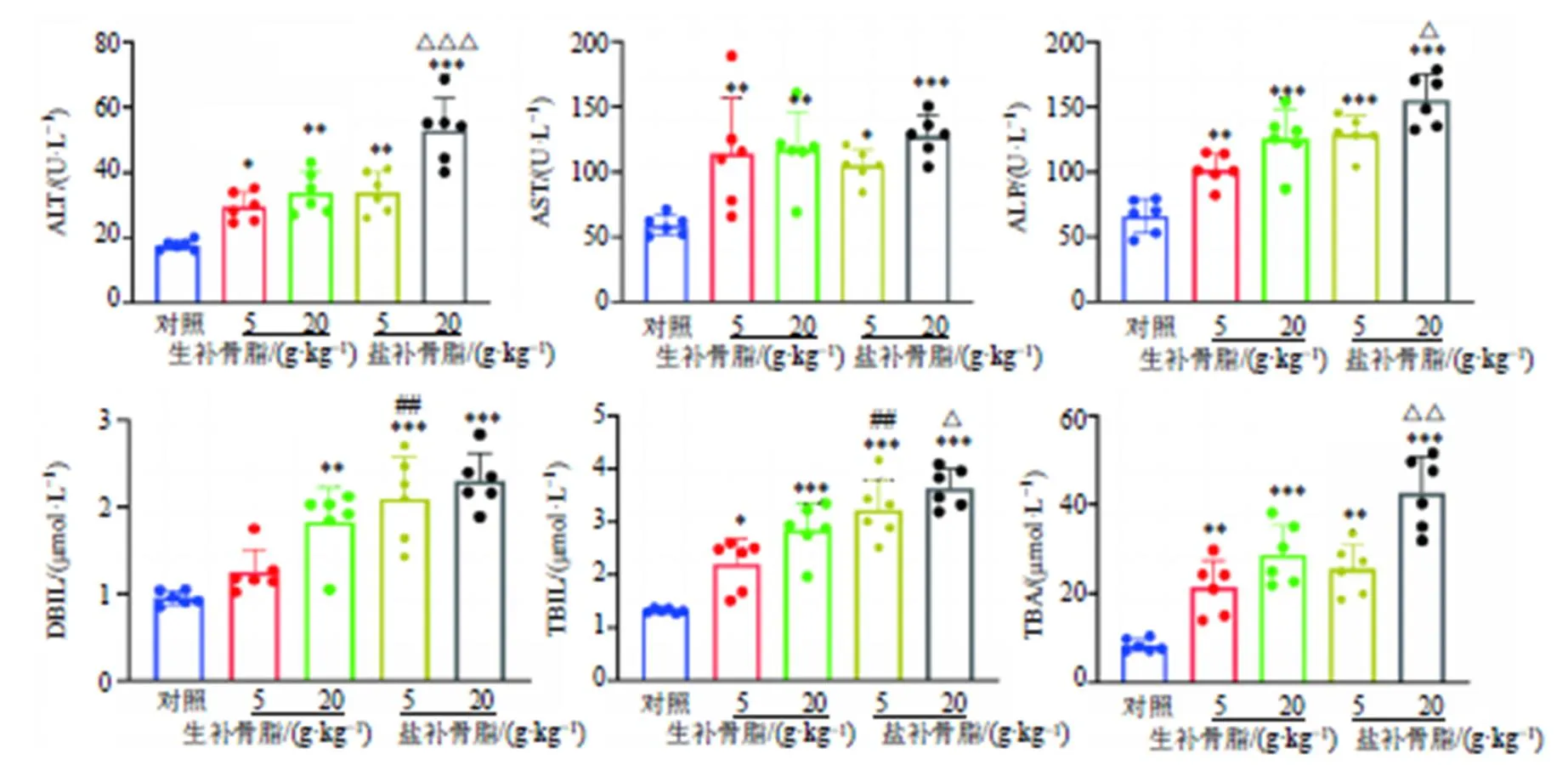
与对照组比较:*P<0.05 **P<0.01 ***P<0.001;与生补骨脂低剂量组比较:#P<0.05 ##P<0.01 ###P<0.001;与生补骨脂高剂量组比较:△P<0.05 △△P<0.01 △△△P<0.001,图5同
表3 生、盐补骨脂对ICR小鼠脏器指数的影响(, n = 6)
Table 3 Effect of raw and salt processed Psoraleae Fructus on organ index of ICR mice (, n = 6)

表3 生、盐补骨脂对ICR小鼠脏器指数的影响(, n = 6)
组别剂量/(g·kg−1)肝脏指数/(mg·g−1)脾脏指数/(mg·g−1)肾脏指数/(mg·g−1) 对照—34.79±4.843.72±0.8310.06±0.54 生补骨脂535.99±3.913.19±0.6410.03±0.60 2036.32±6.43*3.47±1.009.82±1.74 盐补骨脂535.58±2.753.01±0.2510.18±0.42 2041.40±5.22**△△5.58±2.70***△△11.11±1.15*△
与对照组比较:*<0.05**<0.01***<0.001;与生补骨脂高剂量组比较:△<0.05△△<0.01
*< 0.05**< 0.01***< 0.001control group;△< 0.05△△< 0.01rawhigh-dose group
3.5 生、盐补骨脂对ICR小鼠肝组织病理变化的影响
如图4所示,各给药组雌性小鼠肝组织均有不同程度的水肿和炎症浸润,盐补骨脂组小鼠肝细胞水肿更为明显,盐补骨脂低剂量组轻度炎症细胞浸润,盐补骨脂高剂量组炎症细胞浸润更为严重;生补骨脂、盐补骨脂高剂量组部分出现脂肪变性,明显水肿,疑似枯发细胞增多。
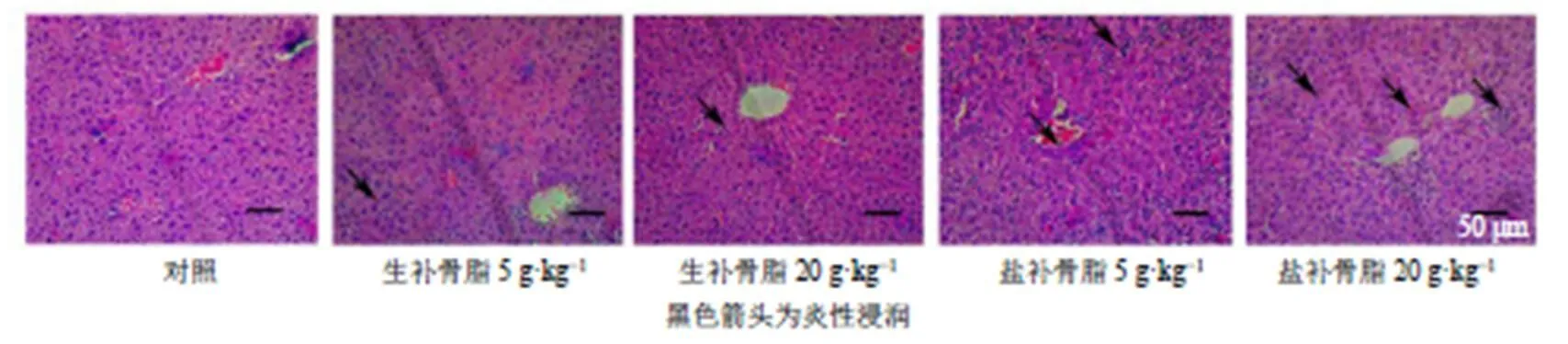
图4 生、盐补骨脂对ICR小鼠肝组织病理变化的影响 (×200)
3.6 生、盐补骨脂对ICR小鼠血清中E2、FSH、IL-6和肝脏中FXR、SULT1E1、E2含量的影响
如图5所示,与对照组比较,生、盐补骨脂各剂量组小鼠血清中E2、FSH和肝脏中E2含量均显著升高(<0.01、0.001),肝脏中FXR含量显著降低(<0.01、0.001);生补骨脂低剂量组和盐补骨脂各剂量组小鼠血清中IL-6含量显著升高(<0.05、0.01、0.001),盐补骨脂高剂量组肝脏SULT1E1含量显著降低(<0.01)。比较生补骨脂和盐补骨脂高剂量组,血清IL-6和肝脏SULT1E1含量有显著差异(<0.05);比较生补骨脂和盐补骨脂低剂量组,肝脏FXR含量有显著差异(<0.05)。
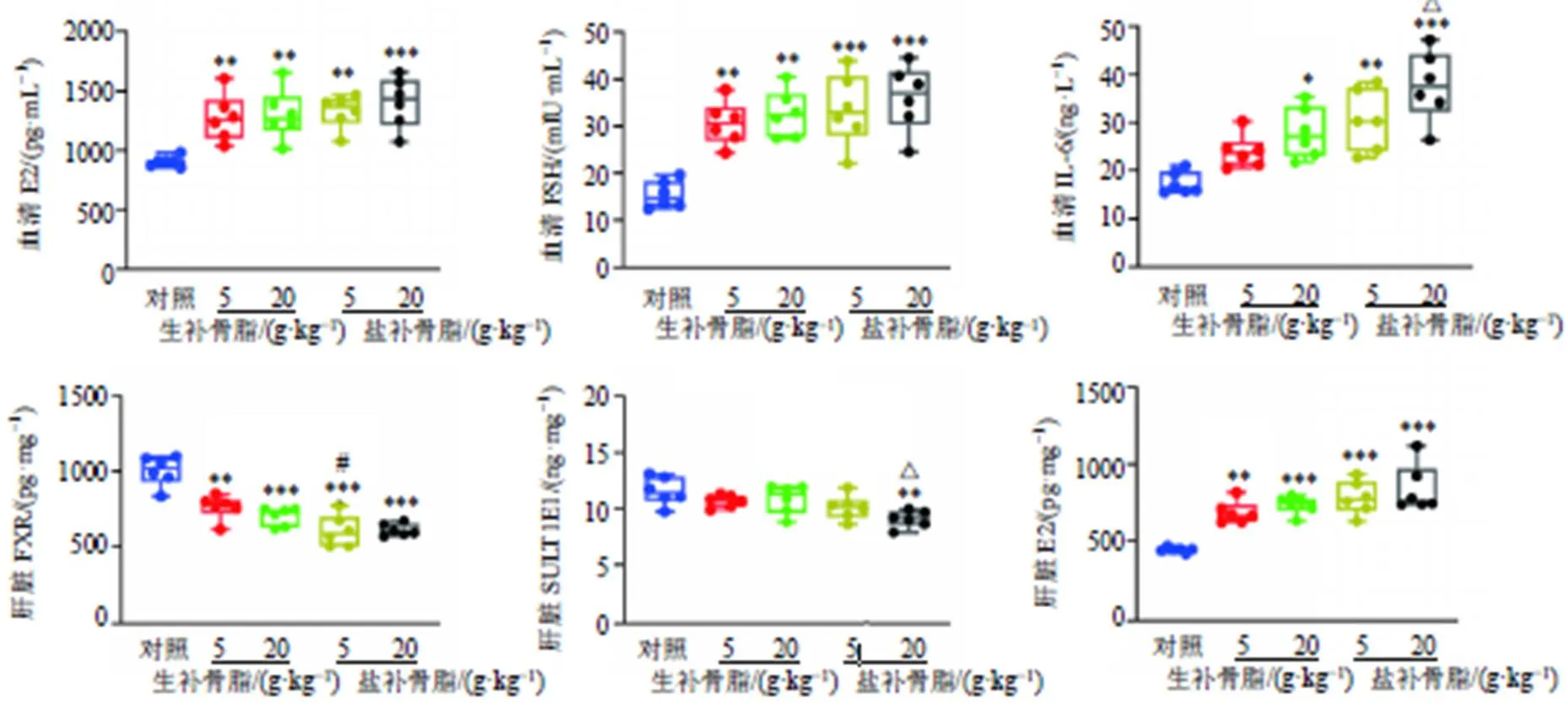
图5 生、盐补骨脂对ICR小鼠血清中E2、FSH、IL-6和肝脏中FXR、SULT1E1、E2含量的影响
4 讨论
《中国药典》2020年版规定补骨脂含补骨脂素和异补骨脂素的总量不得少于0.70%。本研究采用HPLC测定生、盐补骨脂水煎液各成分含量[11],得出盐炙后补骨脂苷、异补骨脂苷和新补骨脂异黄酮相较于生品略有降低,其余检测出的8个成分如补骨脂素和异补骨脂素等含量均有提升。梁灿璨等[12]认为补骨脂盐制后毒性降低,SD大鼠ig生、盐补骨脂7 d,大鼠血清中ALT、AST活性降低,表明补骨脂盐炙后可缓解药物对肾阳虚大鼠肝肾功能的不良反应,同时缓解生品的燥性,盐炙对药物燥性的缓解作用可能与其对体内水通道蛋白(aquaporin,AQP)表达调控有关。补骨脂酒炙后其主要肝毒性成分补骨脂素和异补骨脂素的含量均比生品降低[13]。有学者认为,雷公炮制法使用黄酒对补骨脂进行炮制,与现代常用的2种盐炙法比较,补骨脂苷、异补骨脂苷和补骨脂酚下降更为明显,水处理主要促进苷类成分降解[14]。陶益等[9]研究表明,酒炙和盐炙后补骨脂酚含量较生品下降,而补骨脂素和异补骨脂素含量显著升高,与本研究结果相似。
补骨脂素、异补骨脂素可能既是补骨脂有效成分,补骨脂盐炙后存在增强功效的作用,同时也是其毒性成分。Wang等[15]报道了ig补骨脂素和异补骨脂素(40、80 mg/kg)后,Wistar大鼠体内同种药物同等剂量下雌鼠的肝损伤程度更为严重,且异补骨脂素比补骨脂素的肝毒性更大;补骨脂素和异补骨脂素可抑制大鼠肝脏胆固醇7α-羟化酶(cholesterol 7α-hydroxylase,CYP7A1)、胆酸盐外排泵(bile salt export pump,BSEP)、多药耐药相关蛋白2(multidrug resistance associated protein 2,MRP2)和SULT2A1的表达,增加FXR和MRP3的表达,且大鼠出现多器官毒性,胆汁瘀积性肝损伤较明显。另有报道指出,大剂量异补骨脂素(25、50、100 mmol/L)可使斑马鱼幼鱼肝脏产生大量空泡结构,异补骨脂素通过抑制药物转运蛋白的表达,导致体内异补骨脂素的积累和抗氧化能力的下降,从而导致肝脏损伤[16]。补骨脂酚同样也是补骨脂毒性成分之一,大鼠ig补骨脂酚(52.5、262.5 mg/kg)6周,AST、ALT升高,、羟甲基戊二酸单酰辅酶A(3-hydroxy-3-methylglutaryl-CoA,)、过氧化物酶体增殖物激活受体α(peroxisome proliferator-activated receptor α,)、固醇调节元件结合蛋白-2(sterol regulatory element binding protein-2,)mRNA表达降低,补骨脂酚(52.5 mg/kg)组BSEP表达升高,补骨脂酚(262.5 mg/kg)组BSEP表达降低,补骨脂酚可引起胆汁瘀积性肝毒性,其机制可能与影响肝脏脂质代谢有关[17]。以上提示补骨脂素、异补骨脂素和补骨脂酚可能是补骨脂药效成分同时也可能是其主要毒性成分,而古代人们更注重其药效忽视其毒性。结合本研究结果,发现盐炙后胆汁瘀积性肝损症状更为明显。
临床主要采用盐炙补骨脂水煎液,其主要入血成分是补骨脂素、异补骨脂素、补骨脂苷和异补骨脂苷,其次是补骨脂二氢黄酮及补骨脂二氢黄酮甲醚,而补骨脂苷和异补骨脂苷可通过体内胃肠微环境转化为补骨脂素和异补骨脂素[18-19]。补骨脂中补骨脂酚、补骨脂素、异补骨脂素具有显著的植物雌激素样活性[20]。目前越来越多的证据显示雌激素与胆汁瘀积的发生发展有关[21],雌激素替代治疗骨质疏松易产生肝毒性,胆管炎患者肝脏代谢雌激素水平增高。胆汁酸代谢、肝脏脂质代谢均与雌激素相关,临床女性胆固醇结石的发病率是男性的4倍,雌激素致肝胆疾病越来越引起人们的重视。FSH能够促进卵泡的发育和成熟,并且能促进排卵,它的产生受下丘脑促性腺释放激素的控制,同时受雌激素E2的反馈调控。结果显示,小鼠ig补骨脂后雌激素E2、FSH水平均升高,表明植物雌激素样物质对肝损伤有一定的作用。
IL-6能够调节免疫应答,在机体的抗感染免疫反应中起重要作用。生、盐补骨脂组IL-6升高,其中盐补骨脂高剂量组与生补骨脂组相比,炎症水平更高。FXR通路可以调控人体胆汁酸合成排泄和胆汁酸的正常循环。生补骨脂组和盐补骨脂组肝组织FXR含量均显著下降,且盐补骨脂较生补骨脂下降更为明显。硫酸化反应是雌激素代谢的主要途径,SULT1E1是该反应的关键酶,与对照组比较,盐补骨脂高剂量组肝组织SULT1E1含量明显下降,提示过量雌激素不能及时通过SULT1E1进行灭活,盐补骨脂与生补骨脂具有显著差异。
从中药临床运用特点着手,研究临床不良反应发生的可能机制,从而更有效监测临床用药,是从实践中来,回归于实践中去,本研究表明补骨脂有效成分同时也是毒性成分,且产生肝损伤作用与其含有的植物雌激素样成分有关,而盐补骨脂可能更易引起胆汁瘀积性肝损伤。但本研究缺乏平行考察补骨脂不同炮制方法对成分的影响。目前针对补骨脂的不良反应机制的研究主要集中在单体研究,对单一成分肝毒性较为深入却忽略了补骨脂不同成分之间是否存在相互作用,缺乏整体性,其毒性成分的复杂性、效毒相关性以及与雌激素的深层联系有待进一步研究。
利益冲突 所有作者均声明不存在利益冲突
[1] Cheung W I, Tse M L, Ngan T,.Liver injury associated with the use of(Bol-gol-zhee or Bu-gu-zhi) and its related proprietary medicine [J]., 2009, 47(7): 683-685.
[2] 田文杨, 兰姗, 张力, 等.补骨脂的安全性评价与风险控制措施探讨 [J].中国中药杂志, 2017, 42(21): 4059-4066.
[3] 杨阔, 高茸, 马亚中, 等.补骨脂素药理作用及肝毒性机制的研究进展[J].中草药, 2021, 52(1): 289-298.
[4] 杨莉, 王昭昕, 卢国彦, 等.补骨脂水提药渣大鼠三个月长期毒性试验研究[J].药物评价研究, 2019, 42(6): 1128-1134.
[5] 刘亚蕾, 葛斐林, 朱敬肖, 等.基于被动监测数据和医院病例的一种补骨脂制剂相关肝损伤再评价 [J].中国中药杂志, 2019, 44(19): 4272-4276.
[6] Nam S W, Baek J T, Lee D S,.A case of acute cholestatic hepatitis associated with the seeds of(Boh-gol-zhee) [J]., 2005, 43(6): 589-591.
[7] 蔡涛涛, 黄娜娜, 王亮, 等.补骨脂不同炮制方式对正常小鼠急性毒性实验比较研究 [J].中国药物警戒, 2017, 14(12): 730-736.
[8] 夏亚楠, 余凌英, 王德键, 等.补骨脂不同炮制品对肾阳虚、脾虚大鼠的影响研究 [J].亚太传统医药, 2016, 12(9): 5-7.
[9] 陶益, 蒋妍慧, 李伟东, 等.炮制对补骨脂中12种化学成分含量的影响 [J].中国实验方剂学杂志, 2016, 22(21): 6-9.
[10] Diawara M M, Williams D E, Oganesian A,.Dietary psoralens induce hepatotoxicity in C57 mice [J]., 2000, 9(2): 179-195.
[11] 刘玲, 朱星宇, 陆金兰, 等.盐炙对青娥丸主要成分溶出的影响 [J].中成药, 2018, 40(12): 2714-2718.
[12] 梁灿璨, 吴诗华, 魏羽, 等.补骨脂盐炙前后对肾阳虚大鼠肝肾功能及水通道蛋白表达的影响 [J].中草药, 2017, 48(22): 4713-4718.
[13] 叶斌斌, 敖楠楠, 姜明月, 等.补骨脂酒制工艺的优化 [J].中成药, 2019, 41(1): 182-185.
[14] 李卓柯, 孙婷婷, 刘洋, 等.基于潜在肝毒性成分分析的补骨脂炮制减毒机制[J].中药材, 2021, 44(9): 2091-2094.
[15] Wang Y, Zhang H, Jiang J M,.Hepatotoxicity induced by psoralen and isopsoralen from: Wistar rats are more vulnerable than ICR mice [J]., 2019, 125: 133-140.
[16] Zhang Y, Zhang Y, Li J,.The role of hepatic antioxidant capacity and hepatobiliary transporter in liver injury induced by isopsoralen in zebrafish larvae [J]., 2019, 38(1): 36-44.
[17] Li Z J, Abulizi A, Zhao G L,.Bakuchiol contributes to the hepatotoxicity ofin rats [J]., 2017, 31(8): 1265-1272.
[18] 宋殿荣, 宋红运, 王跃飞, 等.补骨脂水煎液大鼠体内血清药物成分的初步研究 [J].中华中医药杂志, 2010, 25(11): 1863-1865.
[19] Qiao C F, Han Q B, Song J Z,.Quality assessment of[J]., 2006, 54(6): 887-890.
[20] 赵丕文, 牛建昭, 王继峰, 等.6种中药活性成分植物雌激素作用的比较研究 [J].中国药学杂志, 2007, 42(24): 1852-1855.
[21] Liu X, Xue R, Yang C,.Cholestasis-induced bile acid elevates estrogen level via farnesoid X receptor-mediated suppression of the estrogen sulfotransferase SULT1E1 [J]., 2018, 293(33): 12759-12769.
Study of cholestatic liver injury in female ICR mice by decoction ofbefore and after processing
FU Ying-jun1, WU Yu1, 2, MEI Chun-mei2, HUA Zheng-ying2, LI Wei-dong2
1.Department of Pharmacy, Nantong Hospital to Nanjing University of Chinese Medicine, Nantong 226000, China 2.Engineering Center of State Ministry of Education for Standardization of Chinese Medicine Processing, Jiangsu Provincial Key Laboratory of Chinese Medicine Processing, Nanjing University of Chinese Medicine, Nanjing 210023, China
To investigate the difference of cholestatic liver injury in female ICR mice induced by raw and salt processed Buguzhi ().The changes of chemical constituents before and after processing ofwere detected by high performance liquid chromatography.Female ICR mice were continuously given raw and salt processedwater decoction for 30 d, and 24 h after last administration, serum was collected, automatic biochemical analyzer was used to detect liver injury-related indicators alanine aminotransferase (ALT), aspartate aminotransferase (AST), alkaline phosphatase (ALP) activities and total bilirubin (TBIL), direct bilirubin (DBIL), total bile acid (TBA) levels.Liver, spleen and kidney were taken and weighed, organ index was calculated; Hematoxylin-eosin (HE) staining was used for liver histopathological examination; ELISA was used to detect contents of estradiol (E2), follicle-stimulating hormone (FSH), interleukin-6 (IL-6) in serum and farnesoid X receptor (FXR), estrogen sulfate Transferase 1E1 (SULT1E1), E2 in liver.After salt processed, the contents of psoralen, isopsoralen and neobavaisoflavone were decreased, and other eight components contents were increased, among which psoralen, isopsoralen and corylifol A were significantly increased.The genitals of female mice were damaged after ig raw and salt processedwater decoction for 30 d, vaginal mouth of mice was red and swollen with watery infiltration.Compared with control group, ALT, AST, ALP activities and DBIL, TBIL, TBA levels in serum of mice in raw and salt processedgroups were significantly increased (< 0.05, 0.01, 0.001), liver injury of salt processedwas more serious than that of.The contents of FXR and SULT1E1 in liver were significantly decreased (< 0.01, 0.001), and contents of E2, FSH, IL-6 in serum and E2 in liver were significantly increased (< 0.05, 0.01, 0.001).Compared with, IL-6 content in salt processedgroup was significantly increased, and FXR and SULT1E1 contents were decreased more obviously.Psoralen, isopsoralen and Corylifel A may be active components and main toxic components of, salt processedis more likely to cause liver damage than raw.
; salt processed; cholestatic liver injury; estrogen-like effects; psoralen; isopsoralen; corylifel A; psoralen; isopsoralen; neobavaisoflavone
R285.5
A
0253 - 2670(2022)05 - 1434 - 08
10.7501/j.issn.0253-2670.2022.05.018
2021-11-10
国家自然科学基金面上项目(8177390);国家自然科学基金面上项目(81973484);国家重点研发计划(2018YFC1707000);2021年江苏省研究生科研与实践创新计划项目(KYCX21_1754)
符映均,硕士,从事中药学研究。E-mail: woshifyj1987@163.com
通信作者:李伟东,教授,博士生导师,从事中药炮制、中药药效研究。E-mail: liweidong0801@163.com
[责任编辑 李亚楠]
