头孢哌酮舒巴坦治疗下呼吸道感染有效性和安全性的系统评价Δ
2022-02-21李代晓应颖秋翟所迪
李代晓,应颖秋,杨 丽,翟所迪,3
(1.北京大学第三医院药剂科,北京 100191;2.承德医学院附属医院临床药学部,河北 承德 067000;3.北京大学医学部药物评价中心,北京 100191)
下呼吸道感染为临床常见的呼吸系统感染性疾病。在世界范围内,下呼吸道感染与高发病率和死亡率相关[1]。尽管适当的抗菌药物治疗是下呼吸道感染最重要的治疗方法,但随着细菌耐药性变迁及多重耐药菌的出现,治疗下呼吸道感染尤其院内获得性下呼吸道感染的抗菌药物选择压力日益增加。下呼吸道感染的主要致病菌为肠杆菌科细菌、铜绿假单胞菌、不动杆菌、金黄色葡萄球菌、流感嗜血杆菌及肺炎链球菌等[2-4]。其中,肠杆菌科细菌、铜绿假单胞菌及鲍曼不动杆菌为院内获得性下呼吸道感染最常见菌[3]。头孢哌酮舒巴坦为含β-内酰胺酶抑制剂的复方制剂,抗菌谱广,能够覆盖临床分离的最常见的革兰阳性菌、革兰阴性菌,包括肺炎链球菌、金黄色葡萄球菌、流感嗜血杆菌、肠杆菌科细菌、鲍曼不动杆菌和铜绿假单胞菌等。其中舒巴坦为半合成β-内酰胺酶抑制剂,对不动杆菌属有一定活性,能抑制除碳青霉烯酶以外的大部分A类β-内酰胺酶,包括超广谱β-内酰胺酶[5]。2005—2021年中国CHINET细菌耐药监测网数据显示,肠杆菌科细菌对头孢噻肟(或头孢曲松)耐药菌株的检出率居高不下,2021年1—6月肠杆菌科细菌产超广谱β-内酰胺酶菌株的检出率为41.9%[4]。头孢哌酮舒巴坦被广泛应用于下呼吸道感染的治疗,但很少有研究基于循证药学评价其治疗下呼吸道感染的有效性和安全性。因此,本研究对头孢哌酮舒巴坦治疗下呼吸道感染的有效性和安全性进行系统评价,为药物的临床合理应用以及遴选提供证据支持。
1 资料与方法
1.1 纳入与排除标准
纳入标准:(1)研究类型为国内外公开发表的随机对照试验。(2)研究对象为下呼吸道感染患者,性别和年龄不限。(3)干预措施为头孢哌酮舒巴坦,剂量与疗程不限。(4)对照措施为其他抗菌药物单药,剂量与疗程不限。(5)结局指标:有效性结局指标包括临床有效率、细菌清除率,安全性结局指标包括药品不良反应(adverse drug reaction,ADR)发生率。
排除标准:重复发表的文献;数据缺失或错误的文献;基础实验、病例报告和综述等不符合要求的文献;低质量研究。
1.2 检索策略
系统检索PubMed、Embase和the Cochrane Library等英文数据库,中国知网(CNKI)、万方数据库等中文数据库。分别以“头孢哌酮舒巴坦”和“cefoperazone-sulbactam”作为中英文检索词进行全面的文献检索。检索时限均从建库至2021年6月。
1.3 文献筛选与资料提取
由2名研究者独立按纳入与排除标准筛选文献,并交叉核对,如有分歧,则与第3名研究者共同讨论决定最终方案。提取的资料包括第一作者、发表年份、患者例数、年龄、干预措施、疗程、结局指标及偏倚风险评价的相关指标。
1.4 统计学方法
采用Cochrane系统评价员手册5.1[6]推荐的偏倚风险评估工具对纳入研究的质量进行评价,采用RevMan 5.3软件进行荟萃分析(Meta分析)。纳入研究间的异质性采用χ2检验,若各研究间无统计学异质性(P≥0.1,I2≤50%),采用固定效应模型进行分析;反之,则采用随机效应模型进行分析。用倒漏斗图评价发表偏倚。P<0.05为差异有统计学意义。
2 结果
2.1 文献筛选流程与结果
检索得到相关文献6 201篇,剔除重复发表的文献,阅读题目和摘要后进一步阅读全文,最终纳入16篇文献,见图1。

图1 文献筛选流程与结果
2.2 纳入文献的基本特征
最终纳入16篇文献[7-22],共1 347例患者,其中干预组患者665例,对照组患者682例。纳入文献的基本特征见表1。

表1 纳入文献的基本特征
2.3 纳入研究的质量评价结果
纳入的16项研究中,仅2项研究[13,21]提及随机序列的产生方法,其余14项研究提及“随机”;有5项研究[7,10-11,17,22]为随机对照开放试验;所有研究均不清楚是否存在其他偏倚,见图2—3。

图2 纳入研究的偏倚风险图
2.4 Meta分析结果
2.4.1 临床有效率:16项研究[7-22]报告了临床有效率,各研究间异质性较小(P=0.15,I2=27%),选择固定效应模型合并分析。Meta分析结果显示,干预组与对照组患者的临床有效率比较,差异无统计学意义(OR=1.18,95%CI=0.87~1.61,P=0.30>0.05),见图4。同时,以哌拉西林他唑巴坦作为对照药进行亚组分析,共5项研究[7,14,17,21-22],涉及303例患者,Meta分析结果显示,干预组与对照组患者的临床有效率比较,差异无统计学意义(OR=0.80,95%CI=0.39~1.65,P=0.54>0.05,I2=0%),见图5。

图3 纳入研究的偏倚风险详细结果

图4 两组患者临床有效率比较的Meta分析森林图

图5 哌拉西林他唑巴坦亚组中两组患者临床有效率比较的Meta分析森林图
2.4.2 细菌清除率:14项研究[7-18,21-22]报告了细菌清除率,其中干预组分离细菌358株,清除298株,清除率为83.24%;对照组分离细菌365株,清除299株,清除率为81.92%,见表2。各研究间异质性较小(P=0.28,I2=17%),采用固定效应模型进行分析。Meta分析结果显示,干预组与对照组患者细菌清除率比较,差异无统计学意义(OR=1.13,95%CI=0.76~1.68,P=0.56>0.05),见图6。哌拉西林他唑巴坦的亚组分析中,共5项研究[7,14,17,21-22],包含236株菌株,Meta分析结果显示,干预组与对照组患者细菌清除率比较,差异无统计学意义(OR=0.76,95%CI=0.31~1.91,P=0.56>0.05,I2=0%),见图7。

图6 两组患者细菌清除率比较的Meta分析森林图

图7 哌拉西林他唑巴坦亚组中两组患者细菌清除率比较的Meta分析森林图

表2 两组患者细菌分布及细菌清除情况
2.4.3 ADR发生率:13项研究[7,9-12,14-18,20-22]报告了ADR发生情况,均为常见的ADR,如恶心、上腹部不适、轻度腹泻和头晕等,未见严重的ADR发生。其中,干预组患者490例,发生ADR 30例,ADR发生率为6.12%;对照组患者507例,发生ADR 32例,ADR发生率为6.31%。各研究间无异质性(P=1.00,I2=0%),故采用固定效应模型进行分析。Meta分析结果显示,干预组与对照组患者ADR发生率比较,差异无统计学意义(OR=0.97,95%CI=0.58~1.62,P=0.91>0.05),见图8。

图8 两组患者ADR发生率比较的Meta分析森林图
2.4.4 发表偏倚:分别以临床有效率、ADR发生率为指标,以RR为横坐标、SE(log[RR])为纵坐标绘制倒漏斗图,进行发表偏倚分析。结果显示,各研究散点偏左分布,纳入研究可能存在一定的发表偏倚,见图9—10。
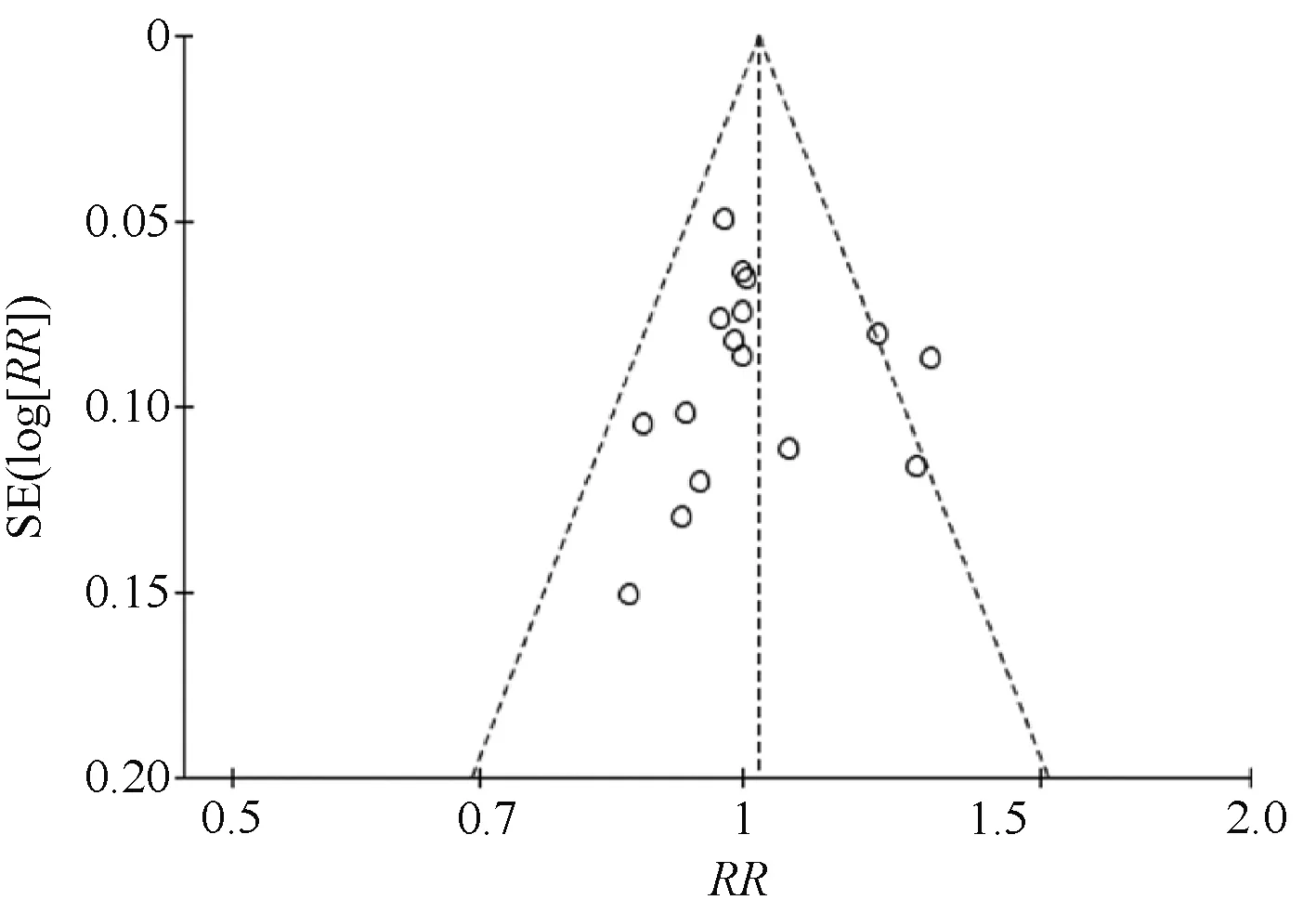
图9 临床有效率的倒漏斗图
3 讨论
3.1 临床疗效
本研究结果表明,头孢哌酮舒巴坦治疗下呼吸道感染的临床有效率、细菌清除率与对照药相当。头孢哌酮舒巴坦与哌拉西林他唑巴坦同为含β-内酰胺酶抑制剂复方制剂,两者抗菌谱类似,对革兰阴性菌具有强大的抗菌活性,对部分革兰阳性菌有一定程度的抗菌活性。两者的不同之处主要包括:(1)哌拉西林对肠球菌有较好的抗菌活性,而肠球菌对头孢哌酮天然耐药。(2)头孢哌酮舒巴坦对不动杆菌有较好的抗菌活性,而哌拉西林他唑巴坦对其作用较弱。(3)药动学方面,哌拉西林他唑巴坦广泛分布在组织和体液中,主要经肾脏排泄清除,对于泌尿系统感染较头孢哌酮舒巴坦更有优势,但肾功能不全患者需要调整剂量;头孢哌酮舒巴坦也能较好地分布到组织体液各处,其中头孢哌酮主要经胆汁排泄,舒巴坦主要经肾脏排泄,对于胆道感染较哌拉西林他唑巴坦更有优势,胆道梗阻患者应注意调整剂量,肾功能不全患者应注意根据舒巴坦调整剂量。(4)哌拉西林他唑巴坦属于青霉素+β-内酰胺酶抑制剂复方制剂,使用前需进行皮试;头孢哌酮舒巴坦属于头孢菌素+β-内酰胺酶抑制剂复方制剂,使用前无需常规皮试,使用更为方便[23]。因此,本研究以哌拉西林他唑巴坦作为主要对标药物进行了亚组分析,结果显示,头孢哌酮舒巴坦与哌拉西林他唑巴坦用于下呼吸道感染的临床有效率和细菌清除率比较,差异均无统计学意义(P>0.05)。Chen等[24]开展的头孢哌酮舒巴坦与哌拉西林他唑巴坦治疗医院获得性肺炎和呼吸机相关性肺炎临床疗效比较的研究中,也得到了类似的结果。根据CHINET中国细菌耐药监测网数据(2021年1—6月),肠杆菌属菌、铜绿假单胞菌和不动杆菌属对头孢哌酮舒巴坦的耐药率分别为17.7%、14.7%和52.7%,对哌拉西林他唑巴坦的耐药率分别为18.3%、13.3%和72.6%[4]。本研究中菌株构成分布也可以看出,分离菌株数排序居前2位的致病菌为肠杆菌科细菌和假单胞菌,依据CHINET监测网数据,上述细菌对头孢哌酮舒巴坦、哌拉西林他唑巴坦的耐药率相近,这一数据也支持本研究得出的临床有效率及细菌清除率相当的结论;尽管不动杆菌对头孢哌酮舒巴坦更为敏感,但本研究结果显示两组患者细菌清除率的差异无统计学意义(P>0.05),可能与分离到的菌株样本量较少有关。

图10 ADR发生率的倒漏斗图
3.2 安全性
本研究结果显示,头孢哌酮舒巴坦的ADR发生率与对照药相当。受原始研究的局限,纳入统计的ADR主要为恶心、上腹部不适、轻度腹泻及头晕等常见的ADR,本次Meta分析未见备受临床关注的头孢哌酮舒巴坦相关凝血功能异常的数据。但在另一项头孢哌酮舒巴坦治疗粒细胞缺乏伴发热的研究中,10%(10/101)的接受头孢哌酮舒巴坦治疗的患者出现凝血酶原时间延长,然而没有观察到与研究药物相关的出血[25]。
3.3 本研究的局限性
首先,纳入的大多数随机对照试验没有开展头孢哌酮舒巴坦体外药敏试验,本研究无法评估细菌对头孢哌酮舒巴坦的耐药率及其对临床结果的影响,因此,依据CHINET中国细菌耐药监测网数据进行了分析讨论;其次,本研究没有进一步对下呼吸道感染进行分类,即社区获得性或医院获得性,未能按发病环境地点区分病原菌分布;另外,部分研究纳入样本量较少,多数研究未详细说明随机方法、随机分配是否隐藏,其中有6项研究属于高偏倚风险,可能会对统计分析结果有一定影响。因此,今后还需开展更多大样本、高质量的临床研究,以期为临床合理用药提供可靠依据。
