空间分辨测量解析三(2,2′-联吡啶)钌(Ⅱ)电化学发光机理的研究进展
2022-02-18胡诗帆王亚锋
胡诗帆,王亚锋,苏 彬
(浙江大学 化学系 分析化学研究所,浙江 杭州 310058)
1 电化学发光概述
电化学发光(ECL)是由电极表面的电子转移反应引发的暗场光辐射[1],可通过电化学反应进行调控,且无需外加激发光,具有时空可控性强、背景信号低和灵敏度高等优点[2-3]。ECL在生物传感、发光器件、核酸检测、免疫分析等研究领域有着广泛的应用[4-5]。以三(2,2′-联吡啶)钌(Ⅱ)(Ru(bpy)2+3)为探针的ECL 是现行免疫分析中最先进的信号转导方法之一。Roche Diagnostics 和Meso Scale Discovery 等公司开发的电化学发光免疫分析仪已被广泛应用于临床诊断中,包括肿瘤标志物、传染性疾病、心血管疾病等多种疾病的早期诊断。
1.1 电化学发光的研究进展
1927 年,Dufford 等[6]在无水乙醚中电解格氏试剂时发现了发光现象。1929 年,Harvey 等[7]用多种不同的金属电极在电解碱性鲁米诺水溶液时,观察到了阴极和阳极区的发光,电化学发光研究的序幕从此拉开。然而,受到仪器设备等限制,电化学发光研究在最初的几十年进展缓慢。直到20世纪60年代,光电倍增管(PMT)和电荷耦合器件(CCD)等高灵敏光电传感器的出现,极大地促进了ECL 的研究发展。60年代中期,Kuwana等[8]用PMT研究了脉冲电压下鲁米诺电化学发光的动力学,并提出了新的发光机理。Hercules和Bard等[9-10]报道了稠环芳烃类化合物在有机溶剂中的ECL。这类有机化合物的电化学发光对溶剂的要求较高,大多不能直接在水溶液中进行反应,因此其应用受到很大的限制。无机金属配合物,如Ru(bpy)2+3等,是目前应用最广泛的ECL探针。1972年,Bard等[11]首次报道了Ru(bpy)2+3在乙腈中的ECL。随后,他们以草酸盐和过硫酸盐作为共反应剂,构建了水溶液中的ECL 体系,拓宽了ECL 的应用范围[12-14]。1987 年,Engstrom 等[15-18]发展了电化学发光成像技术,将电极表面的活性位点和电流密度的分布可视化,研究了电极的边缘效应和电化学发光反应的动力学参数在空间上的变化,为电化学发光反应机理的研究提供了全新的方法。1990 年,Powell 等[19]首次将三正丙胺(TPrA)作为共反应剂用于ECL 中,当发光体和共反应剂均被氧化时,可观察到较强的ECL 信号。同时,该工作还提出了氧化-还原路径,为胺类共反应剂的开发和Ru(bpy)2+3/TPrA 体系在生物、医药、临床等领域的广泛应用奠定了基础。1995年,Wightman等[20]采用快速电位脉冲法研究了超微电极表面单分子的电化学发光,并确定了反应中的速控步骤。21 世纪以来,纳米材料作为新型电化学发光体(如不同结构的量子点:硒化镉、硫化镉、硒化镉/硫化镉/硫化锌[21-22]等)引起了研究者的研究兴趣,也极大地增大了发光分子的选择范围[23]。此外,Xu 等[24]将2-(二丁氨基)乙醇(DBAE)这种毒性低、水溶性好的羟乙基胺类分子作为共反应剂,发现以铂或者金电极作为工作电极时,ECL的强度会显著提高。
1.2 电化学发光反应机理
电化学发光反应机理一般可以分为湮灭型机理和共反应剂型机理[5]。
1.2.1 湮灭型电化学发光 湮灭型电化学发光主要发生在有机溶剂中,并且需要在电极上施加正负双阶跃脉冲电位,电极表面电化学还原和氧化反应产生的高能阴、阳离子自由基A-·和D+·之间发生电子转移反应(其中,A 和D 可以是同种物质也可以是不同物质),形成激发态分子,激发态分子跃迁回基态产生光辐射(图1)。
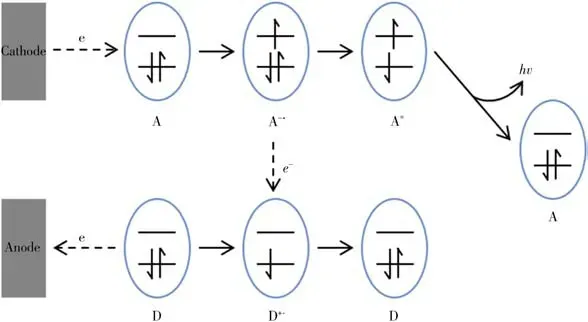
图1 湮灭型电化学发光机理Fig.1 Reaction mechanisms of annihilation ECL



图2 Ru(bpy) 2+3 /TPrA共反应剂型电化学发光的反应机理Fig.2 Reaction mechanisms of coreactant ECL for Ru(bpy) 2+3 /TPrA system
电化学发光反应的过程较为复杂,涉及电极-溶液界面的电荷转移反应、活性中间体的生成与扩散、激发态的生成和辐射复合等,目前对电化学发光反应机理的理解仍不十分清楚。解析电化学发光反应机理对设计新型电化学发光体系,提高发光效率,筛选发光分子和共反应剂,调控发光区域和发展高效免疫分析体系等具有重要意义。
2 电化学发光机理解析
电化学发光是一种表面限域的分析方法,ECL 的发光层限域在电极表面附近,发光层主要由ECL反应过程和反应中间体的寿命所决定[29]。以Ru(bpy)2+3/TPrA体系为例,当Ru(bpy)2+3的浓度较低时,发光层的厚度由TPrA+·的扩散决定,由于TPrA+·不稳定,其扩散距离受限,发光层局域在电极表面附近;而当Ru(bpy)2+3的浓度较高时,电化学发光反应由催化路径主导,发光层的厚度由Ru(bpy)3+3的扩散决定,在一定时间尺度上电化学氧化产生的Ru(bpy)3+3可在溶液中稳定存在,Ru(bpy)3+3的扩散使发光层在空间上延展。因此,改变发光分子或共反应剂的种类和浓度、施加的电位、电位的持续时间等可以改变各路径在ECL 反应中的占比,进而实现对发光层的空间调控。空间分辨测量是一种获得空间分辨信息的有效方法,主要分为横向(平行于电极表面方向)空间分辨测量和纵向(垂直电极表面方向)空间分辨测量。其中,纵向空间分辨测量可以直接对电极表面发光层的厚度等参数进行测量,是研究发光机理最直接和有效的方法之一。目前,扫描电化学显微镜(SECM)和电化学发光显微成像(ECLM)技术是实现电化学发光空间分辨测量的主要方法和工具。
2.1 扫描电化学显微镜(SECM)技术
SECM 是基于电化学反应的微区测量技术[30-31],以超微电极(UME)为工作电极和扫描探针(Tip)[32],具有较高的灵敏度和空间分辨率。Fan 等[33]使用SECM 和超微金属电极研究了电极尖端产生的ECL,得出ECL 强度与电极-基底之间距离的定量关系。同时,实现了对基底表面的成像,空间分辨率达到1 μm。如图3 所示,Miao 等[27]将Ru(bpy)2+3修饰到氧化铟锡(ITO)基底电极表面,以直径为1.5 mm 的半球形金电极作为Tip,研究了Ru(bpy)2+3/TPrA 的ECL 并提出了低氧化电位反应路径。在实验过程中,ITO 电极处于开路状态,发光分子不会在电极表面直接被氧化。在Tip 上施加+ 0.85 V(vs.Ag/AgCl)的氧化电位,溶液中的TPrA 在Tip 表面被氧化为TPrA+·。Tip 沿垂直于基底电极的方向向基底渐近,当Tip 距离基底表面5~6 μm 时,PMT 开始检测到ECL 信号,并且随着距离的进一步减小,ECL强度呈指数型增强。实验结果表明,TPrA+·在水溶液中的最远扩散距离约为6 μm,进一步结合扩散系数计算出TPrA+·的半衰期约为0.2 ms。
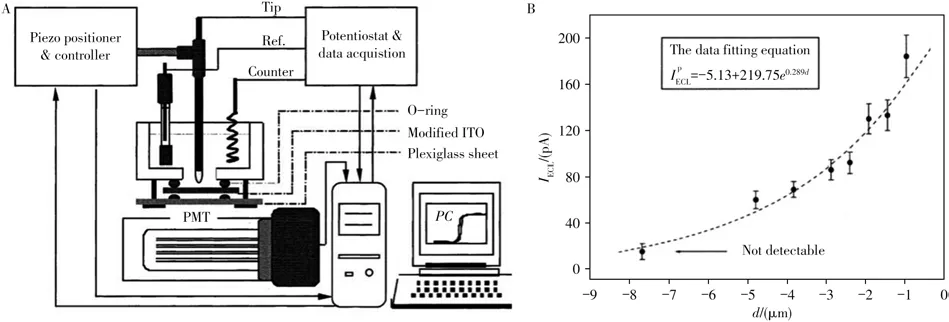
图3 SECM与ECL联用示意图(A),ECL强度随Tip-基底之间距离的变化曲线(B)[27]Fig.3 Experimental setup for studying ECL by SECM(A),dependence of ECL intensity on the distance between Tip and substrate(B)[27]
Bard课题组[34]还运用SECM 研究了湮灭型电化学发光的反应机理,其原理如图4所示。在SECM 探针与基底之间的微小间隙中,电极表面产生的自由基之间发生湮灭反应生成激发态,ECL 的强度与距离相关。以红荧烯和Ru(bpy)2+3作为发光分子,改变探针与基底之间的距离得到一系列ECL 强度-距离曲线,并由这些发光曲线计算出稳态条件下湮灭型电化学发光反应的动力学参数,计算结果与有限元多物理场模拟结果相吻合。

图4 SECM用于研究湮灭型电化学发光机理的示意图(A),及ECL强度-电位曲线随Tip与基底之间距离的变化(B)[34]Fig.4 Schematic illustration of SECM used in annihilation ECL(A),dependence of ECL intensity-potential curve on the distance between Tip and substrate(B)[34]
SECM 在电化学发光反应动力学和机理研究中有着重要的应用,但其空间分辨率很大程度上受到探针尺寸的限制,且超微电极可能会对研究体系有一定的影响。因此,目前电化学发光空间分辨测量主要基于电化学发光成像。
2.2 电化学发光显微成像(ECLM)技术
近年来,随着光学成像仪器灵敏度的逐渐提高,ECL 成像分析发展迅速。ECL 成像需要结合电荷耦合器件或电子倍增电荷耦合器件(EMCCD)实现。CCD 可以将光学信号转换为电流信号,并能将电流信号进行放大和转换,以图像的形式输出,具有响应速度快、分析通量高、成像视野宽的优势[35]。与CCD相比,EMCCD增加了电子寄存器,其检测灵敏度可达到单光子水平,能够显著地提高ECL成像的灵敏度和信噪比。为了提高空间分辨率,ECL 成像通常需要结合显微镜使用,即ECLM[36]。目前,ECLM技术主要应用于免疫分析[37]、酶生物传感[38]、细胞成像[39-40]、核酸分析及指纹成像[41-44]。
Sojic 课题组[45]在亚微米尺寸的光纤阵列表面溅射ITO 层,并在ITO 表面涂覆绝缘材料,仅使锥形尖端暴露。Ru(bpy)2+3与TPrA 在尖端产生的ECL 可以通过光纤传输,并使用CCD 相机对ECL 过程进行成像。阵列电极锥形尖端的直径约为0.6 μm,间距约为4 μm。电极之间的ECL 图像不重叠,尺寸约为1~1.5 μm。计算可得,ECL 发光区域被限制在电极表面约400 nm 的范围内,此即为Ru(bpy)2+*3在电极表面的分布范围。
近年来,ECLM 也被用于研究微球体系的电化学发光机理。Sojic 课题组[46]利用夹心免疫反应将Ru(bpy)2+3固定在直径为12 μm 的聚苯乙烯微球表面,通过俯视和侧视显微成像,研究了微球表面ECL的空间分布。如图5 所示,荧光图像表明Ru(bpy)32+均匀分布于微球表面。因为电子隧穿的距离仅为1~2 nm,所以Ru(bpy)2+3分子在电极表面的直接氧化可以忽略不计。以TPrA 作为共反应剂时,施加+1.1 V的氧化电位,TPrA 在电极表面被氧化为TPrA+·,但由于TPrA+·的扩散距离有限,只在距离电极表面3~4 μm 的范围内观察到明显的ECL 信号。微球顶部的发光信号则来源于微球对底部ECL 信号的物理汇聚,并非源于微球顶部的ECL。以DBAE 作为共反应剂时,在微球表面未检出ECL 信号。这是由于微球体系的ECL 由共反应剂自由基的扩散和分布决定,而DBAE+·的寿命远小于TPrA+·(约为TPrA+·的十分之一),能扩散的距离非常有限,故产生的发光信号无法被检出。因此,虽然Ru(bpy)2+3/DBAE溶液相体系的发光更强且发光效率更高[23],但并不适用于微球免疫分析。该课题组还对Ru(bpy)2+3修饰的微球的不同区域(电极表面附近和远离电极表面的位置)进行成像,证明了共反应剂的氧化是微球体系ECL的关键步骤[47]。除共反应剂外,缓冲溶液也会对微球表面的ECL产生较大的影响。Fiorani等[48]报道了一种通过改变缓冲溶液的浓度调控微球表面发光层厚度的方法。当磷酸缓冲溶液的浓度增大时,缓冲能力增强,起缓冲作用的离子与质子结合的速率增加,使TPrA+·脱质子的速率加快,TPrA+·的最大扩散距离减小,微球表面发光层的厚度减小,发光强度降低。
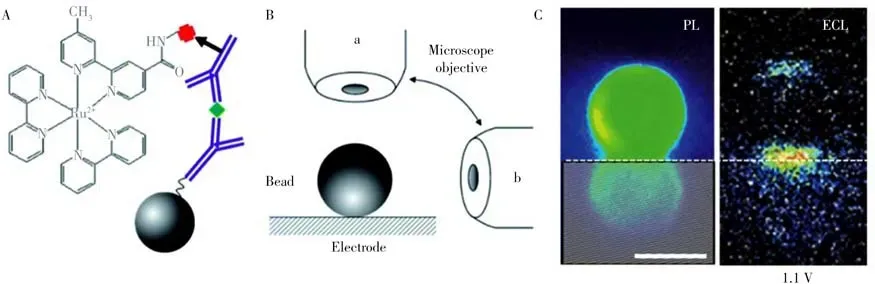
图5 在直径为12 μm的聚苯乙烯微球表面修饰Ru(bpy) 2+3 的示意图(A),俯视(a)和侧视(b)显微成像示意图(B),以及单个聚苯乙烯微球的荧光和ECL图像(C)[46]Fig.5 Schematic illustration of immobilizing Ru(bpy) 2+3 on the surface of polystyrene(PS)bead with a diameter of 12 μm(A),the optical configurations used for imaging the functionalized bead:top-view(a)and side-view(b)(B),and side-view PL and ECL images of single PS bead(C)[46]
Paolucci 课题组[49]结合ECLM、SECM 和质谱等技术,发现了一种能增强ECL 强度的共反应剂中间体。将发光分子在单位时间释放的光子数定义为转化频率(TOF),根据ECL 图像计算不同直径微球的TOF,发现TOF 随微球直径减小而明显增大。此外,将Ru(bpy)2+3修饰在基底上,以TPrA 作为共反应剂,SECM 的探针渐近基底的过程中,同样观察到当探针距离基底表面小于1 μm 时,ECL 强度随距离的进一步减小呈指数型增强,表明电极表面附近存在一种活性更高、不同于TPrA+·的共反应剂中间体。同时,根据ECL 强度与距离的关系曲线计算出电极表面附近和距离电极表面较远处共反应剂中间体的寿命分别为5 μs和700 μs。在ECL过程中,质谱同时检出TPrA+·和二丙胺阳离子自由基(DPrA+·),表明后者是提高电极表面附近ECL 强度的关键。进一步在体系中加入N-二丙基异丁胺(DPIBA),电极表面附近的ECL 强度显著增强。这是因为DPIBA 是一种含有支链的胺类共反应剂,其C—N 键断裂时生成的碳正离子比TPrA 的C—N 键断裂时生成的碳正离子更稳定,所以DPIBA 的C—N 键更容易断裂生成DPrA+·。该工作优化了微球尺寸并在反应体系中加入DPIBA,其ECL强度提高了128%。
Sojic 课题组[50-51]采用ECLM 技术研究了纳米通道内的ECL,并比较了薄层电化学池中共反应剂型和湮灭型电化学发光的特点。纳米通道被固定在SiN壳层中的两个Pt电极之间,长度约为20 μm,高度约为100 nm,其俯视图和截面示意图如图6A、B 所示。将反应体积限制在飞升级,活性中间体在微小体积内的扩散距离很短,能显著增强ECL 的强度。当纳米通道内同时存在Ru(bpy)2+3和TPrA 时,分别在微电极上施加氧化电位和还原电位,TPrA立即被消耗,纳米通道中产生极弱的ECL(图6C);在微电极上只施加氧化电位,无法产生Ru(bpy)+3,仅在纳米通道的两端产生发光(图6D)。而当纳米通道中只有Ru(bpy)2+3时,Ru(bpy)2+3可以在电极之间高效循环,产生均匀的发光(图6E)。作者用电化学发光成像比较了多种反应路径共存时,纳米通道内共反应剂型电化学发光和湮灭型电化学发光的贡献,证明了显微成像技术是解析电化学发光反应机理的重要方法。

图6 纳米流体装置的俯视图(A)和截面示意图(B);纳米通道内湮灭型和共反应剂型电化学发光同时存在(C),纳米通道内只有共反应剂型电化学发光(D),纳米通道内只有湮灭型电化学发光(E)[51]Fig.6 Top-view(A)and schematic cross-sectional(B)images of a nanofluidic device,mixed annihilation and coreactant modes in presence of TPrA(C),coreactant mode(D)and annihilation mode(E)[51]
Guo等[52]采用无电镀金的方法制备了金微米管电极,并通过显微成像技术,研究了Ru(bpy)2+3的浓度以及共反应剂种类对发光层厚度的影响。如图7 所示,以TPrA 作为共反应剂,当Ru(bpy)2+3的浓度由10 μmol/L 增至500 μmol/L 时,ECL 的图像由圆环变为圆斑,对应发光层的厚度由3.1 μm 增至超过4.5 μm。当Ru(bpy)2+3的浓度较高时,催化路径起主导作用,电极表面产生的Ru(bpy)3+3的扩散使发光层在空间延展。而以相同浓度的DBAE 作为共反应剂时,ECL图像的形状不随Ru(bpy)2+3浓度的变化而变化,始终为表面限域的圆环,表明DBAE 自由基不稳定,扩散距离较短。该工作证明了可以通过改变发光分子的浓度或改变共反应剂的种类对电化学发光的空间分布进行调控。Ding 等[53]采用化学沉积法制备了类似的超高密度微孔电极阵列,研究了Ru(bpy)2+3/TPrA 体系在微孔内的ECL 行为。TPrA 自由基在微孔内部径向和轴向扩散的叠加使管壁内侧的ECL 强度最强。当Ru(bpy)2+3浓度较低时,单个微孔中ECL的图像为环形,且形状不随曝光时间的延长而改变。
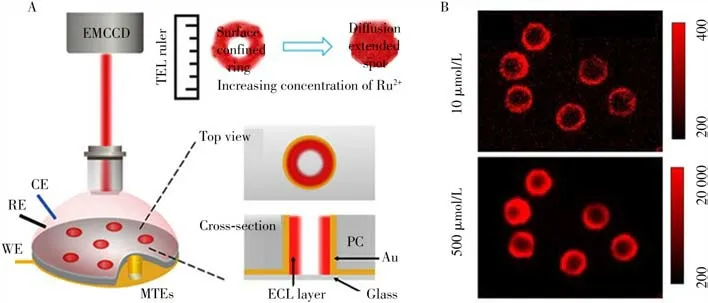
图7 通过微米管电极测量发光层厚度的原理示意图(A)及不同Ru(bpy) 23 +浓度下的ECL图像(B)[521]Fig.7 Illustration of measuring the thickness of ECL layer through microtube electrodes(A),and ECL images recorded in 0.01 mol/L phosphate buffer(pH 7.4)containing 25 mmol/L TPrA and 10 μmol/L/500 μmol/L Ru(bpy)23 +(B)[52]
改变共反应剂的浓度,同样可以实现对发光层厚度的调控。Ding 等[54]在ITO 电极表面制备了惰性半球形光胶点阵列,其直径约为20 μm,高度约为5.1 μm。当在电极上施加适当的氧化电位时,未被光胶点覆盖的电极表面将产生ECL 信号,而光胶点覆盖的位置则不发生ECL 反应,对应于ECL图像中的黑色圆形(图8A)。如图8B-E所示,Ru(bpy)2+3的浓度为500 μmol/L,当TPrA的浓度由20 mmol/L 减小到2.5 mmol/L 时,黑色圆形的面积明显变小,同时圆心的ECL 强度增强,表明随着TPrA 浓度的降低,发光层从电极表面限域扩展至远离电极表面处(几微米)。当Ru(bpy)2+3的浓度较高且TPrA 的浓度较低时,电极表面氧化产生的Ru(bpy)3+3能够向本体溶液中扩散较远的距离,并通过催化路径发光,此时发光层厚度较大;而当提高TPrA 的浓度时,Ru(bpy)3+3与TPrA 的反应速率增加,Ru(bpy)3+3在扩散过程中被大量消耗,其扩散距离变短,相应的发光层厚度也变小(图8F)。

图8 发光层厚度变化对ECL图像中光胶点阵列面积的影响示意图(A);在500 μmol/L Ru(bpy) 2+3 和20 mmol/L(B)、5 mmol/L(C)、2.5 mmol/L(D)TPrA中,光胶点阵列的ECL图像(比例尺为20 μm);在不同TPrA浓度下单个光胶点的归一化ECL强度曲线(E);以及在高、低TPrA浓度下发光层的分布示意图(F)[54]Fig.8 Schematic illustration of modulating the thickness of ECL layer to image an inert photoresist spot(A),ECL images of photoresist spots in phosphate buffer saline containing 500 μmol/L Ru(bpy) 2+3 and different concentrations of TPrA(B:20 mmol/L;C:5 mmol/L;D:2.5 mmol/L,the scale bars are 20 μm),normalized ECL intensity profiles along a single photoresist spot at different concentrations of TPrA(E),and illustration of the thickness of ECL layer at a high and low concentration of TPrA(F)[54]
电化学发光成像可以将激发态分子的分布可视化,在电化学发光机理研究中有着重要的应用。但受到光学衍射极限(~200 nm)的限制,成像的空间分辨率仍为亚微米级,在测量发光层厚度时还存在一定的局限性。
2.3 电化学发光自干涉光谱(ECLIS)
薄膜光学干涉指的是从薄膜的不同界面处反射的两束或多束相干光发生叠加的现象,是一种非入侵式、无需标记、超灵敏的测量方法。薄膜的折射率或厚度的微小变化均会引起干涉光谱形状的变化和光谱峰位置的移动。因此,薄膜光学干涉在痕量检测、分子识别和免疫分析等领域有重要应用[55]。Wang 等[56]将电化学发光和薄膜光学干涉相结合,发展了电化学发光自干涉光谱(ECLIS),将电化学发光空间分辨测量的纵向空间分辨率提高至纳米水平。如图9A 所示,以二氧化硅/硅片作为基底,溅射厚度约为4 nm 的钛黏附层和10 nm 的超薄金层,以此作为工作电极。在ECL 过程中,电极表面附近的发光分子直接发射的光和从电极界面反射的光之间发生干涉,得到含一系列有序排列的干涉峰的干涉光谱。结合双光束干涉模型和传输矩阵模型,对光谱进行模拟解析,即可计算得到发光分子与电极表面的距离或发光层的厚度。将Ru(bpy)2+3分别用3-巯基丙酸或含50 个碱基对的双链DNA 分子固定在电极表面,测得Ru(bpy)2+3与电极表面的垂直距离分别为1.5 nm 和8.7 nm,证明了电化学发光自干涉光谱具有纳米水平的纵向空间分辨率。对于溶液相的Ru(bpy)2+3/TPrA体系,当Ru(bpy)2+3的浓度由1 μmol/L增至1 mmol/L时,干涉峰发生明显的红移和展宽,测得发光层厚度由350 nm 增加至950 nm(图9B)。ECLIS具有较高的纵向空间分辨率,为电化学发光机理的研究提供了新思路。
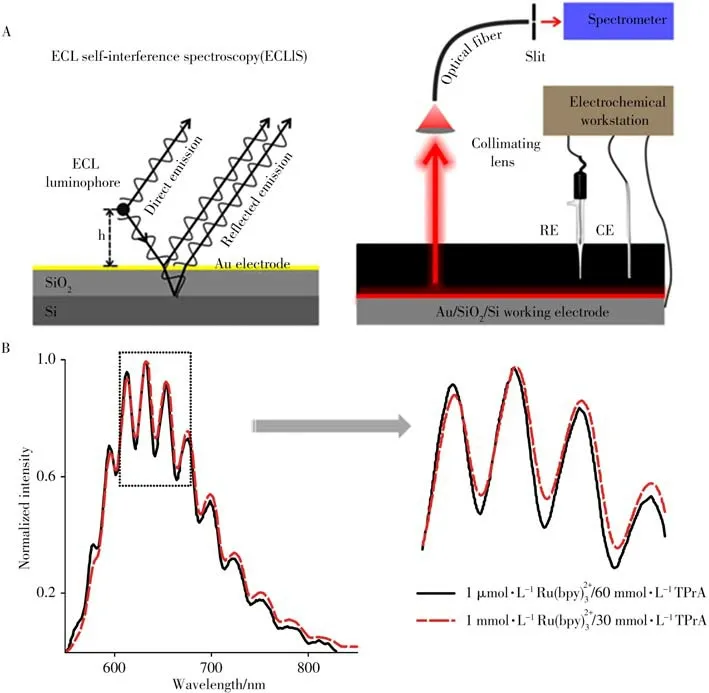
图9 电化学发光自干涉光谱的原理(左)及实验装置(右)示意图(A),以Au/SiO2/Si 电极作为工作电极,施加电位为1.2 V,在1 μmol/L Ru(bpy) 23 +/60 mmol/L TPrA(黑线)和1mmol/L Ru(bpy) 23 +/30 mmol/L TPrA(红线)(0.2 mol/L磷酸盐缓冲液,pH 7.4)中测得的归一化ECL自干涉光谱(B)[56]Fig.9 Schematic illustration of principle(left)and experimental setup(right)for ECL self-interference spectroscopy(A),normalized ECL self-interference spectra obtained using a Au/SiO2/Si electrode in phosphate buffer(0.2 mol/L,pH 7.4)containing 1 μmol/L Ru(bpy) 23 +/60 mmol/L TPrA(black curve)and 1 mmol/L Ru(bpy) 23 +/30 mmol/L TPrA(red curve)at applied potential of 1.2 V(B)[56]
3 总结与展望
ECL具有背景信号低、时空可控性强和灵敏度高的优势。Ru(bpy)2+3作为最经典的ECL发光体,基于其的ECL 体系已在生化分析、生物成像、临床诊断等领域得到广泛应用。虽然对Ru(bpy)2+3体系发光机理的研究已持续了很多年,湮灭型ECL 和共反应剂型ECL 路径也已提出很多年,但目前仍未在实验上得到直接证明,对Ru(bpy)2+3体系发光机理的理解仍不十分清楚,尤其是共反应剂型ECL,涉及的反应过程较为复杂,反应中间体的寿命较短,对不同条件下的反应机理尚无明确定论。目前常用的电化学发光分析方法测量的大多为电极表面的整体平均信息(如发光强度),缺少空间分辨信息,无法准确揭示反应机理。而空间分辨测量能够直接得到电极表面附近Ru(bpy)2+*3或者共反应剂自由基的分布,是最简单、高效的解析发光机理的方法之一。目前,而空间分辨测量主要基于SECM 和ECLM,但SECM使用的探针可能会干扰初始的ECL体系,使测量的结果偏离真实值;而ECLM则受限于光学衍射极限,分辨率仍停留在亚微米水平。ECLIS 是一种灵敏度更高的分析方法,具有纳米级的纵向空间分辨率,有望实现发光层厚度的准确测量,进而解析发光机理。此外,将ECL 与质谱、电子自旋共振技术结合,有望实现对反应中间体的直接测量,进而解析发光机理。
ECL 是目前生化分析中最先进的检测技术之一,而对Ru(bpy)2+3/TPrA 这一经典体系机理的解析也是目前最为重要的研究方向之一。阐明ECL 的机理,除了可提高其分析检测性能外,对设计高效的发光分子、筛选合适的共反应剂、调控发光层厚度和设计新型电化学发光传感器也具有指导性意义,亦有助于拓宽其在生物传感、发光器件、核酸检测、免疫分析、环境监测等研究领域的应用范围。
