基于光热发电的热化学储热体系研究现状与展望
2022-02-16周玥周子健曹田田刘磊彭德骏刘小伟徐明厚
周玥,周子健,曹田田,刘磊,彭德骏,刘小伟,徐明厚
(1.华中科技大学 能源与动力工程学院,湖北 武汉,430074;2.中国石化石油化工科学研究院,北京,100083)
化石能源的广泛使用会引起化石燃料资源匮乏和环境污染等问题,寻找清洁环保的可再生能源是有效的解决方案之一[1]。其中,太阳能资源具有能量总量大、分布广泛、安全可靠、无附加环境污染等显著优势,因而受到广泛关注。利用太阳能发电可以缓解我国长久以来对化石能源的依赖,改善以化石能源为主的能源消费结构[2]。当前太阳能发电技术主要分为光伏发电和光热发电。光伏发电利用光生伏特效应直接将太阳辐射能转化为电能。近年来,光伏发电的成本不断降低[3-4],已率先实现大规模的商业化,但是其仍存在间歇性与稳定性的问题。光热发电利用太阳辐射使介质升温,将辐射能转化为热能;在需要时将热能释放并转化为电能。然而,光热发电受制于发电成本[5]和技术限制,未能实现与其供能潜力相匹配的商业应用[6]。光热发电配备理论上全天候运行的储热系统,供电能力稳定,可以解决太阳能光伏发电的间歇性、不稳定性和难以昼夜持续供应的缺陷[7]。虽然光热发电起步较晚,截止到2020年8月,我国光热发电装机容量仍达到500 万kW[8]。2022 年,国家发展改革委、国家能源局印发的《“十四五”新型储能发展实施方案》中明确指出,到2030 年新型储能实现全面市场化发展[9-10],这将为配备储能系统的光热发电带来重大的发展契机。
1 光热发电储热体系分类
高效、安全的储热体系是光热发电技术大规模应用的关键。基于储热介质及其工作原理的不同,可将主流的储热体系划分为显热、潜热以及热化学储热3种[11-13]。表1 所示为不同储热体系的特点[14-16]。

表1 储热体系的特点与比较[14-16]Table 1 Characteristics and comparison of energy storage systems[14-16]
1) 显热储热利用储热介质自身温度的变化实现热能的存储和释放,存储的热量可通过式(1)计算。常用的储热介质包括混凝土、导热油、熔盐和水泥等[12]。显热储热是目前发展最成熟的储热技术,已实现商业应用,但其质量储热密度较低,一般为0.02~0.03 kW·h·kg-1。
2) 潜热储热又称相变储热,储热介质通过可逆相变吸收和释放热量,热量可通过式(2)计算。常用的储热介质包括熔盐类、合金类与有机类物质(如石蜡)等[13],其质量储热密度通常比显热储热的高,一般为0.05~0.10 kW·h·kg-1。
3) 热化学储热利用可逆化学反应的吸热和放热,热量可通过式(3)计算,而适用于热化学储热的商业应用储热介质尚在开发中。
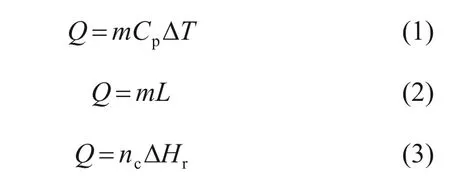
式中:Q为热量;m为储热介质的质量,kg;Cp为储热介质的比热容,kJ·kg-1·K-1;ΔT为储热过程 的温度变化,K;L为单位质量储热介质的相变 潜热,kJ/kg;ΔHr为可逆化学反应的反应焓,kJ/mol;nc为储热介质的物质的量,mol。
在光热发电领域,相较于显热储热和潜热储热,热化学储热具有以下优势:
1) 显热储热和潜热储热系统主要配备蒸汽朗肯循环,而热化学储热系统则是配备超临界 CO2(sCO2)布雷顿循环。sCO2布雷顿循环的工作温度范围更高(>700 ℃),使太阳能光热发电效率提高8%,发电成本也大幅下降[17-18]。此外,sCO2密度大、黏性小、传热效率高、可压缩性好,系统体积小。
2) 热化学储热的储热密度高,是显热和潜热储热的数倍到数十倍,且热化学储热介质所占空间体积小。常见热化学储热介质的储热密度和反应温度如表2所示[16,19-23]。
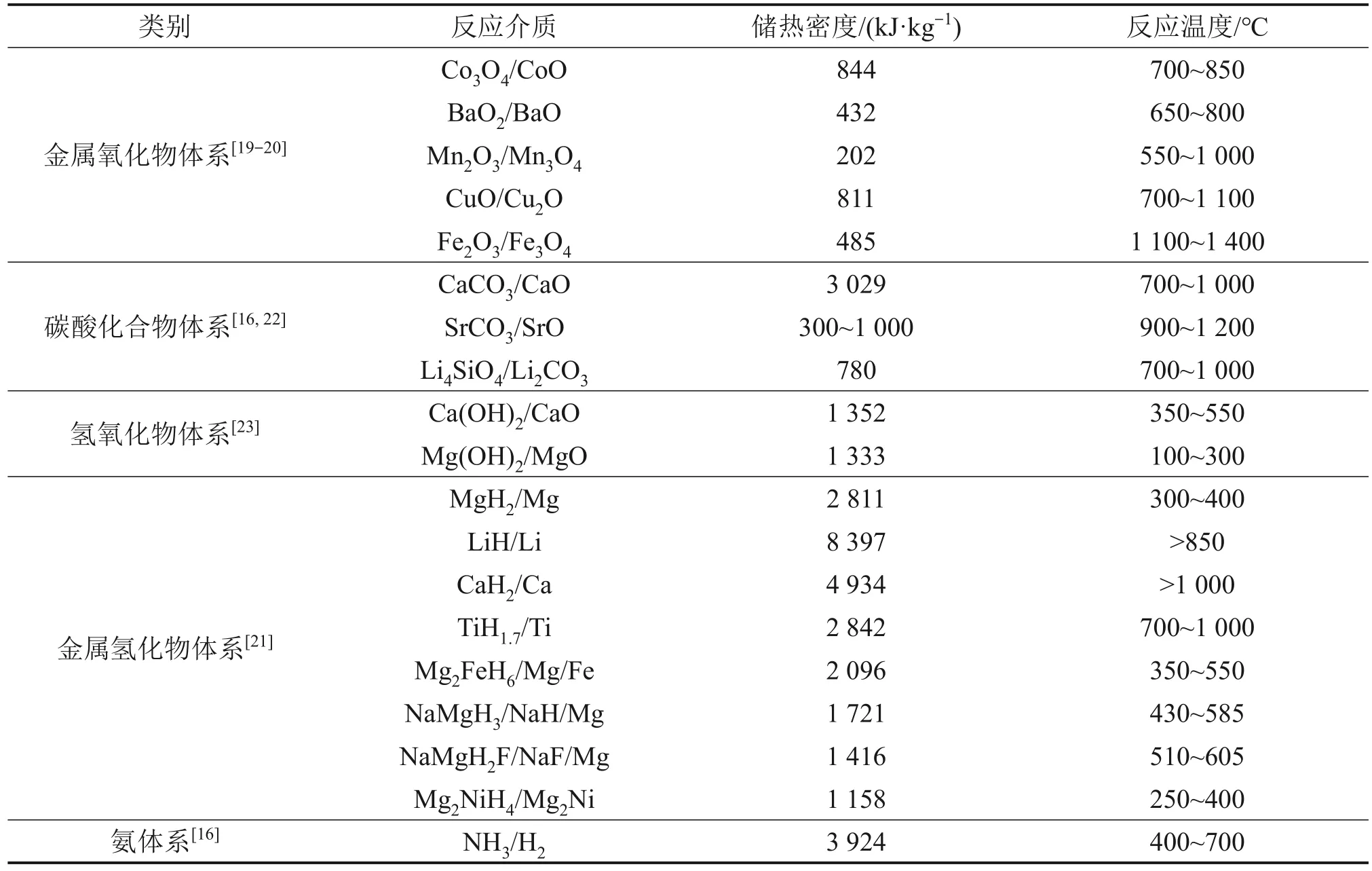
表2 常见热化学储热材料的储热密度和反应温度比较[16,19-23]Table 2 Comparison of energy storage density and reaction temperature of common thermochemical energy storage materials[16,19-23]
3) 热化学储热介质的热能存储可以在环境温度下进行,热损失较小,理论上可以实现长距离运输和跨季节储存[18]。
基于上述特点,热化学储热为光-电高效转化提供了一种可能性,有助于实现太阳能全天候供能发电,同时满足调峰电厂的用电需求。因此,本文综述了不同热化学储热体系(包括储热介质、反应器等)的最新研究进展,为热化学储热未来的发展趋势提供参考。
2 主流的热化学储热体系
基于光热发电的热化学储热介质需要满足以下条件[24-26]:
1) 化学反应完全可逆,热稳定性良好;
2) 无不良副反应和副产物;
3) 高储热/放热反应速率;
4) 在太阳能集热器可达到的温度区间内反应,吸热反应一般在低于1 000 ℃的温度下进行,放热反应一般在高于500 ℃的温度下进行;
5) 反应焓、储热密度大;
6) 成本低、无毒性、无腐蚀性。
目前,适用于热化学储热的材料体系主要可分为金属氧化物体系、碳酸化合物体系、氢氧化物体系、金属氢化物体系和氨体系等。
2.1 金属氧化物体系

式中:MOx+2y为高价态金属氧化物;MOx为还原后金属氧化物。
在众多金属氧化物储热材料中,Co3O4/CoO具有高储热密度(约为844 kJ/kg)、高循环稳定性和良好的反应动力学特性[38-39]。其储放热反应的升温和降温速率会对CoO 的氧化反应造成较大影响,并且氧化反应的速率低于还原反应的速率[40]。高温烧结带来的比表面积降低是影响Co3O4/CoO循环稳定性和再氧化速率的一大因素。AGRAFIOTIS等[41-43]研究了Co3O4/CoO成型材料的热化学储热性能,制备了附着Co3O4涂层的SiC 蜂窝陶瓷和泡沫,并进一步制备了具有多孔泡沫状结构和大密度球状结构的纯Co3O4材料(图1)。研究发现,负载型的Co3O4在100 次循环后仍保持较好的氧化还原性能,宏观的骨架结构没有出现破碎、变形和涂层脱落。而纯Co3O4多孔泡沫在30 个循环后也保持良好的抗烧结性能和结构稳定性。因为不具备“开放”的气体扩散通道,Co3O4球状结构在几个循环后就出现了外观的破坏。保持Co3O4结构的疏松多孔可以有效缓解其烧结,蓬松的结构使Co3O4颗粒之间具有足够大的空隙,因此能够有效地容纳因为热应力和化学诱导带来的体积膨胀。

图1 具有不同外观的储热介质Co3O4[41-43]Fig.1 Energy storage media Co3O4 with different appearances[41-43]
Co3O4微观形貌调控是增强其抗烧结性能的手段之一。LIU等[44]对微纳米尺度的钴基材料进行了形态学修饰,制备了具有立方体微观结构的Co3O4。在30 次循环后,立方体结构的Co3O4的氧化速率约为商业Co3O4的1.5 倍,并且立方体结构的Co3O4在循环后仍能维持立方体微观形貌。虽然Co3O4/CoO 具有优异的性能,也在100 kW 中试级别的实验台架进行了公斤级的试验。但是,钴的地球丰度在2×10-5~3×10-5之间,是一种昂贵稀有的元素,此外钴具有毒性、容易致癌并对环境造成破坏,将会严重限制其大规模应用。
CuO/Cu2O 是具有大规模应用潜力的储热介质,其储热密度与Co3O4/CoO体系相当,而且材料无毒,价格低廉。但是CuO 的还原温度(1 120 ℃)接近它的烧结温度(1 232 ℃)[8],因此它的烧结现象非常严重。研究表明,通过旋转式太阳能反应器快速混合搅拌颗粒可以提高样品的反应活性,并且抑制CuO 的烧结。BaO2/BaO 是一种新兴的金属氧化物储热体系,其储热密度适中,来源丰富,毒性低,且商用BaO2/BaO 具有良好的可逆性、稳定的氧化还原速率;掺杂金属氧化物对BaO2/BaO氧化还原性能的提升较小[45],但温度、压力以及气氛对BaO2/BaO 的储热性能影响较大,因此,可通过改变反应条件来调控其性能[40]。Mn2O3/Mn3O4也被认为是一种具有潜力的储热体系,但该体系的反应动力学速率十分缓慢,对Mn2O3/Mn3O4掺杂第二金属元素可以有效提高它的性能。CARRILLO等[35]研究发现,将20%的Fe 掺杂到Mn2O3中,可以显著提高材料的氧化速率、缓解烧结程度、提高循环稳定性、减少热滞。Fe2O3/Fe3O4体系来源广泛、成本低廉、对环境危害小。但是,Fe2O3/Fe3O4体系的运行温度高达1 300 ℃且氧化还原反应不能实现完全可逆。对Fe 掺杂其他金属元素形成复合金属氧化物(如Cu、Co),能够获得成本低廉、操作温区适宜和储热密度适中的热化学储热材料[46]。
除了单体金属氧化物和复合金属氧化物外,钙钛矿也被认为具备较好的储热潜力[47-48]。钙钛矿的化学表达式为ABO3,具有稳定的立方八面体结构,在高温下具有很强的氧离子传输特性和还原性,在还原过程中释放氧原子产生氧空位,其热化学储热的反应方程式见式(5)。钙钛矿的氧化还原反应是连续的,会在一定的温度区间内出现持续的氧释放/吸收,从而增加系统的操作灵活性[49-50]。
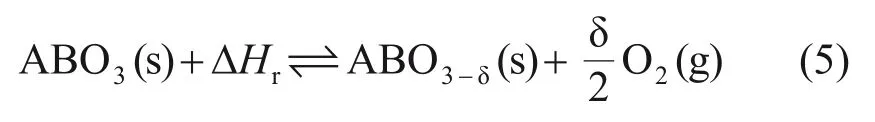
式中:ABO3为未反应的钙钛矿;ABO3-δ为还原后的钙钛矿。
在众多A 位元素(一般为碱(土)金属或La 系元素)和B位元素(一般为过渡金属元素)组成的钙钛矿中,锰酸钙(CaMnO3)的研究最广泛[51-52]。但是,相比其他化学计量的金属氧化物体系,钙钛矿的储热密度没有明显优势,且被还原的钙钛矿易再次被氧化,须将其储存在低氧分压的气氛下。表3所示为不同种类钙钛矿氧化还原的反应焓与特点[50,53-56]。从表3 可见:通过简单地选取不同A位、B位金属并掺杂少量其他元素可以调节钙钛矿的热力学特性。不同元素、不同掺杂比例的钙钛矿之间的氧化还原能力和反应动力学差别巨大,这一特性为提高其热化学储热能力提供了调控方向。因此,寻找由无毒、安全、廉价的元素构成的,且具备高效热化学储热性能的钙钛矿是当前的研究热点。

表3 不同钙钛矿的储热特性比较[50,53-56]Table 3 Comparison of energy storage properties of different perovskites[50,53-56]
2.2 碳酸化合物体系
碳酸化合物体系利用材料的煅烧分解和碳酸化进行储热/释热,反应机理可见式(6)。反应涉及到的CO2需要被压缩存储,给反应体系带来能耗高的问题。KYAW等[57]提出2种存储CO2的方法,第一种是利用CO2吸附剂(如沸石、有机胺类)储存气体,第二种是利用更低工作温度的金属氧化物的碳酸化储存CO2。根据目前的研究,可用于碳酸化合物体系的材料有CaCO3/CaO、PbCO3/PdO、BaCO3/BaO和SrCO3/SrO等。

式中:MCO3为碳酸盐化合物;MO 为煅烧后的氧化物。
学术界针对CaCO3/CaO 体系用于燃烧后CO2捕集进行了广泛地探索,开发出适用于从工业尾气中捕集CO2的钙循环技术[58]。CaCO3/CaO体系在热化学储热利用中是在大于850 ℃、近100% CO2分压下实现的碳酸化,小于800 ℃、低CO2分压下的煅烧分解[59]。CaCO3在高温运行下非常容易烧结。这是由于CO2与外层CaO 反应生成的CaCO3晶粒粗化、团聚,堵塞内部新鲜的、未反应的CaO孔隙,阻止CO2的进一步扩散。适量添加改性材料(如Al2O3、TiO2、SiO2、石墨纳米薄片)或采用有机前驱体制备多孔材料等是有效的抗烧结方法[60]。此外,纯CaCO3粉末的光谱吸收率很差,这会阻碍它在容积式集热器中的应用。研究表明,对白色的CaCO3粉末添加黑色元素可以提高它的吸光能力,从而有效降低聚光倍数,减少光热电站镜场投资(图2)[61-62]。

图2 掺杂Mn、Fe的CaO基复合材料与纯CaO光谱吸收率的对比[62]Fig.2 Comparison of spectral absorbance of CaO-based composites doped with Mn and Fe and pure CaO[62]
粉末状的钙基材料进行循环储热会导致细粉被气流裹挟带出系统,造成原料浪费、粉尘污染,系统内的钙基粉末也会堵塞管道,因此对CaCO3/CaO成型造粒非常有必要。挤压-滚圆法、石墨床铸造法都是可行的方法。其中,挤压-滚圆法制备的颗粒机械强度高,粒径分布特征可控,具有很好的工业应用前景。而石墨床铸造法利用石墨的疏水性、前驱体液滴的表面张力以及液滴自身的重力,可以通过简易的方法获得球形度良好的钙基储热颗粒,并且保留了颗粒的孔隙结构。
SrCO3/SrO 体系的操作温度高达1 000 ℃,使其逐渐被作为热化学储热介质而研究。SrO与CO2反应过程中产生的高温热能是其他碳酸化合物储热体系所不具备的。与传统的气/固反应相同,高温烧结也是SrCO3/SrO体系的一个主要缺点,添加抗烧结剂同样可以有效提高SrCO3/SrO在循环过程中的稳定性[63-64]。PbCO3也是热化学储热的候选介质之一,但是Pb 具有毒性且它的储热能力低于CaCO3,因此,不建议PbCO3/PdO体系用于实际的储热[65]。BaCO3/BaO体系的煅烧温度高达1 400 ℃,会导致高温烧结和BaCO3/BaO 的共晶熔化,因此该体系也不适用于热化学储热[66]。
Li4SiO4与CO2反应生成Li2CO3和Li2SiO3是一个放热的过程,当体系的操作温度为700 ℃时,反应焓高达780 kJ/kg,因此该反应体系也被认为具备热化学储能的潜力。研究发现,Li4SiO4在400~900 ℃下进行了5次循环,呈现出足够的循环持久度[67]。但是Li 元素的储量较小,导致该反应体系的成本较高。此外,Li4SiO4的反应动力学速率缓慢,距离实际工业应用仍有差距。
2.3 氢氧化物体系
氢氧化物体系通过氢氧化物的脱水和水合反应来进行能量的存储和释放,反应方程式见式(7)。可用于热化学储热的氢氧化物有Ca(OH)2、Mg(OH)2、Ba(OH)2、Sr(OH)2等。其中,Ca(OH)2/CaO 的综合性能最为优异,受到的关注较多[68]。
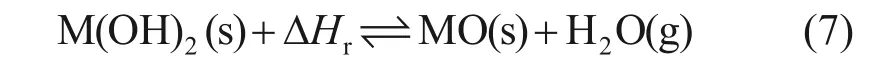
式中:M(OH)2为未反应的氢氧化物。
Ca(OH)2/CaO 体系的反应焓高达104 kJ/mol,循环稳定性好、反应动力学快、材料价格低,并且具备较高的储热密度(1 352 kJ/kg)。与其他高温热化学储热材料的工作温度相比,Ca(OH)2/CaO体系在350~550 ℃的中等温度区间工作,槽式抛物面聚光装置的工作条件可以满足该体系的正常运行[69]。Ca(OH)2/CaO的一个显著缺陷是材料在循环过程中的体积变化较大,易造成颗粒破碎[70],而实际电厂中储热介质的储罐是有限的。因此,提高其机械强度是未来的研究重点。CRIADO等[23]制备了一种壳核结构的Ca(OH)2/CaO 储热材料,CaO为核,CaSiO3为壳,在200次循环后具备很高的机械强度。添加黏结剂如高岭土、富铝水泥、黏土等也可以提高Ca(OH)2/CaO 材料的机械强度[71]。此外,粉末状的Ca(OH)2/CaO材料在循环过程中会发生细小颗粒的结块和团聚,造成导热率下降。XU等[72]发现加入SiO2颗粒可以有效抑制 Ca(OH)2/CaO材料的结块和团聚。
SCHAUBE等[73]模拟研究发现,Ca(OH)2/CaO体系在固定床反应器中采用直接传热方式具有更大的优势,直接传热是通过气态反应物与额外的惰性气体共同流过固体进行反应。他们进一步研究验证了Ca(OH)2/CaO体系在固定床反应器中的稳定性,样品在25 次循环中的转化率和反应速率保持稳定,颗粒反应速率为该体系的主要限制因素[74-75]。然而,在固定床反应器中大规模地使用Ca(OH)2/CaO会导致材料出现严重烧结,限制系统的传热传质性能。ANGERER等[76]采用一种鼓泡流化床反应器,在100 m3的反应器体积内可产生 15 MW的功率,反应器设计如图3所示。
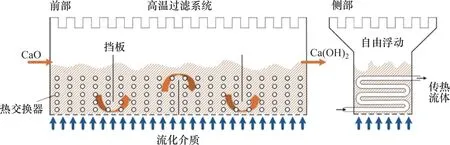
图3 用于Ca(OH)2/CaO储热体系的连续MW级流化床反应器[76]Fig.3 Continuous MW-scale fluidized bed reactor for Ca(OH)2/CaO energy storage system[76]
为了改善材料的流化,PARDO等[77]将Ca(OH)2粉末和Al2O3颗粒按照7∶3 的质量比加入流化床中运行了50 次脱水/水合循环。掺入Al2O3会降低材料的储热密度,所以需要在每个步骤后分离、回收惰性的Al2O3。由于Ca(OH)2材料的低导热性,在固定床中运行需要巨大的存储空间以配备大型热交换器,这将增加运营成本。此外,SCHMIDT等[78]设计和开发了一个采用壳管式换热器的移动床试验装置,在该反应器中Ca(OH)2和Al2O3的混合反应材料在10 次循环中表现出高稳定性,该试验装置已投入运行。
2.4 金属氢化物体系
金属氢化物体系利用某些金属或者合金可以和氢气反应,生成金属氢化物并放出热量,反应方程式见式(8)。金属氢化物体系的突出优势在于它的高储热密度,兼备良好的可逆性和循环稳定性,适用于热能的短期和长期储存。该体系包含的材料种类较多(如CaH2、MgH2、LiH、NaMgH3、Mg2FeH6等)[79],主要的金属氢化物体系的反应温度和储热密度见表2。

式中:MH为未反应的氢化物;M为氢化物反应后的金属或合金。
金属氢化物的工作温度跨度很大,可分为低温储热材料(25~100 ℃)、中温储热材料(100~500 ℃)和高温储热材料(>500 ℃)。
1) 低温金属氢化物以金属间化合物合金为主,具有较快的氢吸收和释放动力学速率,被广泛用于氢压缩、镍氢电池以及室温热能储存。
2) 中温金属氢化物中MgH2的研究最为广泛,它的反应温度为250~500 ℃,储热密度高达 2 811 kJ/kg 且反应也具备良好的可逆性。但是MgH2的反应动力学较缓慢,放热反应比吸热反应更难进行,研究发现可以通过提高反应温度或添加催化剂(如Ni、膨胀石墨、NbF5)来提升反应速率[80]。MISTRY等[81]研究了微米级的雾化MgH2粉末的高温循环,在粉末表面施加了磁控溅射催化剂(Cr,Fe,V 和不锈钢),发现催化涂层可以显著缩短孵化期,催化剂的反应动力学和反应容量能够有效提高,并且稳定地保持了90 次循环。过度晶粒生长和烧结也是MgH2长期循环中存在的问题,纯MgH2的储氢能力在500次循环后下降75%,但是可以通过掺杂第二元素来改善材料的循环稳定性。研究表明添加Ni 或Fe(形成Mg2NiH4或Mg2FeH6)可以保持500次循环的稳定性[82]。其余金属与Mg 的氢化物合金也被用于研究热化学储热,其中部分合金氢化物(如NaMgH3,Mg2FeH6)与MgH2相比适用于更高的工作温区,但是储热密度则有所降低。在氢化物的阴离子中掺入F元素也可以对Mg的氢化物合金起到改性作用,NaMgH2F的工作温度比MgH2的提升了约100 ℃,而且该材料的成本也有所下降。
3) 对于新一代的光热电站来说,必须开发工作温度高于600 ℃的新型氢化物材料来满足电站对热效率提升的要求[83]。TiH1.7、LiH 和CaH2均是具有良好储热效果的高温金属氢化物。其中,LiH的储热密度最高(达8 397 kJ/kg),但是Li在地壳中的含量较低。电池行业对该元素也存在日益增多的需求,这使得LiH体系在大规模的热化学储热中缺乏经济性。相比之下,TiH1.7和CaH2则更具研究前景,尤其是CaH2材料具有丰富的钙基来源并已经通过了公斤级的储热试验[84]。
金属氢化物体系中H2的平衡压力很高,H2的储存和储罐的设计通常是一个难题。高温金属氢化物在加热过程中释放的H2可以作为压缩气体储存,也可以引向低温金属氢化物中进行储存。对于第一种方法,H2被压缩并储存在压力容器或内衬岩洞[85]中,这个过程需要压缩机做功从而会增加系统能耗。为了替代金属氢化物储热系统中的H2存储子系统,研究界提出了由2个不同工作温度的氢化物床层组成的反应系统(图4)[86]。该系统利用聚光太阳能的热量使高温金属氢化物分解成金属和H2,H2被输送至低温子系统中的金属氢化物进行储存。当有能量需求时,反应器的温度下降,低温子系统中的H2受压力驱动重回高温子系统发生反应、释放热量[84]。这是一个“自我维持”的系统,节省了压缩H2的电能消耗[87]。2个反应器子系统的充放电过程是热控制的,通过控制温度来调节2 个反应器的吸收/解吸压力,低温金属氢化物的H2储存能力是影响系统性能的关键因素。AYUB等[88]使用MgH2和V2O5作为储热介质,利用碟式聚光器进行加热,通过数值模拟进行了太阳能热化学储热反应器的热分析,发现在中心位置插入H2管道,增加带翅片的管道数量,并改变翅片的尺寸,使系统的总体能源效率提升了36.89%。

图4 采用金属氢化物作为储热介质的聚光太阳能发电系统[86]Fig.4 Concentrated solar power generation system with metal hydride as energy storage media[86]
金属氢化物体系在广泛的温度区间内具备显著高的储热密度,且该体系具有一定的技术成熟度。设计和建造金属氢化物储热系统是目前的一大挑战,解决氢气的储存问题和系统的腐蚀也是未来研究的重要工作。
2.5 氨体系
氨被广泛用于生产肥料、炸药、硝酸等,因此合成氨工艺发展得非常成熟,这为氨储热体系的发展提供了条件。通过N2和H2反应生成氨气,也可以实现热量的存储和释放,反应方程式见式(9)。氨在常温下以液体形式存在,易于实现与产物的分离,并且无副产物的产生。但是,该反应的操作压力很高(1~3 MPa),且正反应和逆反应都需要催化剂[89]。N2和H2的长期存储也具有一定危险性,这在一定程度上限制了氨基热化学储热的发展。
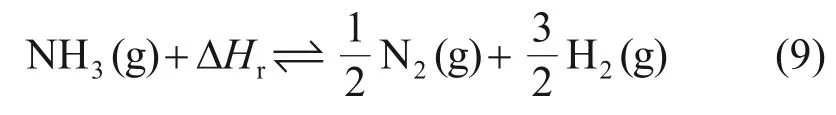
氨基热化学储热系统由吸热反应器和放热反应器组成[90](图5)。前者利用聚光太阳能的热量实现氨分解,后者利用氨合成反应放热。氨和气体产物在2个反应器之间通过压缩泵交替循环,反应器中均配备一个催化剂床层来促进反应的发生。在反应器和分离存储器之间布置了热交换器,通过放热反应器加热蒸汽推动汽轮机做功。

图5 采用氨作为储热介质的聚光太阳能发电系统[90]Fig.5 Concentrated solar power generation system with amino as energy storage media[90]
CHEN等[90-92]对超临界蒸汽耦合氨基热化学储热的系统进行了实验和模拟,发现合成氨可以将超临界蒸汽加热到650 ℃。此外,他们还进行了sCO2作为加热介质的布雷顿循环试验,该循环比蒸汽朗肯循环拥有更高的效率[93]。
3 总结
自2021 年8 月至2022 年8 月,中国青海省的德令哈配备储热系统的50 MW 光热电站年度累计发电量达1.58 亿kW·h,创下全球同类型电站最高运行纪录,这说明我国储热技术已具备产业化的土壤。未来,储热技术将在火电灵活性改造、需求侧管理措施、可再生能源消纳等广泛形式的应用中承担着重要的作用。随着储热应用技术的进步,成本进一步降低,其布局灵活、能量效率高、规模大等优势将不断凸显。
在现有的储热方式中,热化学储热比显热储热和潜热储热的储热密度高,理论上具有无限长的储存周期和运输距离。因此储热介质可以在环境温度下储存,储存期间的热损失为零。目前,热化学储热体系的研究主要处于实验室试验阶段,还未能实现商业化应用。本文对主流热化学储热体系的优缺点进行了比较,如表4所示。

表4 主流热化学储热体系的优缺点比较Table 4 Comparison of advantages and disadvantages of mainstream thermochemical energy storage systems
4 展望
综上所述,未来热化学储热体系的研究重点将从以下几个方向开展:
1) 储热材料的性能是制约其规模化应用的主要瓶颈,需要针对不同的储能场景开发储能密度高、循环次数多、成本低的热化学储能材料。如对综合性能最优的Co3O4金属氧化物体系,通过第二元素掺杂、晶体结构与微观形貌优化等提升其抗烧结能力。此外,应寻找钴基储热介质的低成本替代储热介质。如对碳酸钙体系,应重点关注其循环稳定性的问题以及通过材料组分与结构的设计,提升材料的化学反应活性。
2) 储放热化学反应机理与过程调控研究。热化学储放热循环反应属于表面-体相气/固反应,其路径复杂且耦合热质传递过程,扩散-吸附-化学反应-脱附等过程的耦合机制尚不清晰。因此,应发展反应界面动力学理论,阐明气/固反应的界面热-质传递过程与反应调控机制。
3) 建立系统模型,优化储热反应器、放热反应器和热交换器的设计,研究循环过程中的热量储存、释放的稳态和动态特性;对基于热化学储热系统进行中试放大研究,提升热能利用效率与系统经济性。
