无细胞再生性牙髓治疗的现状及展望
2022-02-14周建苏盈盈王松灵
周建 苏盈盈 王松灵
1.首都医科大学口腔健康北京实验室,北京100069;2.首都医科大学附属北京口腔医院特诊特需科,北京100050;3.首都医科大学附属北京天坛医院口腔和全身健康融合与转化研究实验室,北京100070;4.首都医科大学附属北京天坛医院口腔科,北京100070;5.首都医科大学基础医学院,北京100069
现代根管治疗技术对于保留患有牙髓病和根尖周病等牙髓感染性疾病的牙齿发挥了重要作用,并取得了极大的成功,但是由于根管系统解剖的复杂性和现有根管充填材料的局限性,根管治疗的失败率仍为19.1%~25.3%[1],而根管治疗后的牙齿也因缺乏免疫保护、感知外界刺激和自身修复等功能,存在二次感染和牙根纵裂的风险。再生性牙髓治疗(regenerativeendodontic therapy,RET)利用组织工程的原理,以实现牙髓牙本质复合体的功能性再生和牙根及其周围组织的继续发育为目的,被认为是根管治疗理想的替代方案。其策略主要分为两类:一种是基于外源性干细胞移植(cell transplantation)原理的有细胞再生性牙髓治疗(cell-based regenerative endodontic therapy)[2],另一种是基于内源性干细胞归巢(cell homing)原理的无细胞再生性牙髓治疗(cell-free regenera‐tive endodontic therapy)[3]。
有细胞再生性牙髓治疗利用经典的组织工程原理,将干细胞、支架材料和生长因子放入经过预备的根管内,以获得再生的牙髓牙本质复合体。过去十几年来,有大量相关的体内外研究显示该技术能够再生出具有神经、血管和成牙本质细胞的牙髓样组织,是实现牙髓牙本质复合体再生的潜在方法。但是,该技术同时也面临一些挑战,例如干细胞来源困难、临床应用安全性和有效性有待进一步评价以及临床转化应用投入较高等伦理法规和产业化瓶颈[4]。而基于细胞归巢原理的无细胞再生性牙髓治疗利用内源性干细胞趋化至根管内实现牙髓牙本质复合体再生,具有安全性更高、流程简化和费用更低等特点,可能具有更好的临床转化前景。本文将对无细胞再生性牙髓治疗的研究现状作一综述,并对其临床应用前景进行讨论。
1 无细胞再生性牙髓治疗的发展
牙髓血运重建术(revascularization procedure)被认为是无细胞再生性牙髓治疗的鼻祖。但事实上,该术语最早出现在20世纪50年代,最初指的是外伤牙再植后牙髓组织血运的恢复,尤其是年轻恒牙再植后牙髓组织的活力可以重建。Östby[5]于1961年首次报道了对于牙髓活力丧失的牙齿,通过扩大根尖孔、根管封药和将根尖区血液引入根管内形成血凝块,可以促进根尖周病变的愈合。这项研究在当时并没有引起重视,但为后续的再生性牙髓治疗奠定了基础。2001年,有学者[6]开始尝试利用血运重建来代替根尖诱导成形术,报道了1例被诊断为牙髓坏死的年轻恒牙病例,患牙根管经过5%的次氯酸钠和3%的过氧化氢溶液冲洗、双联抗生素(甲硝唑和环丙沙星)糊剂根管内封药和永久的冠方修复,30个月后随访,牙根得以继续发育,根管壁增厚,根尖孔闭合,且牙髓活力测试呈阳性,首次证实根管内血液的引入能够促进牙髓修复和牙根发育。随后,陆续有更多的病例报告[7-10]使用不同的化学冲洗剂和根管内药物,以探索最佳的治疗流程。
2011年美国牙科协会(American Dental Asso‐ciation,ADA)将牙髓血运重建术纳入常规牙科诊疗项目,并给出详细的临床操作指南,主要包括根管消毒、刺激根尖出血以及冠方严密封闭等步骤,牙髓血运重建术成为根尖诱导成形术一个可选的替代方案(图1)。
细胞归巢最初是指血源性干细胞穿过血管上皮迁移到目标组织并分化为成熟的终末细胞[3],目前这一概念已经延伸为靶向调控自体干细胞定向迁移到特定组织并分化,进而发挥组织再生功能[11]。在牙髓再生过程中主要是将复合有生长因子的生物支架材料注入无髓根管内,以诱导根尖周的内源性干细胞向根管内迁移、增殖和分化。细胞来源可以包括牙髓干细胞、根尖乳头干细胞和骨髓干细胞等(图1)。
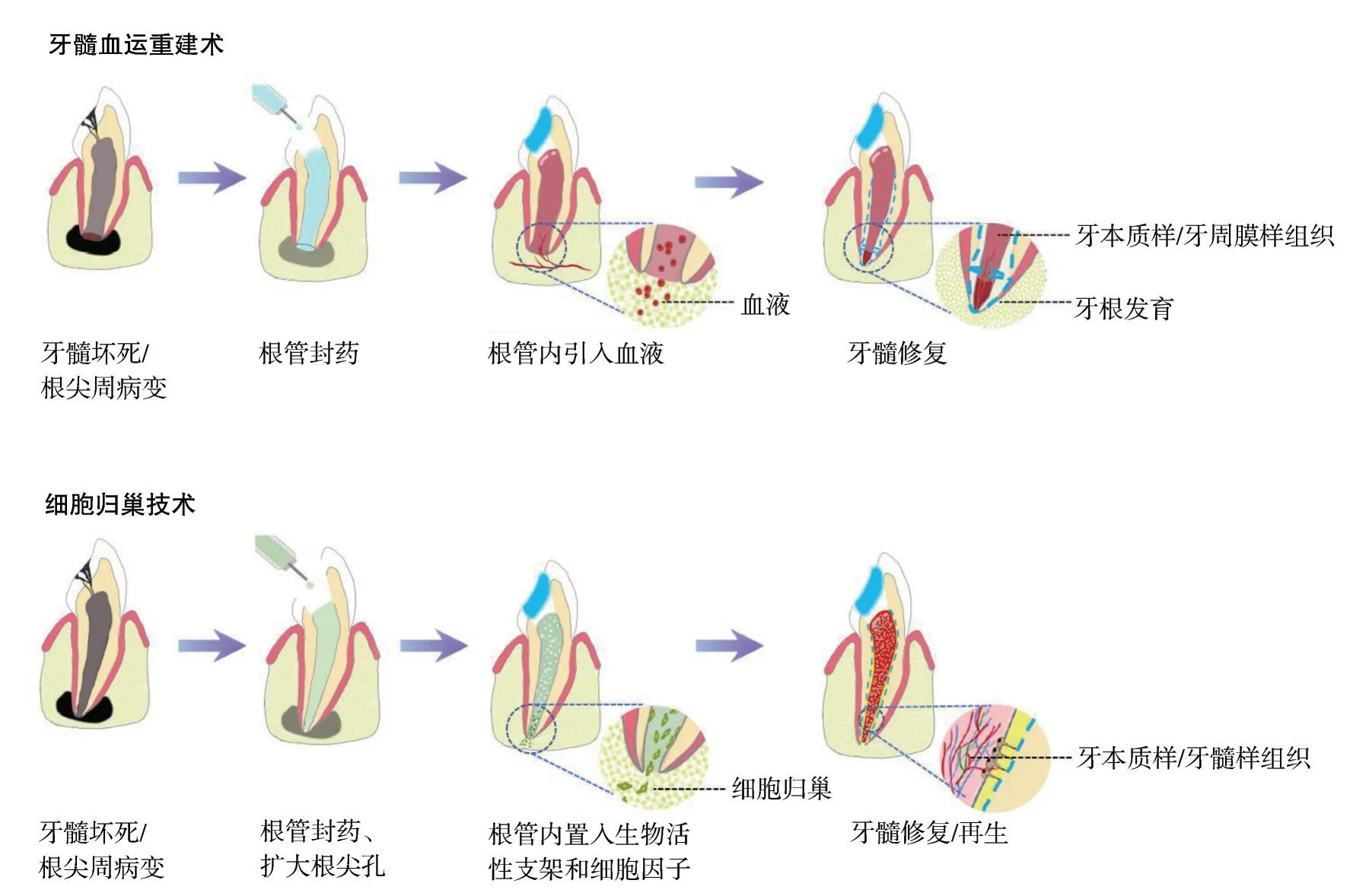
图1 无细胞再生性牙髓治疗原理图Fig 1 Schematic of cell-freeregenerativeendodontic therapy
最近有学者指出,“血运重建”是指为了恢复由于血管阻塞或被切断而发生缺血的组织的血供而进行的外科操作,对于牙髓再生来说,牙髓组织因感染而被破坏,因此并不存在恢复其血供的可能,故“血运重建”不是概括牙髓再生过程的最佳术语,使用“新血管化”(neo-vascularization)更恰当[12]。这些学者由此认为,“牙髓血运重建术”实际上是基于(干)细胞归巢的原理,这一术语并不符合牙髓组织工程的理念,因此建议将其与干细胞归巢技术统一定义为“无细胞再生性牙髓治疗”[3]。本文中的无细胞再生性牙髓治疗包括了所谓的“牙髓血运重建术”和“细胞归巢技术”。
2 无细胞再生性牙髓治疗的适应证
无细胞再生性牙髓治疗最初的适应证仅包括牙髓坏死的年轻恒牙,美国牙髓病学会(Ameri‐can Association of Endodontics,AAE)在2018年发表的“再生治疗的临床考虑”(AAE Clinical Considerations for a Regenerative Procedure)中也将其适应证限定为牙髓坏死且根尖孔未闭的患牙,在相关领域已有大量的病例报道、前瞻性和回顾性队列研究以及随机对照研究[13-16]。2017年,一项meta分析[17]比较了基于牙髓血运重建技术的再生性牙髓治疗与矿物三氧化物凝聚体(mineral trioxide aggregate,MTA)根尖封闭的效果,结果显示再生性牙髓治疗组的牙齿存活率为97.8%(“存活”被定义为随访期间牙齿在口腔中存留),MTA根尖封闭组为97.1%;再生性牙髓治疗组的成功率为91.3%(“成功”被定义为临床无症状、影像学上根尖病损完全愈合),MTA根尖封闭组为94.6%;两组在牙齿存活率和成功率上的差异没有统计学意义,但是再生性牙髓治疗组有79%的病例牙根得到继续发育。另一项meta分析[18]也表明,再生性牙髓治疗对牙髓无活力年轻恒牙的治疗可获得较高的牙齿存活率和成功率,但同时也指出根尖孔的闭合和牙根发育的程度在各项研究中具有不一致性,表明再生性牙髓治疗的效果具有不稳定性,而且也缺乏长期随访的结果。
鉴于无细胞再生性牙髓治疗对年轻恒牙的良好治疗效果,研究者们正在尝试将该技术的适应证推广到成熟恒牙。研究人员将人或猪的离体单根牙经根管预备后,根管内植入不加载细胞的支架材料(如胶原凝胶、胶原海绵和丝素蛋白等)和信号分子(成纤维生长因子、血管内皮生长因子、趋化因子和牙本质基质蛋白等),然后置于啮齿类动物的皮下,探讨异位牙髓再生的可能性,组织学观察证实根管内再生出具有血管和神经纤维的牙髓样组织[19-21]。迄今为止,仅有2项研究报道了成功利用细胞归巢技术在原位再生牙髓牙本质复合体:有研究团队[22]在比格犬牙根发育完全的前磨牙上建立根尖周病变,然后进行根管预备和根管消毒,通过轻度超预备诱导血液进入髓腔,再将载有基质细胞衍生因子-1α(stromal cell-de‐rived factor-1α,SDF-1α)的丝素蛋白放入根管内,3个月后根管内形成具有新生血管的牙髓样结缔组织和衬于天然牙本质壁表面的牙本质样结构。另一项研究[23]利用Wnt/β-连环蛋白(catenin)信号通路的重要配体Wnt3a靶向诱导内源性干细胞归巢,在小型猪下颌切牙根管内原位再生功能化牙髓牙本质复合体,组织学结果显示,干细胞归巢到根管后,除分化为成牙本质细胞并形成牙本质以外,还分化再生出含血管、神经纤维等间质组织的血管神经化牙髓。这两项研究提示,SDF-1α和Wnt/β-catenin信号通路可能是调控干细胞归巢、成牙分化以及血管再生的关键分子之一,并证实了细胞归巢技术原位再生成熟恒牙牙髓牙本质复合体的可行性。
无细胞再生性牙髓治疗应用于成熟恒牙牙髓和根尖周病变治疗的临床数据尚十分稀少,到目前为止仅有少数的病例报道。有3个研究团队[24-26]分别报道了2例、2例和7例牙髓坏死的成熟恒牙进行基于牙髓血运重建技术的再生性牙髓治疗,随访期为8~26个月,结果显示:在随访期内所有患牙的症状都消失或改善,影像学上根尖周病变也消失或减轻,但11颗患牙中仅有1颗对温度刺激和电活力测试有反应,表明无细胞再生性牙髓治疗具有应用于成熟恒牙的潜能,但效果较年轻恒牙差,其原因与根尖孔的大小、干细胞数量和功能状态以及局部微环境等都有关系。
3 无细胞再生性牙髓治疗的瓶颈和研究方向
根据AAE 2016年牙髓术语表中的定义,再生性牙髓治疗是指以生物学为基础的治疗,旨在生理性替换受损的牙齿结构,包括牙本质、牙根以及形成牙髓牙本质复合体。根据这一定义,牙髓牙本质复合体再生的终极目标是在牙髓受损或失去牙髓的根管内实现牙髓牙本质复合体的“发育性”再生,即再生组织应该拥有良好的血运、具有与正常牙髓相似的细胞密度、细胞外基质结构和神经分布,以及能够在根管壁表面分化出新的成牙本质细胞并分泌牙本质。然而,现有研究还没有实现以上目标,目前的临床研究结果提示,对牙髓坏死/根尖周炎的年轻恒牙的无细胞再生性牙髓治疗只是修复(repair)过程,而不是再生过程。有研究[27]发现,当对患有不可复性牙髓炎,保留有完整的上皮根鞘和根尖乳头的年轻恒牙进行再生性牙髓治疗时,牙髓再生是可能的。而对于患有牙髓坏死/根尖周炎的年轻恒牙来说,多数临床研究表明经无细胞再生性牙髓治疗后根管内形成的是异位牙骨质、骨样组织和牙周膜样结缔组织[28-29],而且发生根管内钙化的概率也很高(62.1%)[30]。这样的组织虽然有可能对牙髓活力测试有反应,却不具备免疫防御和形成修复性牙本质等正常牙髓牙本质复合体的功能。
以上研究表明,根管内感染的严重程度和根尖周组织的再生潜能对于牙髓牙本质复合体再生具有重要影响。在未来临床研究方案的制定中,应当考虑以下几点:1)根据不同的牙髓状态探索不同的治疗方案,比如,对于患有不可复性牙髓炎的年轻恒牙,采用过去所指的牙髓血运重建术即可能实现牙髓牙本质复合体再生;而对于患有牙髓坏死或根尖周炎的年轻恒牙,则需要强调根管消毒的作用,譬如开发新的消毒药物或药物组合、研发具有消毒和抗菌功能的支架材料以及使用负压灌溉、激光、passive超声等新技术,而且在加强消毒效果的同时需要尽量保护根尖周组织和根管内环境;2)成熟恒牙根尖孔通常闭合或较小,不利于根尖周组织中的干细胞进入根管内,成人患者的干细胞数量和活性较年轻患者低,细胞再生能力相对较差。因此对成熟恒牙应采取不同于年轻恒牙的方案,比如:在保证既不破坏根尖屏障,又能方便足够多的干细胞归巢到根管内的前提下扩大根尖孔;探索干细胞归巢、增殖及定向分化的特异性调控机制、优化生物活性支架材料和生长因子的组合与投递方式,以增强成熟恒牙根尖周组织中干细胞的归巢、增殖和定向分化能力;3)理想的牙髓再生支架材料除了能够促进细胞附着、迁移、增殖和定向分化,还应该具备以下特征:拥有三维空间结构;具有良好的生物相容性;可降解性,且降解速率应与组织再生的速率相匹配。目前还没有任何一种材料具备上述所有特性,在未来的研究中可尝试将不同的材料相互结合,以获得具有结构稳定、能提供高度仿生的微环境,并模拟天然的细胞外基质的生物材料。此外,多种材料的连续生物打印以及含细胞生物材料等研究热点代表了新的研究方向;4)开展更多的临床研究,尤其是设计良好的、前瞻性的、能够长期随访的临床试验。
4 结论
目前的无细胞再生性牙髓治疗在消除或改善年轻恒牙牙髓和根尖周病变方面与其他治疗方法,如MTA屏障技术相比,成功率无显著差异,但在促进牙根发育方面更具优势。随着对牙髓牙本质复合体发育与再生机制的进一步了解,无细胞再生性牙髓治疗临床应用的推进,牙髓牙本质复合体再生的希望将会成为现实。
利益冲突声明:作者声明本文无利益冲突。
