miR-612靶向调控FOXP1对前列腺癌细胞增殖、迁移及侵袭能力的影响
2022-02-13李文永伍宏亮黄俊峰代昌远李庆文
李文永,伍宏亮,邓 硕,黄俊峰,代昌远,关 翰,李庆文,薛 胜
(蚌埠医学院第一附属医院泌尿外科,安徽 蚌埠 233004)
前列腺癌是男性最常见的癌症诊断之一。前列腺癌是美国男性的第二大死因[1],其发病率在全球范围内呈上升趋势,在我国由于老龄化的进展,发病率也逐年上升,严重威胁男性的健康,前列腺癌常发生骨转移,导致患者预后不佳[2]。尽管手术治疗、化疗及内分泌治疗取得了一定的成果,但仍然无法阻止前列腺癌的进展。因此,迫切需要我们对其分子机制更深入的研究,而前列腺癌异常的能量代谢机制是当前研究的热点,有研究发现肿瘤基因调控代谢平衡从而影响癌细胞的增殖能力[3]。微小 RNA(miRNA)是非编码RNA,可作为基因表达的调节剂。miRNA在细胞增殖、细胞周期、细胞代谢、凋亡、侵袭和转移等方面已显示出其生物学功能[4]。研究发现miRNA-612(miR-612)与多种肿瘤的生长有关,包括结肠癌、膀胱癌、子宫内膜癌、黑色素瘤和卵巢癌[5]。然而,其在前列腺癌中的作用机制仍知之甚少,通过Targetscan分析显示叉头框蛋白P1(FOXP1)可能是miR-612靶基因。FOXP1在多种肿瘤组织中高表达,对肿瘤的发生发展起着重要作用[6]。但miR-612能否调控FOXP1表达而影响前列腺癌细胞增殖、迁移和侵袭能力尚未可知。因此,本研旨在探索前列腺癌细胞中miR-612与FOXP1可能对增殖、迁移及侵袭能力的作用机制。
1 材料与方法
1.1 试剂与材料人前列腺癌细胞系DU145、PC3、LNCaPC-81和人前列腺上皮细胞RWPE1购自中国科学院上海细胞库。胎牛血清、双抗、DMEM高糖培养基、胰蛋白酶来源于美国Hyclone公司;Transwell小室购于美国康宁公司;MTT试剂盒购于美国MCE公司;实时荧光定量PCR(RT-qPCR)试剂盒购于南京诺唯赞生物科技有限公司;逆转录试剂盒购于广州洛唯尔生物科技有限公司;BCA蛋白质测定试剂盒购于美国Abcam公司;ECL Western Blotting试剂盒购于美国Abcam公司;辣根过氧化物酶(HRP)标记的山羊抗兔二抗购于杭州馨然生物科技有限公司;兔抗FOXP1抗体购于美国Abcam公司;FOXP1过表达质粒、miR-612 mimic、miR-612 inhibitor及其对照miR-NC购于苏州赛业生物科技有限公司;Lipofectamine 2000购于美国赛默飞世尔科技公司。
1.2 组织标本的收集选择2020年6月至2021年6月在我院住院期间确诊为前列腺腺泡腺癌患者18例,前列腺癌组织(n=18)和癌旁组织(n=18)经手术切除后立即在液氮中速冻组织,使用前在-80 ℃下储存。所有标本均经病理学证实为前列腺癌。我们的研究得到了本院伦理委员会的批准。所有患者均签署知情同意书。
1.3 细胞培养使用含有100 μg/mL青霉素和50 μg/mL链霉素双抗、10%胎牛血清的高糖DMEM培养基培养PC3细胞,RWPE1细胞采用无血清培养基,置于37 ℃,5% CO2的孵箱中培养,隔两天换液一次,使用0.25%胰蛋白酶消化传代.
1.4 细胞转染选取上述三种人前列腺癌细胞系中miR-612相对表达最低的PC3细胞作为实验细胞,收集PC3细胞制备单细胞悬液(5×104个/mL),100 μL/孔的密度接种于6孔板,用无血清DMEM稀释FOXP1过表达质粒、miR-612 NC、miR-612 mimic、miR-612 inhibitor或Lipofectamine 2000。将转染混合物加入细胞悬液中并孵育6 h后用含有10% FBS的DMEM代替转染混合物。在进行测定之前将细胞培养48 h。
1.5 RT-qPCR使用Trizol提取细胞的总RNA。使用逆转录试剂盒合成cDNA。对于mRNA和miRNA检测,分别在ABI 7500热循环仪(Life Technologies)上使用RT-qPCR试剂盒进行实时PCR。GAPDH或U6基因用作内参。PCR反应条件为95 ℃ 5 min,95 ℃15 s和60 ℃30 s,40个循环。使用2-ΔΔCt方法分析相对表达。
1.6 双荧光素酶报告基因检测用miRWalk(mirwalk.umm.uni-heidelberg.de)预测miR-612的靶基因,通过双荧光素酶报告试验进一步验证预测结果。将PC3细胞分成6组,分别转染miR-612 mimic+野生型WT-FOXP1、miR-NC+野生型WT-FOXP1、miR-612 mimic+突变型MUT-FOXP1、miR-NC+突变型MUT-FOXP1、对照组(野生型WT-FOXP1或突变型MUT-FOXP1),转染后每组以1×104个/孔细胞接种于96孔板,孵育48 h后,100 μL/孔加入细胞裂解液,取上清液加入40 μL萤火虫荧光素底物,充分混合后测定荧光强度,取剩余上清液加入40 μL海肾荧光素酶底物,充分混合后测定荧光强度,使用双荧光素酶报告分析系统(Promega)来确定海肾荧光素酶和萤火虫荧光素酶的活性。
1.7 细胞增殖试验采用MTT法检测细胞增殖。将不同组的PC3细胞1×104个/孔接种到96孔板中,37 ℃、5%CO2培养12 h、24 h、48 h或72 h。然后,加入20 μL MTT(5 mg/mL)。通过使用酶联免疫检测仪(Thermo Fisher Scientific)测定570 nm处的光密度(OD)来检测甲臜的产生。
1.8 细胞侵袭试验使用预涂有Matrigel的Transwell室进行细胞侵袭测定。将300 μL 5×105个细胞/mL的细胞悬液加入上室,下室加入500 μL 10%FBS DMEM。未通过毛孔迁移或侵入的细胞被清除。将滤膜固定在90%酒精中并用0.1%结晶紫染色,并在倒置显微镜(Olympus,日本 )下观察。添加0.5 g/L MTT,并使用Bio-TekTMELX-800TM吸光度酶标仪(Bio-Tek,美国 )测量570 nm处的光密度。测定相对细胞侵袭能力。
1.9 蛋白印迹实验使用BCA蛋白质测定试剂盒测定蛋白质浓度。用10% SDS-PAGE分离蛋白质,转移到PVDF膜,然后在5%脱脂奶粉中封闭。 PVDF膜与兔抗FOXP1单克隆抗体(1∶100)或小鼠抗GAPDH单克隆抗体(1∶100)一起孵育,作为内部参考。之后,将PVDF膜与小鼠抗兔二抗(1∶20 000)一起孵育。使用ECL Western Blotting试剂盒检测免疫复合物。Image-Pro plus软件6.0用于分析相对蛋白质表达,表示为与GAPDH的密度比。
1.10 统计学分析使用SPSS 22.0进行统计学分析,连续数据表示为“均数±标准差”。t检验或单因素方差分析用于分析组间的差异。使用GraphPad Prism 6.0软件进行图形制作。P<0.05为有统计学意义。
2 结果
2.1 miR-612在PC3细胞中表达降低通过RT-qPCR检测miR-612表达结果显示,与癌旁组织相比,前列腺癌组织中miR-612的表达显着降低(P<0.05,图1A);miR-612的表达水平在人前列腺癌细胞系(DU145、PC3、LNCaPC-81)中明显降低,分别与正常人前列腺上皮细胞(RWPE1)相比均有显著的统计学差异(P<0.05,图1B)。

图1 miR-612在前列腺癌细胞及组织中的相对表达
2.2 miR-612的过表达抑制PC3细胞的增殖、迁移和侵袭能力通过细胞转染miR-612 mimic、miR-612 inhibitor后PC3细胞中miR-612的表达水平明显升高或降低(P<0.05,图2A);MTT试验显示miR-612过表达显着抑制PC3细胞增殖,而miR-612敲减增强PC3细胞的增殖能力(P<0.05,图2B);划痕试验结果显示miR-612过表达显着抑制PC3细胞迁移,而miR-612敲减增强PC3细胞的迁移能力(P<0.05,图2C);Transwell试验数据进一步表明miR-612过表达显着抑制PC3细胞侵袭,而miR-612敲减增强PC3细胞侵袭(P<0.05,图2D)。
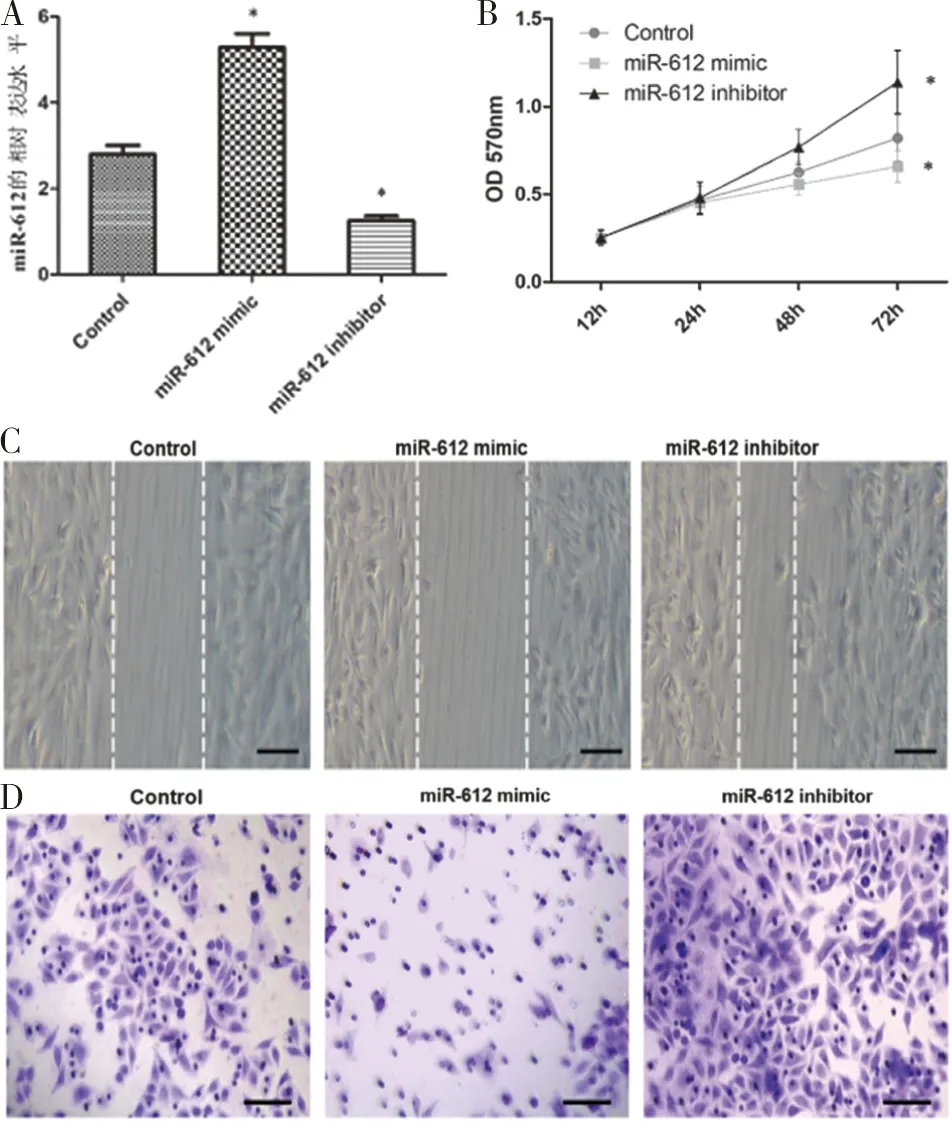
图2 miR-612过表达抑制PC3细胞的增殖、迁移及侵袭能力
2.3 miR-612可能靶向抑制FOXP1基因的表达使用生物信息学预测和Targetscan(http://www.targetscan.org/)进一步分析了miR-612的靶标(图3A、3B)。荧光素酶报告基因测定显示荧光素酶活性仅在与miR-612 mimic和野生型FOXP1 3'UTR共转染的PC3细胞中显着下调(P<0.05,图3C)。然而,其他组的荧光素酶活性没有变化。通过蛋白质印迹进一步检测了miR-612对PC3细胞中FOXP1蛋白质表达的影响,结果显示与对照组相比,过表达miR-612的PC3细胞中FOXP1蛋白表达水平显着降低,但在miR-612敲减后升高(P<0.05,图3D)。

图3 miR-612靶向抑制FOXP1基因表达
2.4 FOXP1参与miR-612介导的PC3细胞增殖、迁移和侵袭结果显示miR-612 mimic+FOXP1组的FOXP1表达水平显著高于miR-612 mimic组(P<0.05,图4A);MTT试验显示miR-612 mimic+FOXP1组细胞增殖能力增强(P<0.05,图4B);划痕试验显示miR-612 mimic+FOXP1组细胞迁移能力增强(P<0.05,图4C);Transwell试验显示miR-612 mimic+FOXP1组促进了细胞侵袭(P<0.05,图4D)。

图4 miR-612调控FOXP1表达影响
3 讨论
miRNA是单链内源性非编码小RNA,长度约22个核苷酸,对调节转录后基因的表达具有重要作用[7]。在不同的肿瘤中miRNA的常表达有异常,对肿瘤的增殖、迁移、细胞周期与凋亡、侵袭和分化等表型的调控密切相关[8]。miR-612已被证明通过调节主要的肿瘤相关生物学行为在多种癌症中表现出肿瘤抑制活性[9],然而,miR-612在前列腺癌中的表达状态及相关机制仍不清楚,本研究中。我们检测到前列腺癌样本中miR-612的表达显著降低,并确定了其在前列腺癌中的临床意义。此外,我们进一步探讨了miR-612在前列腺癌中的作用和潜在机制,FOXP1是前列腺癌中的一种癌基因,被进一步鉴定为PC3细胞中miR-612的直接靶标,体外研究表明,miR-612可以抑制PC3细胞的增殖、迁移和侵袭能力,至少部分是通过直接抑制FOXP1蛋白的表达有关,我们还发现FOXP1 mRNA显着增加,并且与前列腺癌中的miR-612水平呈负相关。
最近研究发现miR-612水平在胃癌细胞中显着降低[10],在本研究中,RT-PCR数据表明,与正常前列腺组织相比,前列腺癌组织中的miR-612显著下调,说明miR-612可能在前列腺癌中充当肿瘤抑制因子,为进一步使用前列腺癌PC3细胞系来研究miR-612在调节细胞增殖、迁移和侵袭中的确切作用,我们用miR-612 mimic转染PC3细胞以上调miR-612,并观察到miR-612过表达导致细胞增殖、迁移和侵袭能力的显著抑制,在其他癌症中也报道了miR-612对细胞增殖、迁移和侵袭等表型的抑制作用。Yang等人发现miR-612通过靶向NOB1抑制宫颈癌的进展[11]。Sheng等人报道miR-612通过靶向AKT2负调控结直肠癌的生长和转移[12]。此外,Wang等人发现miR-612抑制FOXM1表达从而抑制胃癌中的肿瘤血管生成和转移[13]。上述研究结果表明miR-612可能成为前列腺癌新的分子干预靶点。
通过Targetscan预测miR-612的靶基因,结果显示FOXP1可能是miR-612的靶基因,双荧光素酶报告实验及蛋白印迹检测发现miR-612可靶向负性调控FOXP1的表达,进一步研究发现FOXP1过表达可促进前列腺癌细胞增殖、迁移及侵袭能力。FOXP1是FOX转录因子家族的成员,具有广泛的功能。其过度表达在许多类型的淋巴瘤中预后不良,这表明FOXP1可能在其他组织类型中充当肿瘤抑制基因[14]。有研究报道FOXP1在结肠癌中表达异常,参与结肠癌发生、发展过程,可能成为结肠癌诊治的新肿瘤标记物[15]。FOXP1在胃癌组织中表达显著升高,与肿瘤大小、分化程度等病理特征及预后密切相关[16]。此外,FOXP1在肿瘤免疫中也发挥着一定作用,有报道发现FOXP1负调控人乳腺癌中的肿瘤浸润淋巴细胞迁移[17]。在本研究中,我们发现FOXP1过表达逆转了miR-612介导的对PC3细胞增殖、迁移和侵袭的抑制,进一步验证了FOXP1在前列腺癌细胞中充当了miR-612的下游效应因子发挥作用,miR-612/FOXP1轴可能成为前列腺癌的潜在治疗靶点,未来将在更大样本的研究中进一步检验miR-612在前列腺癌中的诊断和预后潜力。
综上所述,我们的研究结果揭示了miR-612在前列腺癌中发挥抑癌基因作用,通过靶向FOXP1部分抑制前列腺癌细胞的增殖、迁移和侵袭能力,miR-612/FOXP1轴可能成为前列腺癌的潜在治疗靶点。
