太湖潜流带有机质含量对硝酸盐还原途径的影响
2022-02-11单雅洁钱佳宁冯家成
李 勇,单雅洁,李 娜,钱佳宁,冯家成,徐 鸿
(1.河海大学浅水湖泊综合治理与资源开发教育部重点实验室,江苏 南京 210098; 2.河海大学环境学院,江苏 南京 210098; 3.河海大学水资源高效利用与工程安全国家工程研究中心,江苏 南京 210098)
潜流带作为地表水和地下水之间物质和能量交换的活跃过渡区域,其物理、化学、生物条件的梯度分布和变化对氮素的迁移转化和界面释放产生了重要的影响[1-2]。一般来说,下行流携带富含溶解氧和有机质的地表水进入潜流带并与浅层地下水交汇,而上行流则携带大量富含硝态氮、低溶解氧及低有机质的浅层地下水进入潜流带并与界面处地表水体交汇[3-4]。研究显示,往往深层潜流带中氨氮含量较高,而富营养化的湖泊水体含有丰富的有机质和硝态氮等营养物质,一旦存在下行流的局部区域,丰富的有机质和硝态氮等容易随着水流进入潜流带,并随着潜流带深度的变化而产生不同的物理、化学、生物变化[5-6]。
众多研究显示,潜流带作为长期较稳定的厌氧场所,对来自浅层地下水和地表水的硝态氮具有重要的还原作用,特别是在有机质含量相对丰富的浅层潜流带中,微生物活性相对较强,容易发生反硝化作用,使得大量硝态氮转化为气态氮的形式得以去除[7]。一般来说,除了占据主导地位的反硝化过程外,当有机质含量较低时,厌氧氨氧化过程会占据一定的主导地位;当有机质的可用性较高时,硝酸盐异化还原成铵(DNRA)过程会成为硝态氮还原的重要途径。富营养化湖泊水体中的有机质大多来自自身大型水生植物和浮游动植物的分解产物以及通过河道输入的陆源物质等[8-10],其中腐殖酸是有机质的重要组成部分。江俊武等[11]对太湖水体的研究显示,类腐殖质对有色可溶性有机质(CDOM)的贡献率在9.6%~18.8%之间,特别是太湖的北部和西部等区域,类腐殖质占CDOM的14.6%~18.8%。腐殖酸有较好的还原性,某些硝酸盐还原菌会氧化腐殖酸,将其作为氧化还原过程的电子供体[12]。
为进一步掌握湖泊潜流带下行流条件下有机质对其中硝酸盐还原的影响,以太湖西部湖区潜流带为研究对象,进行室内原状沉积物柱模拟试验,分别设定腐殖酸与硝酸盐浓度比值为1∶1以及仅输入硝酸盐两种条件模拟潜流带下行水流携带营养物质,结合环境因子如pH值、Eh值进行分析,探索腐殖酸对硝态氮还原途径及氮素在不同深度迁移转化过程的影响。
1 材料与方法
1.1 研究区域及沉积物样品的采集
太湖是我国第三大淡水湖,水面面积2 338 km2,平均水深1.9 m,与219条河流和渠道相连。太湖西北部的海拔高于南部和东部,因此水流通常从西北流向东南[13]。西部湖区枯水期氮素污染主要来源于农用化肥,丰水期以生活污水为主[14]。采用手动垂直插入聚乙烯管的方式于太湖西部湖区采样点W(119°56′17.30″E,31°10′00″N)采集两根原状沉积物柱,其中一根内径15 cm,高45 cm,用于室内模拟试验;另一根内径6.5 cm,高60 cm,用于理化性质分析,所有样品冷藏运往实验室并在1周内完成理化性质指标的测定。
1.2 试验装置和研究方案
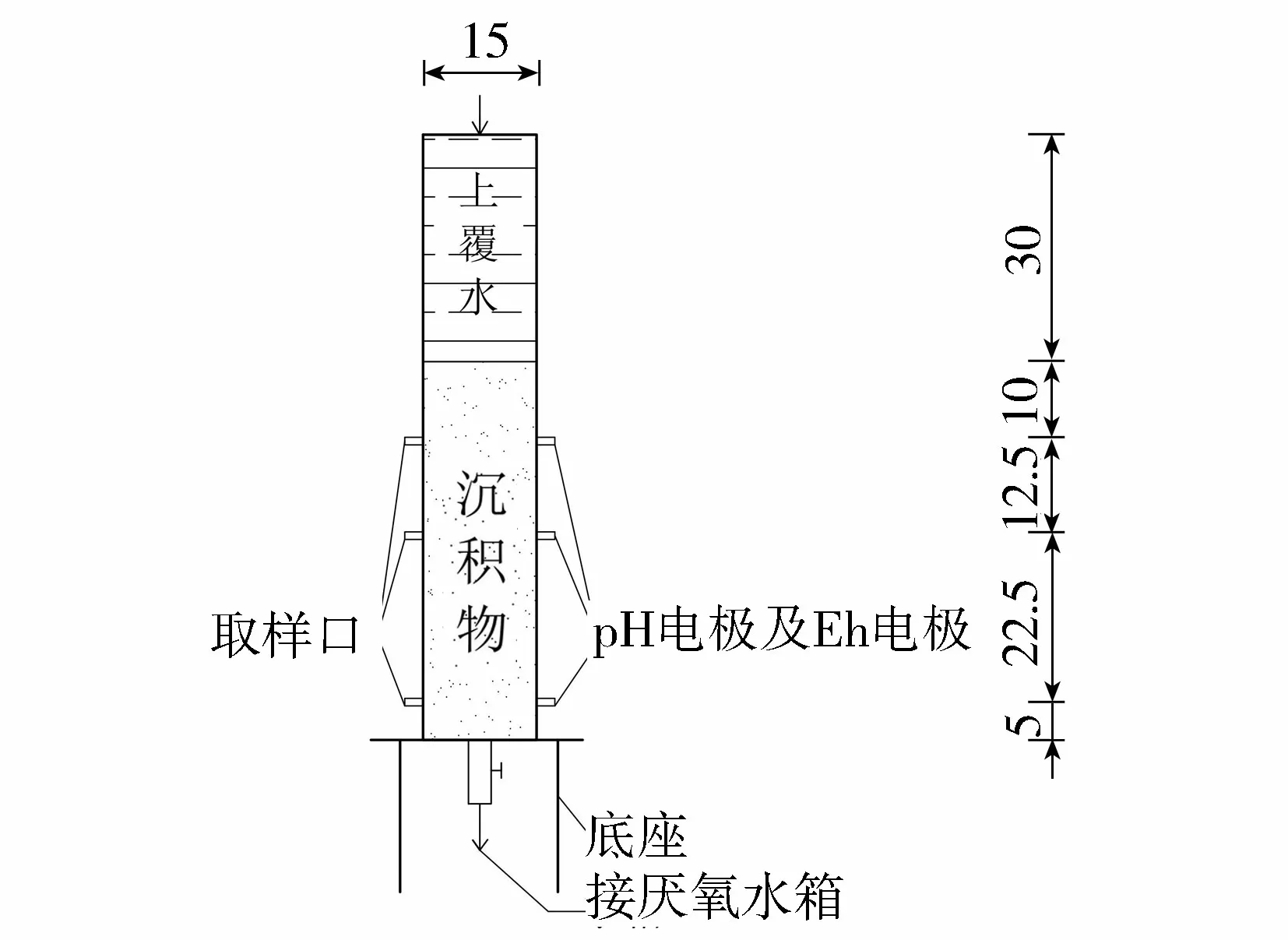
图1 太湖浅层潜流带下行流模拟试验装置(单位:cm)Fig.1 Simulation experimental device of shallow hyporheic zone in Lake Taihu with downwelling hyporheic flow (units: cm)
试验装置以采集的原状沉积物柱为基础,竖直放置,顶端加置上覆水储存段(高30 cm)和进水装置,底端加置底座和排水收集装置(图1)。底端填充5 cm厚的均匀粒径石英砂并在与沉积物接触面铺设土工布,避免柱内沉积物在出水时受到冲刷扰动。试验装置顶端和底端分别设置进水口和出水口,采用双头蠕动泵控制进水,保持进水速率恒定及上覆水水位稳定不变;出水口接厌氧水箱,厌氧水箱设进、出气口及进、出水口,连续充入乙炔气体以保持柱中厌氧环境。在距沉积物顶端向下10.0 cm、22.5 cm和45.0 cm处设置3个取样孔,采用抽滤器采集沉积物中孔隙水样,并安装pH电极及Eh电极以测量柱内pH值及氧化还原电位。
试验开始前连续通入蒸馏水,待原状沉积物柱中物质浓度及环境条件稳定时,记录柱上电极读数并测定各个取水口的相应水样指标作为初始值。为保持原状沉积物柱中条件的一致性,采用同一根原状沉积物柱并设定两个阶段开展试验。阶段Ⅰ渗透流速为2.02 cm/d,相应的配制溶液①硝态氮及腐殖酸质量浓度分别为4.98 mg/L和5.20 mg/L,持续时间为80 d,观察其中不同深度氮素迁移转化特征;随后开展阶段II试验,先通入蒸馏水约25 d以消除上一阶段溶质输入对原状沉积物柱的影响,直到各深度各物理化学指标稳定后同样以2.02 cm/d的流速通入硝态氮质量浓度为5.11 mg/L的配置溶液②,持续时间为57 d,观察无腐殖酸伴随输入情况下不同深度氮素的运移转化情况。为保证进水溶质浓度稳定,每2~3天更换模拟水。
在取样前用针筒将取样口的水样抽干,取样时打开取样口的止水夹,使用真空泵对其进行抽气,将其抽为负压后用止水夹夹住抽气管,静待约2 h后使用针筒抽出待测水样,每次抽取水样5~10 mL以测定氮素及腐殖酸浓度。为观察原状沉积物柱相对稳定后氮素的主要变化过程,首次取样时间在试验开始后第10天,随后每3~5天取样一次,每次记录各监测点位处的pH值和Eh值。
1.3 分析方法
沉积物粒径采用全自动激光粒度分析仪LS13320测定;pH值、Eh值分别采用pH电极和Eh电极测定;沉积物TOC、总氮、硝态氮和氨氮分别采用HJ 658—2013《土壤有机碳的测定 燃烧氧化 滴定法》、HJ 717—2014《土壤质量 全氮的测定 凯式法》、GB/T 32737—2016《土壤硝态氮的测定 紫外分光光度法》和HJ 634—2012《土壤 氨氮、亚硝酸盐氮、硝酸盐氮的测定 氯化钾溶液提取-分光光度法》测定。
将沉积物样品在4 000 r/min条件下离心30 min,取上清液过0.45 μm滤膜后测定孔隙水中无机氮的浓度。孔隙水及试验过程中所取水样的总氮、硝态氮、亚硝态氮和氨氮分别采用HJ 636—2012《水质 总氮的测定 碱性过硫酸钾消解紫外分光光度法》、HJ/T 346—2007《水质 硝酸盐氮的测定 紫外分光光度法(试行)》、GB/T 5750.5—2006《生活饮用水标准检验方法 无机非金属指标》中的重氮耦合分光光度法和HJ 535—2009《水质 氨氮的测定 纳氏试剂分光光度法》测定;使用UV254快速表征腐殖酸中DOC的浓度,记为DOC254,该方法使用广泛并能有效代表DOC中有效碳的浓度[15]。
根据监测深度将原状沉积物柱分为3层,分别是0~10.0 cm、10.0~22.5 cm、22.5~45.0 cm,计算各层硝态氮的还原量、还原速率及氨氮生成量:
(1)
(2)
(3)

使用Excel 2016进行数据统计,Origin 2018进行相关图表的绘制。
2 结果分析
2.1 沉积物基本理化性质
太湖西部湖区孔隙水中TN质量浓度随深度增加而上升,由上层1.69 mg/L逐渐上升到40~60 cm深度的2.92 mg/L;氨氮是无机氮存在的主要形态,变化趋势与TN相似,随深度从1.41 mg/L增加到2.17 mg/L;而硝态氮和亚硝态氮质量浓度相对较低,平均质量浓度分别为0.284 mg/L和0.032 mg/L(图2(a))。沉积物中,TOC质量比随深度增加从8.22 g/kg升高至14.34 g/kg,平均为11.57 g/kg;TN质量比随深度先升高后降低,均值为2.23 g/kg;氨氮及硝态氮质量比相对较小,分层特征不明显,均值分别为0.108 g/kg和0.027 g/kg(图2(b))。

图2 太湖西部沉积物及孔隙水中无机氮垂向分布Fig.2 Inorganic nitrogen vertical distribution in sediment and pore water of the western hyporheic zone of Lake Taihu
2.2 模拟试验中氮素垂向分布变化
a.硝态氮。阶段Ⅰ开始时各层硝态氮质量浓度均持续升高,第21天时各层硝态氮质量浓度达到最大值,随深度增加分别为2.31 mg/L、1.29 mg/L和0.91 mg/L(图3(a))。第21—39天原状沉积物柱内硝态氮质量浓度呈下降趋势,表层降至1.46 mg/L,而中下层均降至0.5 mg/L左右。39天后上层硝态氮质量浓度仍有降低趋势,但相对较缓,中下层略有升高。深度10.0 cm处硝态氮质量浓度一直高于其余两个监测点,而中下层硝态氮质量浓度差异相对较小。阶段Ⅰ结束时,上、中、下层硝态氮质量浓度分别为1.37 mg/L、0.64 mg/L和0.60 mg/L。阶段Ⅱ初期3个监测点硝态氮质量浓度均呈缓慢升高的趋势,第138天以后硝态氮累积速度加快,最终质量浓度随深度增加分别达到2.46 mg/L、1.71 mg/L和1.42 mg/L。在阶段Ⅱ,硝态氮分层特征较阶段Ⅰ更为明显,呈上层大于中层大于下层。总的来说,在原状沉积物柱运行过程中,各层硝态氮质量浓度变化特征相似,阶段Ⅰ硝态氮质量浓度在前21天大幅度上升,后呈降低趋势,而阶段Ⅱ硝态氮持续累积。

图3 原状柱内不同深度孔隙水中硝态氮、亚硝态氮及氨氮质量浓度变化Fig.3 Mass concentration variations of nitrate nitrogen, nitrous nitrogen and ammonia nitrogen in pore water at different depths of undisturbed sediment column
b.亚硝态氮。阶段Ⅰ各层初始亚硝态氮质量浓度差异较大,随着深度增加分别为0.074 mg/L、0.051 mg/L和0.062 mg/L(图3(b))。初期各层亚硝态氮均经历了一个显著下降的过程,第21天时降至0.03 mg/L左右;21天后各层质量浓度变化幅度相对较小。上层第21—65天亚硝态氮质量浓度仍呈降低趋势,但降低速度减缓,从0.035 mg/L降至0.022 mg/L;第65天后出现了短暂的上升,最终质量浓度为0.035 mg/L。而中层亚硝态氮第25天后出现了较为明显的累积,阶段Ⅰ结束时质量浓度升高至0.043 mg/L。下层21天后亚硝态氮质量浓度在0.020~0.035 mg/L波动变化,最终稳定于0.031 mg/L。阶段Ⅱ初期(第106—135天)上层及中层亚硝态氮质量浓度均略有升高,而下层呈降低趋势。第138天后,3个深度处监测点的亚硝态氮质量浓度均呈现升高趋势,且上升速度略快于第106—135天。整体上看,阶段Ⅰ前21天亚硝态氮质量浓度急剧降低,21天后各有变化但变化幅度相对较小;阶段Ⅱ亚硝态氮的变化趋势与硝态氮相似,均出现了较明显的累积。
c.氨氮。阶段Ⅰ各层氨氮初始质量浓度较高,在0.73~0.99 mg/L之间(图3(c))。第21—48天上层氨氮质量浓度稳定在0.32 mg/L左右,中层在0.41~0.58 mg/L之间波动,下层稳定在0.68 mg/L。第48天后各层氨氮质量浓度快速下降,中上层第55天后均保持在0.15 mg/L左右,而下层在55天后仍呈下降趋势,最终稳定在0.20 mg/L。阶段Ⅱ沉积物中各层氨氮质量浓度相对稳定,维持在0.01~0.17 mg/L之间。整体上,阶段Ⅰ各层氨氮质量浓度呈降低趋势,深度45.0 cm处的氨氮质量浓度一直高于其余两个监测点,阶段Ⅱ各层氨氮质量浓度均保持在0.17 mg/L以下。
2.3 模拟试验中pH值、Eh值和HA变化
a.pH值。原状沉积物柱上层pH值略高于中下层(图4(a))。阶段Ⅰ前期(第0—21天)各层pH值较为稳定,其变化幅度均小于0.1。第21—28天各层pH值出现了一定程度的升高,中层上升趋势最为明显,增加了0.20。第28天后上层pH值在第48—55天出现了大幅度上升,而中下层一直保持相对稳定的状态且pH值均在7左右。阶段Ⅱ第106—131天各层pH值相对稳定,第131天后均出现下降趋势,下层变化幅度最大。在同时输入硝酸盐和腐殖酸的阶段Ⅰ,pH值呈升高趋势,在仅输入硝酸盐的阶段Ⅱ,pH值呈下降趋势。

图4 原状柱内不同深度孔隙水的pH值、Eh值、DOC254变化Fig.4 Variations of pH, Eh and DOC254 in pore water at different depths of undisturbed sediment column
b.Eh值。模拟柱中初始Eh值较高(283~290 mV),阶段I初期各深度Eh值急剧下降,在第21天时下降至约-300 mV(图4(b))。第21天后Eh值趋于稳定,其中上层(10.0 cm处)稳定于-300 mV上下;中层(22.5 cm处)Eh值前期下降幅度最大,至第28天时达到-456 mV,随后趋势平稳;而下层(45.0 cm处)Eh值在第21天后仍有继续下降的趋势并最终达到-387 mV。阶段II中,3个深度的监测点处Eh值变化幅度相对较小,其中深度10 cm和22.5 cm处基本保持了阶段I延续的Eh值并有较小幅度的上升,而深度45.0 cm处Eh值在第106—115天内有相对较大幅度的上升,在第115天后趋于稳定并接近深度10.0 cm处的Eh值。总体上,在同时输入硝酸盐和腐殖酸的阶段I试验中,Eh值在前期21天内有大幅度下降,随后维持相对稳定,而在仅输入硝酸盐的阶段II中,Eh值基本维持相对稳定且有微小上升的趋势。另外,各深度处Eh值趋势稳定后22.5 cm处表现出最大的还原性。
c.DOC254。使用DOC254表示HA浓度。原状沉积物柱内下层初始DOC254质量浓度明显高于中上层(图4(c))。随着腐殖酸的输入,阶段Ⅰ前期(第0—25天)上层及中层DOC254质量浓度均有所上升,而下层变化相对较小,保持在11.3 mg/L左右。第25天后各层DOC254质量浓度均呈降低趋势,最终各层DOC254质量浓度在2.33~3.32 mg/L之间,在此期间,中层DOC254质量浓度与其他两层相比相对较低。阶段Ⅱ初期中上层较为平稳,基本延续了阶段Ⅰ末期的质量浓度,而下层呈降低趋势。第131天后3个监测点处DOC254质量浓度波动变化,随深度增加最终质量浓度分别为4.32 mg/L、3.32 mg/L和2.33 mg/L。总体上,阶段Ⅰ中上层DOC254质量浓度呈现出先升高后降低的趋势,而下层初始质量浓度较高,初期变化不大,第21天后呈降低趋势;阶段Ⅱ各层DOC254质量浓度在1.34~6.31 mg/L波动,平均为3.32 mg/L。
3 讨 论
腐殖酸的输入一方面为潜流带营造了适宜发生硝酸盐还原的环境,另一方面提高了硝酸盐还原速率。在腐殖酸输入初期,有机质的输入促进了潜流带中还原环境的形成[16],原状沉积物柱内氧化还原电位快速降低。第0—21天内,柱内呈弱氧化环境且具有较高的初始氨氮质量浓度。在此期间,硝态氮持续累积,而氨氮质量浓度大幅度降低,可能发生了硝化作用与厌氧氨氧化。硝化作用多发生在有氧的沉积物表层,氨氮质量浓度较高时,硝化速率相对较快。陈国元[17]在研究太湖竺山湾沉积物硝化作用时发现,随着NH3-N质量浓度从0.05 mg/L增加到0.85 mg/L,氨氧化速率从(4.58±0.62)mg/(L·d)升高至(28.16±2.27)mg/(L·d)。在相对较高的氨氮质量浓度下,沉积物也具有较高的厌氧氨氧化潜力。罗跃辉等[18]在对太湖西部湖区沉积物厌氧氨氧化潜在速率的研究中发现,厌氧氨氧化速率和孔隙水氨氮质量浓度表现出相似的季节变化特征,随着氨氮质量浓度从1.02 mg/L(春季)升高至3.16 mg/L(秋季),厌氧氨氧化速率从6.57 μmol/(kg·h)升高至10.11 μmol/(kg·h)。另外,原状沉积物柱中还伴有硝酸盐还原过程,见表1。第21天以后柱内呈还原环境,Eh值在-200 mV以下适宜硝酸盐还原反应的发生[19-20]。
在形成还原环境后,伴随着腐殖酸的输入,各深度处硝态氮质量浓度持续降低,第39天后趋于稳定,第21—80天原状柱中平均硝态氮还原速率为0.230 μg/(cm3·d)。在仅输入硝酸盐的情况下,硝态氮及亚硝态氮均出现累积现象。阶段Ⅱ前期(第106—138天)由于柱中仍有阶段Ⅰ残存的腐殖酸作为硝酸盐还原的电子供体,硝酸盐累积速度较缓,平均硝酸盐还原速率相对较高,为0.172 μg/(cm3·d)。而第138天后柱中硝态氮增长速度相对较快,柱中平均硝态氮还原速率降至0.155 μg/(cm3·d),表明停止输入腐殖酸后,电子供体的减少降低了硝态氮还原速率。康丽娟等[21]在太湖环湖河流的研究表明,对于富氮水体(硝态氮质量浓度大于1.41 mg/L)而言,水体中DOC的质量浓度与沉积物反硝化潜力存在较为紧密的相关关系,DOC是反硝化潜力的主要限制因素。杨丽标等[22]在对黄河沉积物反硝化速率的研究中发现,在不另外加氮源的情况下,添加碳源使上覆水有机碳质量浓度为2.4 mg/L时,反硝化速率比原水提高了64.3%,表明有机碳的输入对硝酸盐还原有明显的促进作用。
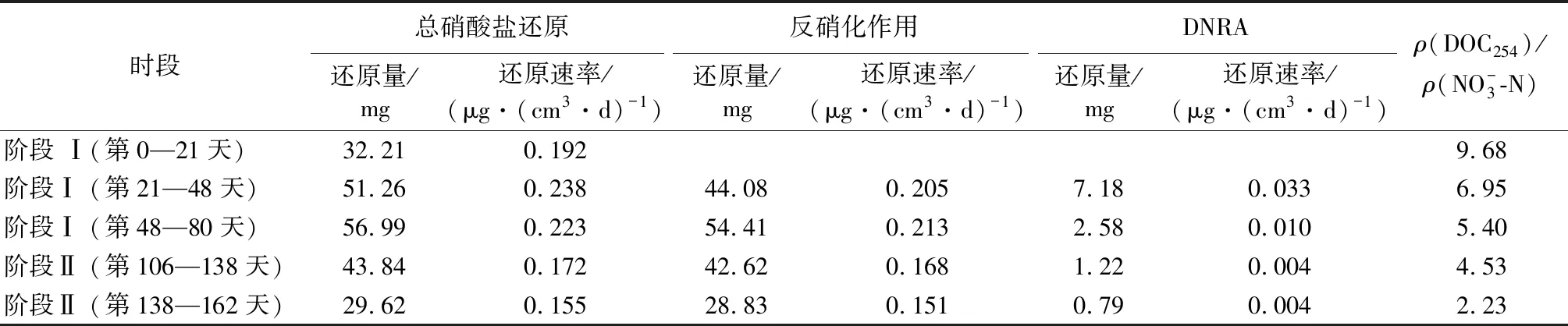
表1 各阶段中硝酸盐还原量和还原速率及不同还原途径贡献的估算
随着下行水流的渗入,硝态氮的还原量逐层递减,上层是硝酸盐还原的主要场所。对于阶段Ⅰ而言,上层硝态氮还原量约占原状沉积物柱总还原量的83.1%,中层占15.9%,硝酸盐还原主要发生在中上层。随着深度的增加,各深度硝态氮质量浓度降低,深度22.5 cm处的平均质量浓度较低,为0.69 mg/L,未给下层提供充足的硝酸盐,因此下层虽然氧化还原电位较低,且有充足的DOC作为电子供体,但对硝酸盐还原贡献相对较小,其硝态氮还原量约为总还原量的1%。
相比阶段Ⅰ,阶段Ⅱ下层硝态氮还原量占还原总量的比例增加,为5.4%,这可能是因为硝酸盐还原速率减小,导致22.5 cm处硝态氮质量浓度略高,给下层硝酸盐还原提供了反应底物,但潜流带中上层还原的硝酸盐仍占还原总量的94.6%。Shelley等[23]在研究英国Rother河的一条支流时发现,在沉积物60 cm深度以下,硝酸盐还原活性较低,硝态氮的还原速率小于1 μmol/h,而在较浅沉积物(0~40 cm)中,硝酸盐还原活性明显增强且波动较大,硝态氮的还原速率在0~17 μmol/h之间,总体上硝酸盐还原总量以及反硝化作用强度随着深度增加而显著减少。Lansdown等[24]对英国Leith河流的潜流带(5~86 cm)进行研究,结果显示,最大的反硝化活性为5.9 nmol/(g·h)(以氮计),出现在深度5~10 cm,且随深度增加明显减弱,也表明潜流带表层具有较高的硝酸盐还原潜力。
反硝化是潜流带硝酸盐还原的主要途径。在腐殖酸和硝酸盐同时输入的情况下,原状沉积物柱内形成稳定的还原环境,特别是在第21天后,反硝化作用对硝酸盐还原的贡献率约为90.0%;在仅输入硝酸盐的情况下,反硝化作用对硝酸盐还原的贡献率为97.3%。Meghdadi等[25]使用同位素分馏分析法估算旱季Ghezel Ozan River潜流带反硝化的贡献率为73.8%,也表明潜流带中反硝化作用对硝酸盐还原具有较高的贡献。有机质质量浓度较高时,原状沉积物柱内可能发生了DNRA作用,随着有机质质量浓度的降低,DNRA作用减弱。21~48 d柱中DOC254平均质量浓度为6.92 mg/L(图4(c)),DOC254与硝态氮平均质量浓度的比值为6.95,DNRA作用占总硝酸盐还原的14.0%。由于反硝化作用大量消耗碳源,48 d后DOC254质量浓度进一步减少,48~80 d平均质量浓度为4.79 mg/L,DOC254与硝态氮平均质量浓度的比值为5.40(表1),DNRA作用对硝酸盐还原的贡献率降至4.5%。而阶段Ⅱ停止输入腐殖酸,DOC254平均质量浓度为3.32 mg/L,DOC254与硝态氮平均质量浓度的比值为2.98,DNRA对硝酸盐还原的贡献率进一步降低,为2.7%。溶解性有机质的浓度是DNRA的重要影响因素,Li等[26]对中国南部岷江河口的研究表明,DOC是DNRA的最佳预测因子,可以解释63%的DNRA方差。Salk等[27]在对Shaws海湾沉积物硝酸盐还原途径的研究中发现高C/N摩尔比的环境更适合DNRA的发生。因此,在C/N摩尔比相对较低的阶段Ⅰ后期(DOC254质量浓度减少)和阶段Ⅱ(无外源有机质输入且硝酸盐不断累积),DNRA受到了一定的抑制。
4 结 论
a.表层沉积物中丰富的有机质为硝酸盐还原过程提供了充足的电子供体。硝态氮伴随腐殖酸随下行水流进入潜流带及其对照试验表明,有机质对硝酸盐还原具有重要的促进作用,在有机质不充分的条件下(即无腐殖酸伴随输入)硝酸盐还原速率降低了26.4%,且出现了硝酸盐累积现象。
b.湖泊表层沉积物是氮素还原的重要场所,是湖泊水体环境中氮素循环的重要过程。室内原状沉积物柱模拟试验发现,在有机质和硝态氮源充足的条件下,浅层沉积物(0~22.5 cm)对硝酸盐还原的贡献达99.0%,而深层沉积物(22.5~45.0 cm)对其贡献相对较小。即使是有机质含量相对较低的条件下,浅层沉积物(0~22.5 cm)硝酸盐还原仍占还原总量的约94.6%。
c.硝酸盐还原途径随着有机质和氮素含量及氧化还原环境而变化。室内原状沉积物柱模拟试验研究发现,在有机质和硝态氮源相对丰富的条件下,反硝化作用是沉积物中硝酸盐还原的主要途径,约占总还原的90%,而DNRA作用对硝酸盐还原的贡献相对较小(5.4%~14.0%),且随腐殖酸浓度的降低而减少(平均为2.7%)。
